作者:中国研究型医院学会呼吸病学专业委员会 北京中西医结合学会呼吸病分会;通信作者:徐作军(Email:xuzj@hotmail.com)
摘要
新型冠状病毒肺炎(COVID-19)是一种急性感染性肺炎,其病原体为2019新型冠状病毒(SARS-CoV2)。自2019年12月以来,全国确诊感染病例数超过8万例。COVID-19在影像学上表现为双肺间质性炎症,约30%~60%的患者出现不同程度的肺间质改变,但大部分患者预后良好。对于如何处理COVID-19引起的肺间质病变方面临床较为困惑,为此我们邀请国内间质性肺疾病领域专家制定了本建议,旨在为国内同道处理COVID-19引起的肺间质病变时提供参考意见。由于目前疫情发生时间短,临床资料和相关研究数据尚不充分,今后将会根据最新的研究结果对本建议进行相应更新。
新型冠状病毒肺炎(COVID-19)是一种急性感染性疾病,主要累及肺部,其病原体为2019新型冠状病毒(SARS-CoV2)[1]。自2019年12月以来,全国确诊感染病例数已超过8万例。COVID-19在影像学上可表现为双肺间质性炎症,约30%~60%的患者出现不同程度的肺间质改变,但大部分患者预后良好[2, 3]。目前临床对于如何处理COVID-19引起的肺间质病变方面较为困惑,为此我们邀请国内间质性肺疾病领域专家制定了本建议,旨在为国内同道处理COVID-19引起的肺间质病变时提供参考意见。由于目前疫情发生时间短,临床资料和相关研究数据尚不充分,今后将会根据最新的研究结果对本建议做相应更新。
一、COVID-19患者肺间质病变的影像学特征
1、病程各阶段的影像学特征
COVID-19的影像学表现类似于严重急性呼吸综合征(SARS)和中东呼吸系统综合征(MERS),以肺部磨玻璃影、实变和间质受累为主要特征。
1、疾病早期:表现为单发或多发的局限性磨玻璃阴影、结节或斑片状磨玻璃阴影,病变内可见细支气管充气征,病变多位于胸膜下,以中下肺分布为主。部分病灶内可见细网格影,而非小叶间隔受累导致的粗网格影。这种病变性质和分布特点提示疾病早期主要累及小叶内间质(图1)[4, 5]。
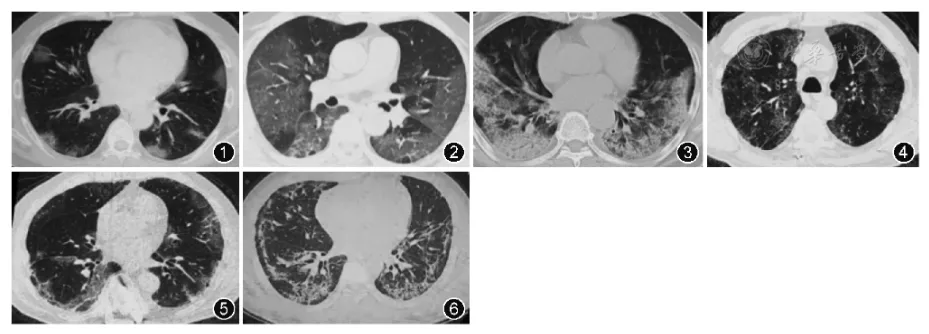
【图1~6】新型冠状病毒肺炎不同病程阶段胸部CT表现:患者男,60岁,因发热、干咳4 d入院,胸部CT示双肺多发斑片状磨玻璃影,主要位于胸膜下(图1);患者男,65岁,双肺呈弥漫性磨玻璃影(图2,3);患者男,58岁,发病第20天胸部CT表现为双肺细网格影(图4,5);患者男,48岁,发病第32天胸部CT表现为双肺纤维索条和细网格影(图6)
2、疾病进展期:常见多发新病灶出现。原有病变多数病灶范围扩大、融合,呈肺小叶分布,病灶内出现大小、程度不等的实变,可有结节和晕征等。在危重症型,双肺可呈弥漫性实变,双肺大部分受累时呈「白肺」表现(图2,3),影像表现可为与非特异性间质性肺炎(NSIP)及机化性肺炎进展期相一致的改变。部分患者在疾病较早期即可出现双肺弥漫的条索、网格影、胸膜下线,提示存在着纤维化过程(图4,5)。
3、修复期:病灶开始逐渐吸收、消散。部分病灶可经历边缘收缩、实变加重的机化过程。有些患者在核酸连续转阴后病灶仍吸收不理想,甚至出现网格影增多、胸膜下线形成,支气管逐渐扭曲和牵张性支气管扩张的纤维化过程(图6)。
2、COVID-19影像学与病理学的关联性
根据目前发表的肺活检病理文献,1例感染14 d死亡的患者病理检查结果显示,病毒主要引起肺泡Ⅱ型上皮细胞损伤及增生,肺泡腔中可见浆液、纤维蛋白性渗出和透明膜形成,肺泡间隔有少许淋巴细胞浸润,属于弥漫性肺损伤(DAD)的早期病变特征(渗出期,图7)[6]。1例在病程第33天死亡的患者肺部病理提示肺泡上皮细胞明显增殖,肺泡内可见浆液、纤维素性渗出物,肺泡间隔可见明显的胶原结缔组织增生(增生期,图8)。1例在发病40 d时接受肺移植患者的肺部病理发现肺组织有大量的肺间质纤维化伴部分透明变性,肺出血性梗死,肺间质有淋巴细胞浸润(图9~12)[7]。这些病理学特征提示新冠肺炎可经历典型的弥漫性肺泡损伤的2个时期:急性期(或称渗出期)和增生期(或称机化期)。前期主要以细胞因子爆发引起肺间质和肺泡上皮细胞的剧烈炎症反应为主,后期可能存在损伤修复,纤维增生等组织机化现象,与SARS肺炎的病理改变类似。文献报道,北京小汤山医院出院的258例SARS幸存者中,51例存在肺纤维化改变[8];随访1年的结果显示分别有23.7%和27.8%的患者仍存在肺弥散功能障碍和影像学的肺间质病变。部分新冠肺炎患者的预后可能会和SARS患者预后表现类似,出现肺功能障碍以及纤维化病灶形成,所以加强对治愈者的长期随访以及适时采取抗纤维化治疗十分必要。
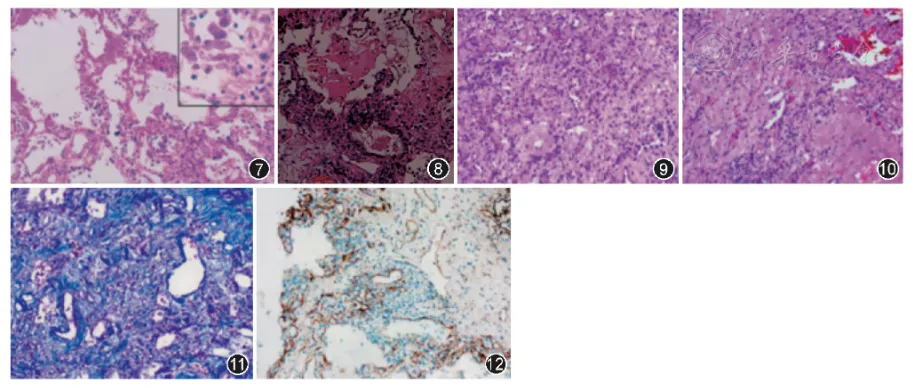
【图7】病理学检查可见肺泡上皮细胞脱落和透明膜形成,符合DAD早期表现,肺间质可见有淋巴细胞浸润 中倍放大,右上角框内为高倍放大
【图8】病理学检查可见肺泡内浆液性或纤维素性渗出物,肺泡间隔可见明显的胶原结缔组织增生和少许淋巴细胞浸润 中倍放大
【图9~12】肺组织病理示肺间质纤维化,伴部分透明变性;图9,10为HE染色,图11为Masson染色,图12为Ⅳ型胶原免疫组织化学染色 中倍放大
二、SARS-CoV2引起的肺损伤及肺纤维化的机制
COVID-19相关的临床和基础研究仍在开展中,对其致病机制目前知之甚少。由于SARS-CoV2和严重急性呼吸综合征病毒(SARS-CoV)在基因序列上的高度同源性、作用受体相同以及临床表现有诸多相似之处,目前对SARS-CoV2致病机制的理解多来自SARS-CoV的机制研究。
1、SARS-CoV2导致肺损伤的机制
SARS-CoV2主要是通过病毒的刺突蛋白(S蛋白)与呼吸道上皮细胞表面的血管紧张素转化酶2(ACE2)蛋白的结合进入细胞内部,介导急性炎症反应,导致肺部损伤[9]。文献报道,SARS-CoV2的S蛋白结合人体ACE2的亲和力是SARS病毒S蛋白的10~20倍[10],这也给SARS-CoV2传染性提供了相应的解释。
在病毒感染引起的免疫反应中,淋巴细胞、单核细胞、中性粒细胞等多种免疫细胞被激活,释放大量的炎症因子/趋化因子,形成「细胞因子风暴」(cytokine storm),这是导致急性呼吸窘迫综合征和多器官衰竭的重要原因。
2、SARS-CoV2导致肺纤维化的机制
SARS-CoV2导致肺泡上皮反复损伤是肺纤维化的启动事件。损伤发生后肺泡上皮不能完成正常的再上皮化、修复延迟,并且分泌大量纤维化细胞因子,启动组织异常修复,肺成纤维细胞和肌成纤维细胞增生,合成大量细胞外基质(ECM),导致肺纤维化。
三、COVID-19引起肺间质病变的临床评估
1、胸部高分辨率CT(HRCT)
HRCT是COVID-19诊断和鉴别诊断以及评价是否有肺间质病变首选且最佳的影像检查技术。
COVID-19诊断的金标准是病毒核酸或血清特异性抗体测定阳性。影像学检查的价值在于更早更快地检出病变、判断病变性质、评估疾病严重程度,以及随访疾病变化情况,是病毒学检测的重要补充手段。
COVID-19在影像学上需要鉴别诊断的疾病包括:(1)其他肺部感染性疾病如其他病毒性肺炎、支原体肺炎、细菌性肺炎等;(2)非感染性疾病,如:血管炎、急性间质性肺炎、结缔组织病相关性间质性肺病、机化性肺炎、药物性肺损伤等。
对于存在肺间质病变病例的放射学复查时间窗目前尚无确切依据,根据目前经验,建议:(1)进展期的非危重症患者,建议1周左右复查胸部CT;(2)修复期患者,若临床表现稳定,可2~4周复查胸部CT,并可随着病程时间逐渐延长复查间隔;(3)急性期危重者则根据临床需要决定。
2、辅助评估肺间质病变严重程度的指标
KL-6在正常肺组织和终末细支气管上皮细胞只有极少量表达,在退变的Ⅱ型肺泡上皮细胞表达增强。外周血KL-6水平可敏感地反映肺泡上皮和间质的损伤程度[11, 12]。
SP-D是Ⅱ型肺泡上皮细胞分泌的细胞表面活性物质的主要成分,在肺纤维化及ARDS患者中显著升高。
晚期糖基化终末产物受体(RAGE)主要由Ⅰ型肺泡上皮细胞产生,研究发现血浆中RAGE水平增加与肺泡细胞损伤有关,并且与肺损伤的严重程度相关。
上皮细胞生长因子受体(EGFR)信号通路在肺纤维进程中发挥重要作用,其配体EGF、TGF-α在肺纤维化患者中显著升高[13]。
3、肺功能检查
间质性肺疾病患者肺功能的特征是限制性通气功能障碍和弥散功能下降。6个月内 DLCO占预计值%下降≥15%和(或)基础DLCO占预计值%<35%是患者预后不良的危险因素[14],需积极的随访监测,随访间隔时间通常为1~3个月。
目前尚缺乏新COVID-19引起间质性肺病患者的肺功能研究资料,急性期患者通常无法完成肺功能检查;且呼吸道传播疾病是肺功能检查的相对禁忌证,因此在COVID-19的传染期不建议进行肺功能检查评估病情。对于病情稳定好转、SARS-CoV2核酸检测连续2次以上阴性,且随访4周无复发者,建议参照普通的间质性肺疾病患者进行肺功能检查。
4、呼吸困难评分(medical research council,MRC)评估病情
MRC评分和圣乔治呼吸问卷(SGRQ)评分,既可评估阻塞性肺通气患者的呼吸困难程度,也可用于间质性肺疾病等限制性肺通气障碍患者,在一定程度上较真实地反映患者的肺功能状况及呼吸困难程度,具有较好的临床价值。由于MRC评分易操作、安全且相对简单快捷,因此建议尝试性用于COVID-19引起的肺间质病变患者的病情评估。
5、6 min步行试验
6 min步行试验是一种简单、安全且廉价的评估患者病情的方法。文献报道,6 min步行试验中氧饱和度降至88%或以下是寻常型间质性肺炎(UIP)和非特异性间质性肺炎患者死亡的预测指标。UIP或NSIP患者的血氧饱和度每降低1%,病死率增加23%。IPF患者6 min步行距离<250 m时,1年死亡风险增加2倍,随访24周后下降50 m提示1年死亡风险增加约3倍[15]。
尽管目前尚缺乏相关循证依据的支持。对于重症期、急性期的患者不建议进行6 min步行试验评估病情,但在康复期可通过6 min步行试验指导患者的治疗及预后的评估。
四、COVID-19引起肺间质病变的处理
需要指出的是, COVID-19引起的肺间质病变不同于特发性间质性肺炎(IIP)和结缔组织疾病相关性间质性肺病(CTD-ILD)。部分COVID-19引起的肺间质病变随着时间的推移,有逐渐好转的趋势。因此对于COVID-19引起的肺间质病变患者,建议早期以严密观察为主,只有胸部HRCT表现为明确间质性病变,且动态随访有逐渐加重趋势,肺功能有明确恶化者,才应考虑给予抗纤维化治疗。
SARS-CoV2感染在不同的患者临床表现差异较大,根据严重程度可表现为轻型、普通型、重型、危重型;根据临床过程可分为急性期(早期、进展期)、修复期和康复期,因此针对每一个患者应给予个体化的管理和精准治疗,治疗方法应综合对症支持治疗、药物治疗、中医药、康复等多种治疗方法,以达到降低远期肺纤维化发生率,或减少肺纤维化进展的目的。
1、急性期治疗
COVID-19患者急性期的肺部病理及影像学表现以炎症渗出为主,而非肺纤维化为主。绝大多数情况下,无法预测患者后期是否会出现不可逆的肺间质纤维化改变,因此该阶段的治疗主要是针对病毒感染本身的治疗及支持治疗,以密切观察和预防为主,不主张过早使用抗纤维化药物。
1、一般支持治疗和抗病毒治疗:可根据目前国家卫生健康委员会与国家中医药管理局发布的《新型冠状病毒肺炎诊疗方案(试行第七版)》中所建议的治疗方案,对患者进行营养支持治疗,并可使用干扰素、洛匹那韦/利托那韦、磷酸氯喹、阿比多尔等抗病毒药物治疗[16]。争取早诊断早治疗,尽量缩短病程,从而减少肺纤维化发生的几率。
2、呼吸支持治疗:对于一般患者,SpO2<92%时可给予氧疗,将SpO2维持在92%~96%,避免过度氧疗。对于需要机械通气的重症患者,应在保证适度的潮气量前提下,尽量使平台压<30~35 cmH2O(1 cmH2O=0.098 kPa);同时避免使用高水平PEEP(>15 cmH2O),从而减少机械通气相关的肺损伤。
3、抗炎治疗:(1)糖皮质激素治疗。糖皮质激素可减轻炎症渗出,但目前对COVID-19患者急性期糖皮质激素的使用还存在较大争议,原则上不推荐针对COVID-19患者包括出现肺间质病变者常规使用糖皮质激素,但对炎症反应过度激活,肺部病变进展迅速,常规手段治疗效果不佳者可试用短时程(3~7 d)的中小剂量糖皮质激素(1~2 mg/kg体重),有助于改善患者病情,并可能改变临床病程。(2)其他抗炎治疗。炎症反应水平较高的危重患者,有条件时还可使用血浆置换、血液滤过等血液净化治疗以清除炎症因子。
4、抗氧化治疗:N乙酰半胱氨酸有较强的抗氧化作用和细胞解毒作用,对于病毒产生的氧化应激反应可能存在保护作用;同时N乙酰半胱氨酸还是痰液溶解剂,有助于肺炎患者排出痰液,且不良反应较少,可在疾病早期使用(400~600 mg,3次/d口服)。
2、修复期的治疗
1、抗纤维化治疗:修复期的主要肺部病理表现是损伤修复,纤维增生等组织机化现象。在该阶段出现肺间质病变的发病机制与肺成纤维细胞的表型改变,转变为肌成纤维细胞,合成大量胶原纤维有关。因此在该阶段,如果胸部影像学上出现肺间质纤维化的征象,如胸膜下线、牵张性支气管扩张、肺结构扭曲或蜂窝样改变等,且病变进行性加重时,才可酌情考虑使用抗纤维化药物。需特别指出的是目前尚无吡非尼酮、尼达尼布治疗COVID-19引起肺纤维化的循证医学证据。
(1)吡非尼酮:抗炎、抗纤维化和抗氧化特性。在动物和体外实验中,吡非尼酮能够抑制重要的促纤维化和促炎细胞因子,抑制成纤维细胞增殖和胶原沉积[17]。吡非尼酮能够显著地延缓肺纤维化患者用力呼气肺活量下降速率,可推荐酌情使用(400~600 mg,3次/d)或吡非尼酮联合N乙酰半胱氨酸治疗。不良反应包括光过敏、乏力、皮疹、胃部不适和厌食等。
(2)尼达尼布:是一种多靶点酪氨酸激酶抑制剂,能够抑制血小板衍化生长因子受体、血管内皮生长因子受体及成纤维细胞生长因子受体。尼达尼布能够显著地减少IPF患者FVC下降的绝对值,一定程度上可延缓肺纤维化进程[18]。可推荐酌情使用尼达尼布(150 mg,2次/d)治疗。常见不良反应为腹泻、恶心呕吐、肝酶升高和血小板减少等。
上述抗纤维化药物存在着一定的副作用且价格昂贵,临床医师在使用时需要评价患者的风险获益比。
2、糖皮质激素治疗:针对部分患者在修复期出现明显肺间质病变,或影像学表现肺间质病变较急性期进展,特别是血清炎性指标升高,肺部影像学以机化性肺炎或NSIP为主要表现的患者,使用糖皮质激素的指征、疗程可适当放宽。建议使用中小剂量激素(1~2 mg/kg体重),疗程可适当延长至2~4周,有助于肺内炎症渗出性病变的吸收,减少肺纤维化的发生。
3、康复期的治疗
患者出院后应定期进行胸部HRCT和肺功能检查,尤其是出院时肺部阴影未完全吸收者,常规随访时间建议出院后第1、4和10个月,以后是否随访取决于患者胸部影像学吸收情况,如果发展为不可逆纤维化阶段,则应该按照肺间质病诊疗常规,3~6个月随访1次。
对于胸部高分辨率CT已经存在明确肺纤维化的患者,建议根据患者肺间质纤维化严重程度、家庭经济状况酌情给予抗纤维化治疗。
对于发展为终末期肺纤维化的患者,可以考虑给予肺移植手术治疗。
4、中医药治疗
COVID-19的肺间质改变,属于中医「瘟疫」所致的「肺痹」。其病因病机为感受疫疠之邪,挟湿毒入肺,痰瘀互结,肺络痹阻,肺失宣肃,脏腑受损[16, 19]。根据本病中医证候特点,拟定COVID-19引起肺间质病变的中医药治疗建议。
1、气阴两虚,挟湿挟瘀。临床表现:活动后气短,胸闷,痰黏难咳,口干,腹胀,乏力,自汗出,大便不调,舌暗红或淡暗,苔薄少,脉细弱。
治法宜益气养阴、利湿通络;推荐沙参麦冬汤、七叶芦根汤加减。
2、肺脾气虚,痰瘀滞络。临床表现:胸闷气短,倦怠乏力,食欲不振,纳差腹胀,或伴呕恶,或头昏沉,大便无力,便溏不爽,舌体胖大,边有齿痕,舌质淡,苔腻,脉缓或滑。
治法宜益气健脾、祛瘀通络;推荐六君子汤、桂枝茯苓丸加减。
3、气虚血瘀,肺络痹阻。临床表现:胸闷气短,活动后略气促,或咳嗽,或胸部隐痛,神疲乏力,自汗,舌淡黯,或有瘀点,苔薄腻,脉细涩。
治法宜益气活血,疏经通络;推荐补阳还五汤合旋覆花汤加减。
4、阴虚火旺,痰瘀阻肺。临床表现:喘息气促,呛咳少痰,口燥咽干,五心烦热,心悸气短,多食善饥,夜寐不安,尿黄、便秘,舌暗红少津,苔薄腻,脉沉细。
治法宜滋阴润肺,化瘀通络;推荐知柏地黄丸、玉女煎加减。
5、脾肾阳虚,肺络痹阻。临床表现:活动后喘息,胸闷气短,咳嗽少痰,少气懒言,腰膝酸软,活动受限,畏寒肢冷,爪甲暗淡,舌淡暗,苔薄腻,脉沉弱。
治法宜温肾健脾,益气通络;推荐阳和汤、二仙汤加减。
5、康复治疗
1、肺康复的意义:肺纤维化患者日常生活活动明显受限,具有低水平的身体机能,高水平疲劳和呼吸困难,这些限制导致生活质量显著降低,进行呼吸康复的综合目的包括:缓解症状、最大限度地提高运动耐量、增加自主日常活动、减轻医疗负担,提高生活质量[20, 21]。
2、呼吸康复计划:包括运动训练、上肢训练、柔韧性训练、神经肌肉电刺激疗法、呼吸功能训练、康复体操及呼吸康复后维持策略等几个部分,其中运动训练是肺纤维化患者呼吸康复的核心环节。
3、患者教育:健康教育是呼吸康复的必要环节,内容包括了解疾病相关的基本知识、就医指征;学会自我疾病管理及目标设定;学会正确的康复锻炼方法等。有效的健康教育可以提高患者及家属对疾病的认识和自我监测的能力,减少病情反复,提高生活质量。
4、心理康复:呼吸功能不能完全恢复到正常状态,容易引起一系列焦虑、抑郁等情绪障碍,同时这些情绪问题又可以进一步导致睡眠障碍和行为问题,在康复期形成身心交互作用的恶性循环,影响个体康复。因此,有针对性的心理康复也是肺纤维化患者康复计划中的重要内容。心理康复主要包括认知调节技术和情绪调节技术。
五、结语
由于COVID-19疫情发生时间尚短,对该病发病机制、传播方式、临床表现、治疗、预后等各方面的研究都还未能深入开展。经过国内外医务工作者的不懈努力,我们已经对该病毒有了粗浅的认识,但是仍有大片的空白领域有待探究。随着对病毒本质认识的不断深入,相信我们会逐步获得诊断、评估、治疗等更多、更强力的有效手段,制定出更全面、更规范的诊疗方案。
执笔:邵池、蒋捍东、张惠兰、李光熙、罗群、孟婕、于文成、苗青、徐作军
专家组顾问:朱元珏(北京协和医院呼吸与危重症医学科),王琦(北京中医药大学东方医院呼吸热病科)
专家组组长:徐作军、蔡后荣、李惠萍、苗青
专家组成员(以姓名拼音顺序):包海荣(兰州大学第一医院老年呼吸科);蔡后荣(南京大学医学院附属鼓楼医院呼吸与危重症医学科);曹孟淑(南京大学医学院附属鼓楼医院呼吸与危重症医学科);曹卫军(同济大学附属上海市肺科医院呼吸与危重症医学科);陈碧(徐州医学院附属医院呼吸科);陈娟(宁夏医科大学总医院呼吸与危重症医学科);陈丽萍(新疆维吾尔自治区人民医院呼吸与危重症医学科);陈起航(北京医院放射科);程真顺(武汉大学中南医院呼吸与危重症医学科);代静泓(南京大学医学院附属鼓楼医院呼吸与危重症医学科);董昭兴(昆明医科大学第二附属医院呼吸与危重症医学科);冯瑞娥(北京协和医院病理科);傅恩清(空军军医大学唐都医院呼吸与危重症医学科);高丽(内蒙古自治区人民医院呼吸与危重症医学科);高凌云(四川省医学科学院四川省人民医院东院呼吸与危重症医学科);葛海燕(复旦大学附属华东医院呼吸与危重症医学科);黄慧(北京协和医院呼吸与危重症医学科);黄燕(空军特色医学中心呼吸与危重症医学科);蒋捍东(上海交通大学医学院附属仁济医院呼吸与危重症医学科);金洪(四川大学华西医院呼吸与危重症医学科);金建敏(首都医科大学附属北京同仁医院呼吸与危重症医学科);李凤森(新疆维吾尔自治区中医医院呼吸与危重症医学科);李光熙(中国中医科学院广安门医院呼吸科);李海潮(北京大学第一医院呼吸与危重症医学科);李惠萍(同济大学附属上海市肺科医院呼吸与危重症医学科);李萍(山西白求恩医院山西医学科学院呼吸与危重症医学科);李振华(中国医科大学附属第一医院呼吸与危重症医学科);路明(北京大学第三医院呼吸与危重症医学科);吕长俊(滨州医学院附属医院呼吸与危重症医学科);罗群(广州医科大学第一附属医院呼吸与危重症医学科);马万里(华中科技大学同济医学院附属协和医院呼吸与危重症医学科);孟婕(中南大学湘雅医院呼吸与危重症医学科);孟莹(南方医科大学南方医院呼吸与危重症医学科);苗青(中国中医科学院西苑医院呼吸科);倪吉祥(三峡大学人民医院呼吸与危重症医学科);彭红(中南大学湘雅二医院呼吸与危重症医学科);饶珊珊(贵州省人民医院呼吸与危重症医学科);王琦(北京中医药大学东方医院呼吸热病科);王笑歌(中国医科大学附属第四医院呼吸科);汪铮(河南省人民医院呼吸与危重症医学科);魏路清(武警特色医学中心呼吸与危重症医学科);徐作军(北京协和医院呼吸与危重症医学科);杨俊玲(吉林大学第二医院呼吸与危重症医学科);杨莉[树兰(杭州)医院呼吸与危重症医学科];于化鹏(南方医科大学珠江医院呼吸与危重症医学科);于文成(青岛大学附属医院呼吸与危重症医学科);张国俊(郑州大学第一附属医院呼吸与危重症医学科);张惠兰(华中科技大学同济医学院附属同济医院呼吸与危重症医学科);张静(天津医科大学总医院呼吸与危重症医学科);张彦萍(河北医科大学第二医院呼吸与危重症医学科);赵铁梅(解放军总医院第一医学中心呼吸与危重症医学科);郑金旭(江苏大学附属医院呼吸与危重症医学科);朱元珏(北京协和医院呼吸与危重症医学科)
* 参考文献(略)
文章来源:中华结核和呼吸杂志2020,43(10):827-833
DOI:10.3760/cma.j.cn112147-20200326-00419
本文完
排版:Jerry


