内容提要
- 新冠患者在呼吸道样本中检测不到SARS-CoV-2 RNA的情况下,粪便中仍长期存在病毒RNA达7个月
- 患者的胃肠道症状(腹痛、恶心、呕吐)与粪便中的SARS-CoV-2 RNA的长期存在有关
- 世卫宣布又有一种新冠疫苗进入紧急使用清单,这是其中第三种中国生产的,也是该清单中中国首款腺病毒载体新冠疫苗和单剂次新冠疫苗
- 菲律宾发现奥密克戎毒株新亚型BA.4感染病例
- 抗新冠病毒小分子口服药物VV116在中国奥密克戎感染者中首个临床研究结果发布
新冠患者在呼吸道样本中检测不到SARS-CoV-2 RNA的情况下,粪便中仍长期存在病毒RNA达7个月?
自2019年底新冠肺炎疫情爆发以来,立刻在全世界范围内形成了大流行。截至目前统计,官方统计有5亿人感染新冠病毒,600多万人死亡。大量实验表明:粪便样本中新冠病毒RNA的阳性率通常落后于呼吸道样本,因此现有的新冠肺炎诊断程序中并没有粪便样本的检测。
目前还没有新冠病毒经由粪便-口腔传染的报道,这就意味着在隔离设施、医院或隔离场所中,通过这种方式传染的可能性较小。但是,潜在的粪便-口腔传播可能会增加旅馆、宿舍、火车、游轮等公共场所种新冠病毒的传播风险。
2022年4月13日Cell Press细胞出版社新推出的医学期刊Med在线发表了来自斯坦福大学医学院的研究文章“Gastrointestinal symptoms and fecal shedding of SARS-CoV-2 RNA suggest prolonged gastrointestinal infection”。该研究发现新冠患者在呼吸道样本中检测不到SARS-CoV-2 RNA的情况下,粪便中仍长期存在病毒RNA达7个月,而粪便中病毒RNA存在与患者的胃肠道症状存在关联。

在这项研究中,研究团队借助于 2020 年 5 月在斯坦福大学启动的测试COVID轻度感染治疗方法的早期临床试验,分析了113名轻至中度新冠患者在新冠确诊后10个月症状的演变,并定期收集粪便样本、呼吸到样本检测新冠病毒RNA。研究人员说,之前的许多研究都集中在重症 COVID-19 患者的病毒样本检测上,这项研究是首次收集轻度至中度 COVID-19 患者的粪便样本中评估病毒 RNA 的存在。
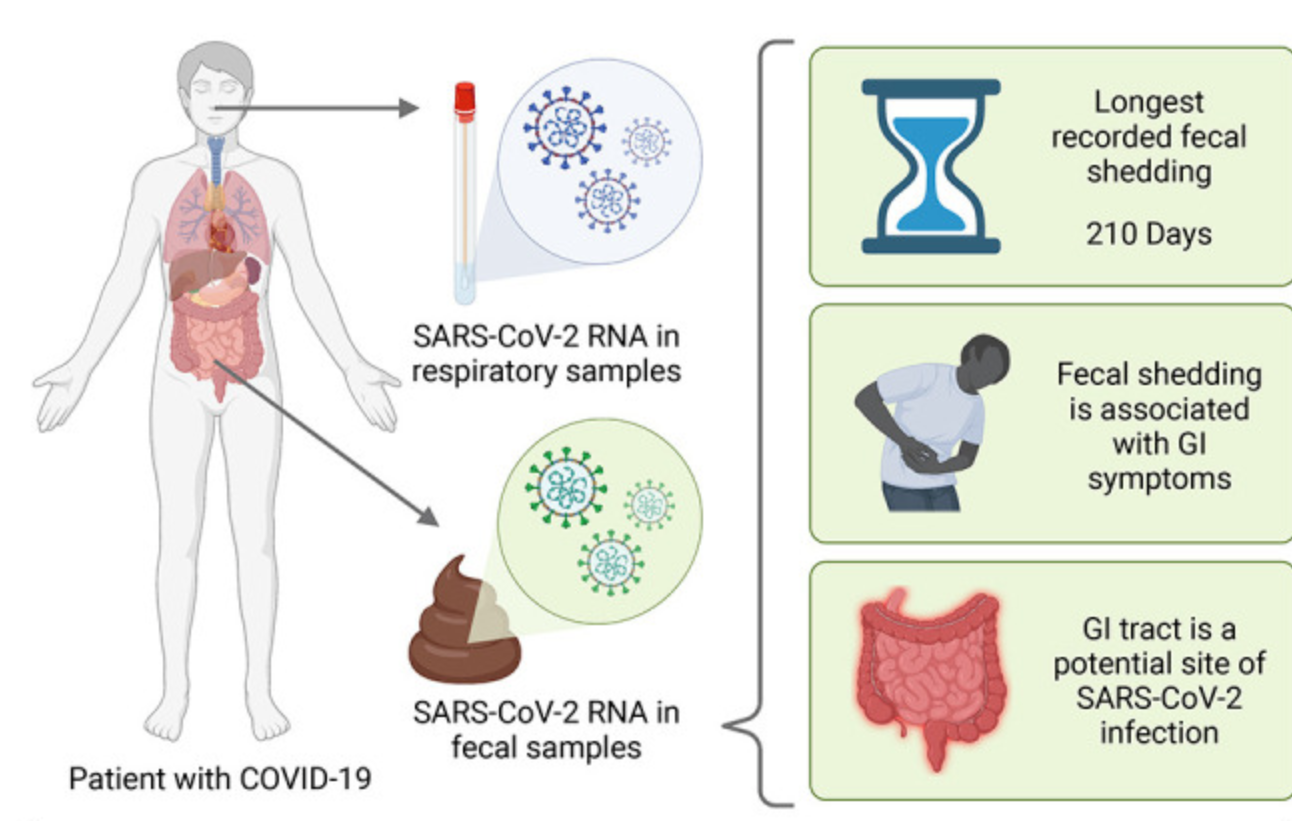
研究人员发现:
1、在诊断后的第一周内,有49.2%的受试者检测到粪便SARS-CoV-2 RNA的存在。
2、12.7%的受试者在诊断后4个月时继续在粪便中检测到SARS-CoV-2 RNA,但此时他们并没有检测到口咽SARS-CoV-2 RNA。
3、3.8%的受试者在诊断后7个月时仍可检测到粪便SARS-CoV-2 RNA,但是诊断4个月及之后所有受试者的口咽部均无法检测到SARS-CoV-2 RNA。
4、结合受试者确诊后的症状演变和粪便SARS-CoV-2 RNA的检测情况,研究人员发现:患者的胃肠道症状(腹痛、恶心、呕吐)与粪便中的SARS-CoV-2 RNA的长期存在有关。
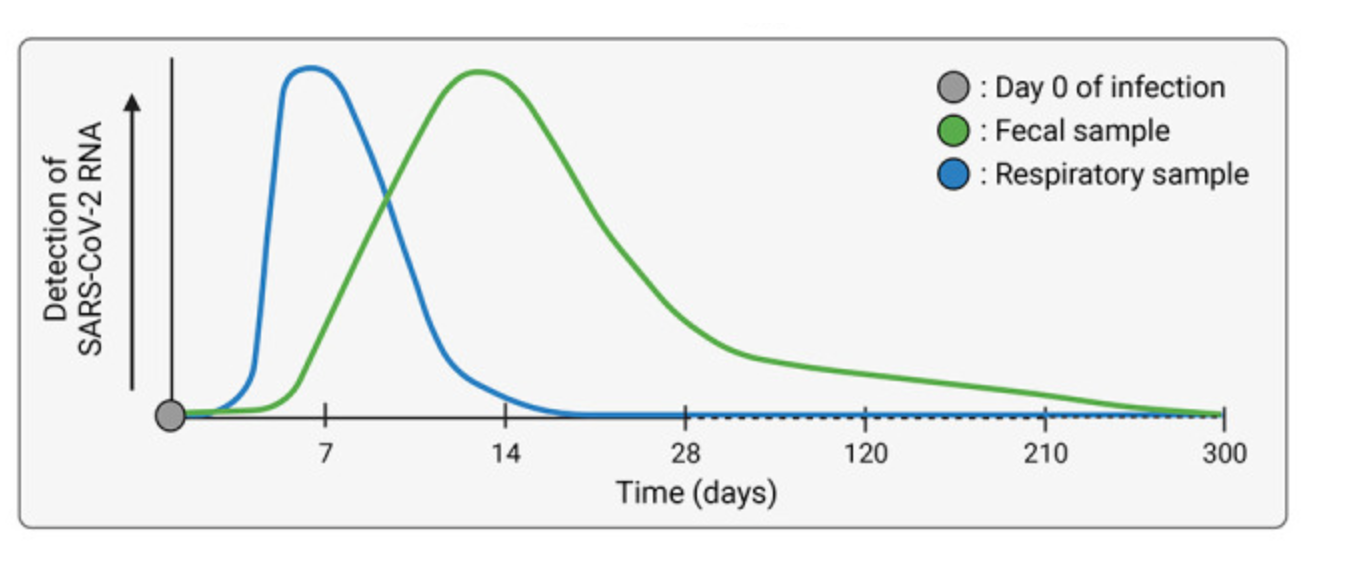
COVID-19病毒主要引起呼吸系统疾病,但这项研究表明,在清除肺部的病毒后,新冠病毒可以感染患者的肠道数周乃至于数月。该文作者、斯坦福大学医学和遗传学副教授高级研究员 Ami Bhatt 博士说:“这可以解释为什么一些 COVID 患者会出现腹痛、恶心、呕吐和腹泻等胃肠道症状。”
Bhatt博士很快指出,虽然RNA是冠状病毒的遗传残留物,但并不是真正的活病毒,因此人的粪便不太可能具有传染性。但是她认为,肠道中长期存在的的 SARS-CoV-2病毒确实对新冠患者的疾病转归存在潜在影响。因为发现那些在粪便中检测到 SARS-CoV-2 RNA的患者,即使他们的呼吸道中已经无法检测到 SARS-CoV-2病毒,但他们仍有很大概率出现胃肠道症状。
与此同时,更多研究也在肠道以外的部位发现了难以消散的病毒储存库。有研究团队分析了在44名COVID-19患者尸检时采集的组织,在心脏、眼睛、大脑等许多部位都发现了病毒RNA的存在,甚至在感染后的第230天还能检测到病毒RNA和蛋白。

最后,Bhatt博士指出,这些发现还对通过测试社区废水中的病毒证据来预测新出现的 COVID-19 爆发的公共卫生工作产生了影响。美国国家传染病基金会医学主任William Schaffner博士表示同意:“如果,正如他们所说,大约 4% 的新冠患者在 7 或 8 个月后仍在粪便中排出病毒残留物,这会使社区中新感染人群的评估变得复杂,这是我们必须考虑并开始展望未来的另一件事。”
世卫宣布又有一种新冠疫苗进入紧急使用清单,这是其中第三种中国生产的,也是该清单中中国首款腺病毒载体新冠疫苗和单剂次新冠疫苗
19日,世界卫生组织宣布又有一种预防由SARS-CoV-2引起的COVID-19疫苗进入紧急使用清单(EUL)。这是经世卫组织验证纳入紧急使用清单的第三种中国生产的COVID-19疫苗,进一步增加了世卫组织验证疫苗的数量,助力疫情的应对工作。
新增加的第11种世卫组织验证疫苗不仅证明了全球科学家和研究人员的独创性和奉献精神,还证明了全人类在应对共同挑战方面的耐力和实力。
疫苗是抗击COVID-19疫情工具箱的重要组成部分。除了要追踪接触者、检测、必要时进行隔离、采取戴口罩和洗手等个人防护措施、完善治疗方法外,2019冠状病毒病疫苗也能帮我们摆脱大流行疫情。
据环球时报,本次中国康希诺生物研制的腺病毒载体新冠疫苗获批世卫组织紧急使用授权,列入紧急使用清单 (EUL)。这是继国药和科兴疫苗后,中国第三款列入世卫组织紧急使用清单的新冠疫苗,也是该清单中中国首款腺病毒载体新冠疫苗和单剂次新冠疫苗。
菲律宾发现奥密克戎毒株新亚型BA.4感染病例
据央视报道,5月21日,菲律宾卫生部发布报告称,该国发现了一例新冠病毒奥密克戎毒株新亚型BA.4感染病例。报告称,该病例是一名菲律宾公民,于5月4日从中东返回菲律宾,5月8日进行的核酸检测结果呈阳性,属于无症状感染者。菲卫生部称,BA.4毒株的传播速度可能会更快。
抗新冠病毒小分子口服药物VV116在中国奥密克戎感染者中首个临床研究结果发布
前言:SARS-CoV-2奥密克戎变异株最早报道于2021年11月,目前已成为世界范围内的主要感染株。VV116是一个由中国科学家研发的口服小分子抗新冠病毒药物,在体外活性实验中表现出了对包括奥密克戎在内的多个新冠病毒变异株的较强抑制作用。已经完成的I期药物临床试验表明,VV116在健康受试者中表现出良好的安全性、耐受性与药代动力学特征。
近期,国家传染病医学中心、上海市传染病与生物安全应急响应重点实验室、华山感染张文宏教授团队与上海公共卫生临床中心范小红教授团队、临港实验室共同合作,完成了一项开放性、前瞻性队列研究,评估VV116对非重症奥密克戎感染者新冠病毒核酸转阴时间的影响,相关成果于2022年5月18日发表在Emerging Microbes& Infections杂志。
上海市公共卫生临床中心沈银忠教授为本文第一作者,复旦大学附属华山医院感染科艾静文,上海市公共卫生临床中心林娜,复旦大学附属华山医院感染科张昊澄、李杨、王红羽为共同第一作者。上海市公共卫生临床中心兼职教授、复旦大学附属华山医院张文宏教授与上海市公共卫生临床中心范小红教授为此文共同通讯作者。

在感染早期或有症状的非重症患者中应用VV116或能够缩短核酸转阴时间:研究数据提示,在使用VV116的奥密克戎感染者中,从开始用药到核酸转阴的平均天数为3.52天;在首次核酸检测阳性5日内使用VV116的患者中,其核酸从首次检测阳性到转阴的平均时间为8.56天,小于对照组的11.13天。有症状的患者中,在本研究的用药时间范围内(首次核酸阳性2-10天)给予VV116,均可以缩短患者的核酸转阴时间。在药物安全性上,使用了VV116的患者中,未观察到严重不良反应。

未来探讨:需要注意的是,作为一项开放性、前瞻性队列研究,本研究所纳入的样本量有限,所有受试者均未发展为重症或危重症。因此本研究未能收集到足够多的数据进一步分析VV116是否对于奥密克戎感染重症化具有预防作用,仅初步评价了非重症感染者中新冠病毒核酸转阴时间这个单一指标。
目前国内正有多项抗病毒药物的II-III期研究正在或准备开展,华山感染团队也正在瑞金医院宁光院士的牵头下,参与了Paxlovid 和VV116的“头对头”临床对照研究。我们也将密切关注未来更大规模的药物临床试验数据结果,以进一步评估药物对于临床恢复时间、临床重症预防及病死率降低的具体作用。
这是国产抗新冠病毒药物对奥密克戎感染者临床研究结果的首个同行评议报道。未来,相信国内医疗领域各团队也将不断努力,获得更多临床试验数据,为新冠病毒感染者包括重症和危重症患者探索更多可行的抗病毒治疗方案。
参考文献:
1.SHEN YZ,AI JW, Lin N, et.al. An Open, Prospective Cohort Study of VV116 in Chinese Participants Infected with SARS-CoV-2 Omicron Variants [J]. Emerging Microbes & Infections, 2022.
2. XIE Y, YIN W, ZHANG Y, et.al. Design and development of an oral remdesivir derivative VV116 against SARS-CoV-2[J]. Cell Research, 2021, 31(11): 1212-1214.
3. QIAN H J, WANG Y, ZHANG M Q, et.al. Safety, tolerability, and pharmacokinetics of VV116, an oral nucleoside analog against SARS-CoV-2, in Chinese healthy subjects[J]. Acta Pharmacologica Sinica, 2022.
来源:生命科学前沿、世界卫生组织、央视新闻、环球时报、华山感染


