新冠状肺炎袭卷鄂地及全国已过去两月,然而人们对于它的致病机理基本未知。原因在于缺少动物实验依据,缺少临床标本依据。因此在目前情况下,尚无针对发病机制的治疗。
作为一名目前在前线抗疫、长期从事急性肺损伤发病机制研究的临床工作人员,综合现有的临床影像资料,作以下方面的机制猜想。希望能给同行及相关基础研究人员一些启发。
一、假说一:经典发病机制
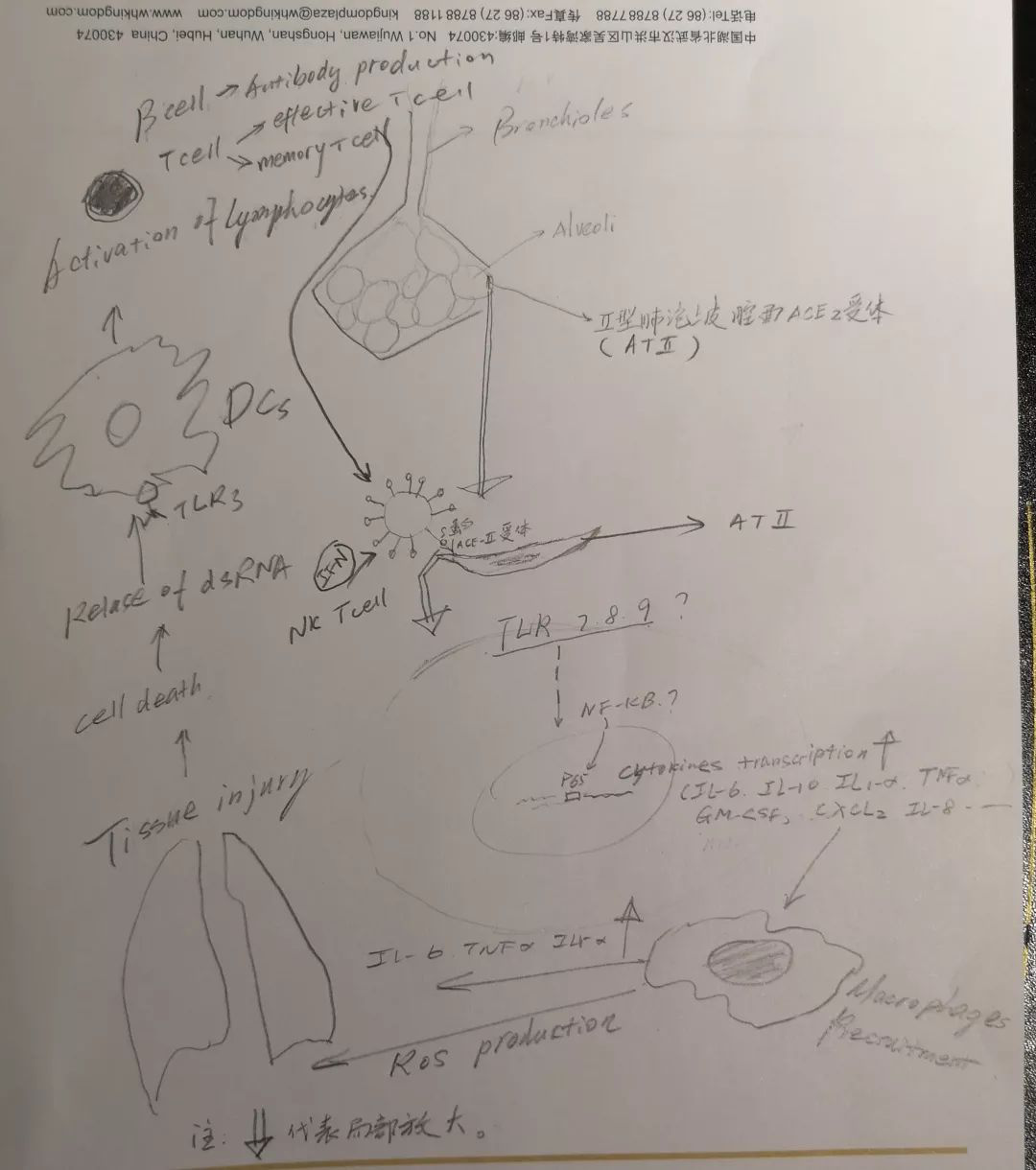
目前广泛证据认为,新型冠状病毒藉由其表面的棘突蛋白(S蛋白)与具有ACE2受体的细胞结合,将其RNA物质注入细胞内。一篇小样本正常人的肺组织标本单细胞RNA排序表明,80%的ACE2受体集中在2型AT。Cov-19在肺内最佳靶细胞可能是II型肺泡上皮细胞(ATⅡ)。病毒进入人体后会激发一系列的炎症、免疫反应,从而介导机体损伤与疾病状态。
TLR7、8、9是可识别外源性核酸物质的Toll样受体。TLR3特异性识别病毒复制的中间产物ds-RNA,仅表达于树突状细胞。上皮细胞内病毒核酸可能藉由TLR7、TLR8、TRL9中的某分子激起细胞内的基因转录水平,释放细胞趋化因子,从而形成后面一系列级联反应的源头。吞噬细胞如巨噬细胞在趋化因子的作用下,穿越基底膜,到达感染靶细胞,聚集到感染上皮细胞,启动炎症级联反应,释放炎症因子如IL-1、IL-6、TNFa,同时线粒体途径激发氧自由基形成。此时机体表现为发热,感染部位血管内皮通透性增高,肺内液体渗出增加,急性肺损伤;受感染细胞在崩解过程中,位于树突状细胞上TLR3可以识别复制中间体ds-RNA,从而将信号传递给淋巴细胞,B淋巴细胞忙于产生中和性抗体或其他抗体(可能);而T淋巴细胞接受信号,从淋巴组织中释放出来,效应T淋巴细胞在抗原刺激下,获得了迁移至病灶部位,释放细胞因子,如INF,参与杀伤靶细胞;NK细胞则不借由抗原递呈,可直接分泌干扰素等物质杀伤靶细胞。一系列的作战过程,留下细胞残片、水肿及代谢产物覆盖于损伤组织的表面,形成透明膜样改变,造成急性肺损伤的基础病理改变,也是我们影像学上大片磨玻璃影及实变影的基础成分。此时患者表现为咳嗽、呼吸困难、胸闷;同时,血常规提示耗竭性淋巴细胞降低(当然,淋巴细胞降低也有可能有其他机制参与有关)。如急性肺损伤导致的器官功能障碍长期不能缓解,病毒血症仍在持续,或继发性二重感染,则会引发序贯性功能损伤,患者最终死亡。
二、假说二:凝血机制障碍
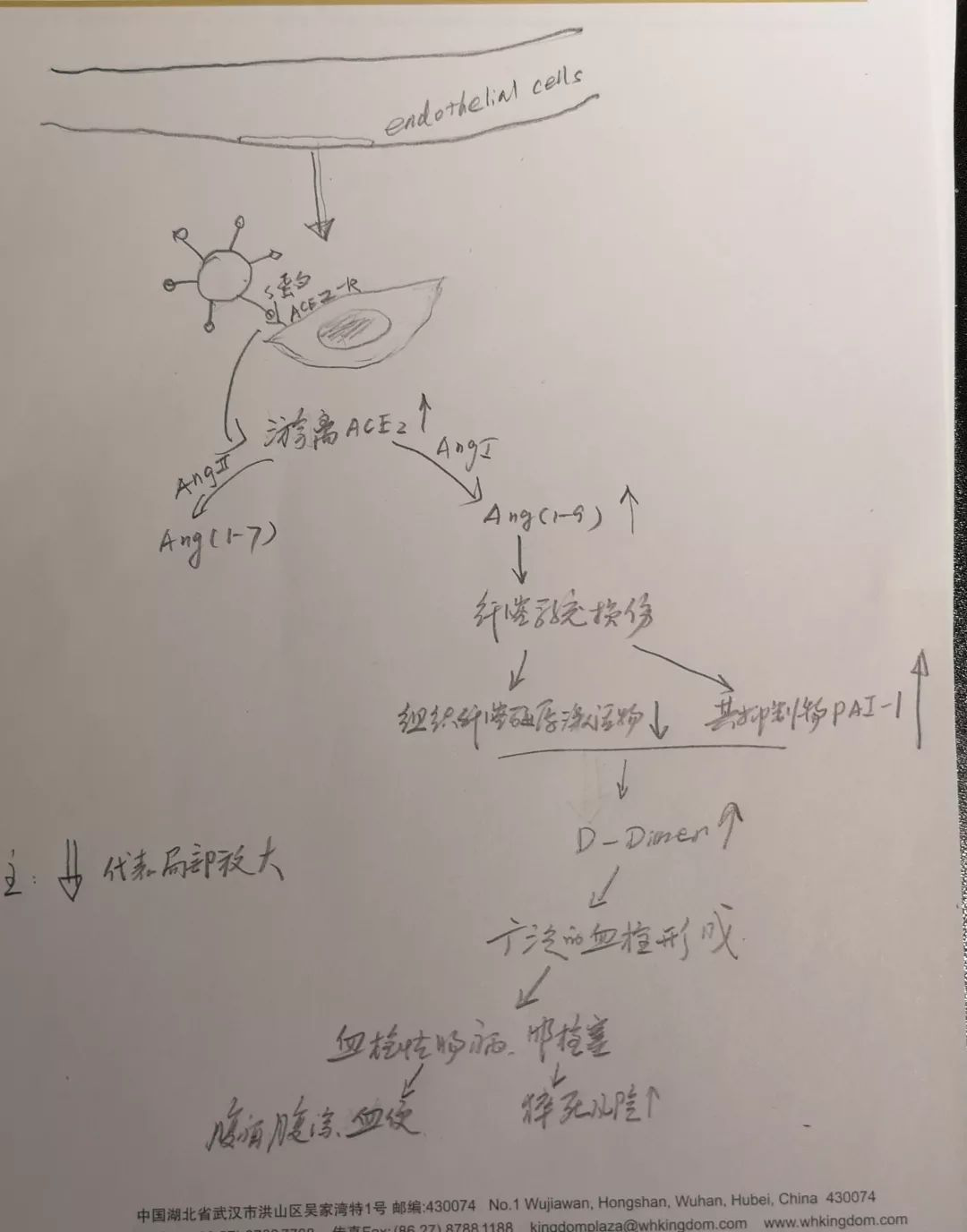
最近的流行病学调查结果发现死亡患者D-二聚体升高水平更明显。脓毒症患者表现出凝血机制障碍DIC是常见的,其具体原因包括组织损伤、休克等。新冠肺炎在病程的早期即合并D-二聚体的升高,是否有其他机制的参与尚未可知,ACE2受体广泛存在于心肌细胞及血管内皮细胞,可激活AngⅡ生成Ang(1-7)、AngⅠ生成Ang(1-9)。一篇动物实验指出:Ang(1-9)可使纤溶系统损伤而导致大鼠静脉血栓形成。ACE2受体由于被广泛的竞争性占用,游离ACE2升高,导致Ang(1-9)升高,降低血浆、组织纤溶酶原激活物,增加纤溶酶原激活物抑制剂(PAI-1)。因此,D-二聚体升高,除感染因素外,尚可能是由ACE2 水平异常改变而致纤溶系统损伤、血栓形成的继发性改变。此时我们尤应注意,在感染过程中D-二聚体明显升高的患者影像学是否合并肺梗死的成分(外周楔形病灶)。临床上我们看到血便、血尿的情况并不少见,是否归因于病毒的直接作用,还是ACE2 相关的纤溶系统损伤待进一步研究证实。
三、假说三:自身免疫攻击
病毒所造成的自身免疫攻击并不陌生,如肺肾出血综合征(Goodpasture Syndrome)。我们在临床中发现多系统器官损伤,包括肾脏、肠道、心脏,有时并不依赖于脓毒症休克等容易造成MODS的情况,那么自身免疫性攻击,有可能存在于患者循环内。最近,我注意到,中国科技大学生医部魏海明教授在临床患者中发现GM-CSF异常升高,当然这也是脓毒症炎症激活道路的下游产物,然而也不排除会激活产生自身抗体的可能。《呼吸界》发布了2例患者病理学改变提示局灶肺泡腔内透明膜形成并不突出,但肺泡腔内可见蛋白性渗出物,结合某些患者影像学在相对后期可出现铺路石样改变,我个人建议行PAS染色确定蛋白液是否为富含磷脂的蛋白质。我们知道GM-CSF自身抗体异常参与了自身免疫相关性肺泡蛋白沉积症患者的发病过程,建议在临床上对某些铺石路样改变患者行GM-CSF抗体检测。
在新冠发病以来,国内各专家短期内进行了大量的基础及临床科研工作。相信在不久的未来,相关发病机制研究会喷涌而出。我们拭目以待!
参考文献
[1] Yu Zhao, Zixian Zhao, Yujia Wang, Yueqing Zhou, Yu Ma, Wei Zuo. Single-cell RNA expression profiling of ACE2, the putative receptor of Wuhan 2019-nCov. BioRxiv. 2020, Jan. 26.
[2] A Mogielnicki, K Kramkowski, J M Hermanowicz, A Leszczynska, K Przyborowski, W Buczko. Angiotensin-(1-9) Enhances Stasis-Induced Venous Thrombosis in the Rat Because of the Impairment of Fibrinolysis. J Renin Angiotensin Aldosterone Syst. 2014; 15 (1), 13-21.
作者介绍

李慧
副主任医师,南京大学医学院附属鼓楼医院呼吸与危重症医学科(目前在武汉同济医院光谷院区工作),研究方向:主要从事肺部感染性疾病的基础及临床研究。曾获得国家自然科学基金青年基金项目1项。2009.12-2011.12曾在美国Vanderbilt University医学院过敏及肺与危重症科访问学习两年。


