我现在在武汉同济医院光谷院区,得益于光谷院区和中法新城院区的几位同事的帮助,我把「加重新型冠状病毒肺炎的血流动力学等变化」的一些救治体会和大家分享。
Q:什么加重了新型冠状病毒肺炎?
在重症新冠肺炎的抢救中,我们确实要把一些能够可逆的、简单实用的技术先做好。同时我们也看到了很多现状,许多重症新冠病人在有创通气的成功率偏低,包括上ECMO的病人的成功率也是偏低。那么原因是什么?一方面,这是一个新的疾病,我们对它的病理生理不了解;另一方面,我们在管理方面还有待加强,确实有很多国家级的医疗队在前线,但是从管理理念、操作质量、对疾病管理的同质性以及统一性方面,我认为还有待提高。我来到武汉之后,很关注低氧血症,如果血流动力学不纠正或者未寻找它的规律,很难把病人治好。我们在前期的工作中关注了一些有关心脏和血管方面的病毒性肺炎的改变,所以也把新冠肺炎作为一个关注的兴趣点。
现阶段我所在的病区主要都是重症病人,但这些重症病人还没有向危重症转变。什么原因让重症转变成危重症?中间有哪些预警的因素?病人一旦发展成重症,哪些症状或者哪些体征是我们特别要重视的?因此,特别要重视新冠病毒肺炎加重的病理生理,在病理生理中我比较感兴趣的一点是对容量和心血管的影响。
今天主要和大家分享四方面内容
第一,新型冠状病毒肺炎加重可能的容量相关因素探讨。如果容量相关的问题解决了,病人的病死率或者由重症加重成危重症的情况是否会减少。
第二,新型冠状病毒肺炎加重可能的心脏损伤因素探讨。在重症和危重症病人身上能否找到有关心脏损伤的规律,或者心脏损伤的规律是否导致重症转化成危重症的原因。
第三,新型冠状病毒肺炎终末期心脏损伤的初步特点。对此进行回顾分析,因为时间紧、任务重,我还没有完全把规律总结出来,第一时间和大家分享或者能得到大家的指导是我非常迫切的愿望。
第四,重症新型冠状病毒肺炎ARDS和高碳酸血症等的影响探讨。如果不是上ECMO的病人或者没有条件上ECMO的病人,高碳酸血症对血流动力学以及病人的氧合的影响也非常大,我们如何应对。
一、新型冠状病毒肺炎加重可能的容量相关因素探讨
我们到武汉有27天的时间,在这期间,我们首先把能够实施的、相对可行性高或者暴露风险低的事情先做好。
Case 1
先看一个病例,女性、64岁、发病5天,无基础病。这个病人在我们收治的病人中属于病程比较短的,由于我们集中收治的武汉重症病人有一个时间段,所以我们收治的大部分病人病程在一周以上,甚至十天到两周。
这个病人的胸部CT表现是一个比较典型的外带的渗出影改变;当时我们常规的进行了一些容量的筛查,发现她的下腔静脉最宽处最宽时测量出的下腔静脉直径只有0.96cm。之后,我们询问病史,首先,她没有明显的口渴、心慌这种休克的表现;其次,也没有明显的纳差或者因为发热后不喝水,容量丢失的表现;另外,没有使用利尿剂或者补液过少的表现。
这个病人给我一个启示,这种病人为什么在入院时就存在下腔静脉直径偏低的表现?所以把我们病区的病人都进行了筛查,我们成立了一个超声小队,筛查的结果令我吃惊。
下腔静脉直径和下腔静脉塌陷指数
肝段下腔静脉测量最宽处最宽时直径
我们特地把病程在7-10天的病人归类,发现69.23%的病人的下腔静脉直径<1.5cm,29.23%的病人的下腔静脉直径在1.5-1.7cm的范围内,1.53%的病人的下腔静脉直径在1.7-1.9cm的范围内,而且下腔静脉塌陷指数(IVC-CI)均>50%。有一方面原因,在院外的容量管理是否存在不足,是否存在低血容量休克,我认为可以考虑为隐匿性休克。所以对于这一阶段而言,我们认为给这些病人补液或者加强经口饮水,可能会对病人远期是否从重症转为危重症有益。
PICCO测量
最准确的还是要对这些病人进行有创通气时的测量,主要用PICCO测量。在很多情况下要使用有创呼吸机的时候才会去进行PICCO测量,有时候无创通气的病人的依从性也比较差,对于这些病人,测量出的数据确实值得讨论。
Case 2
我们来看一个病例,男性,57岁,病程8天,使用了有创通气,PEEP 8,PC 22,VT380,C 25,Lac 2.5,没有使用血管活性药物。根据查体、PCT等方面来看,细菌感染的证据不足。PICCO:MAP 102,CI 2.28(偏低),GEDI 726,SVV15%(偏高),SVRI 1250,ELWI 17,综合分析提示心源性和感染性休克均存在可能。
感染性确实也值得争议,很多教授认为感染性在前期的可能性要小,但是从我们前期做的一些研究来讲,很多病毒感染首先破坏呼吸道上皮细胞,呼吸道上皮细胞的屏障破坏以后,多多少少会混合感染。所以如果是病程较长的病人可能存在混合细菌感染的可能。那么,这种感染性休克是病毒本身还是因为细菌或感染引起?我们在武汉收治的这些病人中,确实有很多病程长、有基础病、年龄偏大的病人,在这种状况下,把病毒单列出来做病理生理的分析存在一定难度。
病毒性脓毒症休克?
很多教授也提到病毒性脓毒症(Viral Sepsis),我觉得这个概念非常好,但是新冠病毒的病理生理特点与其他疾病有什么不同?
病毒——Viral Sepsis
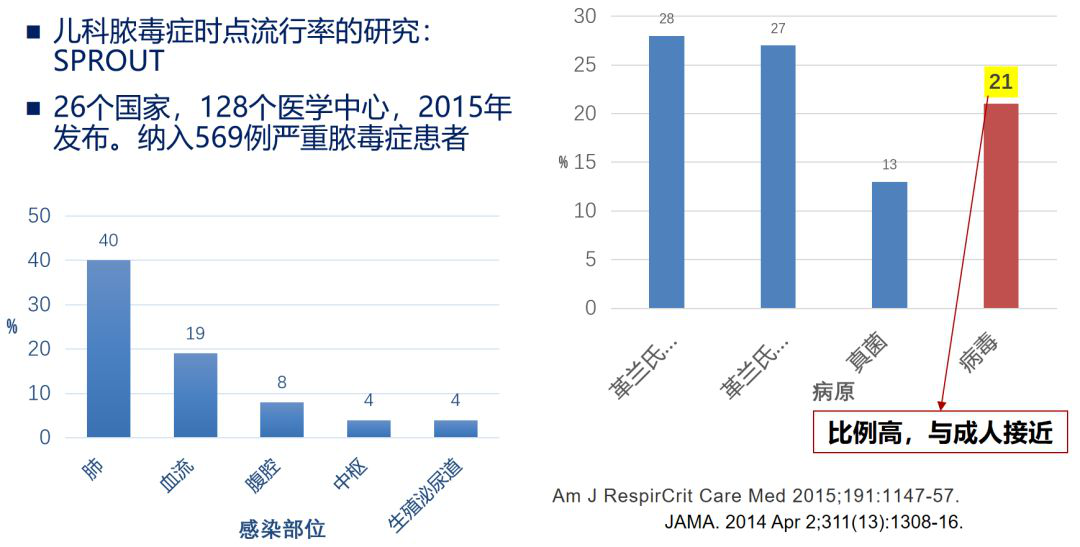
我们先对病毒性脓毒症进行回顾。这是儿科脓毒症时点流行率的研究,在病毒相关疾病中,儿童的检出率或儿童的重视程度可能是重于成人的,病毒所占比例达到21%。
病毒种类


有很多病毒的种类,比如单纯疱疹病毒,它主要通过母婴传播;肠道病毒,因为肠道病毒没有相关的抗体,所以很容易引起全身症状的表现;还有人细小病毒以及流感病毒。
我们最关心的就是把新冠病毒和流感病毒作比较,因为无论是H1N1还是H7N9都出现过ARDS、心肌炎、脑病的表现,高危人群都是低龄或高龄、免疫抑制人群以及孕妇等发生这些表现,但是与新冠病毒相比可能存在差异。所以我觉得存在流感病毒相关的病毒性脓毒症这种说法,但是国内可能在前期的总结中还没有把流感病毒的病毒性脓毒症作为一个主要的依据。
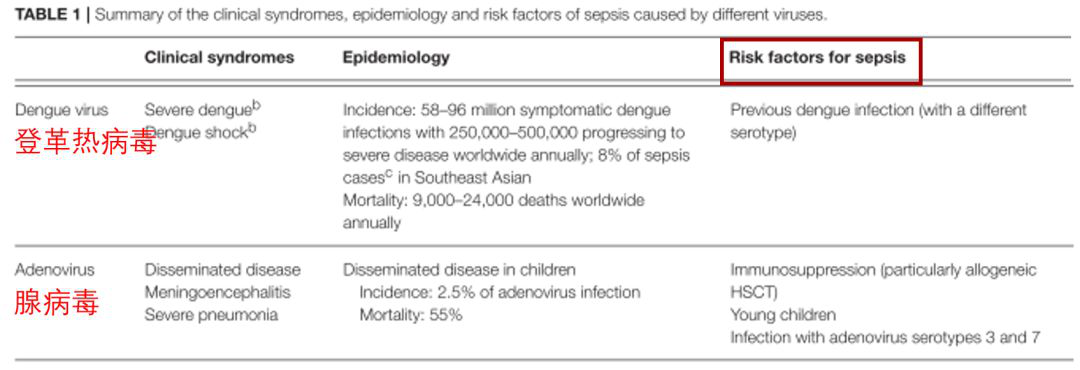
2019年腺病毒较多,腺病毒引起的休克比例不小,特别是对于一些免疫抑制的病人来讲,在年轻人中腺病毒也比较多。腺病毒引起的休克有个特点,包括一些上ECMO的病人恢复还是比较快的。所以从腺病毒的角度来说,我认为值得我们参考,因为腺病毒可能比流感病毒更严重,器官衰竭更明显一些。
病毒——宿主
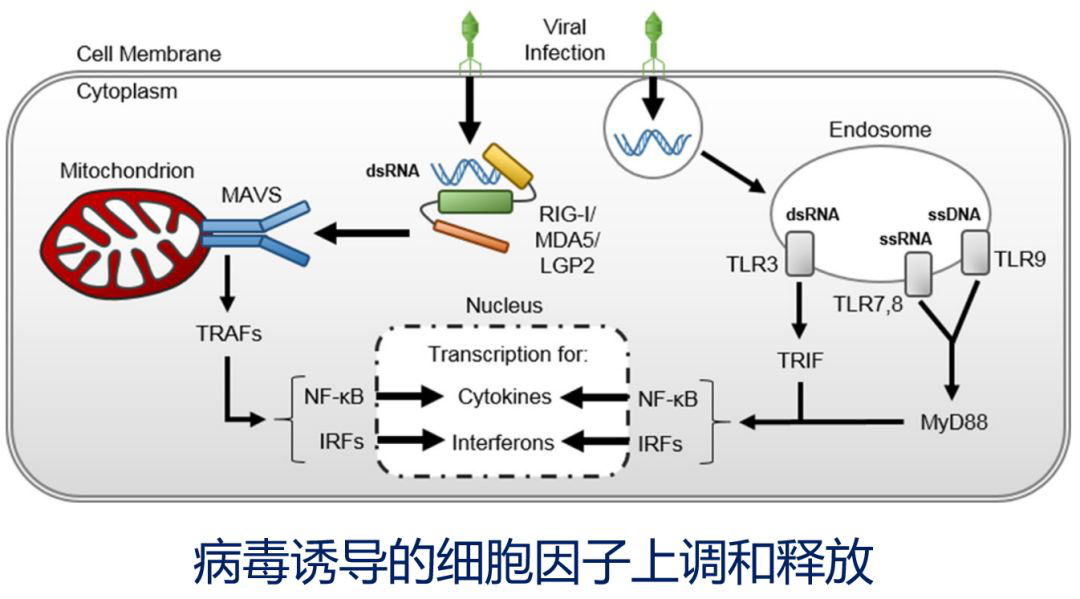
病毒本身与宿主会相互影响,所以我们很期待一些抗病毒药物,曹彬教授也专门给我们讲解了新的抗病毒药物,我们在看到抗病毒药物希望的同时,也要去关注宿主。炎症因子增加是特点之一;从临床测量的结果来看,以白介素2受体升高和白介素6升高为主,这些其实都与巨噬细胞M1活化有关,它不像白介素10,它还是有自身特点的,现在也有单抗。对于细胞因子是否可以用CRRT来清除,也有这样的建议,我们认为在CRRT实施的过程中,有些病人的病程可以延长一点,但是病情稍微缓解一点,与病死率有没有直接关系还期待进一步的研究。
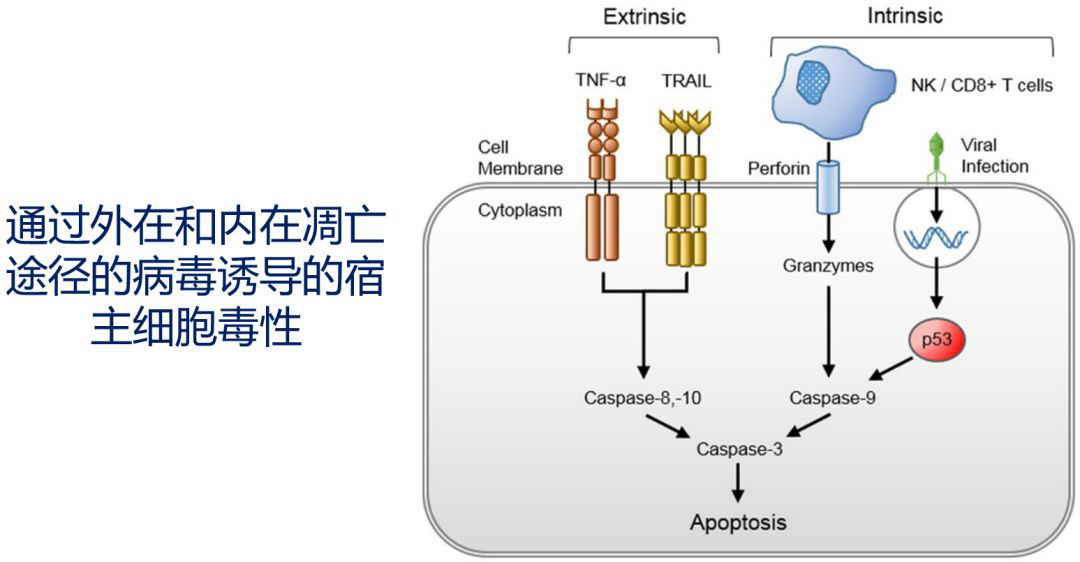
宿主在经过病毒诱导后,也会增加宿主本身的细胞凋亡。特别是我们看到很多顽固性低氧血症的病人,不论如何都维持不住氧合,甚至出现机化性肺炎的表现,后期也出现了肺纤维化。所以这些表现说明病毒在破坏氧合,让宿主自身的毒性或者宿主细胞产生凋亡、纤维化或者机化,激活内在途径。
病毒——免疫正常
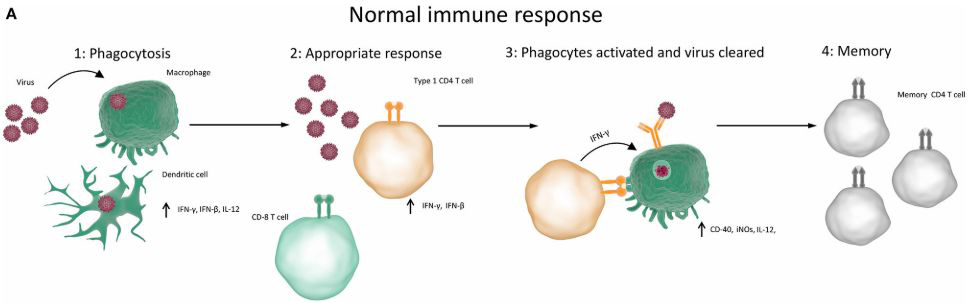
这些途径是大家比较熟悉正常的免疫反应,比如巨噬细胞、树突细胞会吞噬病毒。特别是CD4淋巴细胞,很多新冠病毒感染病人的CD4淋巴细胞非常低。进一步会引起巨噬细胞的活化,去进一步清除病毒,然后CD4淋巴细胞等会产生记忆等效应。
病毒——免疫异常
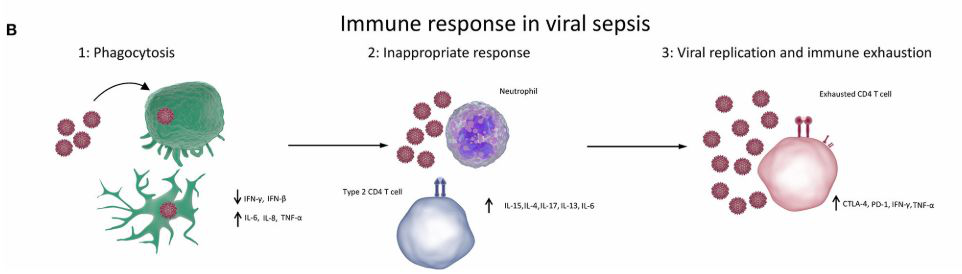
这张图是现在新冠病毒病人出现比较多的情况。确实在病人的肺病理中发现并不是像流感病毒那样,以淋巴细胞的浸润为主,而是以单核细胞和巨噬细胞浸润为主。这样的浸润后,并没有让淋巴细胞,特别是CD4淋巴细胞发挥它的T细胞免疫作用,导致了大量的病毒没有T细胞的作用,而病毒不断复制,处于一个免疫耗竭的状态,甚至在某些免疫器官中,淋巴细胞属于一个极度耗竭的状态。所以一旦巨噬细胞、单核细胞激化以后,后续就没有淋巴细胞在继续发挥作用。从细胞免疫阶段来讲,确实是一个非常棘手的问题。这样的问题一旦发生后,可能直接就导致了一些机化、纤维化,从而我们说病毒载量的持续比较高。因此,我认为病程长必然会带来一些血流动力学的问题。
Viral Sepsis相关研究

流感病毒确实是脓毒症的一个主要问题。除了流感病毒以外,还有其他病毒,但其他病毒都会对心脏产生影响,比如肠道病毒、细小病毒。所以病毒并不是器官特异性选择,特别是新冠病毒。

HPeV阳性者表现为脓毒症样(sepsis like)疾病、脑膜炎。

是否有新冠病毒、流感病毒和其它病毒合并,我们在平时处理重症病人的时候会看到很多病人是合并单纯疱疹病毒感染。虽然我们没有在新冠病毒病人中检测出,但还是推断在器官衰竭的病人中是否可能存在几种病毒感染,比如流感病毒和新冠病毒,也可能是新冠病毒和单纯疱疹病毒合并,特别是用了ECMO或者是有创通气的病人,这种情况还是存在的。
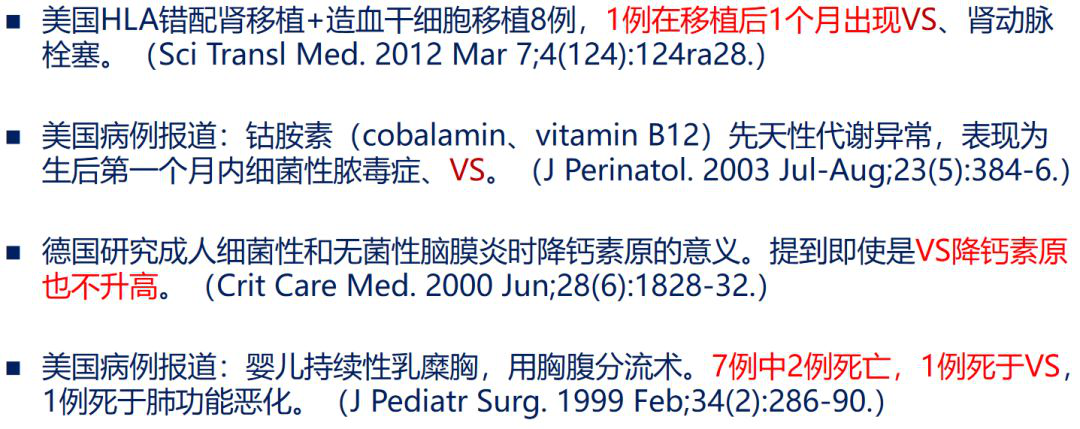
对于免疫低下或免疫抑制人群,比如移植的病人、先天性代谢异常的病人或者乳糜胸的病人。从这几个研究中,我觉得最主要的是与流感病毒一样,新冠病毒病人的PCT不高,但是PCT不高有时候也不一定不是细菌感染,因为细胞免疫抑制以后,PCT值即使有细菌感染也不一定会升高。目前还没有其他更好的指标,PCT还是作为细菌感染参考的值。
Viral Sepsis-小结
这次在武汉的很多重症、危重症或者普通型病人没有出现高热的表现,无特异性,儿童患者发热为最常见症状。甚至体温正常或偏低,这是病毒性脓毒症的一个特别表现。
多种病毒可导致病毒性脓毒症;也有研究发现,42%的病人有混合感染,其中RSV、流感及副流感病毒、鼻病毒、腺病毒最常见,现在也有报道说它们与流感病毒有共同检出;对多种病毒共感染患儿的meta analysis未显示与临床严重程度增加有关。
继发于流感脓毒症的各种肺外并发症,包括但不限于肾衰竭,横纹肌溶解症,脑病,心肌炎和多器官衰竭。肺外并发症也包括血流动力学,病人如果出现严重的氧合障碍或者AKI时会给他上ECMO和血液透析。我曾经总结了一些影响因素,比如我们的操作对于炎症因子反应、炎症风暴或者血管内皮的通透性的影响,其实无论在ECMO还是CRRT都是有影响的,反而IABP可能是影响最小的。
病毒性脓血症一般在新生儿、免疫低下多见,侵袭性操作如ECMO、血液透析时会出现。
进行病毒性脓毒症的诊断,需除外细菌、真菌、寄生虫所致脓毒症。但是从临床来讲,还是有一些相应的倾向性,如果确实没有细菌、真菌的证据,还是要考虑脓毒症是由病毒引起。检测尚无金标准,POC、DFA、NAAT、PCR各有利弊及限制。PCT、CRP在鉴别病毒、细菌无特异性。特异性标记物尚处研究阶段。治疗见SSC4推荐。
明确的病毒性感染,注意预防、并及时处置其导致的脓毒症。
二、新型冠状病毒肺炎加重可能的心脏损伤因素探讨
人感染H7N9禽流感住院患者心脏损伤与死亡的关系
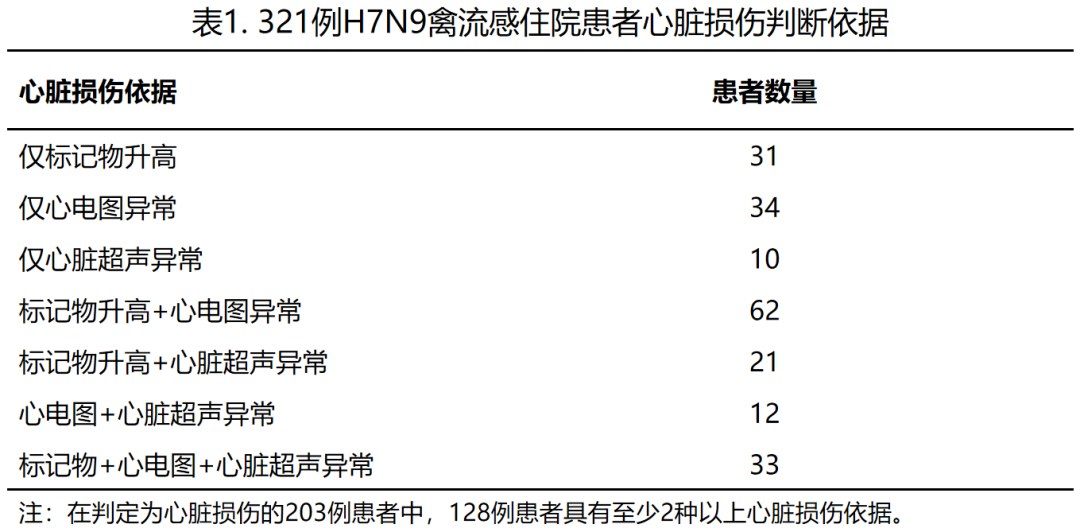
今天我主要把心脏损伤的相关问题和大家分享。我们在前期关注了人感染H7N9禽流感住院患者的心脏损伤情况,经过严格筛选,在321例患者中,发现有63.2%(203例)的病人存在不同程度的心脏损伤。
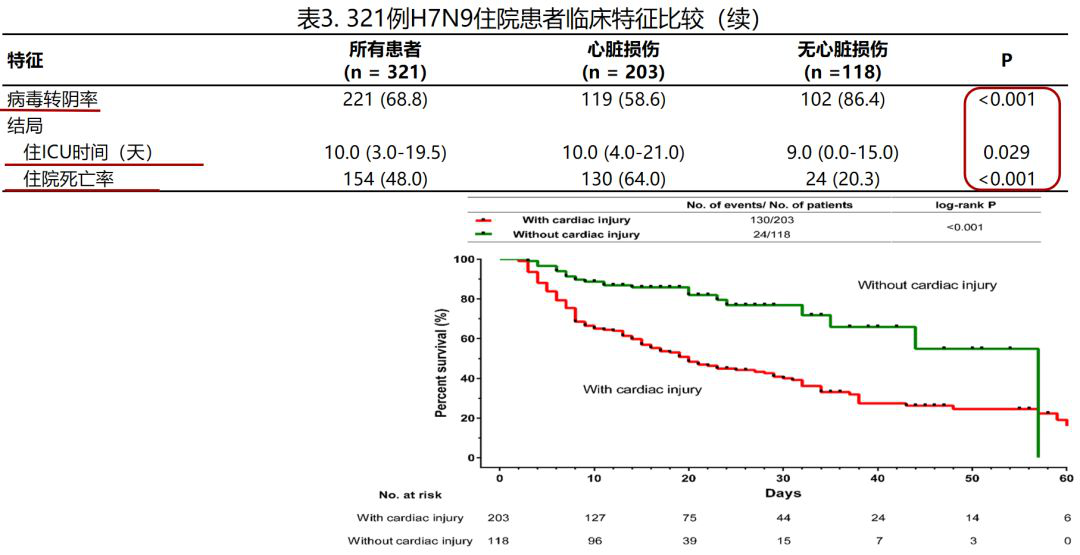
心脏损伤的发生率与住ICU时间(天)、住院死亡率、病毒转阴率直接相关。初步比较两组临床特征及结局,显示与无心脏损伤患者相比,发生心脏损伤患者的病情更重,脏器替代治疗比例更高,病毒转阴率更低;其住ICU时间更久,住院死亡率更高。在这些心脏损伤的H7N9的病人中,没有发现病毒血症的阳性,也没有在现有的心肌细胞中明显检测出有心脏病毒的阳性,这点与新冠病毒不太一样。

混杂因素:年龄≥65岁,APACHE II ≥ 21,PaO2/FiO2≤200mmHg,AKI以及心脏基础疾病。其他方面比如细胞活性药物、乳酸等这些因素都没有得出与心脏损伤有关。多因素分析校正混杂因素显示,心脏损伤与住院死亡率升高独立相关。
COVID-19 肺炎重症心肌损伤
如何区分爆发性心肌炎与脓毒症心肌病?
新冠病毒如此严重,有时病人的病情变化特别快,相应的心脏损伤也比较受关注,引起了大家讨论的话题。提到病毒,大家可能一个比较固定的思维就是是否为爆发性心肌炎FM,但近几年有说法是病毒也会引起脓毒症心肌病SC。
爆发性心肌炎发病比较迅猛,而且有一个典型特点,心肌水肿是爆发性心肌炎与脓毒症心肌病的关键区别点。在临床中可以通过反复的心超检查去测定心肌有无水肿的表现。但一般病程快、疾病急、疾病重的话,可能还是考虑爆发性心肌炎。那么,到底新冠病毒是爆发性心肌炎,还是后面会激发脓毒症心肌病?
病毒引起的爆发性心肌炎病死率高。脓毒性心肌病是脓毒症休克继发,表现为左室扩张和EF下降,一般7-10天可恢复,常见病因是细菌感染,这与爆发性心肌炎完全不同。在武汉的重症新冠病人中,由于病程的程度、基础病、年龄等因素,这些病人是不是在前期就存在细菌感染?
检索流感引起脓毒症心肌病的发生率
我之所以把爆发性心肌炎和脓毒症心肌病罗列出来,我想和大家讲的意思就是,流感病毒引起脓毒症心肌病的发生率很低。我们做了一个检索,只有两篇文章写到流感引起脓毒症心肌病,而且这两篇文章都是合并细菌感染引起的。
脓毒症患者中的脓毒症心肌病的发生率:13.8%
可以这样说,新冠病毒是不是引起脓毒症心肌病的几率也会偏低,因为从前期来讲,我们看到心肌的损伤在7~10天能恢复的几率还是偏小,而且超声上也不太支持。但是如果仅是细菌感染为主的脓毒症,脓毒症患者中的脓毒症心肌炎的发生率为13.8%,还是比较高的。
脓毒症心肌病的诊断
主要有一些明显的功能学改变,比如左室扩张、EF下降、短期恢复这些改变。
爆发性心肌炎大多需要IABP和ECMO治疗
通常需要机械循环支持,例如主动脉内气囊抽吸和静脉动脉体外膜氧合。
COVID-19?
刚才讲到,爆发性心肌炎发病比较迅猛,可能发病的时候病人的情况维持不住导致死亡。我们在武汉有一部分可能是早期收缩的病人,刚入院可能就维持不住死亡了,来不及进行检测、治疗,所以我推断这些病人可能有部分是爆发性心肌炎存在。但是在2019年日本有学者进行研究发现,脓毒症心肌病和爆发性心肌炎可以同时存在,不一定合并细菌感染,认为病毒本身也会合并脓毒症心肌病。所以对于新冠病毒而言,我们还没有总结出来,只能说可能部分早期患者存在爆发性心肌炎合并脓毒症心肌病、部分病程长的患者仅仅合并脓毒症心肌病,后面会给大家介绍这些指标的变化。
三、新型冠状病毒肺炎终末期心脏损伤的初步特点
尸体解剖

第七版诊疗指南介绍了尸体解剖的心脏病理,心肌细胞可见变性、坏死,间质内可见有少数单核细胞、淋巴细胞和(或)中性粒细胞浸润。从我第一时间看到这个病理结果,我没有很震惊,因为做尸检的时候,根据尸检的时间间隔会有一定影响,我觉得大部分病人可能都会有一些变性、坏死,所以我推断可能不一定完全是由病毒引起。心脏病理结果还发现部分血管内皮脱落、内膜炎症及血栓形成。
所以从心肌本身来讲,我认为这样的病理结果没有看出特异性改变。反而心脏的病毒检测,我了解到的都是阳性的表现。从病毒血症、心脏的检测结果来看还是区别于其他流感,特别是从细胞的种类,单核细胞和巨噬细胞为主,也完全具备流感。所以很多人认为新冠肺炎一个新的疾病,新的疾病一定是有新的病理生理,这确实值得我们重视。
部分心肌肥大并慢性缺血改变。可能个别病人中有冠心病的表现,但是这可能也给我们一个提示,如果病程越长的病人,由于低氧血症维持的越长,可能慢性缺血的改变越明显。
部分心肌存在急性损伤,建议结合心肌酶谱。因为目前为止我看到的报道,肌钙蛋白是唯一一个与心肌损伤存在直接联系,很多报道可能并不是与超敏肌钙蛋白联系得很紧密,而是普通的肌钙蛋白,但是超敏肌钙蛋白证据的级别也是比较高的。所以我们不能否认早期存在急性心肌炎症,但是加重的因素中心肌是否为主要因素,缺氧一方面是氧合,另一方面是灌注,如果心肌炎症影响心脏的功能,我觉得灌注下降的时候缺氧是不可能纠正的。
COVID-19 肺炎危重症心肌损伤
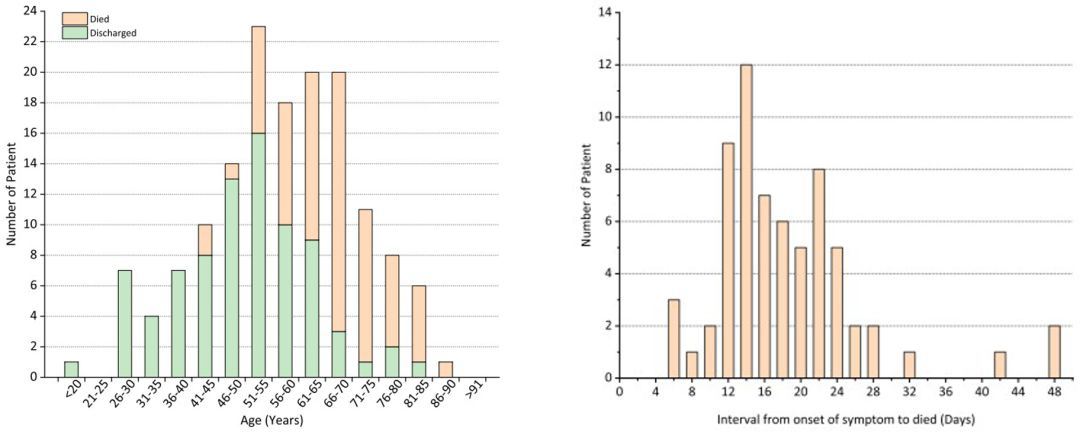
这是武汉的同道发表在《Intensive Care Med 》的文章,我们来讨论一下。文章提到死亡病人的年龄分布在50岁以上为主,年龄分布和我们收治的病人差不多,老龄化是新冠病人的特征。我认为另一个数据(右图)更值得重视,从发病到死亡的时间大部分是从12天以后,到24天是一个死亡的高峰期,也就说撑过24天的危重症病人的淋巴细胞慢慢恢复,可能就会有所好转,这和在重症流感救治的经验有些类似。但是这个死亡的特征与心脏是否有关?
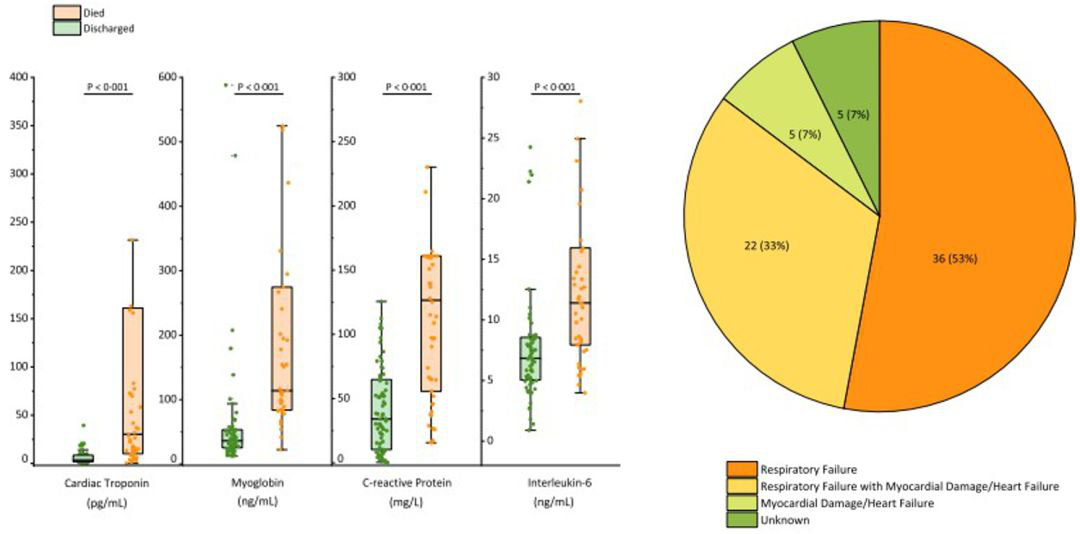
我们的同道也把与心脏相关的肌钙蛋白等指标进行了分析,认为死亡病人的肌钙蛋白、肌红蛋白这些指标远高于存活的病人。也进行了死因分析,如果合并心肌损伤或者心衰,无论有无呼吸衰竭,占整体比例的40%的病人死亡与心脏相关,但是这种关联从这篇文章得出的结论是引起了爆发性心肌炎。但是如果从爆发性心肌炎的临床特征来讲,我觉得还是欠缺一些比如心肌水肿或者其他相关的临床过程的描述,另外,如果从爆发性心肌炎发病的特点来讲,是否符合我们刚才提到的大部分病人是在12天~24天死亡的特点。所以从12~24天死亡的病人来看,我们有理由相信50岁以上、病程12天以上的危重症病人是否已经合并细菌感染,是否也可能因为脓毒症心肌炎引起。从这样的特点来看,我们觉得有必要再进行一些分析。当然这篇文章给我们非常好的解释,认为心脏相关的血流动力学改变是非常重要的。所以回到最开始我说的是不是除了补充的容量之外,有没有心肌的抑制或对应参与这些容量的调节。
Case 3
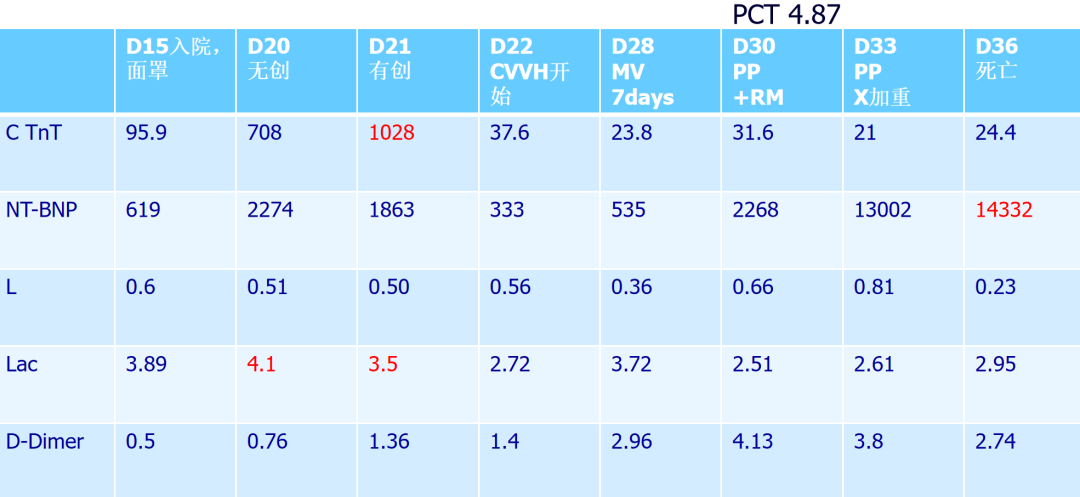
这是一个死亡病人,女性,65岁,糖尿病病人,无心血管疾病。一般我们关注死亡病人的心脏的指标有超敏肌钙蛋白(即C TnT,因为在武汉只能查超敏基肌钙蛋白)、NT-BNP、淋巴细胞总数、乳酸和D-二聚体。这个病人发病15天入院,入院时面罩吸氧,超敏肌钙蛋白很高,为95.9,这还不是最高。发病第20天使用无创通气一天,超敏肌钙蛋白为708。我觉得我们几个重症的教授提的建议都非常及时,如果这个病人1~2个小时不能改善,及时上有创机械通气,发病第21天上了有创通气后发现超敏肌钙蛋白继续增高,达到1028,这时我们发现病人可能有些绝望。但是在发病第22天,使用CVVH开始做血滤的时候,超敏肌钙蛋白的数值下降,为37.6。再持续有创通气一周,超敏肌钙蛋白还在继续下降。到了发病第30天,做俯卧位、肺复张,病人的超敏肌钙蛋白也没有再继续升高。发病第33天,依然维持在极限,直到发病第36天死亡。所以这个病人没有直接因为肌钙蛋白升高引起死亡,当然这是个案。我们在思考肌钙蛋白的增高与病人的死亡是否存在直接的时间关联性,甚至肌钙蛋白的升高也与其他因素有关。
病人入院第一天,乳酸为3.89,很高,入院5天后乳酸为4.1,在无创和有创切换的阶段乳酸是最高的,这个阶段灌注很差,如果总的灌注差,我们相信冠脉灌注一定也差,所以冠脉灌注差的时候,我觉得肌钙蛋白值一定是高的。所以从这个关联度来看,乳酸相对稳定的时候,肌钙蛋白的波动好像不是很大。有关NT-BNP,从619升高到2274,再下降到1863,相对稳定的阶段的数值为333和535,但是恶化的阶段是14332。反而我们看到如果NT-BNP的指标迅速升高,可能与死亡相关。所以我们在血流动力学管理的时候,是否可以参考乳酸值联合肌钙蛋白的值,是否要更加重视NT-BNP的急剧变化,功能学的指标是否比心肌细胞的炎症指标更值得重视。但是这个病人的细胞免疫始终很低,淋巴细胞最高只有0.6,最后死亡的时候也只有0.23。D-二聚体在中间有些波动,病人死亡时的D-二聚体的数值高于正常值。从这个病例我们看出存在肌钙蛋白由低到高、由高到低的演变过程,因此我们是否可以推断病人最严重的时候一定是肌钙蛋白最高、入院时一定是最高或者是入院时较低。
Case 4
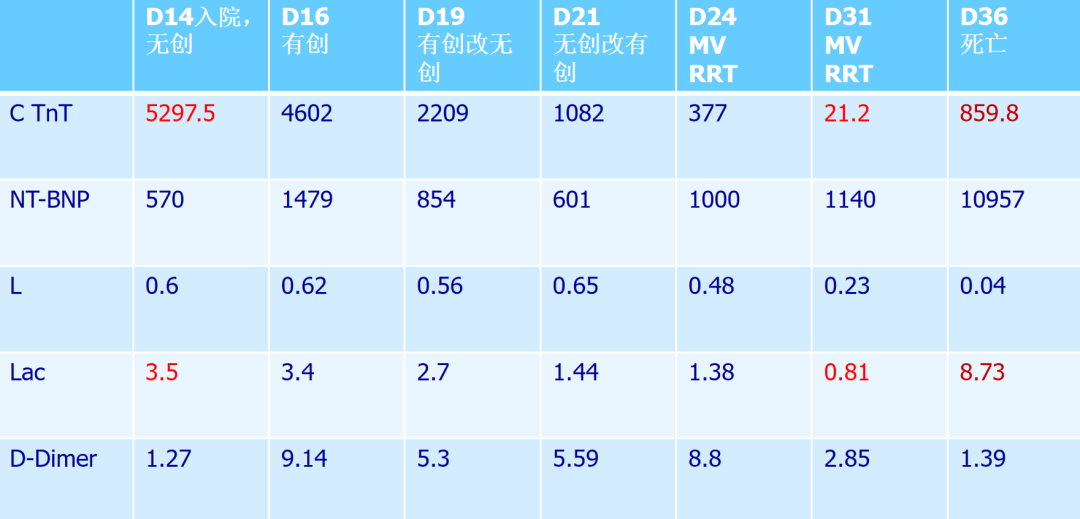
我们再看一个病例,男性,52岁,伴有腹泻,无明显发热,无心血管疾病、无AKI表现,所以对检验值的影响比较小。但是这个病人与上述的病人不同,发病第14天入院,入院时就需要用无创通气,超敏肌钙蛋白非常高,达到5297.5。经过治疗,超敏肌钙蛋白改善,但到最后死亡的时候,突然升高到859.8。由此得出,肌钙蛋白与病人死亡没有明显的关联,但是确实是肌钙蛋白高的病人预后可能不是很好。NT-BNP达到10000多的时候,病人的病死率更高。淋巴细胞也是这样,病人死亡时的淋巴细胞只有0.04,这就是细胞免疫非常低的状况。刚刚验证了一点,如果乳酸高,超敏肌钙蛋白的值相应也是较高。这个病人的D-二聚体非常高,那么是否存在右心的血栓阻塞肺动脉的相关问题,不一定是因为缺氧,是否存在梗阻性休克,因为数值如此之高的D-二聚体确实是提示存在急性肺栓塞的表现。我们在临床上很少看到病人刚入院的超敏肌钙蛋白就达到5000多,但是在新冠病人中,NT-BNP数值达到几万、肌钙蛋白达到几百很常见,甚至肌钙蛋白达到上千。
重症转危重症预警指标?(以下指标仅仅做参考)
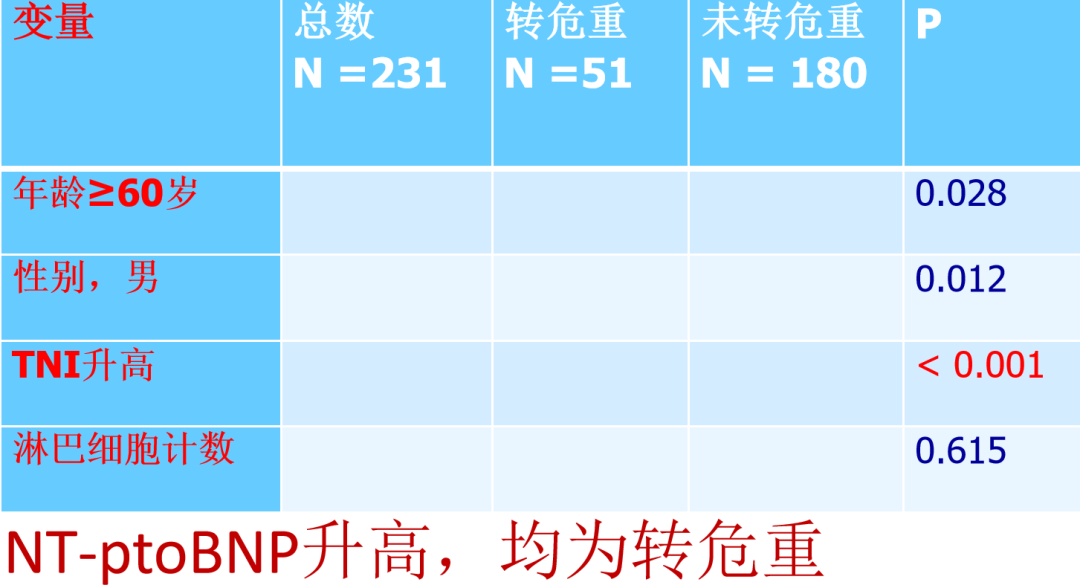
回到我们今天主要讨论的一个话题,就是重症病人转危重症的预警指标,或者我也赞成这种说法,病人有可能会加重或者病危的情况下,用哪些变量进行评估?我们联合了几个院区进行观察,目前还在研究中,没有把具体的数据罗列出来,但是从我们观察的例数来讲,也大概总结完结论了,我觉得还是比较明确的。NT-ptoBNP升高,病人均为转危重,这几乎是所有病例都发生了这样的情况;大部分病人的肌钙蛋白升高会转为危重症;经过追踪观察没有发现淋巴细胞的水平与重症转危重症存在直接关系;相反,男性从重症转危重症转的几率比较大;还有,年龄≥60岁比<60岁的更容易转危重症。
我认为这五个指标是现阶段对我们而言最具有参考意义的,所以一旦在临床中NT-ptoBNP哪怕升高一点,都要高度重视,特别要重视容量、肌钙蛋白等变化,一旦肌钙蛋白有轻微的增高,我们要联合乳酸去观察,是否为灌注的原因、是否因为左室或右室的相应原因进行一些评估。这是我们现阶段进行的一项主要工作。
四、重症新型冠状病毒肺炎ARDS和高碳酸血症等的影响探讨
几乎所有上了有创通气但是没有上ECMO死亡的病人,无一例外的顺应性非常差,只有11、12;第二,都有高碳酸血症;第三,心跳骤停的发生率非常高;第四,酸中毒很难纠正。我们往往碰到这样的病人是非常棘手的。
这是我们最近治疗的一个病人,在做超声的时候,我们发现有创通气的情况下,这个病人的左室很窄、容量不足,但是右室扩张得很明显。
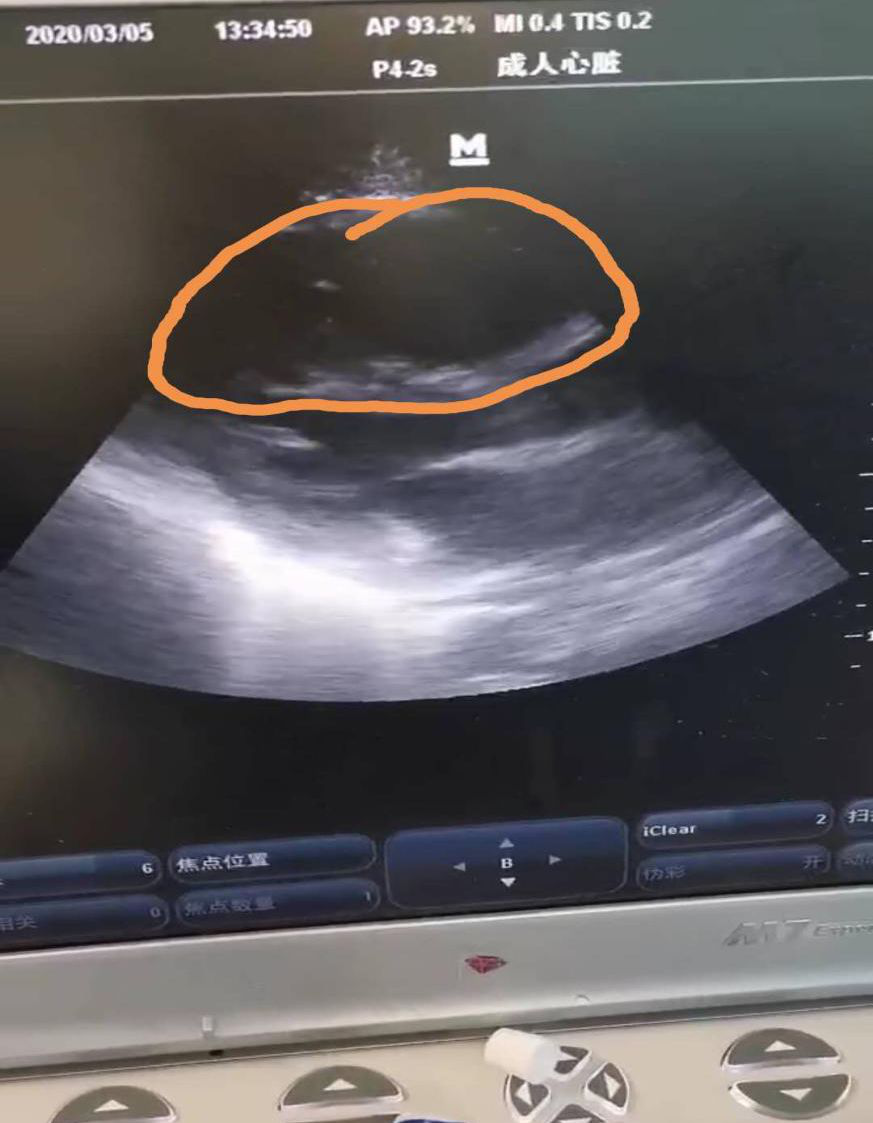
右室的问题无论是肺源性,还是心脏本身的原因,一旦出现右室功能障碍是比较棘手的,因为从外科的原因可能是进行右室的减压,从内科的原因其实还是远端的肺动脉压力高、肺血管阻力高或者出现肺血管重塑。
ARDS-急性肺心病
另外一个和血流动力学相关的就是ARDS急性肺心病的表现。我们来看一个病例,这个病例不是个案。参数设置的很极端,我们要保证一定的氧合,PEEP数值设置为14(较高),氧浓度为95%(较高),PC为26,在这种状况下很容易发生气压伤。
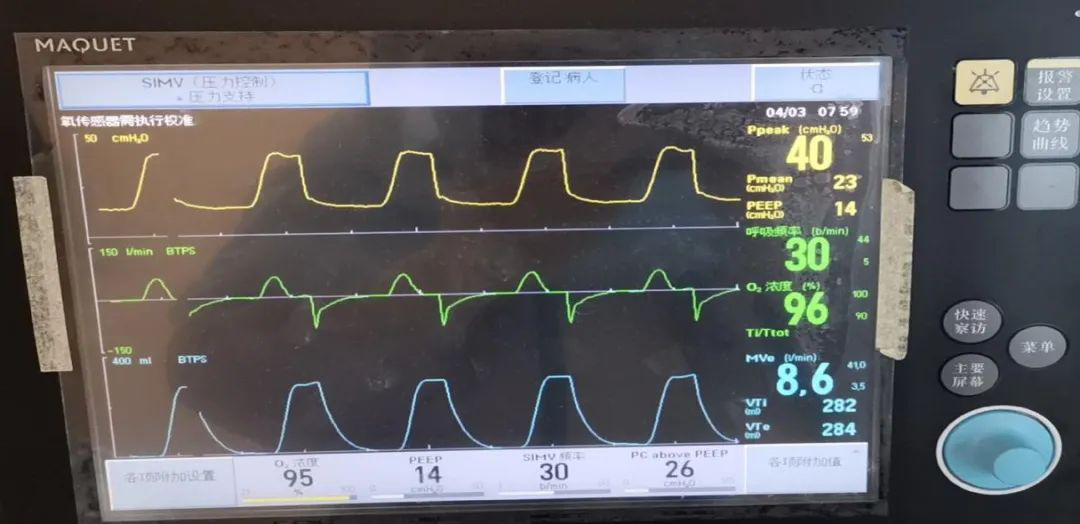
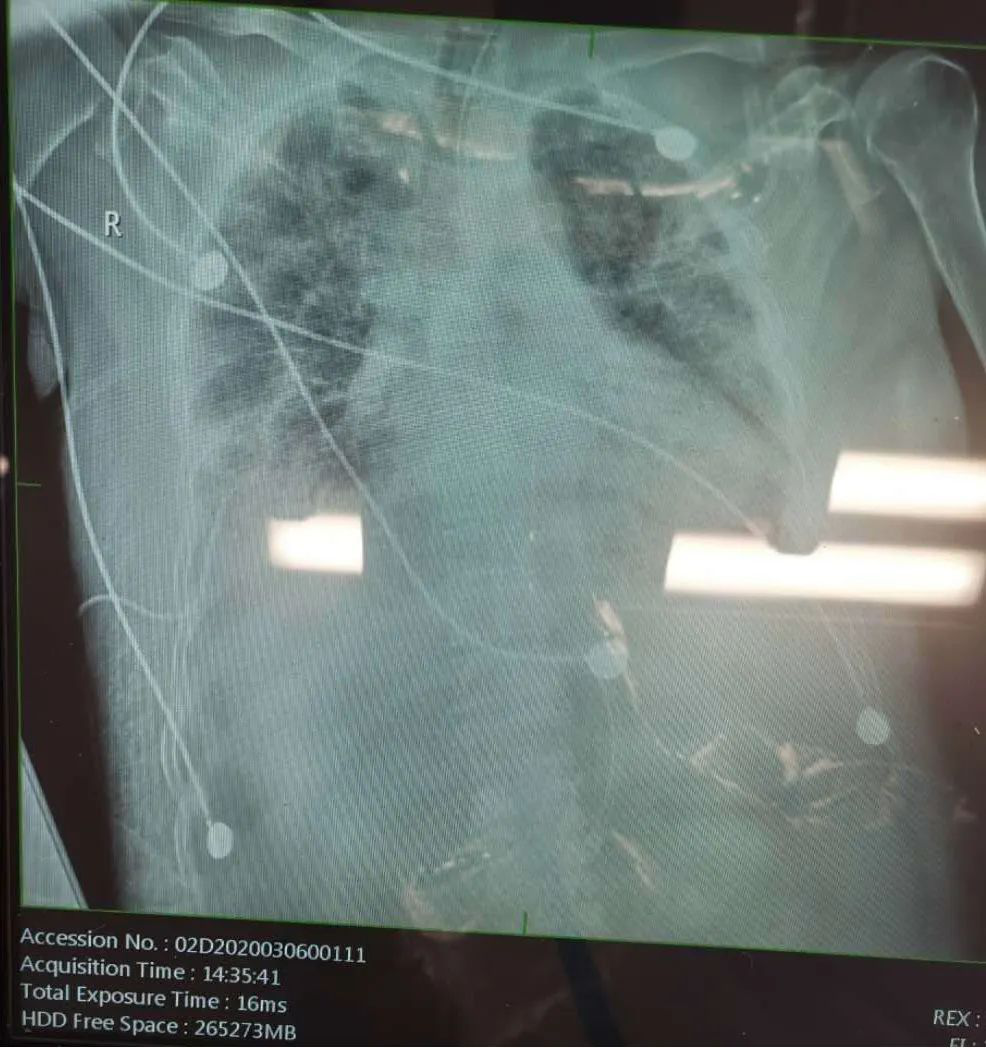
胸片
我们发现CO2也很高,这还不是最高,最高有可能大于150mmHg。在这个阶段很难纠正,我们怎么办?一方面根据血流动力学的结果,他的下腔宽、变异差、右室负荷重,我们还是相应的使用了一些去甲肾上腺素这些血管活性药物维持住,之后给他持续的进行CRRT治疗。我们最近逐步在改善,3月6日的CO2已经降到56mmHg,从胸片也能看到存在肺纤维化的表现,这个病人已经上呼吸机8天,一位78岁的病人。从治疗的反映来说,我认为还是努力地再去尝试一下,通过结合俯卧位或者其他方式去做一些努力。
ARDS-高碳酸血症
因此,高碳酸血症是比较常见的并发症。因为进行肺保护性通气的时候,总有一部分病人的高碳酸血症无法纠正。
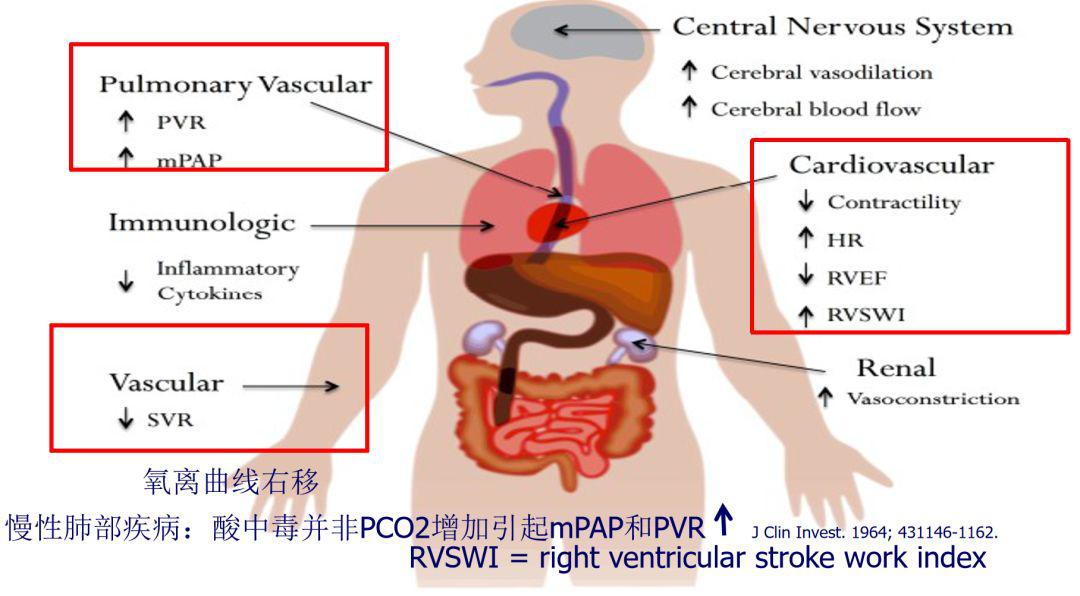
所以碰到以后,高碳酸血症除了引起酸中毒以外,还会加剧肺血管的阻力,引起肺动脉平均动脉压增高,还会导致心脏的收缩能力下降,心率会反射性增高。我们刚才看到超声的印象很深,这又使得EF会急剧下降,血管阻力指数也会急剧下降,这就会带来一系列问题。因为我所管理的病房以重症为主,而不是完全都是危重症的病房,所以对于新冠病人使用ECMO方面没有太多的经验,我还是主要以保护性通气和血流动力学的管理为主。
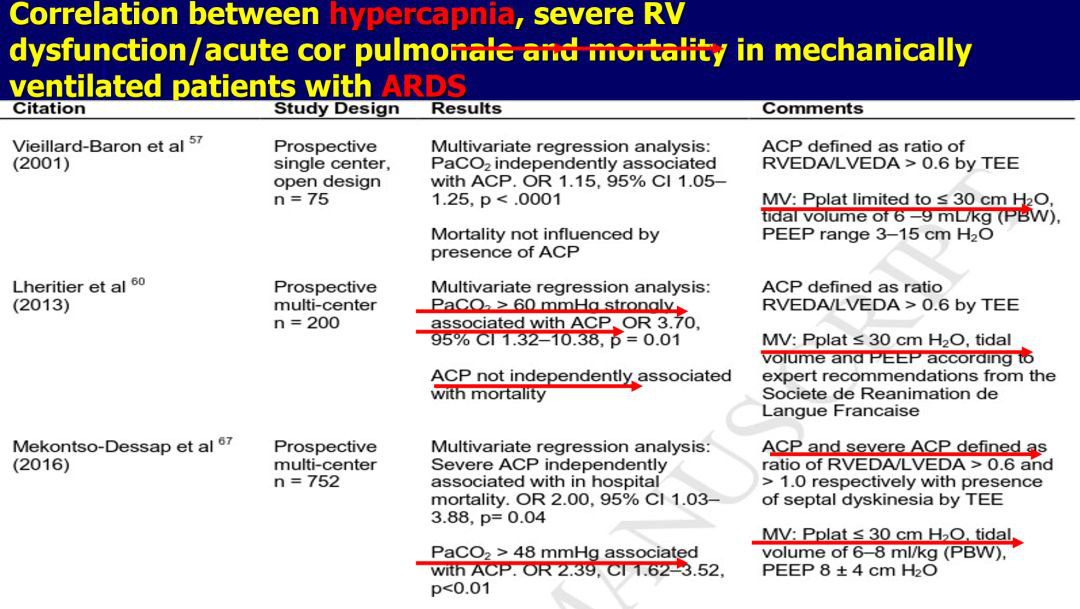
这样的病人往往在处理的对策上,从文献来看,建议监测平台压,如果能监测跨肺压和驱动压就更好了。目前我们可以监测驱动压,能监测到跨肺压最好,但还是没有做到这种程度。我们看到上述病人的参数,想把平台压30cmH2O基本上是做不到的。除非这个病人的病情特别轻,偶尔会有这种病人的病毒是否已经转移或者是以其他疾病为主的情况下,可能顺应性会好一些。大部分病人的平台压30cmH2O是无法做不到的。所以怎么办?如果管不住病人的气体,只能尽量管住他的水,因为气体的风流、气体的交换很难通过呼吸机调节的情况下,我们只能管理好灌注、液体的出和进,好在我们可以做容量反应性评估、CRRT。我认为把病人的水分管住,相应的有些方面可能比管理换气更好,因为还有一些血管活性药物,加上血液动力学监测,为什么这样说?
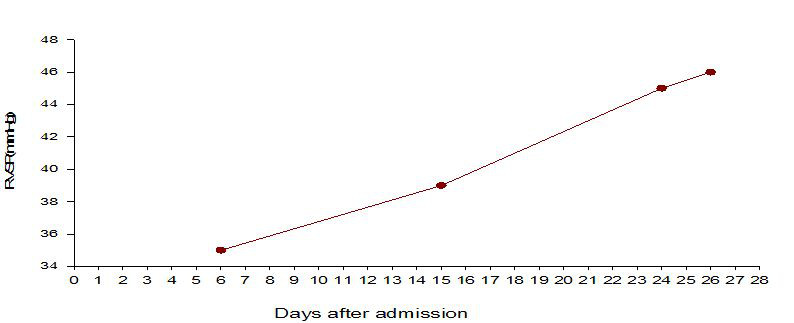
我们刚才也提到了,对于在一些重症病人而言,不说是病毒性肺炎,只要是ARDS病人,随着治疗疗程、病程的延长,无一例外都会发生肺动脉高压,肺动脉高压的原因有一部分是因为病人发生了缺氧性肺血管收缩,还有一部分是因为血栓,从一些尸检报告看到新冠病人的血栓的发生率确实比其他疾病要高很多。

其次,这些ARDS的重症病人都发生了肺动脉的增宽、增厚。在这种表现下,出现右心衰竭以后能纠正的几率很小。所以我们很担心出现这种情况。所以在血流动力学管理方面,我认为一定不能追求数值多漂亮,一定是追求我们的治疗能否有可逆性、可延续性。如果出现纤维化,我们现在也有人在使用一些激素,甚至用一些抗纤维化药物进行治疗。但如果出现肺血管的增厚,有什么药物可以治疗?所以从治疗的可逆性来讲,我觉得关注血液动力学的重塑是很重要的一方面。
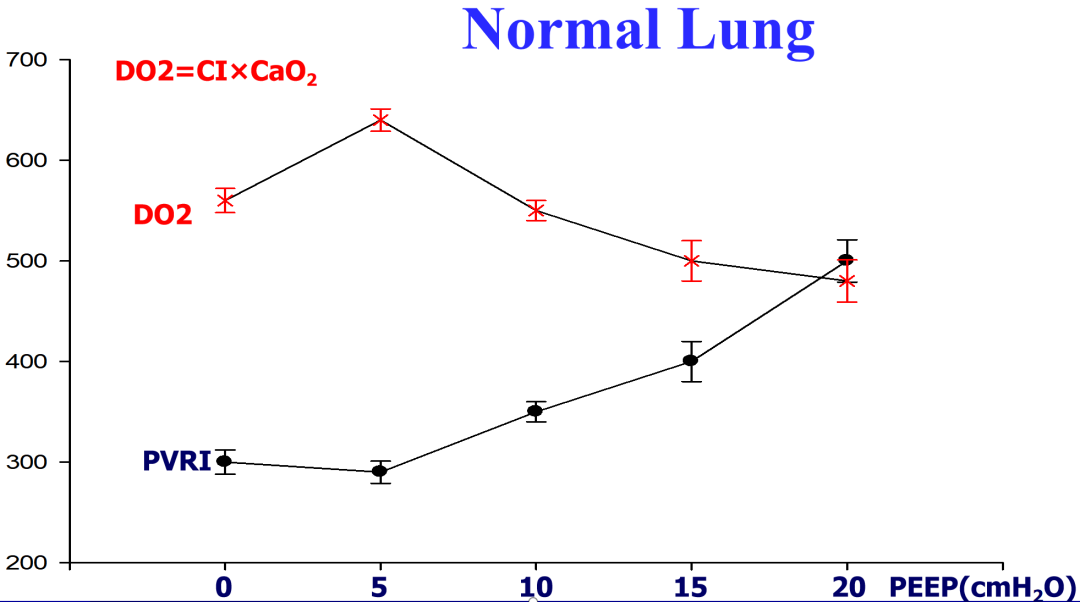
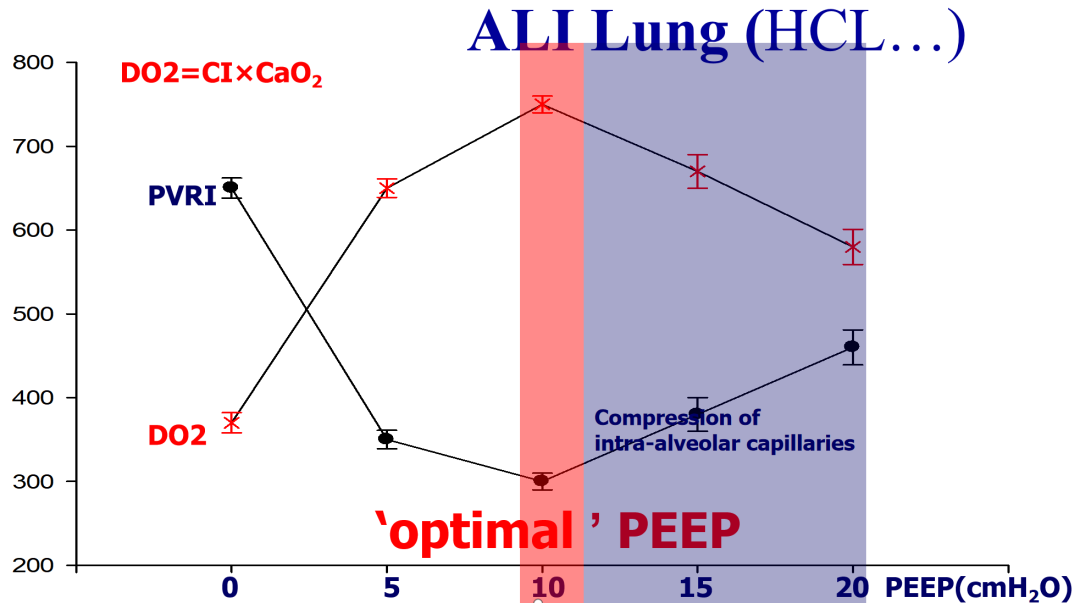
打个比方,在测定最佳PEEP的时候,上个世纪就有这样的研究,如果最佳PEEP没设置好,过高或低都会增加肺血管阻力指数(PVRI),氧供也会受影响,这样的话,病人的关注会越来越差,越来越不可逆。
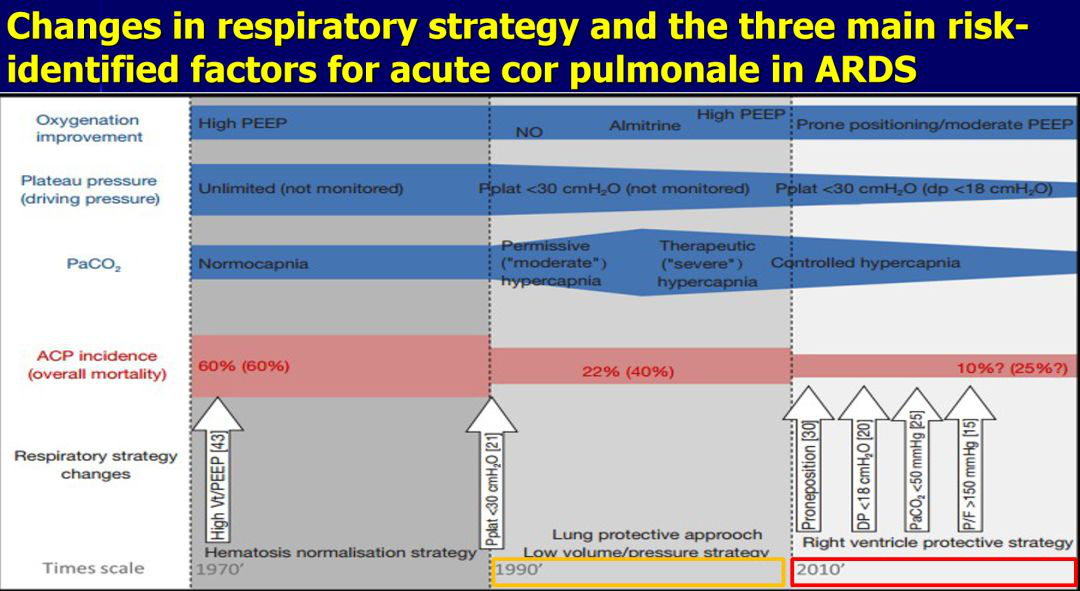
近两年ARDS患者呼吸策略的变化和三个主要的危险因素是一个大家比较熟悉的话题,要做俯卧位、驱动压下降、二氧化碳下降、P/F>150mmHg。从这样一个形势上,因为我们确实接触了很多不是早期的新冠病人,往往是发病10天左右或者10天以上的病人,对于这些病人一旦是重症或危重症的情况下,即使给他上ECMO,我觉得也不是最合适的时机。所以会导致我们现在在一些器官支持的手段上用得很强,大家也在努力,但是总体而言,刚才的胸片出现纤维化的改变,病理上也有纤维化的改变,血管上肯定也有血管的重塑、增厚。在这些改变下,如果仅用器官支持去治疗数据的话,病人很难恢复。
ARDS的液体策略
我刚才提到管理好气体,有时候不如管理好液体。对于ARDS的液体策略而言,毫无疑问,这些病人都要使用血管活性药物,因为血流动力学不稳定的60%的患者出现血流动力学衰竭。我认为只要是重症病人或者是机械通气的病人,这些新冠病人的血流动力学不稳定几乎是100%。
ARDS本身导致循环衰竭的机制
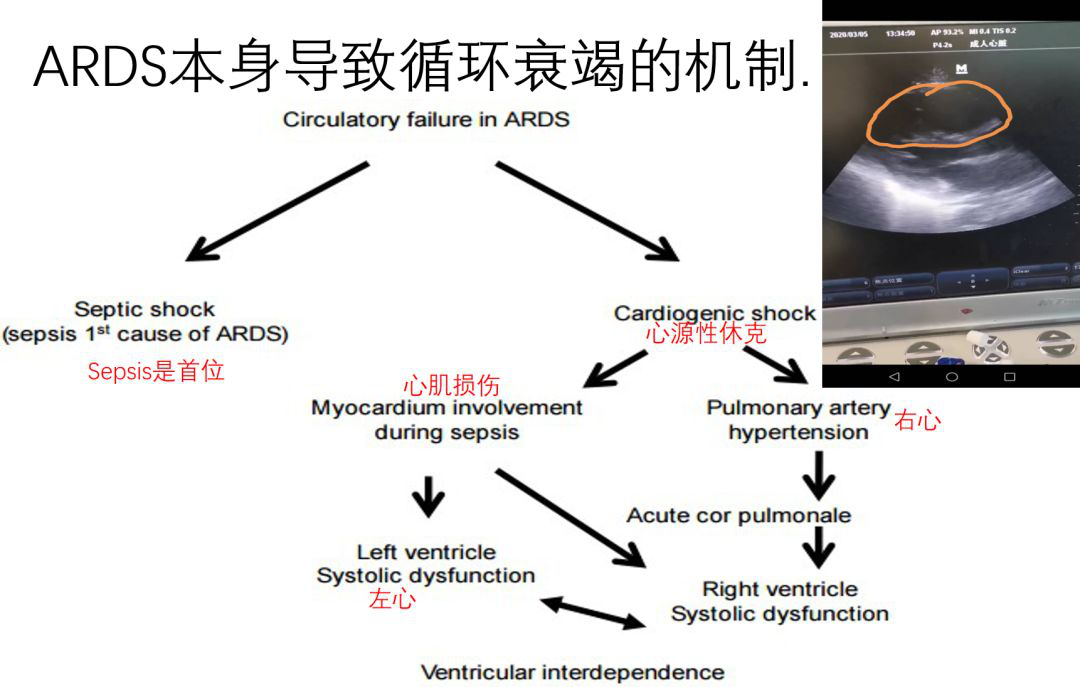
血流动力学不稳定一定不能完全归咎于病毒本身,抗病毒都很重要,抗病毒是病因,其他可能都是对症。但是从ARDS本身来讲,高条件、持续低氧、灌注差,我认为都会引起进一步的加重血流动力学障碍。但是我觉得脓毒症是不可绕过的很关键的一个坎。在新冠病毒的救治中,脓毒症的纠正往往是不断的反复附加的,比如病毒先来了,细菌再来了,气道引流又不通畅,其他的胃肠道的灌注也不通常,往往会带来腹内压的问题、相应的基础病、慢性感染的问题、糖尿病控制的问题,都会交错在一起。所以我个人认为要重视病毒性脓毒症,也更要重视病理生理。病理生理是反复发作的,多种病原的脓毒症交错的,交错的结果就是心源性休克。
心源性休克的一方面原因是心肌损伤,在病毒的参与下,心肌损伤会进一步加重,心肌损伤最突出的一点我个人认为还是右心为主,因为一旦发生了急性肺心病,右心的不肯定性更大,左心相对从我们观察的病例来讲,尽管右心很大,但是左心舒张末期容积很低,它的循环还是能够在低剂量的血管活性药物下维持住,这也是我们看到的左心的代偿能力在这个阶段是远远强于右心的。因为右心是一个低压的、高浓的,相对右心室壁比较薄,代偿性比较差的心室病,也有研究标明左心和右心的心室的功能,甚至细胞机制也存在不同。在这种情况下,因为它外面的应变应力都是不一样的,所以右心的影响非常重要。
Co-existent伴随因素
一旦合并左心功能不全,我觉得现阶段我们能做的还是这三个方法,容量反应性、血管活性药物、CRRT治疗。很多情况下,可能CRRT治疗在武汉还不能完全持续进行,有时候存在一些条件的限制。
脓毒症合并分布性休克,我们除了关注平均动脉压以外,还要把血管麻痹扩展和心肌抑制程度考虑在内。
ARDS- RV failure?
右心需要足够的前负荷,一旦前负荷充足的时候,我们发现肺水肿或者肺水就会增加,因为右心本身的EF偏低,再加上肺循环的阻力增加,所以加上前负荷,右心的灌注变差了,之后会带来进一步的右心障碍。但是如果前负荷过于充足了,肺水就会过多,ARDS就会更加严重,这确实是一个比较矛盾的地方。
俯卧位对血流动力学的影响
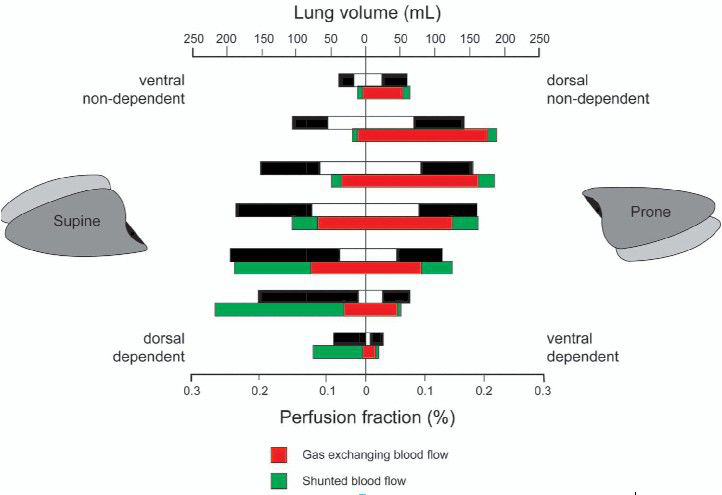
所以一直就有这样的机制,强调俯卧位的重要性。俯卧位确实在重症病人中是一个比较实用的方法,尽管做俯卧位的翻身的护理部特别不容易,但还是克服,通常要几倍的力量去做。还有一些相应的问题,比如老年人的俯卧位,因为老年人的腹部脂肪比较多,老年人可能相应的皮肤不好、基础病也比较多,在俯卧位的同时,我觉得新冠病人俯卧位的效果略于我们常规做俯卧位病人的效果,特别是在血流动力学的波动,在腹内压影响膈肌的功能,特别是在要兼顾俯卧位、肌力、营养、肌松、镇静这些调整方面,确实是一个全新的挑战。
PP—只有在前负荷充足的前提下,提高CO
一定要关注前负荷,如果前负荷不足,做俯卧位可能会带来一些变化。
血液动力学管理的关键步骤
血液动力学的管理还是参照重症ARDS的血流动力学管理。
Step 1:组织灌注是否充足?
首先要关注组织灌注是否充足。刚刚也介绍了死亡病人,如果灌注不充足,必然带来的就是乳酸升高,乳酸的增高其实是一个全身灌注的表现,全身灌注中最重要的要关注冠脉是否灌注,若没灌注必然会引起心肌的缺血、缺氧。病毒本身不会引起爆发性心肌炎的表现,因为它的病程和临床临床表现都不太符合,但是持续的灌注不足会和后续的混合感染一起,甚至少部分病人就是病毒直接引起脓毒症心肌病的表现,就会引起心室壁的扩张和EF下降。
超声评估下腔静脉的大小和充盈动态、脉压变化观察、对干预进行中央静脉压监测这三点我觉得对于新冠病人比较实用。尿量和代酸是临床反应组织灌注的主要指标。
液体复苏与氧合不同步
液体复苏和氧合有时候不同步,为了保证灌注,又要扩容复苏,但是也要减轻肺水肿,所以有时这两个会存在矛盾。比如氧合下降是由于肺水肿增加,后负荷增加引起右心衰竭,限制液体有利于West zone 2通气和血流。
所以这个时候如何同步?第一,看容量反应性,如果容量没有反应性,补了也没有用,容量反应性可能还要兼顾超声和乳酸的指标,当然能够做ppv、svv是PICO我觉得会更加精确,因为这些病人大部分还是在使用肌松。第二,看综合灌注、氧合、血流动力学指标等,除了看乳酸以外,还要兼顾肌钙蛋白等指标,比如心脏的灌注,从意识的判断,脑灌注,组织的灌注,比如从AKI的评估也需要去灌注。血流动力学的关注确实是要持续不断地变化。
ARDS右心衰竭
ARDS出现右心衰可能是补液过多恶化CO、BP和右心功能,要稍微控制一点。另外,血管活性药物建议优选去甲肾上腺素。
Step 2:评估急性肺源性心脏病
血流动力学的优先重点是充分支撑右心室。现阶段我建议使用超声对于新冠病人比较合适。第一,通过超声可以看到右心室负荷是否充足,若右心室负荷充足,补液无益,甚至加重。第二,去甲肾上腺素改善右心功能、维持MAP,我们在去甲肾上腺素的用量上还需要加强,有些病人在去甲肾上腺素用量很大的时候,我们早期联合一点肾上腺素,还是取得了一定的效果。第三,其他方面比如左西孟旦-钙增敏剂,研究中也表明右心和肺循环更匹配。
其他辅助治疗:NO、PG、全身性血管扩张药、抗凝治疗。我认为抗病毒治疗除非有明确的禁忌症才去做一些调整。

和大家分享这些汇总的内容,就是我们关注的是血流动力学,在测量出入量、观察容量反应性、观察灌注的同时,一定要关注右室和左室的变化,因为一旦不可逆是非常困难的。在这个阶段要关注几点,关注会引起肺心病的风险;要充分评估有无肺栓塞的表现;相对保守的缓慢的策略比较现实;在下腔宽度很窄的时候,早期纠正休克,病人的灌注就不会那么差。进展成危重症,其实BMP也是一个灌注的指标,在我们看到的转成危重症的病人基本上BMP会升高。所以早期的灌注,不好说一定是隐匿性修复这个概念,但是确实这些病人在早期需要强化补液、灌注的。
ARDS中ECMO相关血流动力学
这方面大家可能相对做的不是很多,可以简单了解一下。
vvECMO有助于缓解顽固性低氧血症;vvECMO降低肺动脉压力,减轻右心室负荷;vaECMO有助于缓解顽固性低氧血症;vaECMO有助于合并心源性休克患者血流动力学稳定;ECCO 2 R有助于合并高碳酸血症、酸中毒和MV-VILI,血流和气流较低。
复习现有认识和指导
第七版指南

综上所述,也结合现在的第七版指南,确实指南中把循环支持作为一个重点的关注。比如在充分液体复苏的基础上,改善微循环,使用血管活性药物,使用超、有创血压或PiCCO等监测,我特别理解这句话,如果病人可以用心率的变化、皮肤的变化、尿量的变化来评估,我觉得这些病人在早期避免灌注不良就会做得很好。
血流动力学监测
《重症新型冠状病毒肺炎管理专家推荐意见》也很实用,新冠肺炎患者可出现血流动力学不稳定和(或)休克,应仔细鉴别原因。重症型新冠肺炎患者的病程早期以呼吸功能衰竭为主,休克及循环衰竭并不多见。病程后期出现休克和低血压,原因是多方面的,需要仔细鉴别。
新冠肺炎患者休克的常见原因及机制如下:
①心源性休克,②低血容量休克,③感染性休克,④梗阻性休克,⑤其他。第五方面一般是与药物有关,特别是与一些麻醉药物有关。
①心源性休克
对于既往有冠状动脉粥样硬化性心脏病及其他心脏疾病的患者,严重低氧血症,将导致原有心脏疾病加重,可引发心源性休克。很多新冠肺炎患者血清(超敏)肌钙蛋白水平明显增高,甚至超过正常值上限的百倍。推测(超敏)肌钙蛋白升高不仅是心肌缺氧性损害的结果,更可能是病毒对心肌造成的直接损伤。尽管多数患者在(超敏)肌钙蛋白水平升高时并未合并室性心律失常或心源性休克等病毒性心肌炎的常见表现,且心脏超声也缺乏特异性表现,但随着疾病不断进展,仍有部分患者出现心脏功能抑制甚至心源性休克,临床预后极差。
从我个人的理解,我觉得肯定是与灌注有关,甚至大部分病人与乳酸的值有关。如果把心脏超声做得更细,我觉得会更频繁,更有连续性,可能会有意想不到的效果。真正出现心源性休克,就像我讲的爆发性心肌炎,我觉得从我看到的或者同行的病例来讲是少之又少。真正的在前期做好感染、引流,避免脓毒症心肌病更加归于现实。
②低血容量休克
由于患者连续高热,进食进水不足,可能导致前负荷不足。如不能及时干预纠正,将有可能进展为低容量休克。一些进行血液净化和接受利尿剂的患者,由于容量监测不足或不及时,也会因过度脱水或利尿,导致低容量性休克。
我的概念是主诉不太客观,有好多病人主诉说不口渴,但确实评估下来是低血容量,至少是容量低,当然我不敢说是否有一些分布的原因在里面,因为我们也观察了一些老年女性会有一些尿路感染的表现。在特殊的阶段来讲,如果再有新冠病毒感染,我觉得从主诉来讲在这样的容量会很困难,特别是氧合差的时候,有些医生会刻意限制入量,甚至用利尿剂,最后更加重病人的病情,我们面对的确实都是有一定病程、年龄偏大、有基础病的病人。
③感染性休克
感染性休克并不多见,通常较晚出现。重症患者往往在病程的10~14 d左右开始恶化,此时继发的细菌感染将成为较大威胁。临床上可观察到患者体温、血象及炎症指标(如PCT、C反应蛋白(CRP)等)在一度平稳后再次升高,气道内脓性痰,肺部影像学改变加重,提示出现医院获得性肺炎/呼吸机相关性肺炎。部分患者由于实施ECMO、连续性肾替代治疗(CRRT),或中心静脉、股静脉插管,这些血管内植入物可能导致植入物相关性血流感染。
感染性休克不可避免,只要是危重病人,都会成为一个挑战。感染性休克一旦发生后,要动态评估容量反应性,特别是关注BMP,如果是肌钙蛋白升高的时候,只要BMP不持续的在几万以上,我觉得还是有机会的。但如果病人合并AKI或者有慢性肾病的基础,可能NT-BNP没有太多参考价值。但是从现在血流动力学或者感染来讲,我看到有些少部分死亡病人也是阳性的,所以病毒感染或者真菌感染还是一个主要问题。
④梗阻性休克
肺顺应性差,镇静程度不足的患者在实施高水平PEEP、挽救治疗中的肺复张手法时,有可能导致气胸和纵隔气肿。特别是接受有创机械通气的患者,可由于张力性气胸导致梗阻性休克。也可见静脉血栓栓塞导致的梗阻性休克。
梗阻性休克是普遍存在有些肺栓塞的表现。但是我们发现这些病人虽然平均平台压很高,还没有看到出现纵隔气肿气胸的病人,但是是否会逐步出现,我觉得可能会有,确实这些病人做RM的效果都不是太好,做俯卧位可能有一定的作用。
监测和治疗
现阶段是以简单、实用、连续的方法为主。还要摸索血管活性药物和容量复苏的联合。从现阶段,反复的超声评估、反复的BMP监测,特别是要兼顾乳酸和肌钙蛋白,特别是把我们没有的监测手段与病人的实际的变化进行思考。在早期阶段,我们把容量的补充、血管张力的监测以及心脏相应的保护尽量做好,对于心脏的保护来说,比如尽量让病人的冠脉的灌注、早期的容量,甚至在氧疗的目标上,是否还有一些更好的方式。因为还在武汉,而且相信很多地方还是值得商榷的。
这次和大家分享,我想会有利于大家更多的去关注重症新冠肺炎的救治。从救治本身来讲,我觉得现在越来越好,很多病人至少他的住院时间能够越来越长,像前期那样的病死率,我觉得在我们武汉的院区,都是有大幅度的改观。当然也非常感谢几位老师的帮助和支持。我希望大家也能够积极地参与这个平台,把大家的想法、建议都提出来,我觉得这样是对我们最大的支持,因为确实有时候只缘身在此山中,看到的不一定是正确的,希望各位老师批评指正,谢谢。
答疑与讨论
王一民:谢谢郭教授给我们带来了专业性强、实用性也非常强的讲座。我汇总了网友的问题,还有我自己的一点思考,想和您沟通一下。这次对于重症病人的管理,现在很多文献或者已经发表的文章中,大家关注影响预后的指标还是比较少的。我也在曹彬教授课题组关注了这件事情,我们确实也关注了与您提到的类似的表现,包括您说的超敏肌钙蛋白、乳酸、D-二聚体、血清铁蛋白、淋巴细胞计数、白介素6这样的炎症指标,可能都会影响到病人的预后。我们特别希望,我们先关注到这样病人的现象,哪些指标容易影响预后,然后我们再设想一些能够干预的措施,去改变这样的病人的预后。您觉得这些指标中,哪个指标是我们能够改变起来更加容易一点的?比如我看到BMP,看到超敏C反应蛋白增高,我可能想象他的心脏有问题,但液体管理特别复杂,甚至血管活性药物。如果看到白介素6升高,是不是可以像瞿介明教授所说,把妥珠单抗这样的单克隆抗体用上,就可以改变这样的结局。您能从这方面给我们一些建议吗?
郭强:谢谢王老师的提问。从我的体会来说,第一,我觉得BMP确实是一个可以干预而且可以改变的指标。第二,有关白介素6,部分病人比较敏感,部分病人与器官衰竭的程度是有相关性的,我们要做进一步的总结。我认为一个指标能用来作为一个接近性治疗的指标,一定是治疗以后有所改变。如果治疗以后改变的时间短或者没有改变,我觉得这样的指标可能只能用于后期的分析。现阶段的治疗来讲,BMP甚至肌钙蛋白也可以做一些参考。我们还在不断地挖掘一些预警指标,其他教授在具体地进行,我们也在参与。我希望真正能够做一些实用性的指标,因为现阶段有些指标的干扰因素多,比如基础病、老年、各治疗的相关因素的影响、一些药物的干扰。所以从我的想法来讲,我觉得我们还是先关注现有的这些指标。
王一民:很多人都关注到了D-二聚体的异常,这样的升高大家就会想到有血栓的问题,就会使用抗凝药物。但是发现即使用上抗凝药物,很多病人并没有扭转最终出现微血栓或者出现DIC。这是不是告诉我们,我们评价的还不够仔细,或者我们需要盯住凝血的某一个指标,还要对凝血的其他指标更加关注,为什么效果不好?还有第二指标或者次要指标的情况?
郭强:您讲得很对。D-二聚体是一个血栓的指标,也是一个纤溶亢进症的指标,所以D-二聚体值的高低,对病人有意义或是无意义,我觉得都是需要根据客观情况进行评估。从这个阶段我觉得要单纯看一个指标还是很难去做的。因为病人的人群面比较广,尽管都是同样的新冠肺炎,但是合并的疾病、病程、个体的差异都存在,一旦病人的数字增大以后,在做治疗的时候确实存在这样的问题。
王一民:刚才您提到,这次的重症新冠肺炎的病人,如果我的临床经验比较有限,我又想拎出来一个主要的脉络去治疗这样的病人,先按照脓毒症去处理这样的病人似乎是一个比较好的选择,是这样吗?
郭强:对。从整个思路来讲,我觉得先按照脓毒症诊断的规范来做。因为一旦大家做得有规范了,可能相对就知道哪方面是对或错,如果大家都拎不出一个主线,我觉得治疗是比较无序的。
王一民:因为我和您的感受非常一致,我关注到了一些病人,包括收集到的资料来看,在这次的新冠肺炎当中,SOFA评分是一个特别好、特别敏感的指标。我们发现很早期的SOFA评分就给我们一些线索,提示这个病人出现早期脓毒症。您刚才也给我们介绍了非常多的病理生理学的过程,大家有可能拎不出来主线的话,我个人也认为脓毒症可能是我们现阶段比较好遵循的一个规范。
我们回到今天的主要讲述的内容,关注心肌损伤,包括心脏的反应。您刚才提到有关人感染H7N9禽流感住院患者心脏损伤与死亡的关系的那篇文章,关注到了几个指标,包括心肌酶、心脏超声、心电图。对于心脏超声、心电图这方面,您能够给我们提供一些规律吗?
郭强:基本与心肌的肌钙蛋白是一致的。如果肌钙蛋白高的病人,日常的心电图还是偏多,我们评估下来,但是因为我们条件的限制,彩超没有评估的那么细,但是我们从趋势上来讲还是符合的。
王一民:我们往往在重症病人管理的时候,大家会觉得液体管理比较难管理。说起来好像挺容易,就是输液和利尿的事情,但实际上真正到某个病人是特别复杂的过程,包括是否要加血管活性药物,加哪种血管活性药物,选择晶体液的补充,还是胶体液的蛋白的补充,利尿剂的使用,CRRT的时机。我知道肯定是很难让您去归纳出来到底哪种情况应该怎样选择,但是我还是希望您能帮助我们拎出来一个主线。就像脓毒症一样,我可能刚开始就要标准到位的液体复苏。如果我们看到病人的液体管理出现问题的时候,我也希望能拎出来主线,比如先做个超声,看到某些情况,再进行下面的处理;还是先用一些药物去尝试,给病人利尿、脱水,这些方面能不能帮助我们去拎出来一条主线?
郭强:好的,谢谢,这个问题非常好。从我的体会来讲,我觉得碰到这种病人,原来我们都是从判断休克种临床表现,比如心率增快、手足湿冷、尿量减少或者意识模糊的这种表现来判断。但是对于新冠病人而言,特别是病程偏长的,可能是10天以上的这些病人,第一,要评估的不仅仅是这些症状,要评估他的超声、乳酸、BMP、心肌的治疗去评估。第二,我觉得要做容量反应性的评估,如果经过补液、经过改善病人的习惯以后,他的容量反应性很好,我觉得还是可以继续,因为这些病人有时候表述的不是很确切,我不清楚是不是可能与中枢有关,所以完全按照他的主诉来做,我觉得还是有些偏颇。第三,如果有明确的脓毒症,特别是有感染相关的表现时,再使用血管活性药物,我觉得这个是需要去用的。这三步是目前我对于新冠病人的体会。
王一民:我希望各位网友能够体会的一件事情就是之所以我们虽然很难,但是还要给大家拎出来这样的规范是因为我相信很多的医院并没有这么多的血流动力学监测的指标,可能我们能拿到手里的第一就是病人的临床特征,再有能够验血的一些BMP、乳酸、cTnI、cTnT这些指标,还有在床旁能够采集到的超声、心电图这样一些情况,然后再配合着我们可及的血管反应性的实验,应该对病人来说是有比较大的迅速反应的帮助。我们相信像郭教授这样的团队,还有很多重症的团队,会为我们最终去梳理出来哪些预警指标更合适、更恰当、更敏感。但是在现阶段救治病人的时候,还是有我们的一套流程去走的。我再问最后一个问题,除了我们今天看到的病毒、重症病毒性肺炎、脓毒症引起的心脏的损伤外,虽然今天没有涉及到其他器官,但是我也想听听您关注到的其他器官的损伤的情况。比如AKI、严重的肝功能损害、凝血的问题,这些情况您能介绍一下吗?
郭强:我排序说明一下。我观察到的重症和危重症病人,他们其他器官的损害,除了心脏之外,首先是AKI,第二点就是胃肠道,胃肠道受累比较明显;第三点是凝血,我觉得凝血影响比较明显,一般都有凝血障碍出来,然后才会到其他的器官,比如神经系统,因为神经系统也有相关的病理特点。从其他脏器的损伤来讲,我觉得都会多多少少累及。但是,因为从病毒的阳性的程度来讲,可能也会多少累及。我个人觉得比如三个屏障,血脑屏障、胎盘屏障、血睾丸屏障,相对可能还是对病毒有一定作用,因为我也结合一些研究和我自身的体会,我觉得相对神经系统影响会缓慢一点。
参考文献
[1]Am J RespirCrit Care Med 2015;191:1147-57.
[2]JAMA. 2014 Apr 2;311(13):1308-16.
[3]Front Immunol. 2018 Sep 27;9:2147.
[4]Clin Microbiol Infect. (2013) 19:772–7.
[5]Respirology (2016) 21:648–55.
[6]Pediatrics (2014) 133:e538–45.
[7]J Clin Virol. (2016) 80:45–56.
[8]Influenza Other Respir Viruses (2017) 11:372–93.
[9]Clin Microbiol Rev. (2007) 20:49–78.
[10]N Engl J Med. (1999) 340:448–54.
[11]J Clin Microbiol. (2008) 46:1682–5.
[12]ClinMicrobiol Rev. (2017) 30:277–319.
[13]Front Pediatr. 2018 Sep 18;6:252.
[14]Crit Care Med. 2020 Jan 20. doi: 10.1097/CCM.0000000000004207.
[15]J. Crit. Care 2018; 47: 61–4.
[16]J. Intensive Care 2015; 3: 48.
[17]Acute Med Surg. 2019 Feb 10;6(2):192-196.
[18]Intensive Care Med https://doi.org/10.1007/s00134-020-05991-x
[19]J Clin Invest. 1964; 431146-1162.
[20]Guo Q Critical Care2014,18:666-667
[21]Intensive Care Med.2015 doi:10.1007/s00134‑015‑4141‑2
[22]N Engl J Med 371:1695–1703
[23]Anesthesiology ,1984,60:132–135
[24]Crit Care Med ,2006,34:2287–2293
[25]Am J Respir Crit Care Med 2014 190:488–496
[26]《重症新型冠状病毒肺炎管理专家推荐意见》
专家介绍

郭强
苏州大学附属第一医院重症医学科副主任,医学博士,副教授,主任医师;中国医师协会呼吸分会青委会副主任委员;中华医学会呼吸分会青年委员;中华医学会呼吸分会危重症学组委员。
感谢赛诺菲巴斯德对本次直播的大力支持!
感谢江西青峰药业对本季直播的大力支持!


