新冠对人体的影响可能超乎想象。
3月8日,顶级期刊《自然》以“加速预览”的形式,发布了牛津大学Gwenaëlle Douaud团队的重要研究成果[1]。
他们在分析了数百名新冠患者的大脑扫描数据后发现,在感染新冠病毒近5个月后,感染者的眶额皮质和海马旁回的灰质厚度相比未感染者显著下降,整体脑容量下降,嗅皮质相关脑区组织损伤,即使是轻症感染者也会如此。
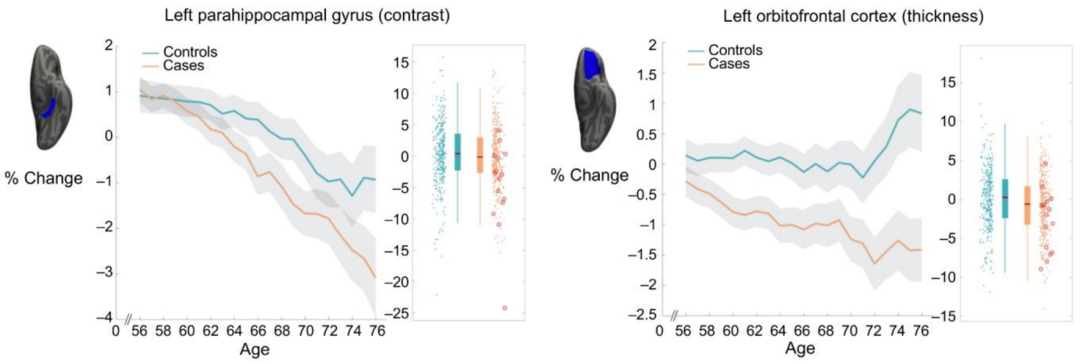
感染新冠病毒之后海马旁回和眶额皮质的变化[1]
当然需要注意的是,该研究纳入的感染者主要受到阿尔法、贝塔变异株影响,该结论是否适用于奥密克戎感染者尚无定论。此外,对于此类损伤是否可以随时间延长逐步恢复,还需要长时间随访。
同一天,陆军军医大学大坪医院王延江教授团队在著名期刊JAMA Neurology发表的一项重要的研究成果[2],从临床角度证实了新冠病毒对大脑的负面影响。
王延江教授团队分析了2020年2-4月期间3000多例60岁及以上的新冠感染者和400多个家属的临床数据,评估患者康复后一年的认知变化。结果他们发现,康复12个月之后,感染者认知障碍的总体发生率高达12.45%,其中重症患者的痴呆发生率为15%,轻度认知障碍(MCI)发生率高达26.54%;相较而言,非重症患者痴呆发生率不足1%,MCI发生率在5%左右。
更让人吃惊的是,新冠对神经系统的长期影响只是新冠后遗症的冰山一角,有研究甚至统计了新冠对人体的50多个长期影响,发现超过80%的新冠感染者会受到至少一种后遗症的影响[3]。还有研究发现,新冠后遗症的风险比季节性流感的要高得多[4]。
据世界卫生组织(WHO)统计的数据,全球确诊感染人数已经超过4.5亿[5],而且这个数字还在不断攀升。结合前面的两个数据不难发现,新冠后遗症对全球公共卫生系统的影响可能是非常深远的。
因此,我们非常有必要全面了解新冠病毒对人体的长期影响,以及人类的应对之策。
一、新冠后遗症普遍且持久
时至今日,新冠疫情已经肆虐了超过两年的时间。随着康复者人数的增多,新冠对人体的长期影响逐渐凸显。到如今,新冠后遗症已经成为人类不得不面对的一个大问题。
尽管如此,学界还没有新冠后遗症的统一疾病定义。大多数机构认为,新冠后遗症是始发症状出现4周或30天之后,在康复者身上出现的持续健康问题[6,7]。WHO也将“新冠后遗症”添加到国际疾病分类代码中,以描述症状持续至少两个月,并且不能用其他诊断来解释的健康问题[8]。
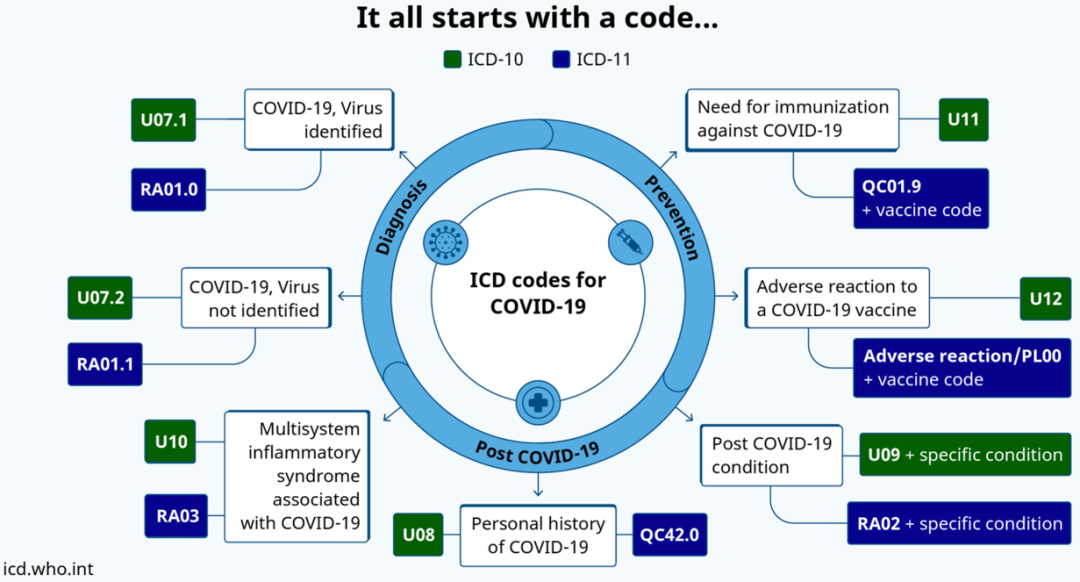
WHO更新的国际疾病分类代码[9]
早在去年8月份,由威尔康奈尔医学院休斯顿卫理公会研究所(HMRI)Sonia Villapol领衔的研究团队,就系统分析了新冠后遗症的研究论文[3]。他们发现,新冠后遗症至少有55种,80%的感染者至少存在一种后遗症。
其中最常见的5种分别是疲劳(58%),头痛(44%),注意力障碍(27%),脱发(25%),呼吸困难(24%)。其他症状还包括肺部疾病(咳嗽、胸部不适、肺弥散能力降低、睡眠呼吸暂停和肺纤维化)、心血管疾病(心律失常、心肌炎)和神经与精神系统疾病(痴呆、抑郁、焦虑、强迫症)等。

新冠后遗症及占比[3]
从上图不难看出,新冠病毒对人体的影响几乎波及所有组织或器官。不过,目前最受关注的还是新冠病毒对呼吸系统、心脏和神经与精神系统的长期影响。接下来,我们就逐一介绍。
肺是新冠病毒感染的主要器官,新冠病毒感染会在一定程度上损害肺组织和肺功能,因此呼吸系统的新冠后遗症非常常见。在不同的研究中,呼吸困难在60-100天的随访期内的发生率为42%-66%[10]。一项美国研究显示,在60天的随访中,分别有6.6%的患者因持续低氧血症需要补充氧气[10]。中日友好医院曹彬等发表的研究论文显示,住院患者出院1年之后呼吸困难发生率仍高达30%[11]。
一项肺功能研究发现,在康复出院30天后的患者群体中,半数患者表现出肺弥散功能下降、呼吸肌力量降低和肺部影像学异常[12]。从影像学结果看,有研究发现94%的出院患者肺部CT影像异常,主要是磨玻璃密度影(GGO)[12];而且肺部CT影像异常不仅限于住院的重症病例,在无症状患者中也有这些现象[12]。还有团队研究了出院后3个月纤维化的情况,他们发现约25%的轻度至中度病例存在纤维化,在重症病例居多的队列中,约65%的康复者存在肺纤维化[10]。曹彬等随访住院患者一年的数据显示,55.1%的患者存在至少一个异常CT表型[11]。
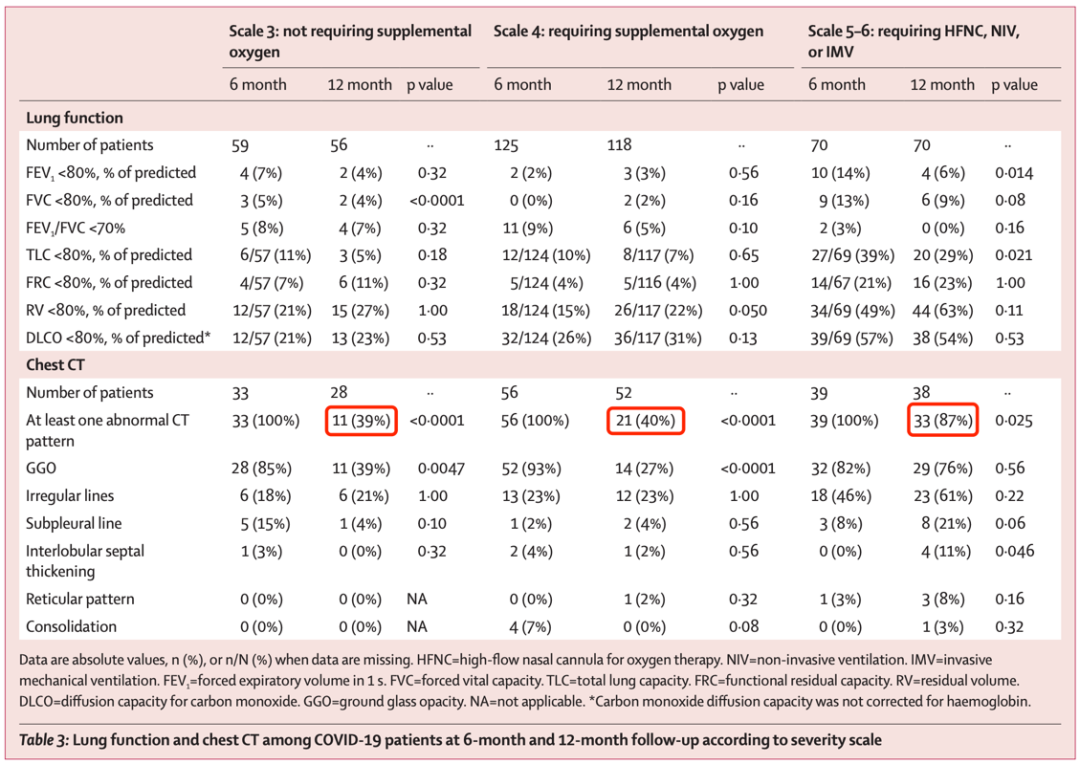
患病一年后,55.1%的患者存在至少一个异常CT表型[11]
通过以上数据,我们可以发现,新冠肺炎对呼吸系统的影响非常深远,而且重症患者受到的长期影响更大。
尽管不是新冠病毒的主要感染器官,心血管的处境和肺也是一样的。
今年2月初,由华盛顿大学医学院Ziyad Al-Aly领衔的研究团队,在《自然·医学》杂志上发表了新冠对心血管系统长期影响研究论文[13]。研究结果让一些科学家大吃一惊。
Al-Aly团队从美国退伍军人事务部采集了153760名新冠患者的临床数据,以及一个多达5637647参与者的同期对照组和一个有5859411参与者组成的历史对照组,中位随访时间接近一年,评估包括脑血管疾病、心律失常、缺血性和非缺血性心脏病、心包炎、心肌炎、心力衰竭和血栓栓塞性疾病等20种心血管疾病的发生情况。
研究结果表明,在长达1年的随访时间里,新冠感染与任何心血管结局增加63%相关,与主要不良心血管事件(MACE,心肌梗死、卒中和全因死亡率的复合终点)增加55%相关。具体来看,新冠感染与脑血管疾病风险增加53%、心律失常风险增加69%、心脏或心包炎症性疾病的复合风险增加102%、缺血性心脏病风险增加66%、血栓栓塞性疾病风险增加139%和心衰风险增加72%相关。
Al-Aly团队还发现,在1年的随访期内,无需住院的新冠患者心血管疾病风险也增加,而且心血管疾病结局随患者新冠严重程度呈正相关。因此,Al-Aly和他的同事呼吁:在给新冠康复者提供护理时,心血管疾病是需要关注的对象。

新冠严重程度与随访1年后的心血管疾病风险[13]
最后,我们再来看下新冠疫情期间颇受关注的精神健康问题。
Ziyad Al-Aly领衔的研究团队于今年2月中旬,又在《英国医学杂志》(BMJ)上发表了新冠对精神健康长期影响的研究论文[14]。
和前一个研究一样,这个研究使用的也是美国退伍军人事务部的数据,其中感染新冠超过30天的参与者153848人,同期非感染对照组5637840人,历史对照组5859251人,随访时间1年。
从研究结果来看,与对照组相比,新冠组精神健康事件诊断或处方的风险增加60%。具体来看,新冠组发生焦虑症的风险增加35%、抑郁症的风险增加39%、压力和适应障碍风险增加38%,使用抗抑郁药的风险增加55%,使用苯二氮卓类药物的风险增加65%。此外,新冠组发生认知障碍的风险增加80%,睡眠障碍的风险增加41%。
与心血管疾病风险一样,非住院新冠患者精神健康事件诊断或处方的风险也增加,而且精神健康事件诊断或处方的风险与患者的疾病严重程度呈正相关。此外,与季节性流感相比,新冠与住院和非住院患者的精神健康结局风险增加有关。
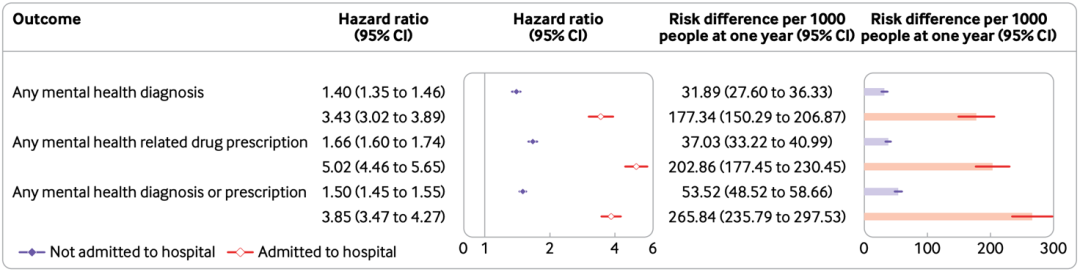
新冠严重程度与随访1年后的精神健康事件相关风险[14]
新冠对人体的影响是广泛而深远的,无论是需要住院的重症患者,还是无需住院的轻中症患者,他们患新冠后遗症的风险都非常大。因此弄清楚新冠后遗症背后的原因,以及避免新冠后遗症发生的手段,才能减轻新冠康复者的疾病负担。
那么新冠后遗症究竟因何而起呢?
二、新冠后遗症可能的原因
实际上,目前我们并没有确切的答案。
不过,科学家基于已有的基础研究和临床研究结果,对新冠后遗症的发生机制已经有了初步认知。
在正式介绍各种推测的机制之前,我们还需要先了解一下新冠病毒能影响几乎人体所有组织或器官的原因。简单来说,就是新冠病毒可以通过遍布人体的血管紧张素转换酶2(ACE2)进入多种组织或器官细胞。

新冠病毒能通过ACE2受体进入多种组织或器官的细胞[15]
有了上面那个大背景,我们就可以来看新冠后遗症可能的机制了。
第一个可能的机制是新冠病毒感染直接导致的细胞或组织损伤。
有研究发现,在呼吸系统内,新冠病毒在内皮细胞内的复制,会对肺和呼吸道造成严重损害[15];在心血管系统,新冠病毒直接感染心肌细胞和内皮细胞,会导致心肌细胞的凋亡和内皮细胞损伤[15,16]。在其他的组织和器官中,新冠病毒的感染,也会导致相关细胞的死亡,进而影响器官的功能,诱发新冠后遗症。
第二个是潜在的病毒库或非传染性新冠病毒片段引发慢性炎症[12]。
很多研究在感染者的多种器官中检测到了新冠病毒的存在,因此这些器官有可能成为新冠病毒的潜在“病毒库”。一些探索新冠病毒脱落期的研究,给病毒库的存在提供了间接的证据。例如,有些患者的病毒脱落时间竟然超过3个月。
除了病毒库之外,还有研究暗示新冠病毒的部分核酸序列可以整合到人的基因组中,而且整合到人体基因组中的新冠病毒片段能够正常转录[17]。或许正是由于病毒库或病毒片段的持续存在,引发的慢性炎症造成了新冠后遗症的发生。
第三个猜测是,慢性新冠肺炎相关免疫耗竭[12]。
众所周知,如果免疫细胞被抗原持续长时间刺激,就会出现功能障碍甚至耗竭。已经有研究发现,在重症新冠患者体内,细胞毒性T淋巴细胞(CTL)和自然杀伤细胞(NK)等抗病毒淋巴细胞的绝对数量明显减少,功能耗竭。还有研究发现,在新冠感染期间,淋巴和骨髓细胞上很多免疫抑制受体表达水平上调。这种免疫抑制和免疫细胞的耗竭,可能会促进新冠感染,进而导致新冠后遗症。
值得注意的是,T细胞上的T细胞受体(TCR)有可能与新冠病毒S蛋白的特定表位结合,模拟细菌性超抗原。如果新冠病毒持续存在,这些抗原可能会触发适应性免疫系统的过度激活,引发低水平慢性炎症,为新冠后遗症铺平了道路。
第四个潜在机制是病毒诱导的自身免疫[12]。
有研究表明,新冠病毒特异性抗体能够与哺乳动物宿主蛋白发生交叉反应。实际上,已经有研究团队在具有神经系统症状的新冠患者体内检测到抗神经元自身反应性抗体。在一项对新冠患者的研究中,研究人员发现52%的患者体内有抗磷脂抗体。在其他的临床研究中,也发现了针对其他人体蛋白抗体的存在。这些证据暗示,新冠病毒诱导的自身免疫可能对新冠后遗症的发生起到重要作用。
新冠病毒(图源:NIAID-RML)
第五个可能原因是免疫代谢异常和线粒体功能障碍[12]。
线粒体不仅是细胞的能量工厂,它还对人体的免疫稳态至关重要。因此,线粒体功能受损,必然会影响人体免疫。
早在新冠疫情爆发之初,就有科学家研究了新冠病毒编码的蛋白与人体蛋白之间的相互作用。根据这些研究,科学家推测新冠病毒的非结构蛋白(NSP)4和8,以及ORF9c可以与线粒体相互作用。也有研究发现了新冠病毒可以劫持宿主的线粒体。
从临床研究数据来看,新冠患者外周血单个核细胞(PBMC)表现出线粒体功能障碍、代谢改变和线粒体因子水平高等特征。还有研究发现不同亚群T细胞出现了线粒体功能障碍,以及死亡风险增加。
线粒体功能障碍一方面会导致免疫稳态失衡,另一方面也会导致受感染细胞代谢重编程。二者可能就是新冠后遗症的幕后推手。
最后一个可能的机制是肾素-血管紧张素系统(RAS)失衡[12]。
RAS在维持身体生理平衡方面有重要作用,它会影响多个器官系统的功能。有研究发现,新冠感染期间,RAS会失衡,而且这种失衡与新冠相关的多器官损伤相关。因此,科学家们推测,新冠感染期间的RAS失衡可能导致了肺、心脏、肾脏和小肠等的终末器官损伤,这有可能就成为新冠后遗症的诱因。

新冠后遗症的潜在机制[12]
总的来说,导致新冠后遗症的原因可能非常多,而且这些机制可能存在不同程度的重叠交织,最终一起导致了新冠后遗症的发生和发展。
不过,以上的六种可能机制是研究人员根据基础或临床研究的推测,至于新冠后遗症的真正发病机制,还需要研究人员开展更多的研究探索。
三、做好新冠后遗症的预防和管理
总结以上所有内容可以看出,新冠后遗症影响的组织或器官非常多、形式多样、机制复杂,而且它影响深远(能持续1年以上),发生率高(重症患者受影响更大)。随着新变异株的出现与流行,新冠感染人数还会不断攀升,新冠后遗症难免会成为一种新的全球性公共卫生问题,给人类社会带来巨大的疾病负担。当然,对于毒力减弱的奥密克戎变异株是否同样会引发上述新冠后遗症,尚需临床研究进一步证实。
因此,我们有必要基于已有的研 究成果,制定合理的预防和治疗策略,将新冠后遗症对人类的影响降到最低。
从近期的研究结果来看,预防新冠后遗症最重要策略是接种疫苗。只要不感染新冠病毒,就不会出现新冠后遗症。目前全球已经有多种疫苗获批上市,无论哪一种疫苗都能有效预防新冠,或者预防感染后进展成重症。这都能降低新冠后遗症的风险。近期还有研究发现,即使接种疫苗之后出现突破性感染,出现新冠后遗症的风险也比未接种疫苗的感染者低[4]。
高危人群可以做好暴露前预防,前不久FDA已经批准将更高剂量长效中和抗体组合Evusheld用于新冠的暴露前预防[18]。只要能大幅降低感染新冠的风险,就能降低新冠后遗症的风险。
对于已经感染的患者,如果进展成重症的风险比较高,可以接受小分子抗病毒药物(如Paxlovid等)或单克隆中和抗体(如安巴韦单抗/罗米司韦单抗等)治疗,降低进展到重症的风险[19-21]。这或许也可以降低新冠后遗症的风险,毕竟多项研究发现相比重症或入院治疗患者,轻症患者发生新冠后遗症的风险相对较低[13,14]。
此外,部分研究显示早期应用抗病毒类药物可加快病毒在体内清除[21,22]。不过,感染早期治疗究竟能不能降低新冠后遗症的风险目前尚不明确,已经获批的治疗药物的三期临床研究长期随访数据或真实世界研究可能会给我们一个明确的答案。
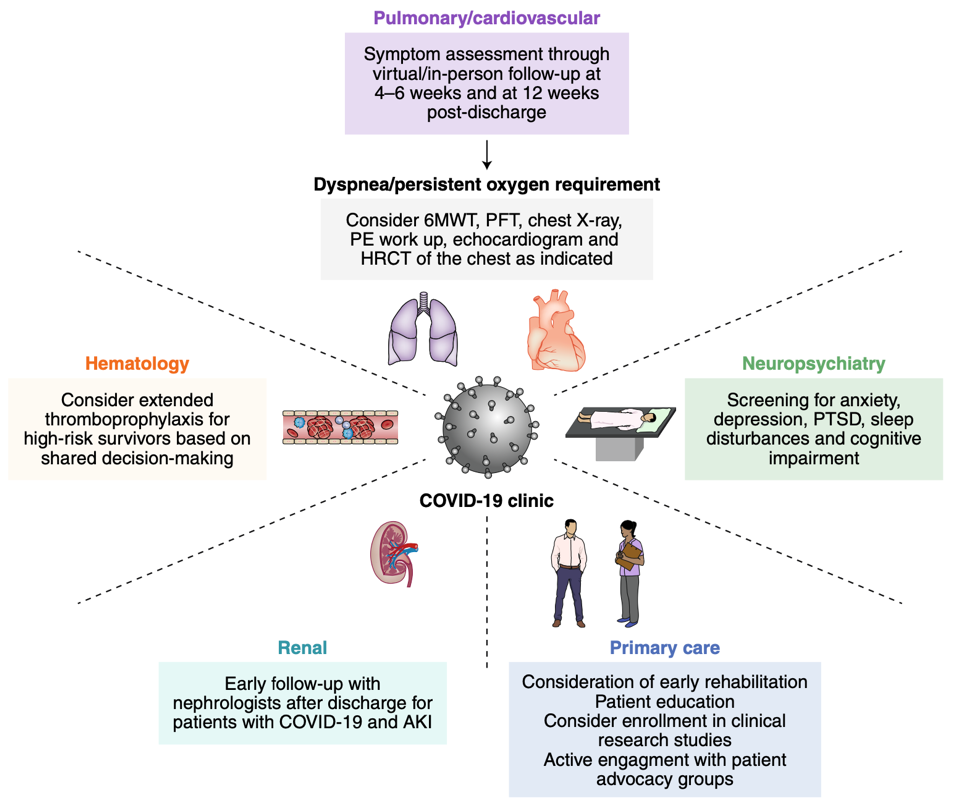
新冠后遗症的多学科护理策略[10]
即使是新冠康复者,也有潜在的降低新冠后遗症的方法。去年年底,由英国国家统计局Daniel Ayoubkhani领衔的研究团队发现,在新冠康复后接种1针新冠疫苗,与新冠后遗症发生风险降低13%相关;如果接种了两针,这种获益还会扩大[23]。当然了,接种疫苗究竟能否降低康复者新冠后遗症的发生率,还需要严格的临床研究探索。
遗憾的是,目前还没有明确的治疗新冠后遗症的有效方法,因此在优化新冠疫苗接种,做好新冠以及预防的基础上,研究人员还需要探索新冠后遗症的机制,深入了解新冠后遗症的成因,以便找到有效的治疗手段。此外,在新冠康复者的护理方面,需要建立多学科合作的综合门诊,以最大限度地降低新冠后遗症对新冠康复者的影响。

《细胞》封面图[24]
或许正如上一期《细胞》封面图所描述的那样,对付新冠后遗症,我们还有很长的路要走。
参考文献
[1].Douaud, G., Lee, S., Alfaro-Almagro, F. et al. SARS-CoV-2 is associated with changes in brain structure in UK Biobank. Nature (2022). https://doi.org/10.1038/s41586-022-04569-5
[2].Liu YH, Chen Y, Wang QH, et al. One-Year Trajectory of Cognitive Changes in Older Survivors of COVID-19 in Wuhan, China: A Longitudinal Cohort Study. JAMA Neurol. 2022; doi:10.1001/jamaneurol.2022.0461
[3].Lopez-Leon S, Wegman-Ostrosky T, Perelman C, et al. More than 50 Long-term effects of COVID-19: a systematic review and meta-analysis. Preprint. medRxiv. 2021;2021.01.27.21250617. doi:10.1101/2021.01.27.21250617
[4].Al-Aly Z, Bowe B, Xie Y. Long Covid after Breakthrough COVID-19: the post-acute sequelae of breakthrough COVID-19[J]. 2021.
[5].https://www.who.int/emergencies/diseases/novel-coronavirus-2019
[6].Mehandru S, Merad M. Pathological sequelae of long-haul COVID. Nat Immunol. 2022;23(2):194-202. doi:10.1038/s41590-021-01104-y
[7].Cohen K, Ren S, Heath K, et al. Risk of persistent and new clinical sequelae among adults aged 65 years and older during the post-acute phase of SARS-CoV-2 infection: retrospective cohort study. BMJ. 2022;376:e068414. doi:10.1136/bmj-2021-068414
[8].Deuel J W, Lauria E, Lovey T, et al. Persistence, prevalence, and polymorphism of sequelae after COVID-19 in young adults[J]. medRxiv, 2022.
[9].https://www.who.int/standards/classifications/classification-of-diseases/emergency-use-icd-codes-for-covid-19-disease-outbreak
[10].Nalbandian A, Sehgal K, Gupta A, et al. Post-acute COVID-19 syndrome. Nat Med. 2021;27(4):601-615. doi:10.1038/s41591-021-01283-z
[11].Huang L, Yao Q, Gu X, et al. 1-year outcomes in hospital survivors with COVID-19: a longitudinal cohort study. Lancet. 2021;398(10302):747-758. doi:10.1016/S0140-6736(21)01755-4
[12].Ramakrishnan RK, Kashour T, Hamid Q, et al. Unraveling the Mystery Surrounding Post-Acute Sequelae of COVID-19. Front Immunol. 2021;12:686029. doi:10.3389/fimmu.2021.686029
[13.Xie Y, Xu E, Bowe B, Al-Aly Z. Long-term cardiovascular outcomes of COVID-19. Nat Med. 2022;10.1038/s41591-022-01689-3. doi:10.1038/s41591-022-01689-3
[14].Xie Y, Xu E, Al-Aly Z. Risks of mental health outcomes in people with covid-19: cohort study. BMJ. 2022;376:e068993. doi:10.1136/bmj-2021-068993
[15].Crook H, Raza S, Nowell J, Young M, Edison P. Long covid-mechanisms, risk factors, and management. BMJ. 2021;374:n1648. Published 2021 Jul 26. doi:10.1136/bmj.n1648
[16].Siripanthong B, Asatryan B, Hanff TC, et al. The Pathogenesis and Long-Term Consequences of COVID-19 Cardiac Injury: State-of-the-Art Review. JACC Basic Transl Sci. doi:10.1016/j.jacbts.2021.10.011
[17].Zhang L, Richards A, Barrasa MI, et al. Reverse-transcribed SARS-CoV-2 RNA can integrate into the genome of cultured human cells and can be expressed in patient-derived tissues. Proc Natl Acad Sci U S A. 2021;118(21):e2105968118. doi:10.1073/pnas.2105968118
[18].https://www.fda.gov/drugs/drug-safety-and-availability/fda-authorizes-revisions-evusheld-dosing
[19].Teresa Evering. Oral presentation. IDWeek 2021 Virtual Conference, Sep 29 – Oct 3
[20].安巴韦单抗注射液说明书/罗米司韦单抗注射液说明书(2021年12月8日)
[21].Hammond J, Leister-Tebbe H, Gardner A, et al. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19[J]. New England Journal of Medicine, 2022.
[22].Weinreich DM, Sivapalasingam S, Norton T, et al. REGEN-COV Antibody Combination and Outcomes in Outpatients with Covid-19. N Engl J Med. 2021;385(23):e81. doi:10.1056/NEJMoa2108163
[23].Ayoubkhani D, Bermingham C, Pouwels K B, et al. Changes in the trajectory of Long Covid symptoms following COVID-19 vaccination: community-based cohort study[J]. medRxiv, 2021.
[24].https://www.cell.com/cell/issue?pii=S0092-8674(21)X0006-2#fullCover
本文内容来源自「奇点网」,作者:BioTalker


