推荐语
在此次新冠之战的救治中,有很多典型病例引发专家们的关注。从今天起,《呼吸界》推出「新冠医案」系列,把专家们在新冠救治中的实践经验和思考与大家分享。 (也随时欢迎老师们分享更多真知,投稿邮箱editorhuxijie@163.com)
2019冠状病毒病(COVID-19)全球爆发以来,国际上公认COVID-19整体病死率并不高,但COVID-19的重型、危重型患者的病死率不容乐观,尤其在疫情爆发早期,ICU内28天病死率甚至高达50% [1] 。因此,避免轻症患者发展为重症或危重症,及时进行有效治疗,成为当前全球COVID-19救治的重点。本例新冠肺炎随疾病的演进及时采取保护性治疗对预后起到决定性作用。
临床资料
患者,男,41岁,已婚。以「咳嗽、发热14天,活动后气短10天,加重伴咳血1周」为主诉,于2020年2月4日19时收入沈阳市传染病院,负压转运仓抬入病房。患者于1月20日由武汉回辽宁当天出现阵发性咳嗽、无痰,自觉发热,周身酸痛,未测体温,未予重视,于家中观察2天未见好转。
于22日至当地医院发热门诊,测体温38.9℃,考虑为新型冠状病毒疑似患者,采样检测并予以奥司他韦胶囊口服,炎琥宁静点。23日结果回报新型冠状病毒核酸检测结果阳性,24日出现呼吸困难,转至当地定点医院住院治疗。
予鼻导管吸氧,重组人干扰素α1b雾化吸入,左氧氟沙星、炎琥宁静点,洛匹那韦/利托那韦口服抗病毒治疗7天,呼吸困难、咳嗽加重(活动后尤为明显),并有胸痛、咳血,调整治疗为高流量吸氧,洛匹那韦/利托那韦、美罗培南、甲泼尼龙、血必净、丙种球蛋白、多索茶碱静点,经治疗患者热退,但仍有阵发性咳嗽、咳少许血痰,经鼻高流量吸氧(流量40L/min,FiO2 60%),指尖血氧饱和度为95%。
为进一步治疗于2月4日以「新型冠状病毒感染肺炎」转至沈阳市传染病院。发病以来,无抽搐及意识障碍,偶有腹泻,无剧烈腹痛,无尿频、尿急、无尿痛,饮食、睡眠欠佳。
既往史
一般健康状况良好,既往有「心肌缺血」3年,曾查出冠状动脉属支(具体不详)有狭窄,胃炎病史20余年。否认高血压病史,否认糖尿病史,否认慢性呼吸道疾病。无食物及药物过敏史。吸烟、饮酒少量。无家族遗传倾向疾病。
流行病学史
辽宁人,16年前至武汉定居,家距「海鲜市场」约3公里,1月18日由武汉乘坐高铁至北京西,1月20日由北京自行开车至辽宁。
入院查体
体温 35.8℃,脉搏 77次/分,呼吸 29次/分,血压 125/87mmHg,SPO293%(HFNC,FiO2 60%,流量45L/分)。神志清晰,查体合作。浅表淋巴结未触及肿大,口唇无发绀,咽部充血,扁桃体无肿大。双肺动度正常,听诊:呼吸音粗糙,双肺可闻及水泡音和少许哮鸣音,无胸膜摩擦音。心率:77次/分,心音纯、律整,无病理杂音。腹软无压痛,肝脾未触及。生理反射存在,病理反射未引出。
本次入院前辅助检查
新型冠状病毒核酸抗体阳性(1月23日CDC检测),血常规:白细胞:7.1×10^9/L;中性粒细胞百分比:78.3%↑;淋巴细胞百分比:13.0% ↓;淋巴细胞绝对值:0.9×10^9/L↓;血清淀粉样蛋白 A:>320mg/L ↑;C 反应蛋白:23.52mg/L↑(1月26日);白细胞:16.2×10^9/L↑;中性粒细胞百分比:88.6%↑;淋巴细胞百分比:4.0%↓;红细胞:3.25×10^12/L↓;血红蛋白:126G/L↓;血小板:320 × 10^9/L;C反应蛋白:12.32mg/L ↑ ;血清淀粉样蛋白A:115.2mg/L↑;(2月3日)。发病时的肺部CT影像(1月23日)如图1(ABC):双肺见散发片状磨玻璃样影,部分靠近胸膜。
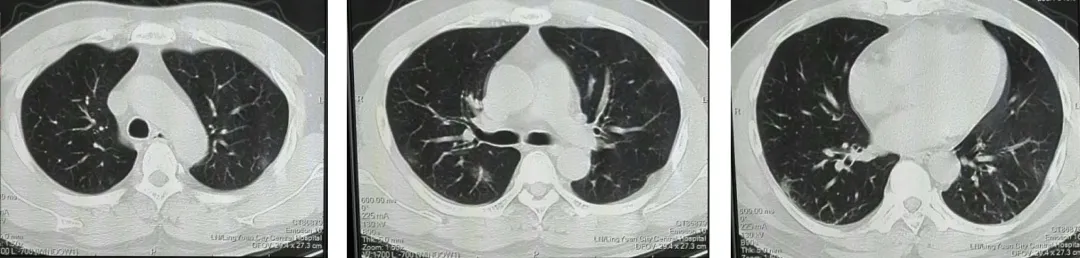
图1:A上叶;B中叶;C下叶
核酸阳性后7天复查肺部CT影像(1月30日)如图2(ABC):双肺大片融合磨玻璃样影(内见增粗的血管影),磨玻璃样影与空气潴留共存,主要病变位于中外带胸膜下区。
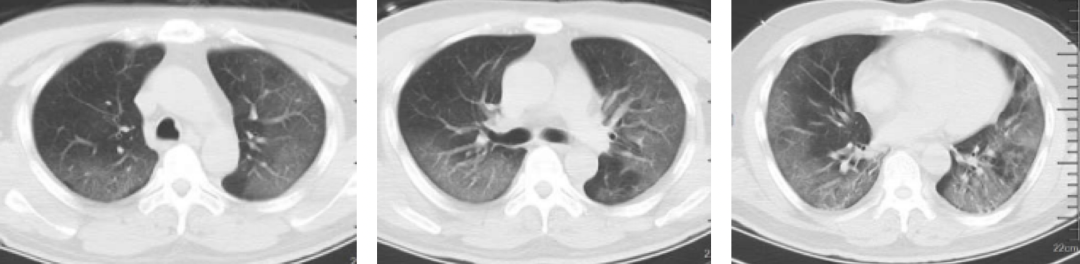
图2:A上叶;B中叶;C下叶
本次入院后化验检查:白细胞计数 16.7 10^9/L↑、血小板计数 384.0 10^9/L↑、血红蛋白 148 g/L、中性粒细胞百分比 96.5 %↑、中性粒细胞数量 16.08 10^9/L↑、淋巴细胞数量百分比 1.0 %↓、淋巴细胞计数 0.2 10^9/L↓,凝血酶原时间 13.00 秒、D-二聚体 0.68 mg/L,C反应蛋白:10.76 mg/L↑,丙氨酸氨基转移酶 61 U/L↑、白蛋白 28.0 g/L↓、总胆红素 17.0 umol/L,钾 4.70 mmol/L、钠 127.0 mmol/L↓,尿素 6.50 mmol/L↑、肌酐 46.0 umol/L↓,心肌肌钙蛋白I测定 0.10 ng/ML。
本次入院诊断
1.新型冠状病毒肺炎(COVD-19)危重型合并细菌感染;
2.ARDS;
3.低蛋白血症;
4.多器官功能受累(肝脏、心脏等);
5.电解质代谢失常(低钠、低氯、高钾血症)。
入院后根据国家卫健委《新型冠状病毒感染的肺炎诊疗方案(试行一到七版)重症、危重症治疗的推荐意见 [2]制定本患者的治疗方案。
首先给予鼻高流量湿化吸氧(HFNC,流量40L/分,FiO2 60%,温度37℃),延用洛匹那韦/利托那韦500mg,日3次,口服,甲强龙40mg,日1次静推。此时指尖血氧饱和度波动于85%-98%,床上活动后指尖血氧饱和度明显下降同时伴有呼吸困难,呼吸频率波动于17-38次/分。
次日(2月5日)重新评估患者的临床表现,调整治疗方案,停用洛匹那韦/利托那韦,改用阿比多尔0.2,tid 口服,加用利奈唑胺0.6,q12h,口服,血必净等对症治疗。无创通气及HFNC序贯治疗,连续观察3天,动脉血氧变化分别为76mmHg,68mmHg,87mmHg,动脉血二氧化碳有逐渐上升的趋势,PaCO2 高达50mmHg。潮气量(VT)波动于200-300ml(身高170cm,体重80kg)。于2月8日将无创改为有创机械通气,模式SIMV,FIO2:45%,PEEP:10cmH2O,PS:15cmH2O,RR:18次/分,指尖血氧饱和度98%。给予递增式PEEP肺复张治疗,PEEP最大升至20cmH2O,但VT仍为230ml左右。观察8小时后改俯卧位通气,SIMV+压力控制模式,FIO2:45%,PEEP:15cmH2O,PS:16cmH2O,RR:18次/分。2月9日查体:体温37.4℃,脉搏98次/分,呼吸18次/分,血压140/90mmHg(去甲肾上腺素泵入中0.3mg/h),指尖血氧饱和度98%。动脉血气:PH 7.45,PO2 83mmHg,PCO2 50mmHg,HCO3-34.8mmol/L,VT仍为200ml左右,于2月9日下午行ECMO治疗。ECMO治疗8天(2月17日)脱机,有创通气治疗10天(2月18日)拔管。在这个期间药物抗病毒药阿比多尔口服10天,改为磷酸氯喹500mg,bid口服 3天。抗生素:美罗培南1g,q8h静点7天,利奈唑胺由口服改为600mg,q12h静点7天,卡泊芬净50mg qd 静点10天。抗凝药:低分子肝素钙0.5,bid,皮下注射7天后改为0.5mg qd 皮下3天,序贯利伐沙班10mg 口服9天。激素:甲强龙40mg qd 静推3天,改为口服24mg 6天,改为12mg 3天,改为8mg 3天,改为4mg 3天。其他:保肝,补充白蛋白等对症治疗。
动态床旁平片2月9-18日(脱机、拔管):如图3所示(ABCDEF)。
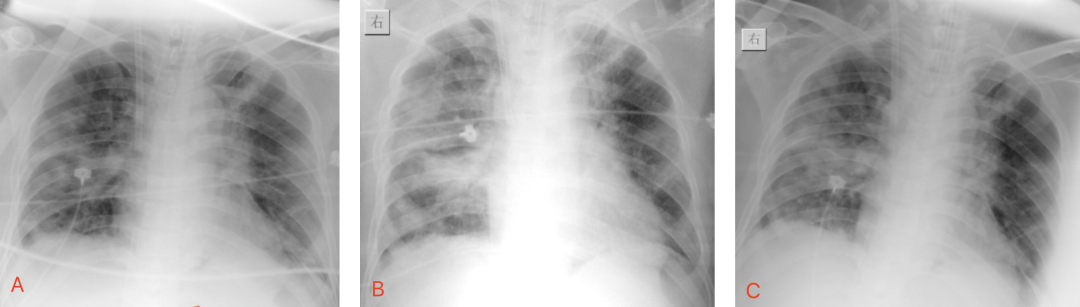
【图3】A:9日双肺多叶小片状阴影,以右侧为重,可见肋膈角;B:10日双肺多叶小片融合大片状阴影,右中下部实变影;C:11日 较10日双肺无明显变化
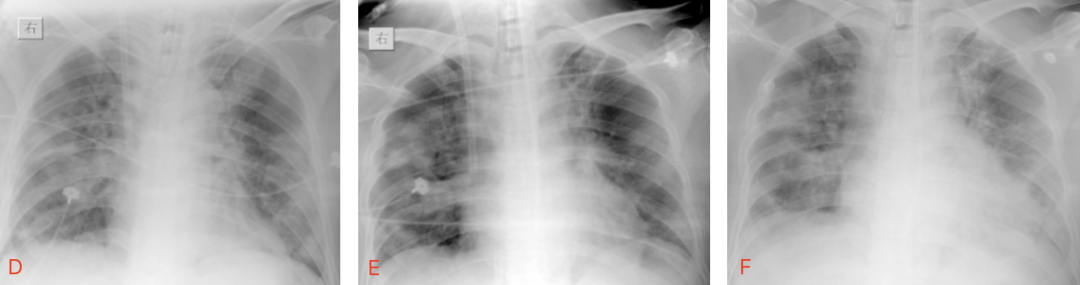
D:12日 双肺多叶小片状及融合阴影,左肺较11日透过度降低,可见肋膈角;E:16日 较12日双肺多叶阴影明显吸入,透过度较前改善;F:18日双肺无明显变化
血气分析动态变化:2月9-18日PH:7.47±0.04、PCO2 46.33±2.13(mmHg)、PO2 90.33±14.07(mmHg)、HCO3 33.98±3.31(mmol/L),16日后基本恢复正常水平。如图4。
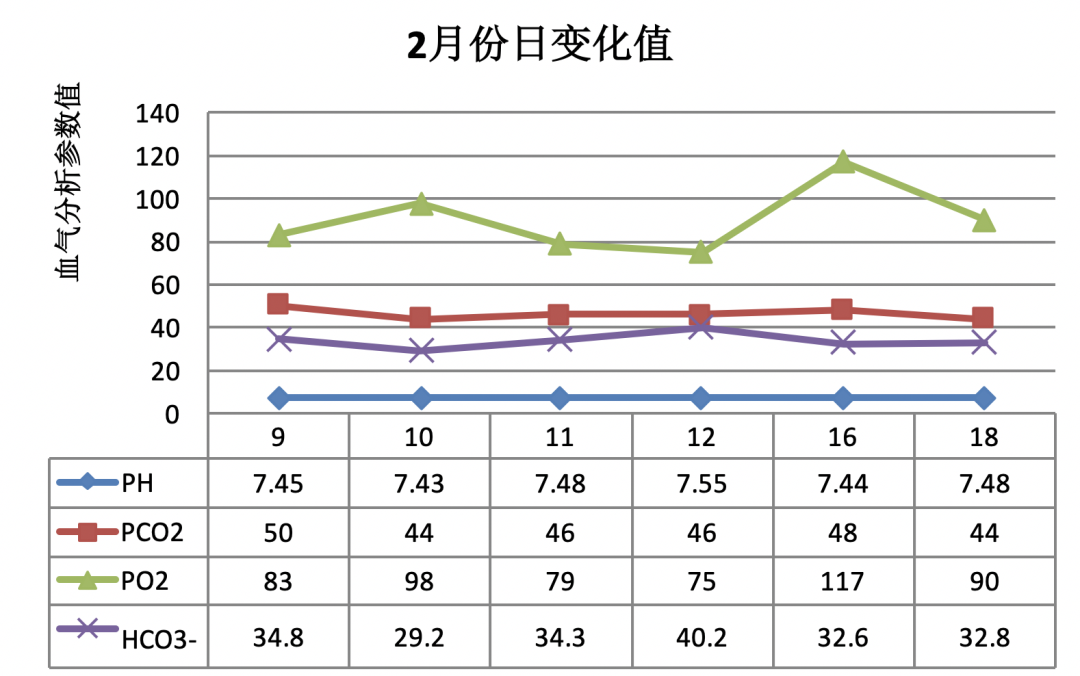
图4
整个疗程32天(2月4日-3月8日),临床症状缓解,核酸检测两次阴性,达到「诊疗方案」的标准出院。
出院后随访:出院5天(3月13日),患者无明显呼吸困难。图5(ABC)肺部CT显示:右肺上、中叶见浅淡的斑片影。
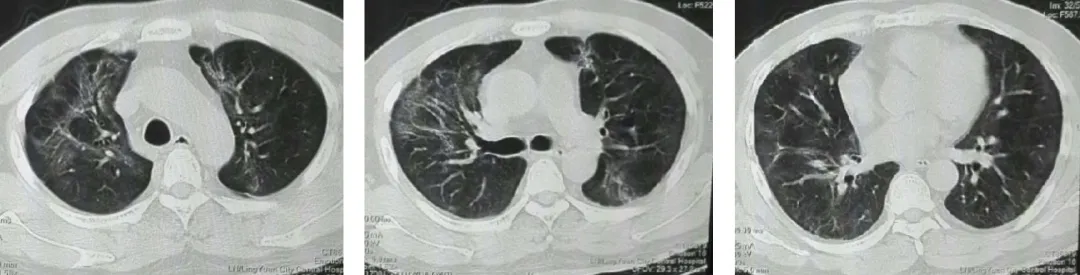
【图5】A 上叶;B 中叶;C 下叶
出院1个月(4月8日),肺部CT:双肺残留条索阴影,图6(ABC)。
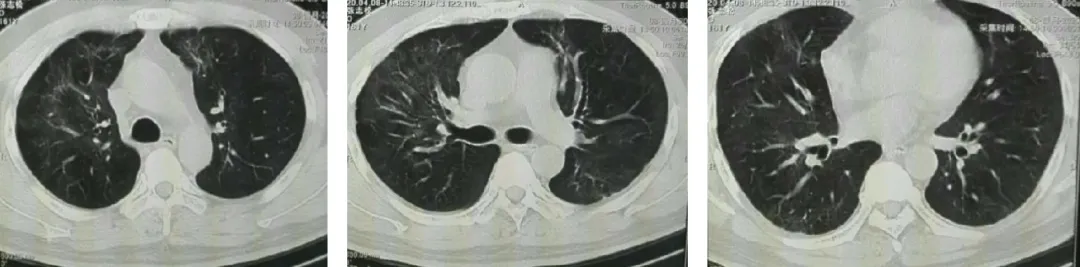
【图6】A 上叶;B 中叶;C 下叶
出院2个月余(5月12日):双肺基本恢复正常影像状态,如图7(ABC)。肺功能:VC max:3.04L, FEV1%:87%,FEV1/FVC:101%,MEF75 66%, MEF50 98%,MEF25 167%。血常规:白细胞计数8.39×10*9/L, 中性细胞数百分数51.2%,中性细胞数绝对数4.30×10*9/L, 淋巴细胞数百分数37.8%,淋巴细胞数绝对数3.17×10*9/L ,红细胞计数4.84×10*12/L血红蛋白145.00 g/L血小板287.00×10*9/L,总蛋白73.80 g/L,白蛋白46.7 g/L,球蛋白27.10 g/L。均恢复正常。
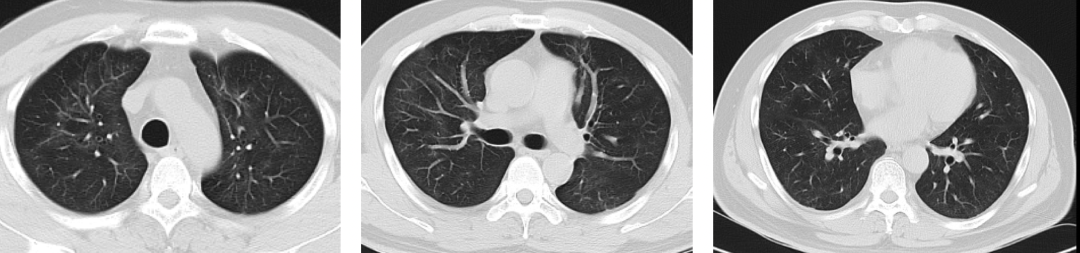
【图7】A上叶;B 中叶;C 下叶
讨论
2019年的新型冠状病毒(2019n-CoV)是可感染人类CoV(HCoV)的最新成员,属于β冠状病毒 [2]。冠状病毒引起的人类疾病主要是呼吸系统感染,其中HCoV-229E、HCoV-OC43、HCoV-NL63和HCoV-HKU1仅诱发轻度上呼吸道疾病,在极少数情况下可引起严重感染,其引发死亡的主要原因是严重的肺损伤导致呼吸衰竭及其他重要器官的功能衰竭 [3]。在临床的救治过程中,如何早期发现疾病恶化,如何抢先干预是降低死亡率的关键。
最新研究表明 [4],高龄、SOFA评分高、淋巴细胞持续低水平、D二聚体水平升高等提示病例可能进展至危重型,并提示不良预后。危重型病例常合并有中-重度ARDS、急性肾损伤、心脏损伤、凝血异常等多系统受累表现,因此在抗病毒治疗基础上的器官支持尤为重要。
本例患者确诊后,抓住病情演进的几个关键点
外周血淋巴细胞进行性下降,动脉血氧、二氧化碳的变化趋势,潮气量的改善量,结合患者的临床体征及动态胸部影像变化,不断修正治疗手段,由高流量氧疗到无创通气,由无创(8h后SPO2<90%)过渡到有创机械通气,在俯卧位通气(10h)状态下仍无法提升潮气量及缺氧状态情况下,抢先加用体外膜肺氧合(ECMO)治疗,经10天的治疗,成功脱机,拔管。达到出院标准。
本例特点:在患者出现发热、呼吸道症状一天后就明确诊断,随之严格遵循新冠肺炎诊疗方案进行治疗,但仍在治疗20天后从新冠肺炎普通型转向危重症。进入危重症期积极防治并发症,预防继发感染,及时进行器官功能支持及呼吸管理这是器官功能保护性治疗,降低死亡率的关键。
近期,德国的研究团队在《Nature》在线发表了题为「Virological assessment of hospitalized patients with COVID-2019」的文章 [5]。该研究纳入了来自慕尼黑的9位患者,通过对患者口咽/鼻咽拭子样本的分析发现:患者首次出现症状后第1-5天,新冠病毒的RNA水平处于较高水平,病毒RNA平均载量为6.76×10^5 copies/swab,最高可达7.11×10^8 copies/swab。第5天后开始下降,但同时一定比例的患者血清IgG抗体才开始出现。他们认为新型冠状病毒在感染早期尤其是症状出现的第1-5天在口咽/鼻咽处是快速复制高峰期,此时针对病毒的抗体是分泌量不足,提示人体对新冠病毒的免疫应答可能具有滞后性。
研究 [6]发现在人体未能产生足够抗体之前,人体免疫系统以非特异性免疫应答为主,干扰素α是一类主要的非特异性免疫应答细胞因子,其可以通过诱导细胞产生抗病毒蛋白等免疫调节机制帮助人体建立「抗病毒状态」。
一项体外实验 [7]揭示了新冠病毒能降低多种细胞因子的表达水平,这使得人体免疫细胞没有产生足够内源性干扰素,导致机体重要脏器尤其是肺部严重感染时,免疫系统也无法及时作出免疫保护。所以,新冠病毒感染后可能会严重影响机体内源性干扰素表达,如果及时补充足量的外源性干扰素,或可以帮助机体尽早建立有效的免疫应答状态。
本例救治成功之处
1、典型的流行病学史,由武汉(正值新冠疫情流行高峰)回当地,属输入性病例,快速的确诊,及时治疗。尽管没有有效的抗病毒药物,但及时有效的对肺部的保护性治疗是成功的关键。2、患者年轻,无典型的基础疾病,在进入危重症期的抢先干预,为患者体内产生大量内源性病毒抗体赢得了时间,加之早期重组人干扰素α1b雾化吸入的外源性抗体的补偿,使患者预后良好。
出院2个月后随访,患者肺功能恢复正常,肺部影像基本吸收,恢复到发病前的工作和生活状态。
* 基金项目:沈阳市科技局防治新冠肺炎科研攻关应急专项(YJ2020-0-019)。
参考文献
[1]Fei Zhou,Ting Yu,Ronghui Du,et al.Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China:a retrospective cohort study[J].Lancet. 2020 28 March-3 April;395(10229):1054–1062.Published Online March,2020,https//dio.org/10.1016/S0140-6736(20)30566-3.
[2] 国家卫生健康委员会.新型冠状病毒肺炎诊疗指南(试行第七版),2020.
[3] Chaofu Wang,Jing Xie,Lei Zhao,et al. Aveolar Macrophage Activation and Cytokine Storm in the Pathogenesis of Severe COVID-19.Nature research 2020. Doi:10.21203/rs.3.rs-19346/v1.
[4] N. Petrosillo,G. Viceconte,O. Ergonul,G. Ippolito,E. Petersen. COVID-19, SARS and MERS:are they closely related?[J]. Clin Microbiol Infect,2020 Jun;26(6):729-734. Doi:10.1016/j.cmi.2020.03.026. Epub 2020 Mar 28.
[5]Roman Wölfel, Victor M. Corman, Wolfgang Guggemos, et al. Virological assessment of hospitalized patients with COVID-2019 [J]. Nature volume 581, pages465–469(2020). Published: 01 April 2020. Doi:10.1038/s41586-020-2196-x.
[6] Qiong Zhou, Xiao-Shan Wei, Xuan Xiang, et al. Interferon-a2b treatment for COVID-19[EB/OL].https://www.medrxiv.org/content/10.1101/2020.04.06.20042580v1.
[7]Emily Mantlo, Natalya Bukreyeva, Junki Maruyama, et al. Potent Antiviral Activities of Type I Interferons to SARS-1 CoV-2 Infection. Antiviral Res. 2020 Apr 29;179:104811. Doi:10.1016/j.antiviral.2020.104811. Online ahead of print.
专家介绍

夏书月
沈阳医学院附属中心医院 副院长 呼吸与危重症学科主任,学科带头人,二级教授,医学博士,博士生导师,中华医学会呼吸分会肺血管组 委员,辽宁省医学信息与健康工程学会 副理事,辽宁省医学会呼吸分会 常委,辽宁省医学会呼吸分会危重症学组组长,辽宁省预防医学会微生态学专业委员会 常务,辽宁省抗癌协会肺癌专业委员会 常委。

吴云海
主任医师,教授;沈阳市六院重症医学科主任;辽宁省医学会重症医学分会委员;辽宁省细胞生物学学会休克与脓毒症专业委员会副主任委员;辽宁省中西医肝病委员会委员;中国重症血液净化协作组委员;辽宁省医师协会重症医学医师分会委员;长期从事危重症医学的基础与临床研究。


