目前,肺癌的高发病率和高死亡率对医生造成重大的压力。虽然,近年来肺癌的靶向治疗和免疫治疗等的进展,肺癌预后都得到了一定的改善。但是总体而言,肺癌的预后相对其他肿瘤却不太理想。不同分期肿瘤的预后不同,肺癌ⅠA1期的5年生存率为90%左右,IV期在10%一下。在初诊患者中,多数患者为中晚期肺癌,早期肺癌患者不足20%(图1)。因此,提高肺癌早期诊断水平是从根本上改善肺癌预后的最重要途径之一。
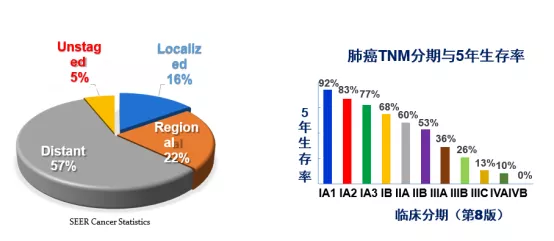
图1:肺癌不同时期的比例(左),肺癌TNM分期与5年生存率(右)
大数据、AI、机器人、组学技术(Omics)的发展对肺癌的早期诊断有很大的帮助,具体表现在影像诊断、内镜诊断及Bio-markers方面。尤其内镜诊断技术占据非常重要的地位。
近年来,肺癌的内镜诊断技术有相当程度的进步,例如荧光支气管镜、窄谱支气管镜、共聚焦显微成像、光学相干断层成像(OCT)、细胞内镜、电磁导航等。其中,临床上应用最多的是导航支气管镜。
一、导航支气管镜新技术及其评价
导航支气管镜最早是虚拟导航,后来有超声导航、电磁导航、4G电磁导航、LungPro导航……
1、虚拟导航支气管镜(virtual navigation bronchoscope,VNB)
虚拟导航支气管镜或仿真气管镜导航,通过引导支气管镜到达所指定的病变部位,减少不必要的透视。可以缩短支气管镜插入的实施时间,减轻患者的痛苦和减少操作的危险性(图2)。
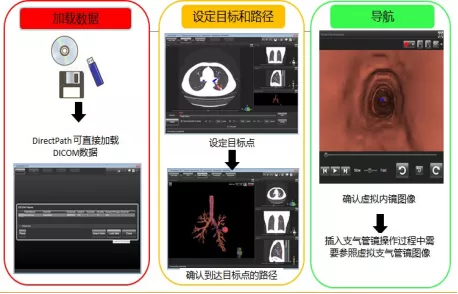
图2:虚拟导航支气管镜操作步骤
特点:
①只具备规划导航路径的功能,其主要价值在于辅助术者在 虚拟导航系统生成的气道内图像和导航路径下,更高效的选择正确的支气管分支抵达目标病灶,通常用于辅助细镜/超细镜、REBUS操作;
②VBN不能针对基于术前CT的重建图像与术中实际差异进行实时的匹配和调整;
③当操作工具(鞘管、REBUS、活检工具等)不在内镜视野内时,VBN不能提供电子或影像信息帮助定位,需其他定位技术配合。
2、超声导航支气管镜
临床价值:可以实现末端支气管(肺周围型病变)精确定位。
实时超声:可提供小气道及其周围组织的360度超声图像(图3)。
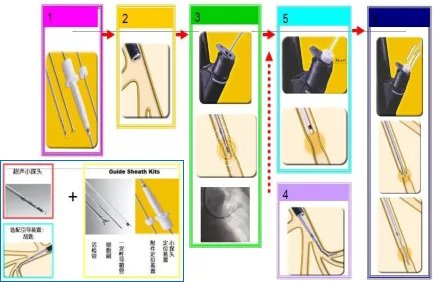
图3:超声导航支气管镜操作步骤
小探头超声:
识别小探头超声REBUS典型图像尤为重要,REBUS提供了从设备头端旋转探头向外发散的二维平面内的360度超声视图,REBUS可以实时定位支气管镜所能触及的远端病变,或支气管镜视野下不可见的更远端的病变。
典型病灶图像有:实性病灶-同心视野,实性病灶-偏心视野,磨玻璃病灶-暴风雪征,肺组织-正常充气(图4)。其中,磨玻璃病灶的识别比较困难,这要求临床医生在术前对其有足够的认识。
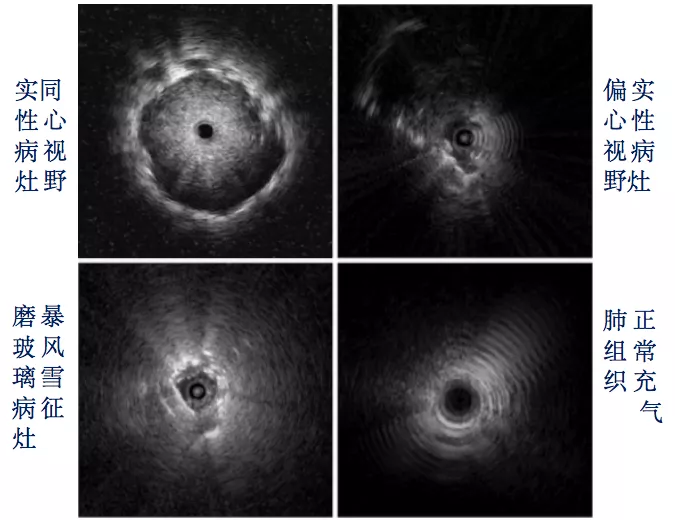
图4:典型病灶图像
2017年《Respirology》发表了一项数据分析:56项研究中,小探头超声的总体诊断率70.6%,总体并发症率2.8%[1]。
特点:
①REBUS本身只具备病灶定位功能,需要联合其他技术来提升导航控制和病灶定位能力。
导航路径:CT手工绘图、虚拟导航、细镜或超细支气管镜。
末端定位调整:C型臂,当病灶距支气管镜末端较远、或存在大角度支气管分叉时,定位成功率下降。
②REBUS图像问题
暴风雪征在临床实际应用中不易于识别,特别是小的纯GGO病灶;
偏心视野病灶的REBUS图像无法告诉术者病灶相对于探头所在气道的具体空间方位,需要借助C型臂调整;
肺不张易被错误的识别为病灶。
3、电磁导航支气管镜(superDimension™)
近年来,随着技术的改进,电磁导航支气管镜在临床上已经有一定的普及。目前,电磁导航支气管镜在国内主要应用于腔内病变,腔外病变的活检系统已经开发,并在国外应用于临床(图5)。

图5:腔内病灶常规导航活检(左),腔外病灶经支气管活检工具(右)
电磁导航支气管镜具体操作过程为:病例筛选-术前计划-术前准备-导航手术-活检采样等。
电磁导航支气管镜在真实世界研究(Navigate)
电磁导航支气管镜在真实世界研究中,诊断率为72.9%;恶性肿瘤的敏感性、特异性、阳性预测值和阴性预测值分别为69%、100%、100%和56%;并发症研究结果为,气胸发生率4.3%,需要住院或干预的气胸发生率2.9%(35/1215),出血发生率2.5%,麻醉相关死亡1例,无ENB操作相关死亡病例[2]。
特点:
①superDimension ™电磁导航用于肺外周病变的诊断率为72.9%,气胸发生率4.3%,出血发生率2.5%。
②TBAT有效的解决了支气管腔外病灶的导航活检问题。
③导航易受生理运动(呼吸、心跳、大血管搏动)影响。探头位置在导航图像上存在来回漂移的现象,并且其实际位置与在导航图像上显示的位置可能存在一定差异;系统通过电磁感应器位移计算对前后(胸到背)、左右4个方向呼吸运动的影像进行了校正,减少了图像漂移的幅度;生理运动的影响可通过术者经验和操作来克服。
④导航管和活检工具是否进入病灶通常需要联合其他影像方法确认。
4、4D电磁导航(Veran)
4D电磁导航是一种全方位导航。4D电磁导航能通过常规导航解决支气管腔内病灶,也能通过TBNA和针钳有效的解决腔外病灶,
更好的「地图」∶Veran同时扫描吸气/呼气CT,从—开始就具备更好的「地图」;
追踪移动的结节:Veran具备呼吸门控技术,可实时追踪手术过程中的呼吸移动,减少人为误差,并且可以做到自动注册,动态校准;
减少盲目取样∶Veran拥有Always On Tip Tracked活检工具,真正的实时导航,减少X射线辐射;
更精确的控制,更好的接近方式∶Veran可从支气管镜导航到经皮导航无缝切换,增加多种导航途径(图6)。
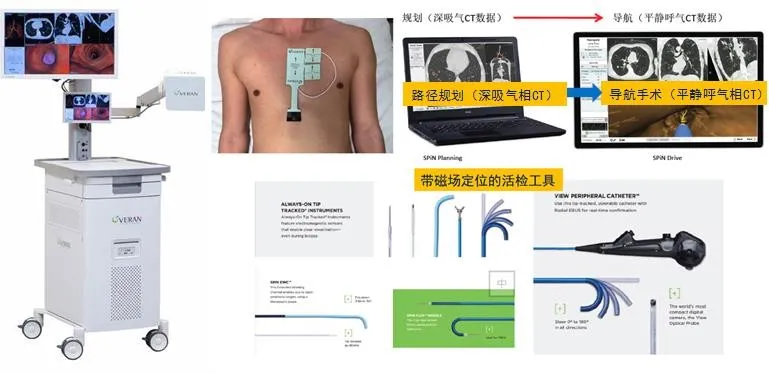
图6:4D电磁导航操作步骤
特点:
①4D电磁导航用于肺外周病变的诊断率为80-90%;
②TBNA和针钳解决了支气管腔外病灶的导航活检问题;
③导航受生理运动(呼吸、心跳、大血管搏动)影响,系统通过呼吸双相CT(吸气相用于导航规划,平静呼吸相用于导航定位)一定程度上减少了图像漂移的问题;
④尽管活检工具自带电磁感应器,但仍需要联合其他影像方法确认是否活检工具进入病灶。
5、LungCare™电磁导航
①LungCare™电磁导航已在临床开展应用;
②「近距离瞄准隧道技术」(ENB-TPNA)解决了支气管腔外病灶的导航活检问题;
③导航受生理运动(呼吸、心跳、大血管搏动)影响;
④导航管和活检工具是否进入病灶需要联合其他影像方法确认(图7)。
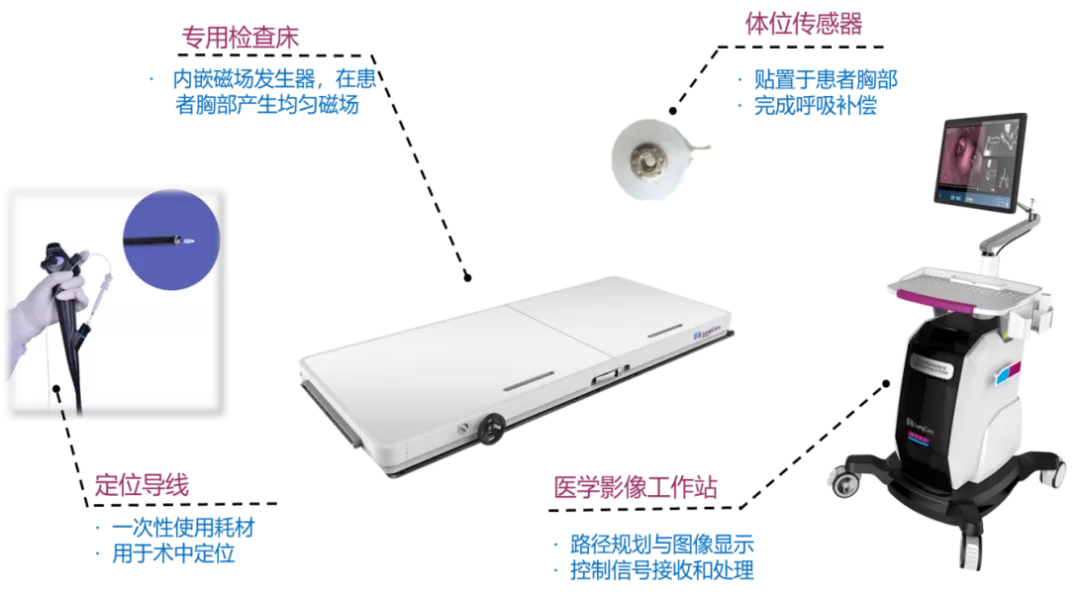
图7:LungCare™电磁导航功能
6、LungPro™导航
通过CT数据导入,进行系统3D重建,在识别和标记病灶时,系统会生成4种路径以供挑选。LungPro™导航在实际临床应用中,一方面,增强气道内现实导航,另一方面,气道外病灶经肺实质建立隧道BTPNA(图8)。
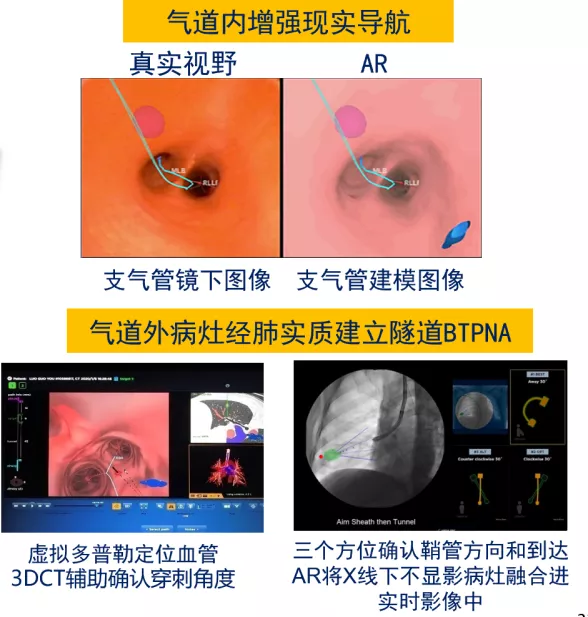
图8:支气管镜真实视野与建立隧道
特点:
①初步研究显示LungPro™导航用于肺外周病变的诊断率和安全性较好。
②BTPNA术式有效的解决了气道外病变的活检问题。BTPNA减少术中X线暴露时间较长;虚拟多普勒定位血管和3DCT辅助确认穿刺角度的技术,使得BTPNA术式在肺外1/3肺野的气道外病灶活检有一定安全性的优势。
③最后病灶定位需要联合其他影像方法确认。
7、Cone-beam CT(CBCT)导航
Cone-beam CT(CBCT)导航能够全方位地显示病灶,是基于CBCT和增强现实透视的导航(图9)。
①术前PET-CT显示右下叶横膈旁12×11×7mm实性病变FDG摄取;
②B-D.基于CBCT和增强现实透视(AF)导航;
③E-F.两种不同角度下增强现实透视确认活检定位,病变用蓝色勾画;
④预设的支气管内导航路径,通过工作站内程序进行分割并标记物为紫色点[3]。
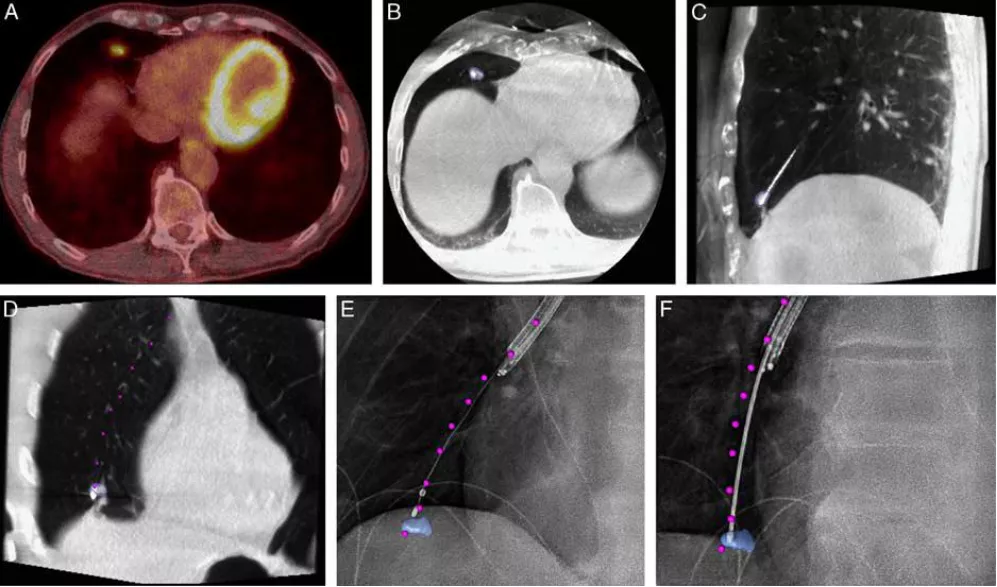
图9:CBCT现实透视导航
特点:
①Conebeam CT具有实时影像和三维重建功能,结合图像分割和增强现实技术,有较好的导航和定位能力;
②Conebeam CT联合REBUS和ENB用于肺外周病变,诊断率90%,安全性良好;
③Conebeam CT导航的X线暴露时间相对更长。
8、复合导航技术
以上导航各有特点,患者的诊断率基本可达70%~90%。实际临床应用中,需要多个导航工具联合应用以增加精准性和活检成功率(表1)。选择导航时会对其技术进行比较,也要考虑成本问题。
表1:各导航技术比较
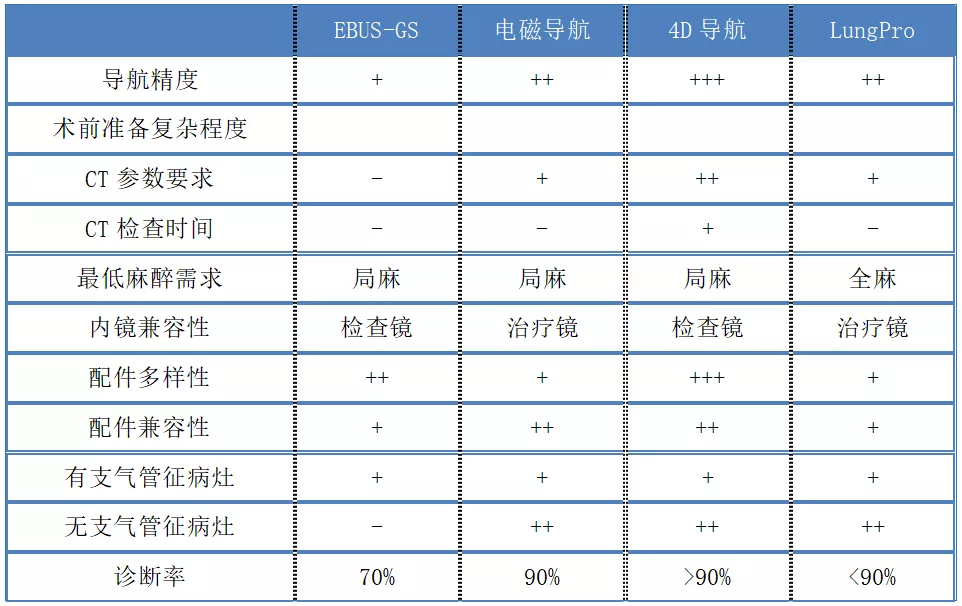
单一导航技术不能解决所有问题,多种导航技术联合建立的复合导航技术能更好的提升综合处理能力(表2)。
表2:复合导航技术
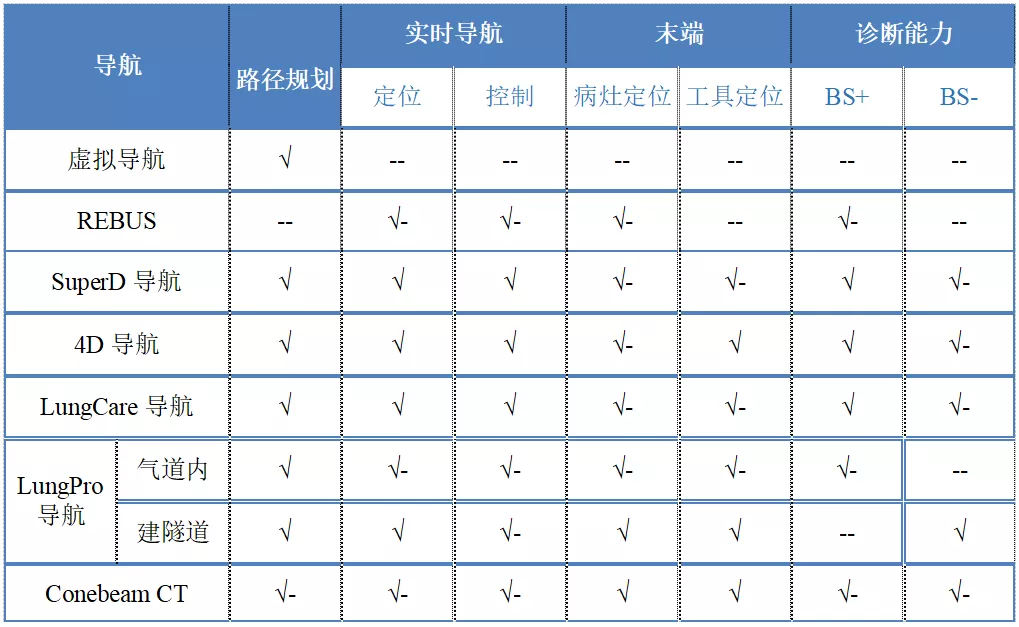
二、导航支气管镜临床应用相关问题
1、术前评估
①病灶大小:病灶越大,导航技术准确性越高,10mm左右的病灶需要一定的导航技术水平(图10)。

图 10
②病灶密度:实性病灶较GGO病灶更易定位(图11)。
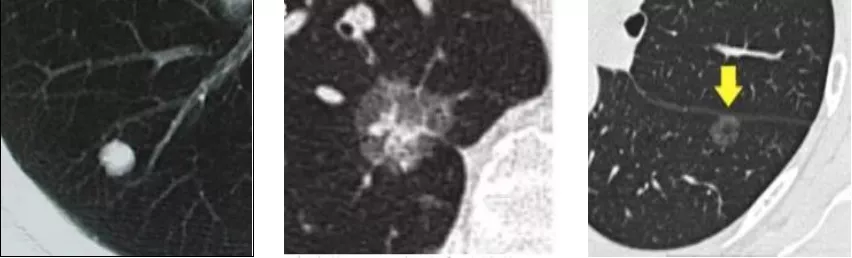
图 11
③是否有支气管进入病灶:支气管征阳性灶诊断率较高(图12)。

图12:支气管进入病灶中心(左),支气管位于病灶边缘(中),无支气管进入(右)
④病灶位置:距胸膜近病灶气胸风险高,靠近心脏、血管的病灶出血风险高(图13)。

图 13
⑤活检部位:转弯角度大病灶操作难度高,肺尖后段的病灶—气道复杂、转弯角度大(图14-左)。
⑥患者的自主呼吸:中叶、上叶病灶受呼吸运动影响小,下叶近膈肌病灶受膈肌运动影响大(图14-右)[4]。

图14:肺尖后段的病灶(左),自主呼吸CT时(右)
2、路径规划
①CT要求
常规参数:层厚≤1mm,(部分系统针对CT机品牌进行参数优化)。
部分系统做CT时需要放置定位标记,CT检查时间距手术时间不能过长,避免出现术前计划与实际情况不符。
②路径规划
操作相对简单,部分自动规划路径需要人工修正。
3、麻醉方式
①表麻
没有静脉麻醉药物不良反应的相关风险;
呛咳、憋气、躁动、胸部不适等反应较多,可能导致手术中断,操作时间相对延长,部分患者可能有恐惧、痛苦记忆;
可配合术者深呼吸和屏气,胸膜粘连有气胸风险病例术中有疼痛反应可发出预警。
②镇静或全麻
呛咳、憋气、躁动、胸部不适等反应很少,操作时间相对较短,手术过程无记忆;
对患者一般情况要求更高、静脉麻醉药物不良反应、有一定的费用;
TBNA或打隧道多选择镇静,降低气胸风险。
4、注册匹配
所有的实时导航(电磁、LungPro、CBCT)在开始导航操作前均需要注册匹配(不同设备的方法有区别)。
注册匹配将真实支气管结构与三维CT重建的支气管树结构相匹配;注册匹配需要消耗一定时间;少数患者存在匹配度不佳的情况,需要重新注册匹配。
5、导航操作
按照系统实时导航指示到达病灶(图15)。

图 15
6、病灶定位
①REBUS、透视、Conebeam CT可独立确认;
②电磁导航通常需要联合其他方法确认定位准确;
③活检后行ROSE有助于对活检阳性的确认(图16)。
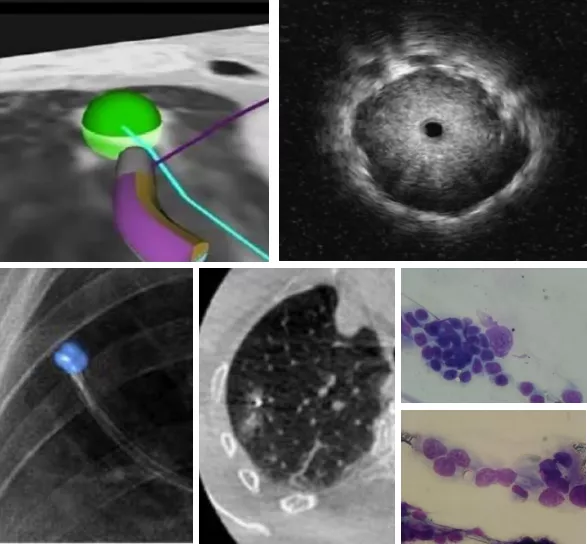
图16:病例:患者活检为腺癌,阳性
7、并发症及预防
①气胸(发生率<5%,多较轻微)
主要发生在临近胸膜病灶。尽量选择离胸膜较远的位置活检,最好联合透视观察活检装置与胸膜的相对位置。
警惕存在胸膜粘连的病灶。局麻下钳夹过程中患者出现疼痛反应,松开活检钳,变换钳夹角度尝试,或终止活检。
②出血(发生率<5% ,多较轻微)
导航路径避开血管,活检时原则相对远离血管的位置或方向;导航鞘管有压迫止血的作用。
8、电磁导航病例
病例1:右上肺14mm结节,肩胛遮挡,电磁导航活检,肺腺癌,EGFR+(图17)。
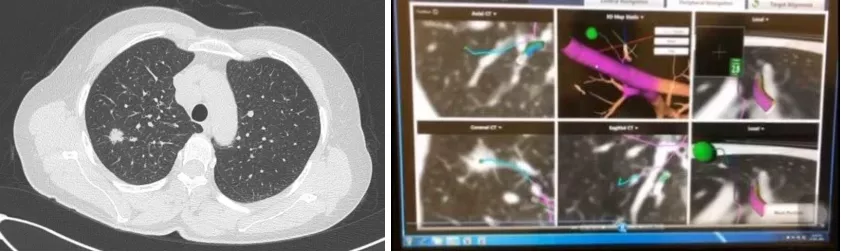
图 17
病例2:右下肺21mm结节,多支粗大血管穿行其中,肾功能不全、长期透析,电磁导航活检,SCLC(图18)。
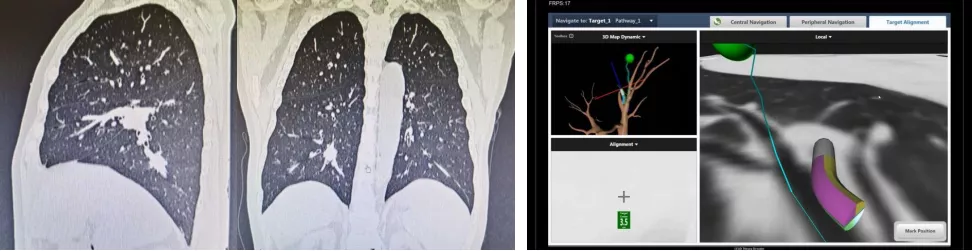
图 18
病例3:男性,68岁,左肺上叶病变,吸烟指数10包年,已戒烟20年,局麻下4D电磁导航+活检,病理报肺腺癌,手术切除(图19)。
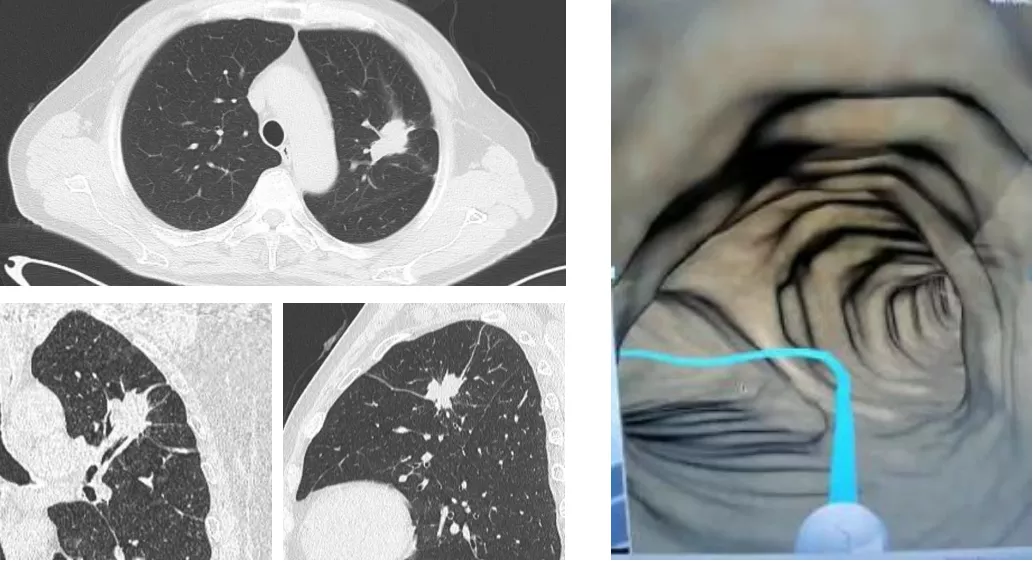
图 19
三、导航支气管镜的发展方向
1、导航支气管镜发展为诊疗一体化平台
导航支气管镜将是肺癌早期诊断和治疗的基本平台。
①诊断
多种导航技术联合,兼容各种活检工具可以对双肺病灶的多点、多次采样;为最后的病理诊断、分子学诊断提供组织标本。
②定位
通过导航支气管镜进行显色剂、发光剂、造影剂局部注射定位、矢量定位、金属标记定位等有助于外科精准的手术切除病灶。
③治疗
通过导航支气管镜可以实现对肺部肿瘤消融治疗、粒子植入放疗、感染性疾病局部给药治疗、肺大疱消融治疗等。
2、导航技术与智能化的微创手术机器人融合
未来,导航支气管镜会和智能化的手术机器人进行联合,肺癌的早期诊断和治疗水平将会得到极大的提高。
小结
1、导航支气管镜用于肺外周病变(肺癌)的诊断率在70-90%;
2、对不同的患者选择更合适的技术、多种技术联合有助于进 一步提升诊断能力;
3、导航支气管镜的应用不断拓展,并与AI、微创手术机器人等新技术融合,未来将成为呼吸内镜诊疗一体化关键平台。
参考文献
[1] Respirology. 2017 Apr;22(3):443-453.
[2] J Thorac Oncol. 2019 Mar;14(3):445-458.
[3] J Bronchol Intervent Pulmonol 2020;00:000–000.
[4] Chest. 2015 May;147(5):1275-1281.
专家介绍

陈良安
教授,博士生导师,解放军总医院呼吸与危重症医学部学术主任,全军呼吸病研究所所长,主任医师、教授。中华医学会呼吸病学分会副主任委员,中华医学会内科分会主任委员,中国医师协会呼吸分会副会长,全军呼吸病专业委员会主任委员,北京医学会呼吸病分会候任主任委员。
本文由《呼吸界》编辑 Asiya 整理,感谢陈良安教授的审阅修改!
本文完,排版:Jerry
未经许可,请勿转载


