
慢性阻塞性肺疾病(COPD)是一种异质性肺部疾病,其特征是由于气道和/或肺泡异常引起的慢性呼吸道症状,导致持续的、进行性气流阻塞。COPD急性加重(AECOPD)是许多患者的疾病的一个关键特征。急性加重更容易发生在症状较重的患者身上,并进一步增加疾病负担,以及更频繁的病情恶化的风险。因此,早期发现和诊断慢阻肺急性加重是有必要的。然而,由于 COPD加重的异质性,对它的定义一直存在争议。这些变化和争议导致了在早期识别和治疗方面的困难。

关于慢阻肺急性加重的定义的争议
慢阻肺急性加重的主要症状是气道炎症引起的呼吸困难增加、粘液产生增加和明显的空气滞留。还有其他症状,包括咳脓痰和痰量增加,以及咳嗽和喘息增加。然而,慢阻肺急性加重是具有不同病因、致病性、症状、频率、严重程度和生物标志物的异质性事件。大多数慢阻肺急性加重的定义都包含基于症状的成分和基于事件的成分。现在最广泛接受的定义是GOLD2023指出的,慢阻肺急性加重是“14天内、以呼吸困难和(/或)咳嗽和咳痰增加为特征的事件”。GOLD2023将慢阻肺急性加重严重程度划分为:轻度,患者仅需吸入短效支气管扩张剂治疗;中度,患者需要使用抗生素、全身糖皮质激素或两者兼有;重度,患者需要急诊就诊或住院治疗。现有的基于患者对症状的感知的定义缺乏特异性和敏感性。其他呼吸系统疾病或非呼吸系统疾病可能有类似的表现并导致误诊。慢阻肺急性加重的诊断往往依赖于患者的病史和症状,以及其他必要的检查。与此同时,大多数情况下很难在疾病变化的早期识别急性加重,并将急性加重与症状的日常变异区别开来。因此,许多专家主张我们需要一个新的定义,包括已证实的生物标志物,以及对有类似症状的一些疾病的鉴别。
在临床实践和大规模临床研究中,如何区分急性加重和慢阻肺症状的日常变异也存在争议。大多数研究将至少连续两天的呼吸道症状恶化并在至少连续5天后消失并恢复到每日基线水平定义为慢阻肺急性加重。慢阻肺急性加重严重度的定义也各不相同。在TORCH研究中,中度加重和重度加重分别定义为需要全身使用糖皮质激素和/或抗生素治疗及需要住院治疗。在UPLIFT研究中, 急性加重定义为恶化或新出现以下呼吸症状(咳嗽、咳痰、脓痰、喘息、 呼吸困难),持续三天或以上需要抗生素和/或全身类固醇治疗,并根据所需治疗分为轻度、中度和重度。同时,在WISDOM研究和“噻托溴铵在早期慢阻肺研究”中,下一次急性加重与这一次超过7天的时间间隔可定义为新的急性加重,否则将合并为一个。目前,对于如何确定病情恶化的开始和结束日期,还没有国际共识或标准化的定义。
慢阻肺急性加重早期识别的重要性
患者对急性加重的识别和报告情况一般较差。据报道,近50%的慢阻肺急性加重未被报告,导致了长期预后不佳。一项队列研究表明,每次急性加重都会增加后续急性加重的风险,而下一次严重恶化之间的时间间隔将会缩短。早期发现和识别急性加重以及开始进行医疗干预对于预防病情进展非常重要。一旦诊断为慢阻肺加重,越早治疗开始,患者症状缓解就越快,生活质量越好,住院风险就越低。
慢阻肺急性加重的识别
约2/3至3/4的急性加重是由病毒或细菌感染引起的,而其他1/3的急性加重是由非传染性因素引起的,包括空气污染、暴露于过敏原、治疗依从性差。慢阻肺急性加重的特征是由于触发引起的症状加重,全身炎症反应随之加重。这种炎症的爆发加重了现有的气道受限,气道阻力增加。气道和全身炎症导致呼吸困难、呼吸肌功能障碍和通气功能不全。由于COPD的异质性,很难根据临床特征对慢阻肺急性加重进行聚类。一些研究人员认为,根据气道炎症类型将急性加重分为以下内型:促炎内型(细菌优势)、辅助T型2(Th2)内型(嗜酸性优势)、辅助T型1(Th1)内型(病毒优势)和低炎症型(缺乏炎症细胞)。基于痰中炎症标记物(白细胞介素1β)和Th2 和Th1内型的血液标记物(嗜酸性粒细胞和C-X-C基序趋化因子配体10[CXCL10]),有助于识别这些内型。在这一病理生理过程的基础上,2021年,罗马会议提出以下定义:“病情加重是指以呼吸困难和/或咳嗽、咳嗽恶化(14 d内)为特征的事件,可伴有呼吸急促和/或心动过速,通常与气道感染、空气污染或其他气道刺激因素所致的局部和全身炎症反应增强有关。” 这些事件可能会危及生命,需要进行充分的评估和治疗。
相较于既往的分级标准,“罗马提议”的亮点是引入了量化指标,提出严重程度的分级(轻度、中度及重度)应基于6个临床可测量的变量,包括呼吸困难的严重程度(VAS评分)、血氧饱和度、呼吸频率、心率、C反应蛋白及动脉血气分析(如有必要)。该“提议”建议临床医生和研究人员应使用5个易于评估的参数(呼吸困难、呼吸频率、心率、氧饱和度和血清CRP)来评估COPD急性加重的严重程度。在确诊慢阻肺急性加重之前,临床医生应充分鉴别诊断,至少有28种疾病可能有与其相似的症状。其中,有三种疾病(心力衰竭、肺炎和肺血栓栓塞)需要特别考虑。同时,这些疾病和慢阻肺急性加重往往共存并相互影响。
用于评估慢阻肺急性加重的临床工具
呼吸道症状的恶化是识别慢阻肺急性加重的关键。每日症状监测被认为是捕获病情变化的准确方法。已经建立了一些量化和评估症状的标准化方法。许多研究旨在评估这些方法评估COPD病情加重的能力。慢性肺疾病加重工具(EXACT)、圣乔治呼吸问卷(SGRQ)、COPD评估测试(CAT)都得到了广泛验证,并显示了有效的患者报告结果(PRO)。SGRQ可以识别COPD的加重和缓解。然而,由于它评估时间长,患者难以完成,在临床实践中很少使用。CAT是一份调查问卷,旨在评估和量化COPD症状对患者健康状况的影响。虽然它被开发用于评估稳定期COPD受试者的健康状况,但研究发现,它作为一种简单的工具,也具有帮助识别患者急性加重风险。EXACT是在慢阻肺急性加重期间记录的症状日记。EXACT和CAT在评估急性发作频率、持续时间和严重程度方面均显示出较高的价值。然而,在临床实践中,EXACT和CAT仍然过于复杂。
目前,中国已经开展了一项注册研究,以获取COPD住院和出院后临床状况的真实数据,并对慢阻肺急性加重的早期预警模型进行了研究。最近,一种有效的COPD病情加重识别工具(CERT)被开发出来,为患者提供简单易行的指导,旨在帮助所有GOLD组的患者识别中度和重度病情加重。另一项多中心、观察性、横断面研究(NCT03556475),旨在开发和验证中国慢性阻塞性肺疾病(COPD) 患者慢阻肺急性加重发生和严重程度的多变量预测模型,研究已经完成,研究结果尚未公布。
许多研究人员开发了预后预测工具,使疾病个性化管理成为可能。但目前还没有在慢阻肺的日常诊疗中使用这样的工具。2017年发表的一项系统综述确定了27个预测COPD患者病情加重的预测模型,但这些模型均被认为效力不佳。Adibi 等人开发了一个新的模型,急性COPD加重预测工具(ACCEPT),以在个体水平上预测COPD加重的发生率和严重程度,并在 ECLIPSE队列中经过了外部验证。结果表明,它可以作为一种决策工具,以个性化治疗和预防恶化。
此外,肺功能和小气道功能测试也是评估病情恶化的有用工具。气流限制越严重,急性加重的风险就越高。ΔPEF和ΔCAT与住院病情加重的风险独立相关。通过强迫振荡技术(FOT)测量的肺功能的日间变化可能会更有意义。Zimmermann等人发现,使用FOT远程监测的SDXinsp可能是早期检测慢阻肺急性加重的敏感标志物。
慢阻肺急性加重的生物标志物
生物标志物在疾病的早期识别、疾病的严重程度和表型分类评价、疗效和预后评价方面具有很大的潜力。我们希望找到一些好的标志物来改善目前慢阻肺急性加重的诊断模式[表1]。
表1 在慢阻肺急性加重中使用的一些生物标志物
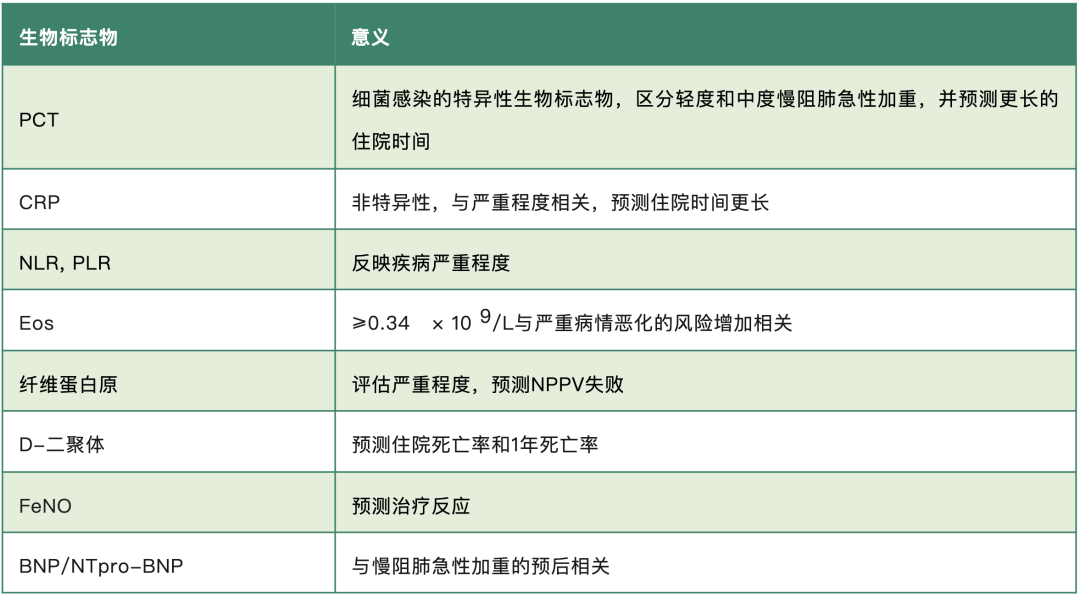
诊断和治疗
慢阻肺急性加重的发病主要由呼吸道病毒、细菌等感染引起,区分病因和提供个体化治疗是急性加重患者管理中的重中之重。
C反应蛋白(CRP)是一种急性期蛋白,是慢阻肺急性加重中研究最多的非特异性急性期蛋白。它可作为慢阻肺急性加重感染的生物标志物。然而,CRP特异性不高,并且在细菌和病毒感染中都会升高。降钙素原(PCT)和CD64是细菌感染的特异性生物标志物,对慢阻肺急性加重患者抗生素的使用具有重要指导意义。此外,Quint等人发现,血清干扰素诱导蛋白-10(IP-10)水平升高可能是鼻病毒感染的标志。
可溶性尿激酶型纤溶酶原激活物受体(suPAR)与免疫系统活性呈正相关,是一种新型的炎性生物标志物。一项荟萃分析评估了其在慢性阻塞性肺病中的临床价值。结果发现,慢阻肺急性加重患者的suPAR水平较高,治疗后水平下降。suPAR具有早期识别慢阻肺急性加重的潜力。
硫化氢(H2S)是一种气体信号分子,由肺中的多种细胞产生,参与重要的生理过程。内源性硫化氢参与了COPD的发病机制,并与疾病的严重程度和活动性相关。Saito等人发现痰/血H2S 比值在慢阻肺急性加重患者均高于稳定期COPD患者、健康吸烟者和非吸烟者。H2S比值检测慢阻肺急性加重的临界值为≥0.44。敏感性和特异性分别为93.1%和84.5%。此外,Sun等人发现地塞米松不能抑制香烟烟雾暴露的大鼠肺泡巨噬细胞中脂多糖诱导的肿瘤坏死因子-α(TNF-α)释放。然而,地塞米松联合硫化氢可显著抑制TNF-α的释放,提示外源性补充H2S可改善其对糖皮质激素的反应。
呼出气一氧化氮(FeNO)水平升高与肺功能下降和COPD症状恶化相关。FeNO可以作为预测慢阻肺急性加重患者整体治疗反应的生物标志物。FeNO200(呼出的一氧化氮,流速为200 mL/s)用于评估外周气道/肺泡炎症。虽然在慢阻肺急性加重患者中,循环嗜酸性粒细胞计数与FeNO200之间没有相关性 ,FeNO200>10ppb意味着慢阻肺急性加重患者激素治疗反应良好。
严重程度评估
PCT和CRP作为一种强大的生物标志物,也可用于评估慢阻肺急性加重患者的疾病严重程度。帕扎利等人发现不同严重程度的慢阻肺急性加重患者血清PCT水平差异有显著性。当PCT界值为0.07 ng/mL时,PCT区分轻度、中度慢阻肺急性加重的敏感性和特异性分别为82%和91%。Pazarli等人发现慢阻肺急性加重患者唾液中CRP和 PCT水平明显升高,且唾液中CRP浓度与血液中CRP浓度密切相关。唾液中CRP的测量可能是一种评估慢阻肺急性加重严重程度的无创检测方法。血清淀粉样蛋白A(SAA)是由肝细胞合成的一种极其敏感的急性反应蛋白。当受到炎症因子的刺激时,它可迅速上升,在8-12小时内达到峰值,在炎症得到控制后可迅速恢复正常。Bozinovski等人的研究显示慢阻肺急性加重患者SAA高于对照组,慢阻肺急性加重中SAA是比CRP更敏感和特异的炎症标志物。SAA与慢阻肺急性加重的严重程度相关,并可用于指导是否需要住院治疗。
纤维蛋白原作为炎症和纤维化发展以及组织损伤的关键调节因子,已被用作COPD严重程度评估的生物标志物。较高的基线纤维蛋白原与慢阻肺急性加重、COPD住院和全因死亡率的增加相关,并与慢性阻塞性肺病的严重程度相关。一项研究发现,在慢阻肺急性加重期间,纤维蛋白原水平较高,并在病情加重后40天恢复到基线水平。循环纤维蛋白原水平可用于测量慢阻肺急性加重的严重程度,在使用NPPV治疗的慢阻肺急性加重患者中,纤维蛋白原>3.55 g/L可以独立预测NPPV的失败。
慢阻肺急性加重的主要机制是炎症信号的放大,可引起红细胞形态学的改变。红细胞分布宽度(RDW)、中性粒细胞与淋巴细胞比(NLR)和血小板与淋巴细胞比(PLR)是一些简单和基本的参数,很容易从最简单和容易获得的血常规结果中获得。系统回顾提示RDW可能单独或与其他参数相结合,用于慢阻肺急性加重患者的诊断和风险分层。Koc等人发现在重症监护病房治疗的患者的 RDW明显高于在呼吸系统病房治疗的患者。NLR和PLR也可以作为COPD患者急性加重期间疾病严重程度评估的一种有用和容易获取的工具。
风险预测
症状恶化伴CRP水平的升高提示慢阻肺急性加重。一项前瞻性队列研究发现,CRP>3 mg/L结合白细胞升高(9×10 9/L )和纤维蛋白原>14 μmol/L可预测5年内急性加重的风险增加。较高的CRP和PCT水平也预示着更长的住院时间。在慢性阻塞性肺疾病(COPD)中存在嗜酸性粒细胞炎症,在稳定期疾病和病情恶化期间均有报道。在COPD患者中,血嗜酸性粒细胞水平升高(≥0.34×109 /L),严重急性加重的风险会增加1.76倍。COPD Gene研究发现,血液EOS计数≥300/μL使慢阻肺急性加重的风险增加1.32倍。
预后
心肌损伤标志物显著和持续的增加是慢阻肺急性加重危重状态的信号。大量研究证明,B型利钠肽(BNP)、n末端脑利钠肽前体(NT-pro-BNP) 和心肌肌钙蛋白(cTn)所代表的心脏生化标志物与慢阻肺急性加重的预后相关。Høiseth等人发现慢阻肺急性加重患者心肌肌钙蛋白T(cTnT)的中度升高与长期预后不佳相关。该研究包括1145例最初诊断为慢阻肺急性加重、左心室射血分数(LVEF )正常的患者。结果显示,慢阻肺急性加重患者入院时BNP升高和左心室功能保留与更差的住院预后和需要重症监护相关,可用于对这些患者进行风险分层。大多数慢阻肺急性加重患者的血液处于高凝状态,并伴有低氧血症和二氧化碳滞留。D-二聚体是纤维蛋白溶解的产物,在许多与血栓形成和溶栓相关的情况下可能会增加。血浆D-二聚体水平升高与不良结局相关。一项前瞻性研究的结果显示,血清D-二聚体水平(≥985 ng/L)是住院死亡的独立危险因素。suPAR在严重的急性和慢性疾病中升高,并与短期死亡率升高相关。对于慢阻肺急性加重患者,在30天内死亡的患者的中位suPAR水平显著高于存活的患者。suPAR水平的升高可以独立预测慢阻肺急性加重患者的30天死亡率(HR 2.0,95% CI:1.7-2.4)。
移动医疗保健在慢阻肺急性加重中的应用
移动健康(mHealth)是通过使用移动通信技术提供医疗服务,包括移动远程医疗、平板电脑、医院信息解决方案,特别是可穿戴技术。移动医疗软件与硬件的结合对COPD等慢性疾病的管理产生更积极的影响。移动健康仪器和远程监测平台可以提供关于触发慢阻肺急性加重的外部因素的信息,并能够纵向收集患者的生理和临床状态的数据。这种数字医学解决方案——通过升级对急性事件的监测——可能改进慢阻肺急性加重早期识别。
在COVID-19大流行期间,许多诊所使用远程医疗服务护理慢性阻塞性肺病患者,减少来院就诊,防止感染向高危人群传播。指南中已建议可使用远程医疗完成对疑似慢阻肺急性加重患者的评估。一个用于早期识别慢阻肺急性加重的远程监测系统应该有四个部分:第一,一个评估外部因素的装置,如家庭空气质量监测传感装置和/或各种开放获取环境数据平台的空气质量传感设备;第二,确定慢阻肺急性加重高危患者的具体问卷,并对患者症状进行纵向收集;第三,可穿戴传感器自动捕获生命体征数据(身体活动、呼吸频率、心率和睡眠 模式);第四,用于检测慢阻肺病情加重的远程患者监测技术,如肺量计仪、脉搏血氧计、电子吸入器等。使用远程监测来预测慢阻肺急性加重是遥感、个人可穿戴装备和数据处理和分析的结合,由各种人工智能(AI)方法支持协助医疗决策。共同设计的模式应包括结构化的患者访谈、卫生专业人员的核心小组、患者的共同参与和卫生专业人员为主导的讨论。经过几次迭代之后,开发人员与所有涉众共享建议的解决方案,来进行验证。然后,通过可视化相关的在线工具来改善患者的体验和长期的依从性。
一项系统回顾总结了远程监测技术对慢阻肺患者的影响。远程监测结合常规护理(8项研究,1033名参与者)对急性加重及住院次数的影响不大。远程监测可能对减少住院后再入院有积极作用。没有证据表明这些远程医疗干预措施会造成危害。另一项系统评估则发现,远程监测可以减少急诊就诊次数。事实上,远程患者监测对慢阻肺比其他慢性疾病更有效。在纳入系统评估的13项随机对照试验中,30%的患者报告住院次数减少,所有队列研究(n=9)都积极支持远程监测。
移动健康设备也被用于药物使用监测。安装在吸入器上的数字传感器可以捕捉药物使用的日期、时间和位置,从而提供缓解用药和紧急使用药物的真实数据。这些传感器定期通过智能手机或无线集线器将药物使用数据传输回服务器。该设备还可用于提高慢阻肺患者的依从性。物联网(IOT)是指设备和其他“事物”的网络,它内置了传感器、软件、电子设备和网络连接,通过无线网络通信整合这些数据,并将数据发送到云平台。一些基于移动电话的物联网(mIoT)平台已被开发并用于伴有/无呼吸衰竭的稳定期慢阻肺患者病情监测。
总之,慢阻肺急性加重给慢阻肺患者的家庭和社会带来了沉重的负担。及时识别慢阻肺急性加重将改善慢阻肺患者的最终预后。然而,目前基于特征性症状和事件的慢阻肺急性加重的定义存在争议。生物标志物和临床评估工具有助于慢阻肺急性加重的诊断和治疗。移动健康和可穿戴设备的发展将改变慢阻肺等慢性疾病的现有管理模式,特别是在COVID-19大流行期间,已显示出足够的价值。
How to cite: Zhang J, Chen FM, Wang YL, Chen YH. Early detection and prediction of acute exacerbation of chronic obstructive pulmonary disease. Chin Med J Pulm Crit Care Med. 2023;2:102-107. doi: 10.1016/j.pccm.2023.04.004.
作者介绍

第一作者:张静
北京大学第三医院呼吸与危重症医学科 副主任医师、副教授。

通信作者:陈亚红
北京大学第三医院呼吸与危重症医学科;主任医师、教授、博士生导师,博士后合作导师。北京大学第三医院呼吸与危重症医学科副主任,北京大学医学部慢性气道疾病中心副主任,科研伦理综合办公室主任。专业特长:呼吸系统常见病及疑难危重症疾病;研究方向:气道慢性炎症疾病。中华医学会呼吸病学分会肺功能学组副组长;中国康复医学会呼吸康复专业委员会常委;北京慢性病防治与健康教育研究会呼吸病学专业委员会主任委员;中国抗癌协会肿瘤呼吸病学专业委员会常委;中华医学会呼吸病学分会慢阻肺学组委员;中国医师协会呼吸病分会慢阻肺工作委员会委员;中国基层呼吸疾病防治联盟副主席;中华结核和呼吸杂志、中华健康管理学杂志等编委、中华医学杂志英文版通讯编委。承担多项国家级和省部级科研基金,获得北京市科技新星计划支持和教育部新世纪优秀人才支持计划。研究结果获得北京市科技进步三等奖和中华医学科技奖三等奖。
供稿:陈亚红;编辑:魏佩芳;审核:郝秀原
本文转载自订阅号「呼吸与危重症医学英文版」
原链接戳:深度解读|慢阻肺急性加重的早期识别和诊断
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


