
目前,肺部感染是全球首位感染致死因素,疑难危重的呼吸道感染性疾病的发病原因、传播规律与致病机制尚不完全明确。我将向大家汇报疑难重症呼吸感染性疾病诊治研究。主要围绕两个方面,一、疑难危重呼吸感染性疾病的临床与基础研究,包括重症肺炎(社区获得性肺炎,CAP / 医院获得性肺炎,HAP)、新型冠状病毒病(COVID-19);二、关于新型非抗生素治疗重症肺部感染疾病方法探究,包括间充质间质细胞 (MSCs)、间充质间质细胞外囊泡 (MSC-Evs)。
一、疑难危重呼吸感染性疾病的临床与基础研究
1、重症肺炎:
1)成人严重社区获得性肺炎(SCAP)的病因
经过两年多的研究,2022年,我牵头肺部感染学组在《Emerging microbes & infections》发布国内第一个重症肺炎领域的多中心、前瞻性临床流行病学研究,明确了目前重症CAP前五位常见病原体的分布:流感病毒23.2%(具有明显的季节性分布模式)、肺炎链球菌19.6%、肠杆菌科14.6%、嗜肺军团菌12.6%、肺炎支原体11.1%。这对我们整体处理成人SCAP起到很好的指导性作用。
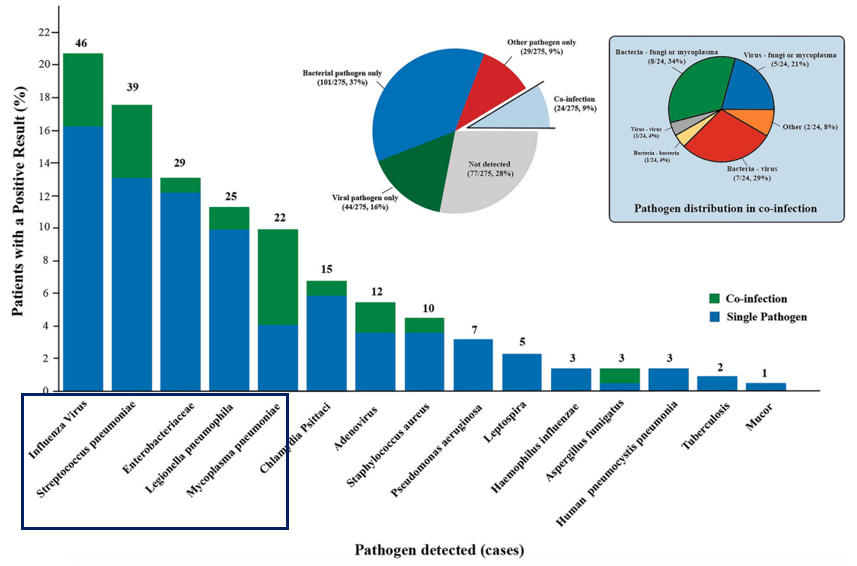
2)预测严重社区获得性肺炎(SCAP)患者预后
单纯明确临床流行病学还远远不够,对SCAP预后相关生物标志物特征的有限了解,阻碍了临床结果的改善。因此,我们同时进行了相关研究,纳入275 例 SCAP 患者的临床标本(BALF、血液、痰液),采用了宏基因组和转录组联合筛选方法,从结果中可以看到, 30 天死亡组和存活组的宿主基因表达模式存在显著差异。我们的研究确定了 12 个与结果相关的临床特征。对宿主的基本反应进行了评估,并确定了与细胞活化、免疫调节、炎症和新陈代谢相关的富集基因。值得注意的是,omics 数据、临床特征和参数被整合在一起,发现预测SCAP患者预后的生物标志物,构建包含了6个特征的模型用于预测 30 天死亡率,其 AUC 为 0.953(95%CI:0.92-0.98)。
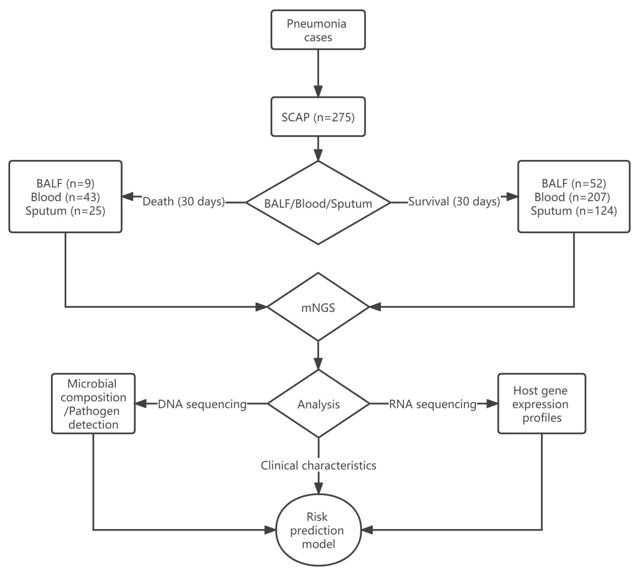
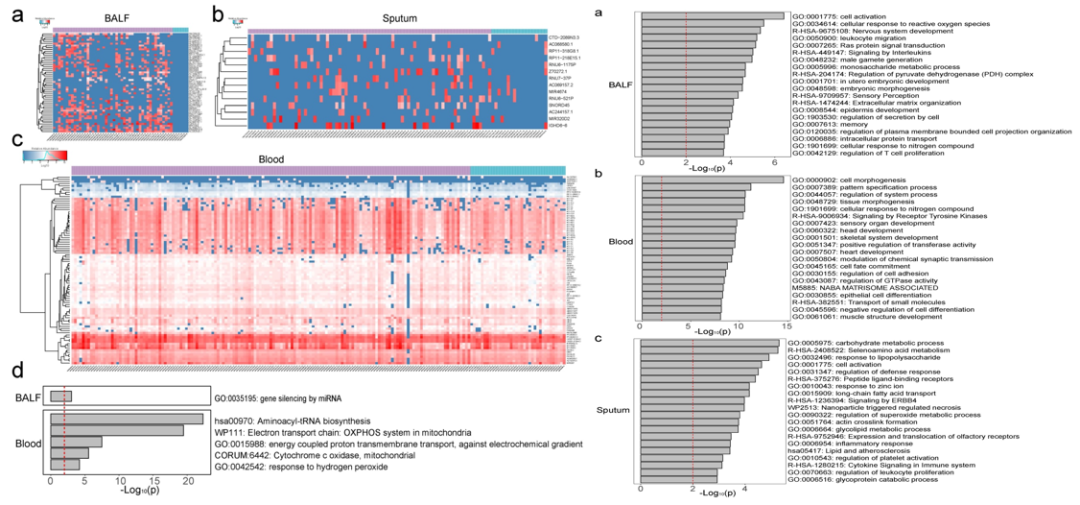
30 天死亡组和存活组的宿主基因表达模式存在显著差异:
3)MuLBSTA评估病毒性肺炎的90天死亡风险
在观测重症肺炎时,我们发现CURB-65评分常常会低估患者严重程度,尤其是对于流感等病毒性肺炎患者的病死率。因此,我们瑞金医院团队共同完成了一项工作,招募2015年5月至2019年5月期间在上海瑞金医院就诊的528例病毒性肺炎患者。采用多重实时 RT-PCR 技术检测呼吸道病毒。收集入院时的人口学信息、合并症、常规实验室检查、免疫学指标、病原学检测、放射影像和治疗情况,旨在进一步明确病毒性肺炎患者的临床特征并预测其死亡风险。
结果发现,76 名(14.4%)患者在住院 90 天内死亡。在多变量逻辑回归模型的基础上计算出预测性MuLBSTA 评分以预测死亡率,加权评分包括多叶浸润、淋巴细胞≤0.8x109/L、细菌合并感染、吸烟史、高血压和年龄≥60 岁,死亡率风险分层的临界值为 12 分,灵敏度为 0.776,特异性为 0.778,预测能力优于 CURB-65。
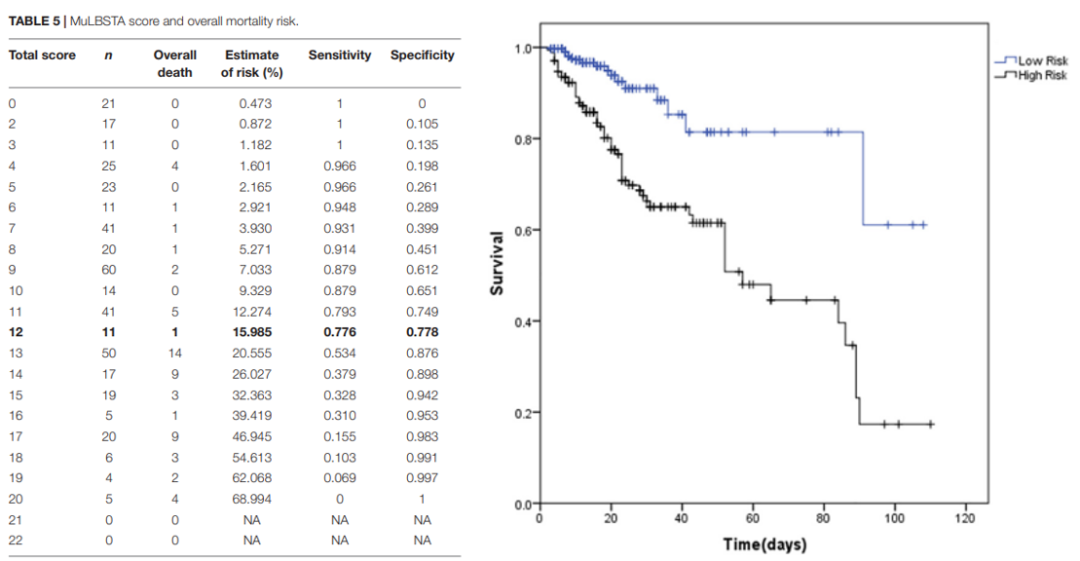
4)B7型腺病毒是国内外广泛流行的高致病性重症病毒毒株
我国2012–2015年发热哨点监测数据显示,60.7%为B7型腺病毒,国外腺病毒监测网数据也显示流行株包括B7型腺病毒,同时,高致病B组腺病毒不利用经典受体进入细胞,进入呼吸道上皮的通路目前尚不清楚。我们通过CRISPR膜蛋白功能基因组筛选rHAdV-B7宿主因子,发现了与高致病性重症相关腺病毒的新型宿主因子A,为寻找有效干预药物改善预后提供了新机制新靶点。
2、新型冠状病毒病(COVID-19)
1)疫情之初,我们瑞金医院就与武汉金银潭医院合作,进一步明确2019-nCoV肺炎的流行病学和临床特征,纳入2020年1月1日至1月20日武汉金银潭医院的99例2019-nCoV确诊病例,分析受试者的流行病学、人口统计学、临床和放射学特征以及实验室数据。目前他引 10000余次,在中国学者发表的四大顶级医学期刊论文影响力排名第6。

2)在新冠疫情中,早期筛选和识别患者是防疫关键,需要重视从疑似到确诊(或排除)的过程,我们在上海 16 个区 25 家医院的发热门诊开展了一项多中心观察性队列研究,所有在研究期间就诊的患者均被纳入研究范围。研究人员介绍了COVID-19筛查策略,然后对疑似病例进行监测和分析,直至确诊为病例或排除病例。

我们招募了2020年1月17日至2月16日期间前往发热诊所就诊的患者。在53 617名前往发热门诊就诊的患者中,1004人(1-9%)被视为疑似病例,188人(占所有患者的0-4%,疑似病例的18-7%)最终被确诊为确诊病例。分析中排除了 154 名数据缺失的患者。暴露史、疲劳、白细胞计数低于 4 × 10^9 per L、淋巴细胞计数低于 0-8 × 10^9 per L、磨玻璃混浊和双肺受累是确诊 COVID-19 的独立危险因素。本研究发现的相关独立风险因素可有助于早期识别该疾病。
3)羟氯喹的使用曾经是热点话题,我们团队的研究最终发现,无论核酸转阴时间,还是临床症状改善时间都没有获益。相反,使用羟氯喹的胃肠道等不良反应还明显增多。因此,我们研究结果发表在BMJ之后FDA指南中也进行了第一时间修改。
4)大家或许体会到,有些COVID-19患者自始至终都没有发热,也就是所谓的新冠病毒隐形感染,即SSIS(Silent SARS-CoV-2 infection stage)。还有一些患者前期没有临床症状,后续最终出现症状,转为确诊患者,我们如何回答这些关键科学问题:如,哪些患者最终会发病,哪些患者感染后不发病?机体宿主的免疫机制在其中起到了怎样的作用?
针对这个问题,我们团队运用了多组学方法进行了相关免疫学特征研究。最后发现各类患者都具有共性特点:与健康对照组相比,感染COVID-19后,PBMC中cDC、NK细胞减少,B细胞增加。然而,在持续隐性感染者中,T细胞过度活化、单核细胞功能部分受损;而潜伏期患者的单核细胞分化功能明显丧失,同时淋巴细胞耗竭。这个研究已在Cell Research上作为封面论文发表。
5)“加强针”预防危重症的内在机制?
SARS-CoV-2感染及灭活疫苗接种后抗体水平变化趋势也是一直被关心的问题。相关研究发现,超过70%自然感染新冠康复患者在感染后的12个月内,体内新冠抗体水平依然保持阳性,但呈下降趋势,Omicron亚型对于目前疫苗会产生免疫逃逸。真实世界研究显示,三针接种灭活疫苗与mRNA疫苗可显著减少有症状感染及感染后重症风险,从抗体角度来看,抗体滴度在9个月到12个月后不再具有保护作用,因此无法从这一角度回答接种三针后减少重症风险机制的这个关键科学问题。
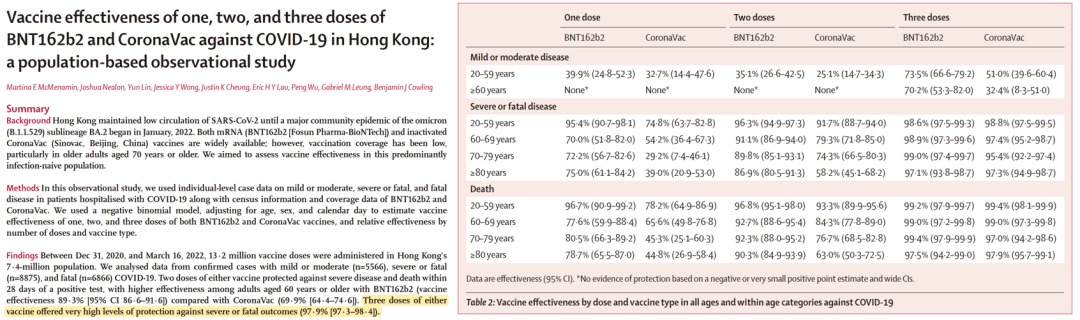
所以,我们在思考灭活疫苗对Omicron的保护机制与免疫特征?在前期研究基础上,2022年爆发的Omicron疫情中两个关键因素已改变:第一,人群已接种了不同剂次的灭活疫苗。第二,毒株已由原始株转变为奥密克戎( Omicron )BA.2.2。这带来相应的科学问题,感染者中是否存在保护性免疫反应特征?
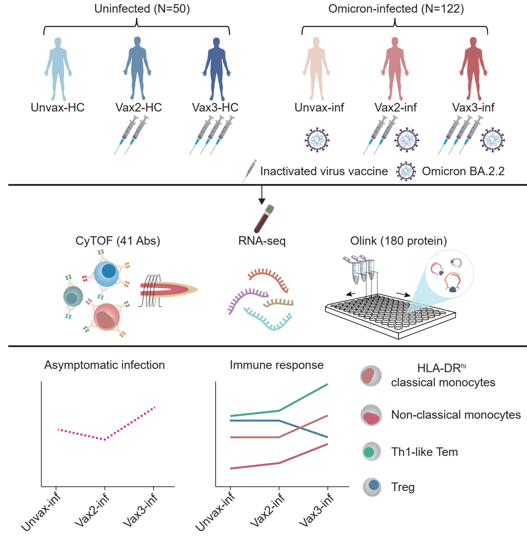
去年,上海春夏季节奥密克戎爆发流行期间,我们进行了两个队列的研究(下图),第一组分为没有接种疫苗、接种两针、接种三针后发生奥密克戎感染的,另一组是没有接种、接种两针、接种三针后没有发生奥密克戎感染的作为对照。我们做了近500例样本的多组学研究。

为了排除高龄、基础疾病对免疫的影响,我们入组患者年龄在18至65岁之间,性别、BMI等相似;排除恶性肿瘤、慢性肝肾疾病或免疫缺陷等严重合并症。相关研究最近已被《Cell》正式接收、上线。研究结果提示,提示打了三针加强针后,感染人群中,中性粒细胞增加;感染组中经典与非经典单核细胞下降,但接种三剂疫苗出现明显回升,同样,树突状细胞(DC)也存在同样的现象。但是免疫抑制的细胞,包括PD-1、CTLA-4,在接种第三针后数量下降。
整体来看,三次接种促进急性反应期中单核细胞分化及Th1反应包括:促进感染后CD4+ T细胞活化;促使CD4+T细胞向Th1类型分化;同时,在触发感染急性期,加强单核/树突状细胞的分化与活化,从而对感染后发展为重症、危重症产生一定的保护作用;而且激活的先天与获得性细胞免疫或可有助于预防感染后症状的发生。
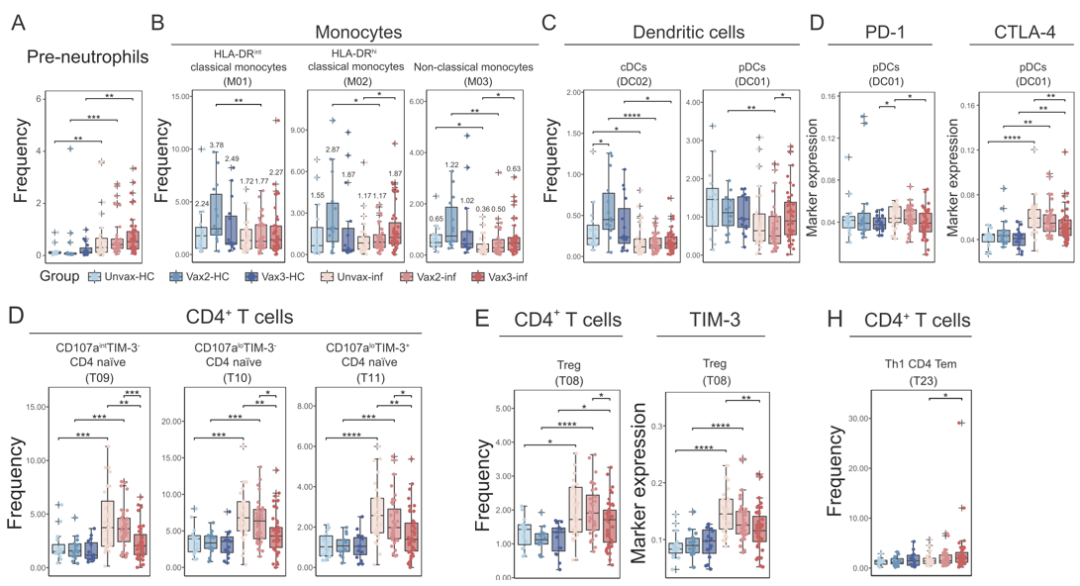
我们也分析了有症状、无症状和疫苗接种的关系,和之前的研究一致,我们也发现感染者接种三针疫苗后,与没有接种或者接种两针疫苗组相比,其无症状感染者的比例下降。
从另一个角度训练免疫(trained immunity)思考,。健康对照组接种三针疫苗或接种两针疫苗与没有接种疫苗相比,共有168个差异基因;而感染者接种三针疫苗与接种2针疫苗或者没有接种疫苗相比,一共有389个差异基因,两者的“重叠部分”共有33个差异基因。
这33个基因有什么特征?我们发现,其中有19个基因是在单核细胞里面表达最高,进一步做PPI的基因互作分析,共鉴定了15个关键的node基因,包含TREM1、C5AR1和FOSL1等调节单核细胞活化的关键基因。其中,TREM1被证实在微生物感染过程中通过促进单核细胞活化的发挥抗感染功能。这些结果提示,疫苗引起单核细胞的训练免疫机制在病毒感染过程中发挥了重要作用。
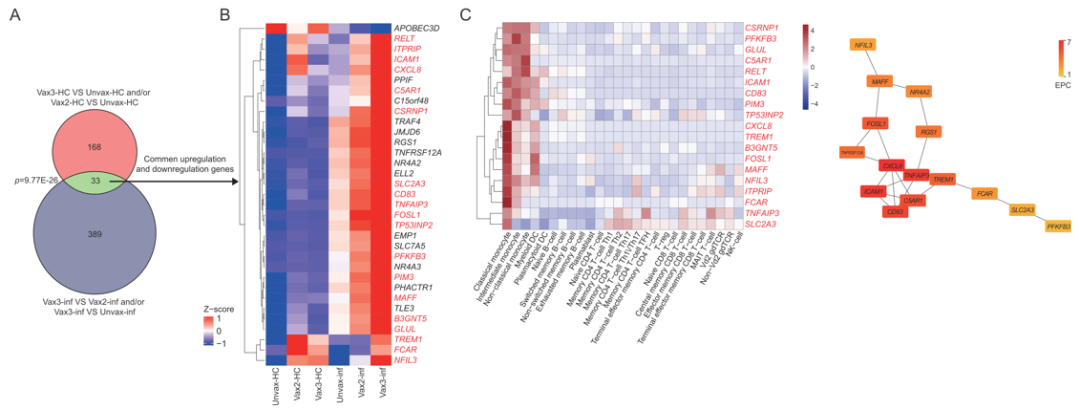
最后,在加强疫苗接种诱导单核细胞活化和分化方面,我们得到两个相关的模块,其中较大的模块包含三个子模块:先天免疫激活,T细胞或者NK细胞活化、体液免疫;而更小的模块主要包含调节性T细胞增殖。这些结果提示:三针加强针疫苗可以诱导单核细胞的活化和分化,从而在Omicron病毒感染的情况下形成潜在的保护性免疫反应。
使用下图简要总结一下,接种加强针之后如何起到保护重症危重症的作用?主要是单核细胞,无论是经典的还是非经典的单核细胞明显活化、增强;诱导Th1反应;抑制Treg的增殖。综合来看,一些核心的固有免疫和细胞免疫研究结果回答了这个科学问题。
二、新型非抗生素治疗方法——间充质间质细胞及其细胞外囊泡(MSCs & MSC-Evs)
尽管肺部感染性疾病方面已经研发出大量抗感染药物,但重症感染的死亡率仍然居高不下、抗生素使用的耐药情况逐年恶化,因此我们思考,除了抗感染药物外,有哪些其他干预措施?
我们团队自2008年开始探究非抗生素治疗新模式,发现MSCs & MSC-EVs是有广泛应用前景的非抗生素治疗手段。
在ARDS模型中,发现MSCs与Ang1肺损伤治疗中具有协同作用,Ang-1mRNA维持血管内皮细胞的完整性,MSC-Evs降低肺蛋白通透性、减轻炎症。KGF-siRNA预处理可部分消除MSCs释放MVs的治疗作用。在铜绿假单胞菌肺炎模型中也有效果。
MSC-Evs有何临床转化研究?目前发现MSC-EVs具有与MSC相似的表型和功能效应,但干细胞等还有一系列问题需要克服,如制备、存储、运输,以及成瘤风险、副作用、注射方式等担忧。
在这个基础上,我们重点关注、开展了雾化MSC-Evs的 I/II期临床研究,目前hMSC-Exos雾化吸入治疗ARDS完成了爬坡试验,已完成前三组即18例;也在进行 hMSC-Exos雾化吸入治疗耐药菌肺部感染所致ARDS的有效剂量探索,该部分尚未揭盲,已完成26例,预计今年年底、明年上半年完成全部相关研究,期待与大家分享研究结果。
致谢:上海市呼吸重症感染重点实验室、上海交通大学医学院附属瑞金医院呼吸与危重症医学科、病毒室、微生物科;合作部门和团队:陈赛娟 诸江 余山河 陈仕俊-国家转化医学研究中心(上海)、徐金富-上海市肺科医院;张静-复旦大学附属中山医院;朱迎钢-复旦大学附属华东医院

专家介绍

瞿介明
医学博士,主任医师,二级教授,博士研究生导师,上海交通大学医学院附属瑞金医院党委书记。中华医学会呼吸病学分会主任委员、中国医师协会呼吸医师分会副会长、上海市医师协会呼吸内科医师分会会长、上海市医学会呼吸病学专科分会第十届主任委员、上海市呼吸感染性疾病应急防控与诊治重点实验室主任、上海交通大学医学院呼吸病研究所所长等。研究方向及成果:呼吸系统感染性疾病的病原学机制及呼吸系统危重症的干预、机制探索及临床应用研究。作为负责人承担国家自然科学基金项目、科技部国家重点研发项目、科技部国家重点基础研究子课题等十余项课题。获上海市科技奖进步一等奖,国家教育部科技进步二等奖、上海市科技进步二等奖等科技成果奖,在cell、the Lancet、BMJ、Cell Research等国际权威杂志作为第一和通讯作者发表SCI论文130余篇,IF 1100余分,他引2万余次,主编或者副主编10部专著。
本文由《呼吸界》编辑 Jerry 整理,感谢瞿介明教授的审阅修改!
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


