
编前语
PCCM疑难病例讨论直播重磅归来!受新冠疫情等因素影响日子里,同行们亲历、见证了呼吸学科的诊疗管理水平的发展变化,其中危重症、疑难病例的救治经验尤其宝贵。在近一年时间里,《呼吸界》后台经常收到过许多读者的留言,他们反复询问PCCM疑难病例讨论直播何时再启,感谢呼吸界同行的信任和厚爱。
10月9日19:00,呼吸领域极高水平的MDT——「PCCM疑难病例讨论」直播在中日医院开讲第一期,这是一位新冠危重症患者,抗病毒时机已超时间窗怎么办?呼吸支持如何选择?
男性,58岁 ,河北省保定市人,2022-12-24入院,2022-12-25转入MICU。
主诉:发热伴咳嗽、咳痰、呼吸困难15天,加重8天。
现病史:患者15天前(2022.12.9)发热,Max 39℃,伴畏寒,伴咳嗽、咳痰、呼吸困难、咽痛,自服布洛芬、阿莫西林等药物治疗。8天前(12.16)仍有发热,体温 39℃,伴呼吸困难加重,就诊于当地医院,指脉氧80%(未吸氧),予吸氧、甲强龙抗炎以及抗细菌感染。2022-12-21测鼻咽拭子新冠核酸 :阳性,血常规及炎症指标:白细胞、淋巴细胞正常,C-反应蛋白升高,降钙素原正常。胸部CT:双肺胸膜下多发磨玻璃影。血气分析(吸氧条件不详):pH 7.48,PaCO2 29mmHg,PaO2 56mmHg。1天前复查胸部CT提示双肺病灶较前加重,遂转入我院急诊,予高流量吸氧+莫西沙星治疗。复测新冠核酸:阳性,血常规及炎症指标:白细胞升高,淋巴细胞较前下降,CRP较前明显升高,PCT正常。血气分析(面罩15L/min):pH 7.47,PaCO2 32mmHg,PaO2 71mmHg。凝血功能:D-D、FDP明显升高,起病以来,精神、食欲、睡眠欠佳,大小便正常。
既往史:2型糖尿病 1年,空腹血糖约7mmol/L;未接种新冠疫苗
个人史、婚育史、家族史无特殊。
体格检查:体温37.2℃,脉搏93次/分,呼吸23次/分,血压116/55mmHg,SpO2(HFNC FiO2 1.0,45L/min)93%;神清,精神差,查体欠配合;双肺呼吸音清晰,双下肺可闻及湿啰音;心腹查体无特殊,双下肢无凹陷性水肿。
外院胸部CT
2022-12-16(起病7天)
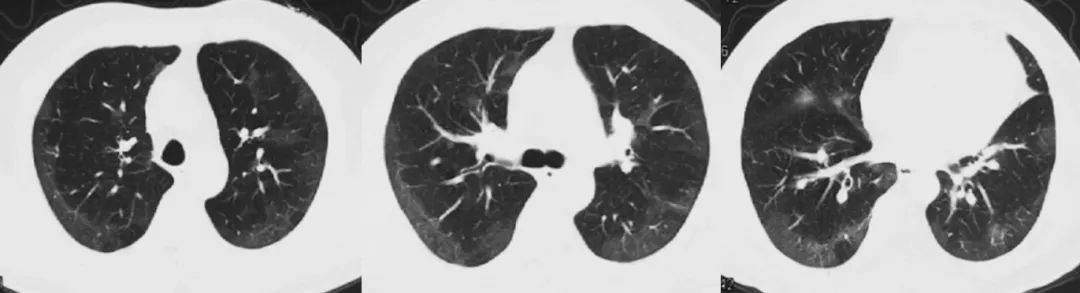
2022-12-21(起病14天)
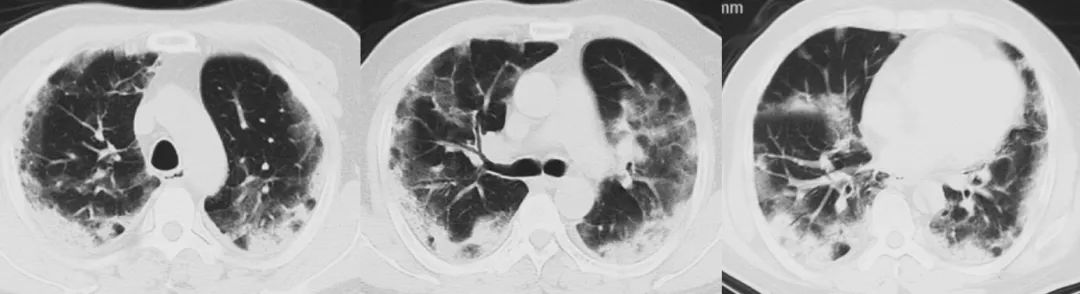
病例特点总结
中年男性,新冠流行期,急性起病,发热伴咳嗽、咳痰、进行性加重的呼吸困难,既往2型糖尿病病史;未接种新冠疫苗,查体:SpO2(HFNC:FiO2 1.0)93%,双下肺闻及湿性啰音,咽拭子新冠核酸:阳性,血常规:白细胞升高、淋巴细胞减低、CRP升高、PCT正常,胸部CT:双肺弥漫磨玻璃影、斑片影及实变影,7天内进展迅速,血气分析:氧合指数89mmHg,呼吸性碱中毒。
入院诊断
新型冠状病毒肺炎(危重型)
急性呼吸窘迫综合征
2型糖尿病
治疗
一、第一阶段(2022-12-25至2023-1-8):早期强效抗炎,撤离ECMO
主要包括:呼吸支持、抗病毒、抗细菌、抗炎、抗凝、其他脏器功能评估与支持等方面。
1. 呼吸支持:
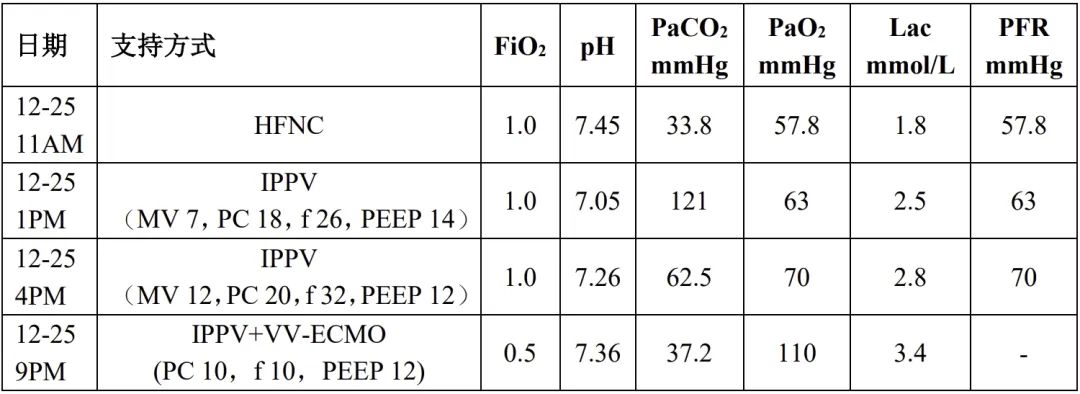
讨论要点:ECMO上机指征及模式选择?
黄琳娜大夫:目前呼吸支持条件高,上调PC、呼吸频率、PEEP、FiO2已无空间,且会造成气压伤、CO2潴留、循环障碍等风险,肺复张同样存在上述问题。俯卧位通气是改善氧合及保护右心的很好通气策略,可试用。若俯卧位无效,Ⅱ型呼衰持续不纠正,可考虑行ECMO。患者同时合并循环异常,考虑既往无肺动脉高压、右心功能不全及肺栓塞证据,我们判断患者可能为ARDS所致急性肺源性心脏病,因此VV-ECMO通过纠正低氧及CO2潴留后右心功能及循环可能得到很快改善,因此我们并未选择VA或VAV-ECMO支持。
这个病人在选择VV-ECMO模式是最合适的,而VA是非常危险的,因VA-ECMO通常为下肢引血及下肢回血,因此“富氧”静脉血主要供应患者下半身,而供应心脏和大脑是为经患者自身肺后的“乏氧”静脉血,可能会因为低氧造成严重心脑血管事件。所以在选择VA-ECMO时不仅要评估心脏循环功能,还要评估肺的氧合能力。这个病人新冠后ARDS,自身肺功能很差,所以不应选择VA-ECMO。
2. 抗病毒:无(超窗)
3. 抗细菌:哌拉西林/他唑巴坦经验性抗感染,积极获取病原学
4. 抗炎:地塞米松+巴瑞替尼+托珠单抗(8mg/kg,×2剂,间隔48h)
- 抗炎疗效评估
①炎症指标
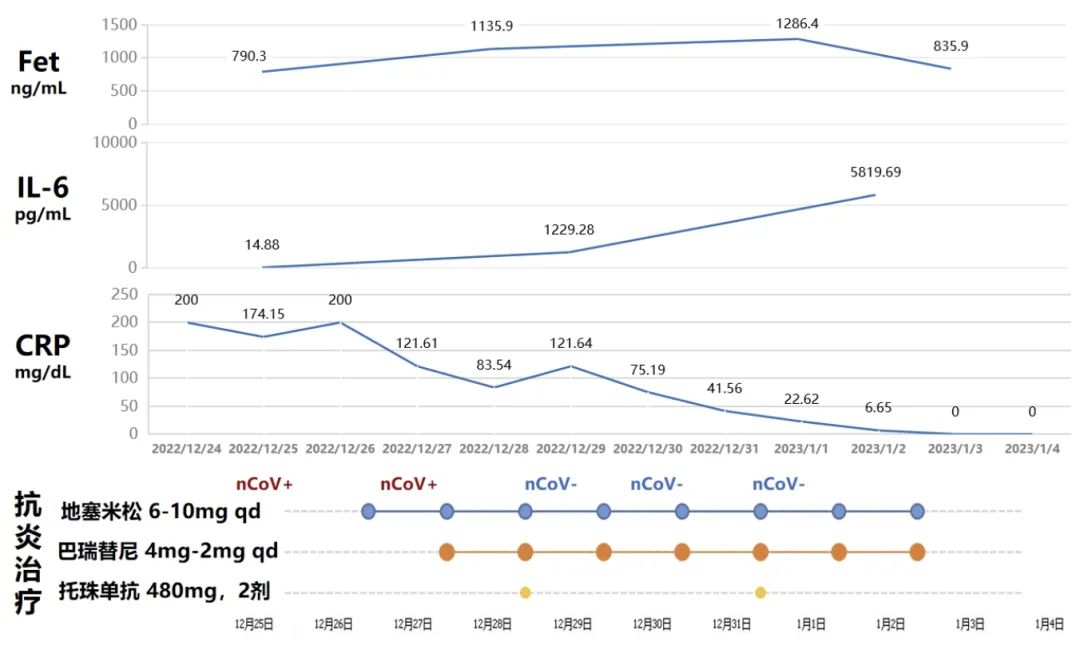
②呼吸功能评估
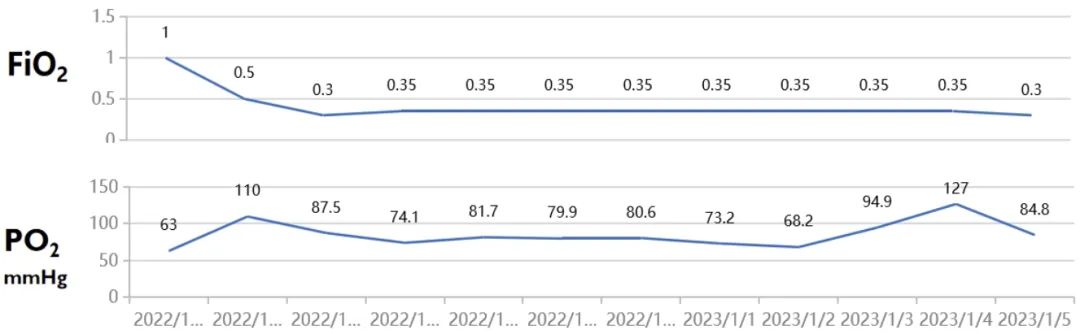
③ 影像学评估
2022-12-30(起病21天,入ICU6天,ECMO支持5天)
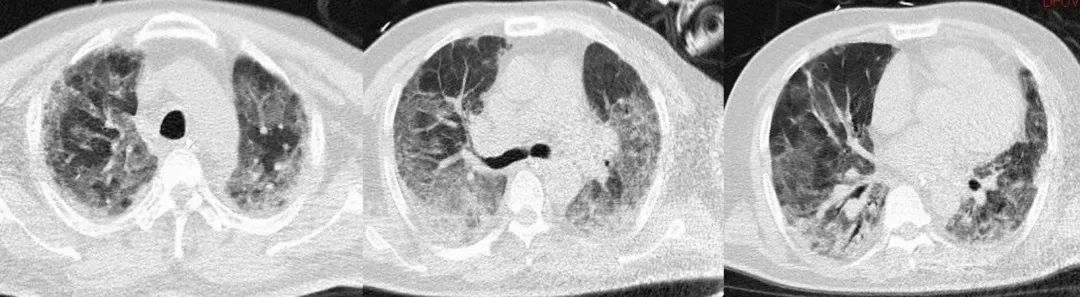
2023-1-3(起病25天,入ICU10天,ECMO支持9天)
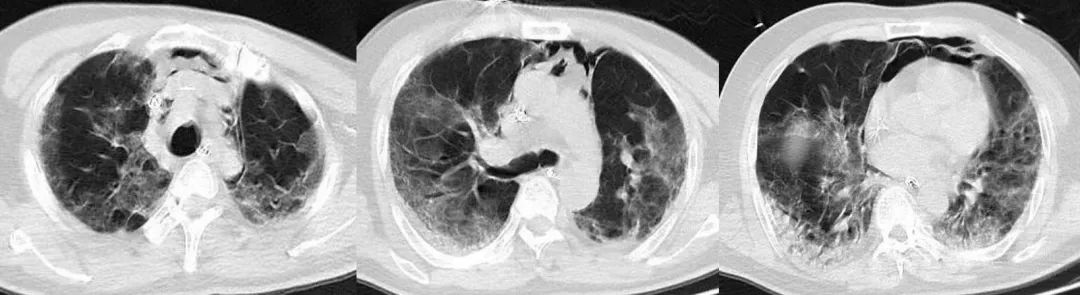
5. 抗凝:低分子肝素4000iu qn
ECMO第3天(12-28)进行了气管切开;第5天(12-30)出现气压伤,下调呼吸机压力支持水平,加强了镇静镇痛。ECMO第10天(2023-1-9),患者出现寒战,休克,白细胞明显升高,血红蛋白(100g/L→57g/L),考虑ECMO导管相关血流感染,并发不明原因血红蛋白下降,于1-4夹闭ECMO气源后患者呼吸机支持参数不高,1-5撤除ECMO,撤离后患者PFR 210-220mmHg。ECMO撤机后为防止气压伤加重,加强镇静、镇痛;维持低水平呼吸机参数;继续其他肺外脏器功能维护及支持。
讨论要点:撤离ECMO时机抉择?
黄琳娜大夫:需要考虑两个问题:原发病是否控制及是否出现严重并发症。在并发症方面需考虑感染、出血、气压伤的主要矛盾。
ECMO 支持7天后感染风险大大增加,而我们经历的大部分ECMO导管相关BSI并没有找到明确病原证据,且此次休克无法用其他部位感染解释,因此考虑最可能是ECMO导管相关BSI,而治疗除抗感染外最彻底的办法就是尽快拔除或更换ECMO导管。
患者Hb下降不能除外与抗凝过度导致隐匿部位出血相关,患者Hb下降较快,我们只能减量或停用抗凝,而抗凝不足则会导致血栓形成造成凝血因子进一步消耗从而加重出血造成恶性循环,此时ECMO抗凝管理较为困难。
患者虽然有较严重的纵隔气肿,但并未发生气胸,而且患者氧分压及影像明显好转。因此,我们权衡气压伤加重及感染、出血的风险,选择撤离ECMO并加强镇静镇痛防止气压伤加重。
二、第二阶段(2023-1-9至2023-1-25):炎症反应持续,启动第二轮抗炎
患者在ECMO撤离后第4天,1-9凌晨再发病情变化,主要表现为突发休克,需要大剂量升压药维持,同时伴氧合的下降。我们进行了休克相关评估:患者入院后累积正平衡9000ml,WBC、PCT未见升高,LY无明显降低,气管镜下分泌物不多。D-Dimer升高,床旁彩超:下腔正常,但吸气塌陷率>50%,左心及右心均未见异常。下肢肌间静脉新发血栓,未见气胸及大量胸腔积液。
讨论要点:如何鉴别本患者休克类型?
郭翎茜大夫:休克是ICU患者最常见的病情变化之一,也是影响患者预后的关键因素。在ICU内最常用的休克分型是按照病理生理类型进行鉴别。
低血容量休克:患者在入院前期是液体正平衡,床旁超声提示下腔宽度正常,吸气塌陷率>50%,未发现新发出血部位,暂不考虑。
心源性休克:患者液体正平衡,NT-proBNP升高,但查体无左心衰体征,床旁心超提示LVEF正常,且未见左室舒张功能异常,暂不支持。
梗阻性休克:患者无新发气胸、心包及胸腔积液等肺外梗阻性因素。虽然患者D-Dimer升高、下肢肌间静脉血栓形成,但床旁心超检查右心无扩张,肺动脉无增宽,高危肺栓塞引起的休克暂不支持。
分布性休克:患者无急性过敏、疼痛等影响血管张力的因素。结合前期高度可疑ECMO导管相关血流感染并发感染性休克情况,此次患者体温升高、有创机械通气时间长、深镇静镇痛状态存在痰液引流障碍风险,我们考虑感染性休克可能性大。但患者白细胞及PCT无明显增高、气管镜下无明显分泌物、BALF病原学阴性,同时需排外其他部位感染来源。
治疗上,尽管未找到明确感染证据,但患者的休克仍持续,因此我们先按感染性休克处理:①调整抗生素:多粘菌素+替加环素+阿米卡星+万古霉素覆盖ICU内3种常见MDR G-杆菌;②加用氢化可的松;③更换PICC、动脉/拔除血滤管;④积极液体复苏。
1-10经补液治疗后患者循环趋于稳定,我们为了寻找其他感染灶并评估肺内病变情况,外出胸腹盆CT检查提示:双肺病灶较前渗出增多,腹盆腔内未见明显异常。
2023-1-3胸部CT
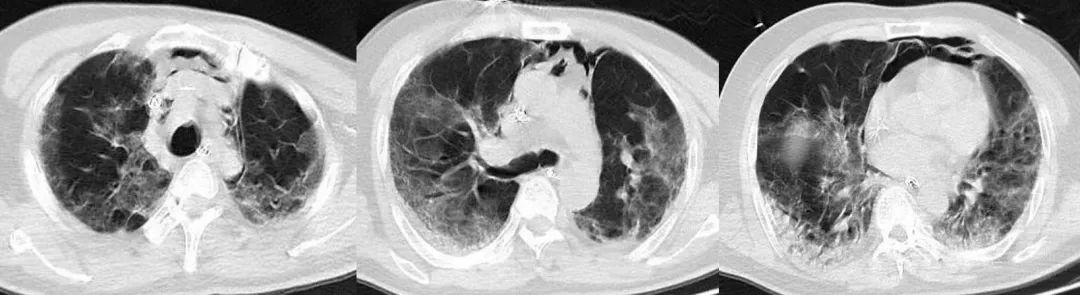
2023-1-10胸部CT
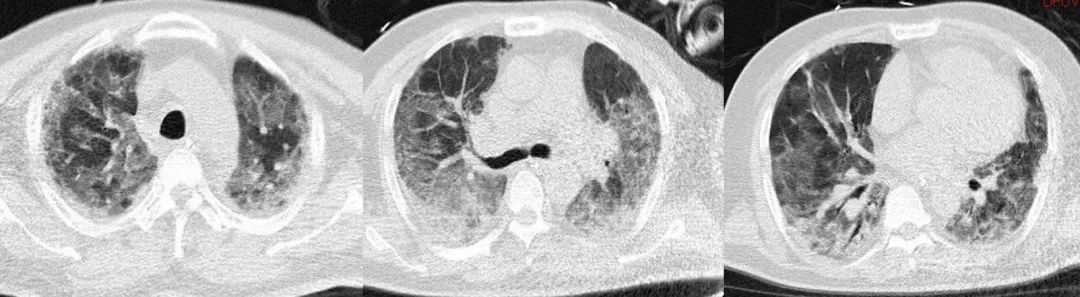
讨论要点:患者无肺内及其他部位感染证据,调整抗生素及液体复苏后循环仍难以稳定,复查CT提示原部位、原性质渗出影,下一步休克治疗方案选择?
王业明大夫:此次感染性休克未找到支持继发细菌或真菌感染的证据,但该患者既往糖尿病史,无新冠疫苗接种史,是新冠感染继发重症的高危人群,发病后未行抗病毒治疗,经抗炎治疗暂时抑制了炎症反应,但随着抗炎治疗的停用,体内存留的新冠病毒可能仍在刺激着患者产生炎症反应。
患者BALF新冠病毒阳性,我们考虑到是否由于viral sepsis、炎症反应持续导致休克可能。
因此,我们加用了Paxlovid抗病毒,同时增加了抗炎强度,再次应用了两次托珠单抗,由于兼顾后期感染问题将激素逐渐减量,继续给予补液后休克纠正。复查CRP、Fet、IL-6明显下降;复查胸部CT双肺渗出较前吸收;氧合逐渐好转,氧合指数稳定于200~mmHg。但患者镇静镇痛减量后呛咳明显,降低PC水平后呼吸频率明显增快,无法撤离有创呼吸机。
三、第三阶段(2023-1-26至2023-3-15):继发感染、新冠后期间质性肺炎处理
1-26患者BALF细菌培养提示:耐碳青霉烯的鲍曼不动杆菌(CRAB),抗生素调整为多粘菌素+舒巴坦3g q8h。1-30患者出现感染性休克,留取PICC及外周血培养提示:CRAB(PICC导管血及外周血)及分散范菌(PICC导管血),抗生素调整为多粘菌素+舒巴坦3g q8h+替加环素。
讨论要点:肺内及血流CRAB感染的流行病学、药敏、“最佳”药物治疗方案?
微生物室鲁炳怀教授:鲍曼不动杆菌在临床中致病力相对较弱,其突破血管能力也较弱。因此,其在肺内分离率高,但血液中的分离率仅为2.5%-3%。另外,鲍曼不动杆菌耐药率高,碳青霉烯耐药率高达80%以上;在肺移植科和ICU比例会更高,和鲍曼不动杆菌本身具有天然耐药机制同时又有诸多获得性耐药机制相关。此外,患者在前期高强度的抗感染治疗同时血培养阳性,考虑通过PICC导管短时间内大量入血。
陈玥临床药师:根据现有证据,鲍曼不动杆菌感染尚无任何药物或组合方案被证明最优。在CRAB感染的危重患者中,提倡早期联合治疗,组合方法旨在克服多种耐药机制并抑制进一步的耐药性。协和医院的一项回顾性研究证明多粘菌素联合高剂量舒巴坦优于其他方案。既往研究表明鲍曼不动杆菌血症病死率超过50%,替加环素在最新的IDSA指南已不推荐用于CRAB血流感染。但对于本患者,当时考虑病情危重且同时合并肺内及血流CRAB感染;此外,多粘菌素+舒巴坦组合抗菌谱窄,因此在多粘菌素、舒巴坦基础上联合了替加环素,现在看来可能并无必要。
患者2-17,3-6,3-16动态复查胸部CT,双肺渗出逐渐吸收,气压伤好转但残留小叶间隔增厚、网格影及支气管扩张等间质性肺炎表现;因患者呛咳明显、有创呼吸机撤离困难,予强效镇咳治疗并于2-12加用尼达尼布,同时进行脱机训练及肢体康复,至3-2完全脱机。6-19入院随访,遗留膈肌功能障碍及轻度间质性肺炎,继续呼吸康复。
讨论要点:新冠肺炎后期抗纤维化治疗的必要性?
王诗尧大夫:半数重症新冠患者会出现持续30天以上的肺间质浸润,包括网格影及牵拉支气管扩张等,其中1/5的患者会持续存在间质改变,但在长期随访中发现,大部分病人的间质改变可以逐渐好转。关于此类患者的抗纤维化治疗,大部分人不建议抗纤维化治疗。但对于既往存在基础肺间质异常或肺间质纤维化的病人,每一次感染都可能造成AE-ILD,这类病人建议早期加用抗纤维化治疗。对于其他患者,建议观察1-3月,如果3月以上纤维化仍不吸收,患者症状明显及肺功能恶化,可考虑在经济条件允许的情况下加用抗纤维化治疗。
后续胸部CT动态变化:
2023-2-7胸部CT
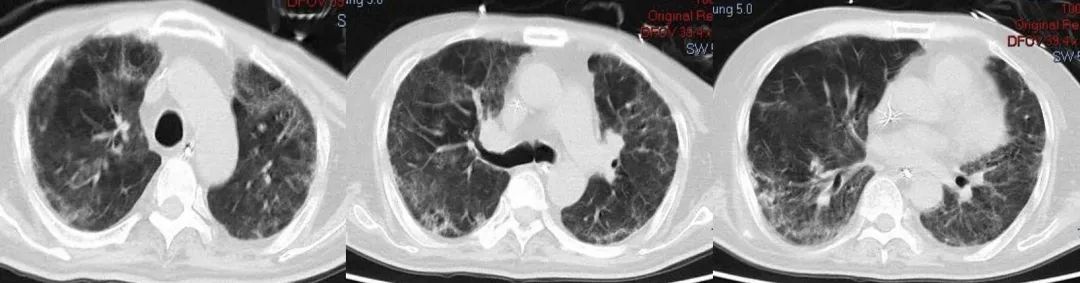
2023-3-16胸部CT
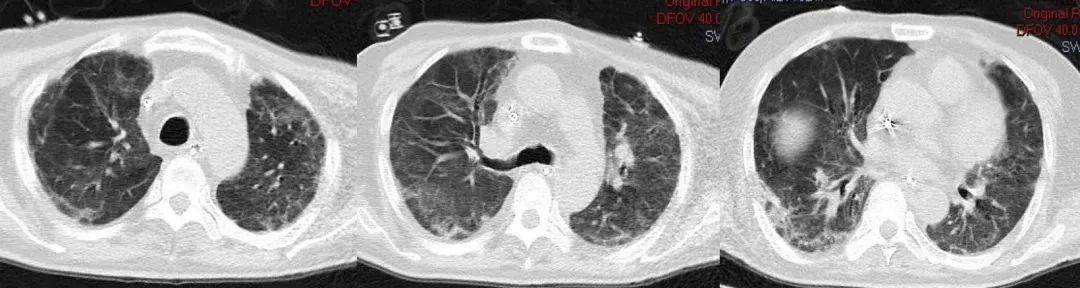
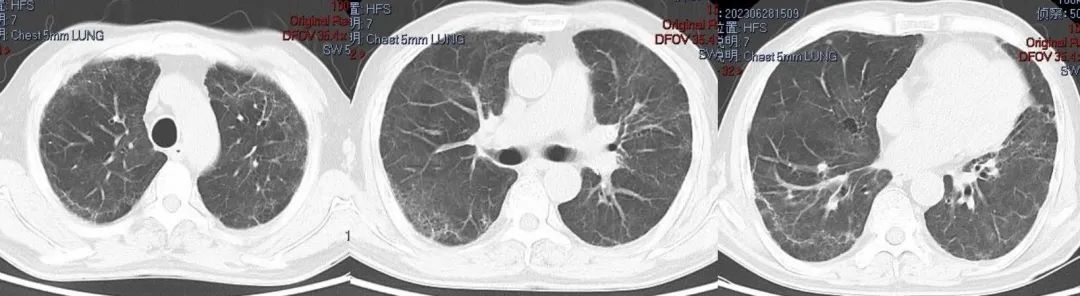
2023-6-28胸部CT
大咖发言
刘敏教授:
患者第一份CT(2022-12-26)表现为双肺胸膜下多发磨玻璃影,是典型的新冠肺炎表现。随着病程进展,胸膜下磨玻璃影、实变范围增大并出现牵拉支扩。期间患者经历了有创机械通气、ECMO等呼吸支持治疗,并经历了第一轮抗炎治疗,2023-1-3CT双肺渗出影有所吸收,但新发纵隔气肿。后患者于2023-1-10CT再次出现新发磨玻璃渗出影,不能除外合并PCP、CMV等病毒或肺水肿可能,需再次完善病原学检查。后续患者病情好转,双肺磨玻璃及实变逐渐吸收,残留新冠后肺间质浸润。在出院3个月后(2023-6-28)的随访中,双肺肺间质浸润明显好转。
詹庆元教授:
关于ECMO模式选择方面的补充:这个病人在选择VV-ECMO模式是最合适的,而VA是非常危险的,因VA-ECMO通常为下肢引血及下肢回血,因此“富氧”静脉血主要供应患者下半身,而供应心脏和大脑是为经患者自身肺后的“乏氧”静脉血,可能会因为低氧造成严重心脑血管事件。所以在选择VA-ECMO时不仅要评估心脏循环功能,还要评估肺的氧合能力。这个病人新冠后ARDS,自身肺功能很差,所以不应选择VA-ECMO。关于撤离ECMO时机的补充:在评估撤离ECMO之前要进行充分评估,首先要看原发病有没有控制,患者复查胸部CT肺部渗出有吸收,氧分压有改善,但改善得不明显,我们需要完善ECMO-CPT评估撤机可能性。另外还可通过加强镇静镇痛、降低氧耗,从而改善氧合。其中最重要的问题是权衡利弊,此时ECMO的利是改善氧合及通气,同时防止气压伤加重,弊端是感染和血红蛋白下降的问题。如果撤离后,患者氧合能维持,那就选择撤机,如果氧合不能维持,我们还要考虑其他措施,如更换ECMO导管等。
曹彬教授:
新冠肺炎是一个持续变化的疾病,应全面细致地评价整个病程中患者肺内及肺外脏器功能变化,及时发现影响患者预后的危险因素并干预。患者入院时即使患者已超出最佳抗病毒时间窗,如果仍有病毒复制,给予抗病毒治疗仍可改善患者预后,避免进一步发展成重症,这是我们做的不足之处。抗炎治疗的指征是重症肺炎合并低氧,疗效评估则需通过评价氧合改变和影像变化确定。
代华平教授:
如果药物可及,在患者发病时或入院时启用抗病毒治疗,有可能避免发展成重症。明确的肺纤维化,需要影像学有蜂窝、牵拉支扩等肺结构改变的提示,这类改变是不可逆的。但新冠继发的肺间质改变,大部分为炎症刺激所致,影像学表现为磨玻璃渗出影、细网格影及牵拉支扩等,在后续的康复过程,即便无药物干预,大部分患者最终可以恢复。该患者在住院后期应用了尼达尼布抗纤维化,3月后肺间质改变明显吸收,很难确定是自然病程还是药物作用。
王辰院士:
患者第一诊断为“重症社区获得性肺炎”,同时子诊断新型冠状病毒肺炎(危重型),两者之间是否有概念重复,我们应该避免诊断扩大化,突出病因诊断。新冠病毒会导致患者淋巴细胞减低并处于免疫抑制状态,气管插管后可能会增加预后不良风险,清醒ECMO或能成为可替代的呼吸支持方式,从而避免有创机械通气造成患者后续继发感染及大量抗感染药物造成其他脏器损伤的问题。及时启用抗病毒治疗可避免发展成重症,而在重症患者中,即使抗病毒时机已超出最佳时间窗(起病5天内),但若病毒仍在复制,给予抗病毒治疗仍可使患者获益,此外,病毒CT值仅可作为参考,不能以某个特定的cutoff值作为是否启动抗病毒治疗的指征,临床大夫应尽力为患者获取最佳药物治疗的机会,以“医学科学”为立足点,并全方位地评估患者状态,帮其获得更好的预后。我们要在“促防诊控治康(健康促进、预防、诊断、控制、治疗、康复)” 六个领域,以“语药械食居环(语言、药物、刀械、饮食、起居、环境)”六个“法宝”,形成“六合格局”,全方位照护健康。
作者介绍

黄琳娜
中日友好医院呼吸与危重症医学科,主治医师,医疗组长。中国医学会呼吸病学分会(CTS)认证的PCCM专科医师。熟练掌握多种呼吸系统常见疾病的诊治,尤其是呼吸衰竭的救治、呼吸支持技术等ICU多种脏器监护与支持技术。以重症感染为主要研究方向,建立及管理科室重症流感、重症COVID-19、重症侵袭性曲霉菌感染、重症肺孢子菌肺炎及免疫抑制肺炎数据库。以第一作者及通讯作者发表SCI论文10篇,中文核心期刊论文多篇。作为子课题负责人参与中国医学科学院项目1项,参与科技部国家重点研发计划1项。

肖仁森
南昌大学第一附属医院PCCM科 主治医师;中日友好医院PCCM专培学员 专培3年级。
识别下方二维码
进入《呼吸界》直播间观看回放

- 感谢泰德制药对本期PCCM疑难病例讨论直播的大力支持
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


