
急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是一种多种病因引起的急性、弥漫性炎症性肺损伤,是全身炎症反应在肺部的表现,组织病理学常表现为弥漫性肺泡损伤(diffused alveolar damage,DAD)。ARDS在ICU中的发病率约5-10%,常在急性打击后一周内出现单纯氧疗难以纠正的低氧血症,氧合指数显著下降,胸片或CT呈双肺渗出影。ARDS病死率高达40-50%,是严重威胁人类健康的一种呼吸系统综合征。
从1967年Ashbough首次提出ARDS的概念,到1988年的Murray肺损伤评分量化了肺损伤的严重程度,到1994年欧美联席会议统一了全球的ARDS-AECC标准,再到2012年诊断条件更为清晰且实用的柏林定义,ARDS的诊断标准经历了多次变更。截至2022年,全球公认的仍是2012年的柏林定义。具体如下:①起病一周内有明确的危险因素(如肺炎,脓毒症等),或在1周内出现新的/突然加重的呼吸系统症状(呼吸困难);②双肺渗出影,不能用肺不张、肺结节或胸水解释。③呼吸衰竭不能完全用心力衰竭或液体过负荷解释,需要行客观检查(如心脏超声)已排除高静水压性肺水肿;④氧合指数,在CPAP/PEEP≥5cmH2O的前提下,氧合指数(PaO2/FiO2,P/F)≤300mmHg。其中根据P/F的水平将ARDS患者分为轻度中度和重度。轻度ARDS:200mmHg<P/F≤300mmHg(CPAP或PEEP≥5cmH2O),中度ARDS 100mmHg<P/F≤200mmHg(PEEP≥5cmH2O), 重度ARDS:P/F≤100mmHg(PEEP≥5cmH2O)。
ARDS本身是个临床综合征,诊断缺乏金标准,不能单纯依靠氧合指数甚至是否存在弥漫性肺泡损伤的病理表现来确诊
该定义虽然在全球范围内对ARDS的诊断标准达成了共识,也有利于开展同质性的临床研究,但经过多年的临床实践后发现该定义也存在诸多局限性。原因是ARDS本身是个临床综合征,诊断缺乏金标准,不能单纯依靠氧合指数甚至是否存在弥漫性肺泡损伤的病理表现来确诊。其次,诊断ARDS的四个条件均存在各自的问题。
①急性起病一周的定义,2020年以来新冠病毒感染的流行告诉我们很多患者在危险因素(如新冠感染)出现后>1周甚至2-3周的时间才出现呼吸困难,但是患者同样应该诊断为ARDS。但是急性起病的时间窗到底应该定在多长时间,目前还没有定论。
②以胸片作为诊断的条件之一,主要是方便该诊断标准可以在全球通用,从影像的准确性来讲,CT是优于X线的,但高辐射性和转运风险限制了CT的广泛应用。从影像的便捷性、安全性和连续性来讲,胸部超声又是更有优势的。另外不同的阅片者对于同一份胸片的解读也可能是不同的。同时有研究显示单侧和双侧肺浸润患者的临床预后是相似的,提示双肺浸润可能不需要作为ARDS定义的一部分。
③虽然射血分数正常更支持ARDS的诊断,但某些病因如脓毒症引起的ARDS可同时合并脓毒性心肌病,而ARDS患者同时合并心源性肺水肿也是可能的,因此不能因为存在心功能不全或容量过负荷而否认ARDS的诊断。
④关于CPAP/PEEP≥5cmH2O作为判断氧合指数的前提也一直存在争议。1994年的AECC标准,专家们认为虽然PEEP可改善分流,但效果具有时间依赖性且存在强烈的个体化,因此并未将PEEP纳入诊断前提。但2012年的柏林标准考虑到PEEP对氧合的显著影响,又将低水平的PEEP/CPAP纳入诊断条件之一。然而使用NPPV的患者仅能诊断轻度ARDS,中重度诊断的前提还是要求有创通气和至少5cmH2O的PEEP。
这种定义对临床实践显然不够友好。2016年全球最大规模的ARDS前瞻观察性研究LUNGSAFE研究显示,NPPV被广泛应用于各级ARDS患者,且也呈现出分级越重死亡率越高的趋势。因此NPPV情况下ARDS显然可以同样被分为不同严重程度的等级。另外5cmH2O的cutoff值似乎也缺乏依据,更多的来自于专家建议。例如部分研究就采纳了10cmH2O的PEEP作为诊断重度ARDS的标准。另外在医疗资源相对短缺的不发达地区或是贫困地区,血气分析以获得氧合指数也是难以企及的。
10年来很多新技术的广泛应用和高质量临床研究的实施,让我们对ARDS的诊断标准有了新的观察视角
在10年来的临床实践中,很多新技术的广泛应用和高质量临床研究的实施,让我们对ARDS的诊断标准有了新的观察视角。首先是2015年卢旺达首都基加利(Kigali)的基加利医学与健康学院的Riviello ED等人针对不发达地区缺乏血气,胸部影像、呼吸机等现状,根据2007年Rice等的研究结果(其在比较ARDS患者的SpO2/FiO2(S/F)与PaO2/FiO2(P/F)对应关系的研究中发现S/F = 64 + 0.84 x (P/F) (p < 0.0001; r = 0.89). 对应关系为P/F 200≈S/F 235,P/F 300≈S/F 315),选择以S/F替代P/F,联合胸片或肺部超声评估双肺阴影的方式诊断ARDS,其中氧合的诊断标准是S/F≤315且SpO2<95%。结果发现,在1046例住院患者的中,42例(4%)符合Kigali版本ARDS定义,39%的ARDS患者入住ICU,死亡率为50%,而按传统柏林定义则无人能被诊断为ARDS。这就是著名的Kigali校正(2015)。
其次,近10年来高流量鼻导管氧疗(HFNC)因其舒适性、高效加温加湿功能、低水平PEEP的提供等优势开始广泛应用于急性低氧性呼吸衰竭的患者中。FLORALI的研究结果更是进一步肯定了HFNC治疗急性低氧性呼吸衰竭的地位。FLORALI研究将310例急性低氧性呼吸衰竭患者随机分为HFNC,普通氧疗和NPPV组,结果发现,相对于普通氧疗和NPPV,HFNC组患者更少的有创通气时间和更低的90天病死率,在P/F<200亚组中,HFNC组的气管插管率更低。此后,随着新冠感染的全球流行,也有了更多证据提示HFNC可降低气管插管率和改善其他临床预后。随着高流量氧疗装置的广泛使用和呼吸机的相对短缺,以呼气末正压作为前提诊断ARDS意味着可能漏诊一部分ARDS患者。因此部分专家提议可以把HFNC流量30L/min支持下且符合其他柏林标准的患者也纳入ARDS诊断人群,以便更早的识别出ARDS患者,从而使早期干预试验也具有可行性。
胸部超声(LUS)因其床旁便捷性、可重复性、无创等优势已成为一种有前途的替代X线或胸部CT的成像技术,不仅可以判断患者肺水肿(ARDS最重要的影像学特征)的成因、量化不同部位的严重程度,而且在鉴别其他肺部和胸膜疾病(包括胸腔积液、气胸、实变和肺泡间质综合征)方面也表现出高灵敏度和特异性。
2023年全球该领域的专家们共同提出了ARDS的新定义
因此2023年全球该领域的专家们共同提出了ARDS的新定义(详见表1,表2和图1)。首先,作者肯定了ARDS是一种急性诱发因素导致的急性肺部弥漫性炎症损伤,导致肺泡上皮和肺毛细血管内皮通透性增加,肺水肿和重力依赖性肺不张,肺含气组织减少,进一步引起分流和死腔的增加,病理表现多种多样,包括肺水肿、炎症、透明膜形成和肺泡出血等。临床表现为低氧血症和双肺弥漫渗出影。新定义要点包括:
①诱因。由各种急性诱发因素如肺炎、肺外感染、创伤、误吸、休克、输血等所诱发。
②肺水肿起源。肺水肿的成因需除外主要由心源性、液体过负荷所引起的肺水肿,同时也需要除外主要由肺不张导致的低氧血症;
③在诱发因素出现后1周内出现急性呼吸衰竭或呼吸衰竭加重;
④胸片或胸部CT表现为双侧渗出影,或胸部超声(操作者经过良好培训)提示双侧B线或实变征象;
⑤氧合:
a HFNC或NPPV患者,HFNC流量≥30L/min或NPPV/CPAP的呼气末压力≥5cmH2O前提下,P/F≤300mmHg或S/F≤315(如果SPO2≤97%);
b插管患者,
轻度ARDS:200< PaO2/FiO2 ≤300 或 235 ≤SpO2/FiO2 ≤315(如果SpO2≤97%)
中度ARDS:100 < PaO2/FiO2 ≤200 或 148 < SpO2/FiO2 ≤235 (如果SpO2≤97%)
重度ARDS:PaO2/FiO2 ≤100 或 SpO2/FiO2 ≤148(如果SpO2≤97%)
c 未行HFNC或正压通气患者,根据SpO2/FiO2 ≤315(如果SPO2≤97%)也可诊断ARDS。

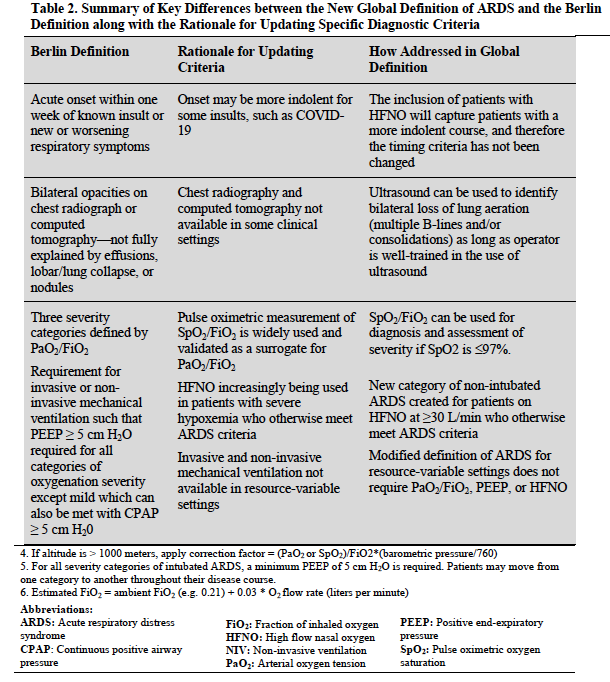
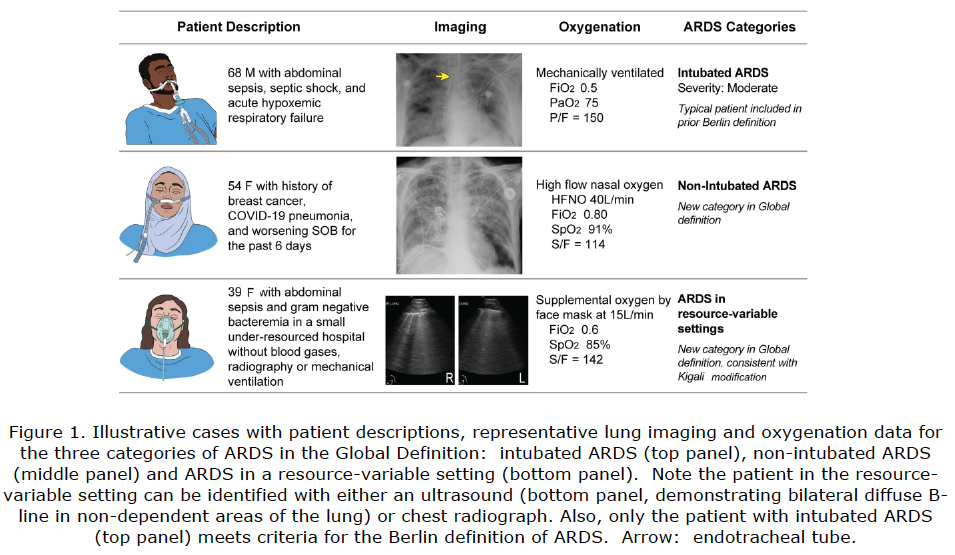
新的诊断标准虽在保留柏林标准基本组成部分的前提下做了少量修改,但对病理生理学的理解和证据并未改变。
首先,仍以7天作为急性起病的时间窗,原因是有HFNC可以更早的识别出ARDS患者。
其次,承认即便存在其他引起呼吸衰竭的疾病或病因,如心衰、液体过负荷、肺不张、胸水、慢性阻塞性肺疾病、肺动脉高压、间质性肺疾病等,只要急性呼吸衰竭不是主要归因于以上疾病,那么ARDS仍然可以诊断。
第三,在保留经典影像学胸片的前提下,纳入更为精准的胸部CT和资源受限地区的胸部超声检查作为ARDS诊断的影像学手段,扩大了影像学的实操性。
第四,根据资源的可及性将患者分为非插管患者、插管患者和资源有限环境的患者。采纳了基加利建议,不再强制要求在正压情况下判断氧合,也可不需要血气分析获得氧分压,而是用氧饱和度这样简单无创的方式判断氧合,在资源受限地区甚至也不需要正压通气和氧疗的流量限制就可以诊断ARDS,体现了诊断标准的灵活性和因地制宜的态度,具有更强的可操作性。
新定义使全球研究人员能够比较 ARDS 各类别(非插管、插管、资源有限)患者的治疗和临床预后。对资源有限的低收入国家开展ARDS相关临床研究也创造了条件。但是新的诊断标准也带来了新的问题,如无需气管插管的患者,为什么高流量氧疗的流量界定为≥30L/min,该条件下获得的P/F和有5cmH2O呼气末正压情况下获得的P/F差别有多大,可以看做同一组人群进行临床研究吗?不同肤色人群脉氧饱和度准确性和漏诊隐匿性低氧血症的问题。引入肺部超声协助ARDS的影像学诊断手段有一定的优势,例如方便快捷,无创且可动态观察,但也同时带来了与弥漫性肺实质疾病难以鉴别和操作者异质性这些为人诟病的争议,同时肺超声还可能高估ARDS,导致假阳性率的增加。
因此未来我们需要更多的临床实践去评价新诊断标准的科学性和可靠性,例如使用肺水肿放射学评估 (RALE) 评分纳入ARDS定义中等。
总之,2023年ARDS全球新定义纳入了临床实践和科学证据的变化,并促进在诊断和治疗资源(包括呼吸支持设备、胸部 X 线或CT和动脉血气分析)获取有限的环境中的应用。此外,新定义也解决了柏林定义的部分局限性,并扩展了研究 ARDS 自然病史的能力。最后,新定义为 ARDS 的研究提供了更大的灵活性,并为前瞻性研究培育了更多的研究领域。
部分参考文献
[1] ARDS Definition Task Force; Ranieri VM, Rubenfeld GD, Thompson BT, Ferguson ND, Caldwell E, Fan E, Camporota L, Slutsky AS. Acute respiratory distress syndrome: the Berlin Definition. JAMA. 2012 Jun 20;307(23):2526-33. doi: 10.1001/jama.2012.5669. PMID: 22797452.
[2] Riviello ED, Kiviri W, Twagirumugabe T,et al. Hospital Incidence and Outcomes of the Acute Respiratory Distress Syndrome Using the Kigali Modification of the Berlin Definition.Am J Respir Crit Care Med. 2016;193(1):52-9.
[3] Bellani G, Laffey JG, Pham T, Fan E, Brochard L, Esteban A, Gattinoni L, van Haren F, Larsson A, McAuley DF, Ranieri M, Rubenfeld G, Thompson BT, Wrigge H, Slutsky AS, Pesenti A; LUNG SAFE Investigators; ESICM Trials Group. Epidemiology, Patterns of Care, and Mortality for Patients With Acute Respiratory Distress Syndrome in Intensive Care Units in 50 Countries. JAMA. 2016 Feb 23;315(8):788-800. doi: 10.1001/jama.2016.0291. Erratum in: JAMA. 2016 Jul 19;316(3):350. Erratum in: JAMA. 2016 Jul 19;316(3):350. PMID: 26903337.
[4] Matthay MA, Arabi Y, Arroliga AC, Bernard G, Bersten AD, Brochard LJ, Calfee CS, Combes A, Daniel BM, Ferguson ND, Gong MN, Gotts JE, Herridge MS, Laffey JG, Liu KD, Machado FR, Martin TR, McAuley DF, Mercat A, Moss M, Mularski RA, Pesenti A, Qiu H, Ramakrishnan N, Ranieri M, Riviello ED, Rubin E, Slutsky A, Thompson BT, Twagirumugabe T, Ware LB, Wick KD. A New Global Definition of Acute Respiratory Distress Syndrome. Am J Respir Crit Care Med. 2023 Jul 24. doi: 10.1164/rccm.202303-0558WS. Epub ahead of print. PMID: 37487152.
[5] Liufu R, Wang CY, Weng L, Du B. Newly Proposed Diagnostic Criteria for Acute Respiratory Distress Syndrome: Does Inclusion of High Flow Nasal Cannula Solve the Problem? J Clin Med. 2023 Jan 29;12(3):1043. doi: 10.3390/jcm12031043. PMID: 36769691; PMCID: PMC9917973.
作者简介

黄絮
中日友好医院呼吸与危重症医学科,副主任医师,副教授,硕士生导师,医学博士;中华医学会呼吸病学分会呼吸治疗学学组委员;中国医学装备协会呼吸病学装备技术专业委员会委员;中国老年学和老年医学学会老年呼吸与危重症医学分会委员;中国康复医学会呼吸康复专业委员会呼吸与危重症医学学组委员;北京医学会重症医学分会青年委员会委员;曾任中国医师学会重症医学医师分会青年委员会委员;美国AHA心肺复苏主任导师;thorax杂志中文版编委;北京市住院医师规范化培训第二届专业委员会委员;中华医学会医疗鉴定专家库成员;国家感染防控专家库成员。
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


