一般情况
患者女性,79岁,因「发热三周」于2023年05月04日入住我院RICU。
病史情况:患者三周前不慎受凉后出现畏寒、发热,最高体温39.3℃,稍咳嗽,少量白粘痰,近日为黄脓痰,活动后气喘,04-21至我院急诊就诊,查胸部CT示肺动脉稍增宽,所示肺动脉及主要分支未见确切充盈缺损;慢支-肺气肿改变,两肺多发肺大疱,两肺多发炎症改变,两肺多发结节、斑结及钙化灶,多为陈旧性病变,双侧腋窝及纵隔多发淋巴结显示,两侧胸膜增厚,主动脉壁部分钙化,心影增大,心包少量积液。予「头孢曲松、左氧氟沙星」静滴一周,效果欠佳。后至上海xx医院住院诊治,先后予「比阿培南、可乐必妥、稳可信、氟康唑」抗感染,「盐酸氨溴索、糜蛋白酶」化痰,「甲泼尼龙40mg」抗炎,「那曲肝素」抗凝、「白蛋白」补充蛋白等治疗,效果欠佳。后转我院进一步诊治。既往有「干燥综合征」病史20余年,平时口服「帕夫林」。「2型糖尿病」病史一周,未用药。
入科查体:T 36.0℃、P 115次/分、R 32次/分、BP 140/78mmHg、SPO2 50%(吸氧7L/min)神志清,精神萎靡,呼吸促。两肺呼吸音粗,闻及Velcro罗音。心律齐,各瓣膜听诊区未及杂音。腹平软,无压痛,反跳痛,肝脾肋下未及,移动性浊音阴性,双下肢无水肿。
辅助检查:04-21本院胸部CT:肺动脉稍增宽,所示肺动脉及主要分支未见确切充盈缺损;慢支-肺气肿改变,两肺多发肺大疱,两肺多发炎症改变,两肺多发结节、斑结及钙化灶,多为陈旧性病变,双侧腋窝及纵隔多发淋巴结显示,两侧胸膜增厚,主动脉壁部分钙化,心影增大,心包少量积液。(图一)
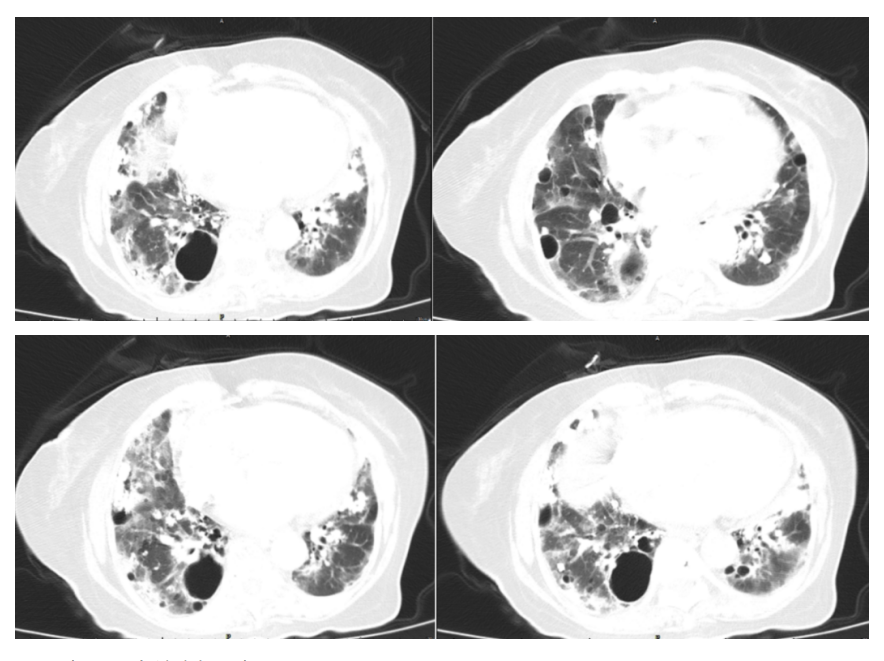
图一(04-21急诊胸部CT)
05-03 上海xx医院【痰培养】白色念珠菌、溶血葡萄球菌阳性。
05-03 上海xx医院【床边胸片】两肺渗出,钙化灶。
入院当日完善相关检查:
05-04本院【血气分析】酸碱度(PHT) 7.47↑,二氧化碳分压(PCO2T) 49↑mmHg,氧分压(PO2T) 65↓mmHg,氧饱和度(SO2) 93.3%,钾离子浓度 3.8mmol/L,钠离子浓度 145mmol/L,血糖 14.20↑mmol/L,乳酸 1.3mmol/L,全血剩余碱(BE) 10.4↑mmol/L,细胞外液剩余碱(BE-ect) 11.7↑mmol/L,标准碳酸氢盐浓度 34↑mmol/L,实际碳酸氢盐浓度(cHCO3-) 35↑mmol/L,阴离子系(AG) 9mmol/L;
【血生化】前白蛋白 47↓mg/L,乳酸 1.69mmol/L,丙氨酸氨基转移酶 22IU/L,天门冬氨酸氨基转移酶 44↑IU/L,碱性磷酸酶 148↑IU/L,白蛋白 32↓g/L,尿素 9.9↑mmol/L,肌酐 35↓μmol/L,尿酸 99↓μmol/L,乳酸脱氢酶 694↑IU/L;
【血凝】APTT 30.8秒,PT 11.5秒,INR 0.97,TT 17.60秒,Fg 2.2g/L,纤维蛋白降解产物 120↑mg/L,D-二聚体定量 40↑mg/L;
【氨基末端B型利钠肽前体】 3710.0↑pg/mL;
【血常规】白细胞计数 15.12↑x10^9/L,中性粒细胞% 92.9↑%,淋巴细胞% 3.0↓%,中性粒细胞计数 14.04↑x10^9/L,淋巴细胞计数 0.45↓x10^9/L,单核细胞计数 0.59x10^9/L,红细胞计数 3.59↓x10^12/L,血红蛋白 97↓g/L,血小板计数 194x10^9/L,C反应蛋白 184↑mg/L;
【床边胸片】两肺纹理增多增粗模糊,两肺多发斑片模糊影,右侧为著,两肺中下野多发斑片结节状钙化灶;两侧胸腔少量积液可能;心影增大,主动脉迂曲伴壁钙化;(图二)
图二(05-04床边胸片)
入院诊断
重症肺炎、急性呼吸窘迫综合征(重度)、干燥综合征、2型糖尿病。
诊治经过
入院后予:
a.一般治疗:心电监护、计24小时出入量、留置深静脉导管、肠内营养支持等;
b.呼吸支持:高流量氧疗-BiPAP交替使用;
c.对因治疗:美罗培南1.0q8h、万古霉素 0.5q12h抗感染,醋酸卡泊芬净50mg qd抗真菌,甲泼尼龙40mg q12h抗炎,依诺肝素钠4000IU qd抗凝等治疗;
d.寻因治疗:送检相关检查,三大常规、生化、免疫功能及病原学检查及心超、双下肢血管B超等检查;
e.治疗过程中动态监测血气分析、感染指标、血流动力学、心、肝、肾功能、内环境及血药浓度,动态评估病情。
经上述积极治疗后,患者氧合改善欠佳,氧合指数波动在80-150mmHg,高流量氧疗、无创呼吸机参数难以下调。
05-05肺泡灌洗液NGS:白色念珠菌、光滑念珠菌、溶血葡萄球菌;
05-09 痰培养:鲍曼不动杆菌++++;
且患者再次出现发热,抗生素调整为美罗培南+多粘菌素+万古霉素抗感染,醋酸卡泊芬净抗真菌。
图三(免疫相关指标)
05-11根据图三结果风湿免疫科会诊诊断:干燥综合征,抗合成酶抗体综合征,肺部表现为干燥相关肺大泡,抗合成酶相关间质性肺炎表现,合并感染可能大,建议积极寻找感染微生物,同意目前甲强龙80mg治疗基础上积极抗感染治疗,余免疫抑制剂暂不考虑。
图四(床边胸片)
05-12患者05-11床边胸片示两肺纹理增多增粗模糊,两肺多发斑片模糊影,较前片明显进展,两肺中下野多发斑片结节状钙化灶,两侧胸腔少量积液可能,心影增大,主动脉迂曲伴壁钙化。05-12血气分析示氧合指数71mmHg。与患者及其家属沟通后气管插管-有创机械通气(先后予A/C-VC模式、A/C-PC模式、PRVC模式)。
05-15患者症状改善不明显,甲泼尼龙加量至160mg。
气管插管-有创机械通气后,患者氧合指数改善不明显,05-17氧合指数下降至57.5mmHg,予俯卧位通气(5.17至5.24,每日16小时)。
5-25呼吸机模式调整为PSV模式,同时肺康复训练
6-3甲泼尼龙减量至40mg
6-5 通过自主呼吸试验SBT,拔除气管插管,双通道鼻导管吸氧-BiPAP(晚)序贯呼吸支持
6-9复查胸部CT:两肺弥漫性多发炎症改变,慢支-肺气肿,两肺多发肺大泡,两肺多发结节,斑结及钙化灶,多为陈旧性病变。
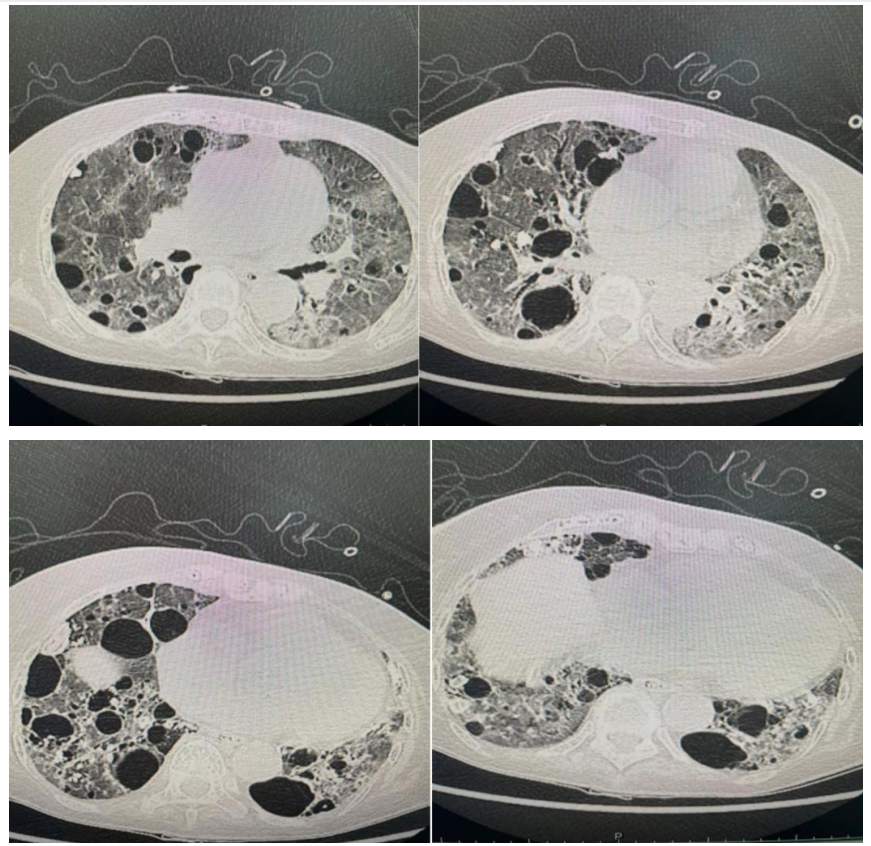
后转呼吸科普通病房康复训练,糖皮质激素逐渐减量。
讨论
1、急性呼吸窘迫综合征(ARDS)的全球新定义
急性呼吸窘迫综合征 (ARDS) 是一种急性呼吸系统疾病,其特征是双侧胸部影像学浸润伴非心源性肺水肿所致的严重低氧血症。COVID-19大流行导致急性呼吸窘迫综合征增加,并突出了与这种综合征相关的挑战,包括其不可接受的高死亡率和缺乏有效的药物治疗。新的全球ARDS定义扩展了柏林ARDS定义,接受HFNO≥30L/min治疗的急性呼吸衰竭患者可被诊断为ARDS,这是一种新的非插管ARDS。指脉氧可以代替动脉血气用于ARDS的诊断。该患者入院初期高流量氧疗-BiPAP交替使用呼吸支持治疗,根据ARDS全球新定义诊断急性呼吸窘迫综合征(重度),早诊断,利于早治疗。
2、急性呼吸衰竭的病因
患者急性呼吸衰竭的病因系感染所致,还是抗合成酶抗体综合征相关间质性肺病的急性加重?该患者05-03 外院【痰培养】白色念珠菌、溶血葡萄球菌阳性,后我院05-05肺泡灌洗液NGS:白色念珠菌、光滑念珠菌、溶血葡萄球菌;05-09 痰培养:鲍曼不动杆菌++++,入院初予美罗培南+万古霉素抗感染,醋酸卡泊芬净抗真菌,后调整为美罗培南+多粘菌素+万古霉素抗感染,醋酸卡泊芬净抗真菌。积极、充分的抗感染治疗后,患者的影像学进展,且氧合差,05-12气管插管-有创机械通气,氧合改善不明显。此时考虑该患者病因抗合成酶抗体综合征相关间质性肺病急性加重为主,05-15甲泼尼龙加量至160mg,05-17俯卧位通气。
抗合成酶综合征 (ASS) 被定义为特发性炎症性肌病 (IIM) 的一种亚型,但其临床表现远远超出了肌肉。其特征是肌炎,关节炎,间质性肺疾病,雷诺现象,技工手和发热等症状的组合。间质性肺疾病常为首发症状,易合并机会性感染,并迅速发展为呼吸衰竭。首选治疗大剂量糖皮质激素,该患者糖皮质激素加量至160mg每日后,明显获益,且KL-6水平逐步下降。KL-6的血清水平被认为可用于(1)检测疾病的存在,(2)评估疾病活动度,以及(3)预测各种类型的ILD的结果。
3、俯卧位通气在ARDS患者中的应用
在ARDS治疗中,俯卧位通气(PPV)能显著改善患者通气血流比例(V/Q)失调,促进萎陷肺泡复张,减少呼吸机相关肺损伤,解除心脏对于部分肺组织的压迫,有利于肺扩张和体位痰液引流,从而改善ARDS患者的生存率。俯卧位通气治疗作为机械通气治疗的一个环节越来越受重视,其具有改善氧合,改善高碳酸血症,利于肺保护性通气策略的实施及改善右心功能等作用,并可以降低病死率。俯卧位通气的适应症日本指南推荐中重度ARDS接受俯卧位,德国指南推荐氧合指数<150mmHg行俯卧位,每天至少16小时,欧美指南中推荐重度ARDS患者接受每天至少12小时俯卧位。本病例患者系重度ARDS患者,我们帮其实施了每日16小时俯卧位通气,且持续8天,患者的氧合明显改善,恢复仰卧位后氧合指数>150mmHg且持续6小时以上,所以停止俯卧位通气。该病例未见脸部压疮,血流动力学紊乱,呕吐,意外脱管等不良反应。患者最终成功脱机拔管,预后良好。
参考文献 (可上下滑动浏览)
1.Meyer NJ, Gattinoni L, Calfee CS. Acute respiratory distress syndrome. Lancet. 2021 Aug 14;398(10300):622-637. doi: 10.1016/S0140-6736(21)00439-6. Epub 2021 Jul 1. PMID: 34217425; PMCID: PMC8248927;
2.M.A. Matthay, Y. Arabi, A.C. Arroliga,et al.A New Global Definition of Acute Respiratory Distress Syndrome.American Journal of Respiratory and Critical Care Medicine 2023;207:A6229.doi:American Journal of Respiratory and Critical Care Medicine 2023;207:A6229.
3. Opinc AH, Makowska JS. Antisynthetase syndrome - much more than just a myopathy. Semin Arthritis Rheum. 2021 Feb;51(1):72-83. doi: 10.1016/j.semarthrit.2020.09.020. Epub 2020 Dec 22. PMID: 33360231.
4. Ishikawa N, Hattori N, Yokoyama A, Kohno N. Utility of KL-6/MUC1 in the clinical management of interstitial lung diseases. Respir Investig. 2012 Mar;50(1):3-13. doi: 10.1016/j.resinv.2012.02.001. Epub 2012 Mar 8. PMID: 22554854.
作者:丁荣1,冯耘2,时国朝2,方洁2,葛晓2;单位:1.江苏省泰州市第四人民医院;2.上海交通大学医学院附属瑞金医院
专家介绍
时国朝
上海交通大学医学院附属瑞金医院 主任医师,博士研究生、博士后导师;上海交通大学医学院附属瑞金医院呼吸与危重症医学科行政主任;上海交通大学医学院呼吸病研究所常务副所长;上海交通大学医学院慢性气道疾病诊治中心副主任;中华医学会呼吸病学分会委员;中国医师协会内科医师分会常务委员;中国医师协会呼吸医师分会委员;发表SCI论文60余篇,作为第一完成人荣获上海医学科技奖二等奖。
冯耘
上海交通大学医学院附属瑞金医院 主任医师、副研究员、硕士研究生导师;就职于上海交通大学医学院附属瑞金医院;美国杜克大学访问学者;中国老年医学会呼吸病学分会呼吸危重症学术委员会委员;上海市医学会呼吸病学专科分会青年委员会委员;上海市医学会呼吸病学专科分会重症学组副组长;曾荣获上海市人才培养计划、上海市优秀专科医师及上海交通大学医学院“九龙医学优秀青年人才奖”;以第一作者及通讯作者发表SCI论文30余篇,第一完成人获得专利2项,参与编写专著3部。
方洁
上海交通大学医学院附属瑞金医院 副主任药师;卫生部临床药师培训基地抗感染专业带教药师;中华医学会临床药师培训基地带教老师;上海市医学会临床药学分会青年委员;上海市医学会临床药学分会呼吸学组副组长。
葛晓
上海交通大学医学院附属瑞金医院 呼吸治疗师;毕业于四川大学华西临床医学院呼吸治疗系;主要工作方向为危重症患者的呼吸支持、气道管理,呼吸康复、床边重症超声、床边气管镜等。
丁荣
江苏省泰州市第四人民医院 副主任医师,科后备人才;2015,2023两次至上海交通大学医学院附属瑞金医院呼吸与危重症医学科进修学习;熟练掌握呼吸科常见病、多发病的诊治、电子支气管镜技术,擅长呼吸危重症、肺部感染性疾病、慢性气道疾病的规范化诊治、睡眠呼吸暂停低通气综合征等的诊治;主持、参与市、区级社会发展项目三项。曾获“海陵区青年岗位能手”、“十佳医师”、“海陵区优秀医师”、“十佳党员”等称号。
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


