近日,国际知名期刊《Frontiers in Oncology》发表了一篇题为《Peripheral Blood Autoantibodies Against to Tumor-Associated Antigen Predict Clinical Outcome to Immune Checkpoint Inhibitor-Based Treatme nt in Advanced Non-Small Cell Lung Cancer》的文章,首次揭示了「『肺癌自身抗体』检测在免疫治疗疗效预测」重要临床价值与广阔临床应用前景。

《权利的游戏》有一句名言:「information is power」,在战争之中,情报就是力量。这句话用在免疫治疗与肿瘤的战争中,再合适不过。
2014年7月,第一款PD-1抑制剂在日本上市。随后,一股肿瘤免疫治疗的风暴席卷了全球。随着免疫检查点抑制剂在我国获批上市,免疫治疗大大改变了传统的肿瘤治疗策略。但是目前差不多只有20%-40%的肿瘤患者可以从免疫治疗中获益。
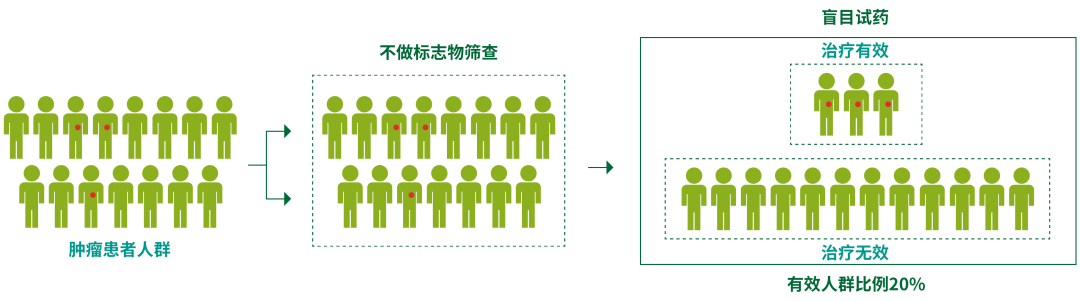
越来越多的临床数据证明:目前,我们仍未找到一个可以精确预判PD-1疗效的临床指标,通过现有的单个预测指标,仅能有限地、局部地判断PD-1抑制剂有效的概率是否能升高。
同济大学附属上海市肺科医院 苏春霞教授团队、 第三军医大学附属新桥医院贾罄竹教授团队、 华中科技大学附属同济医院褚倩教授团队历经两年,对肺癌患者免疫治疗随访的样本进行了系统的真实世界研究,首次揭示了「肺癌自身抗体多靶点检测」在免疫治疗疗效预测的重要临床 价值, 为临床预测免疫检查点抑制剂药物 的治疗效果提供重要的新技术手段与线索。
研究起源
肿瘤和机体免疫系统之间存在复杂的相互作用,体液免疫是其中的重要参与者。机体可针对肿瘤相关性抗原(Tumor-associated antigen,TAA)产生自身抗体,即肿瘤相关自身抗体。一方面,肿瘤相关自身抗体已被广泛发现和研究,在肺癌早期诊断中的价值已经得到了广泛认可,2019世界肺癌大会(WCLC)公布了英国NHS肺癌筛查研究结果,证实自身抗体在肺癌前瞻性大样本队列研究筛查获益;另一方面,肺癌自身抗体用于免疫治疗疗效预测前景被全球学者看好。
研究简介
研究分为两个队列:发现集为来自上海市肺科医院的37例一线接受ICI为基础的单药或联合治疗的晚期肺癌患者,验证集为来自上海市肺科医院、第三军医大学附属新桥医院和华中科技大学附属同济医院的129例接受ICI为基础的单药或联合治疗的晚期肺癌患者,无论治疗线数。
主要研究目的:免疫治疗ORR和无进展生存期(PFS)与自身抗体的关系。
探索性研究目的:免疫相关性肺炎与自身抗体的关系。
研究方法:采用ELISA的方法检测外周血中自身抗体水平,抗体阳性定义为健康人群中自身抗体表达水平的均值+2倍标准差。在发现集中,检测前期研究中确认的与肺癌相关性较高的43种TAAbs,结合免疫治疗疗效,筛选与ORR和PFS有关的自身抗体。在验证集中采用「双盲」(即检测人员对临床疗效未知,临床数据收集人员不参与标本检测)的方法验证筛选的自身抗体对免疫治疗疗效的预测价值。
研究结果
1 患者基线特征
患者的免疫基线特征如表1所示。研究共纳入166例患者,包括34例EGFR突变患者。自身抗体的阳性率约为50%。初诊患者自身抗体的阳性率显著高于经治患者(65.9% vs. 38.8%, p=0.003)。
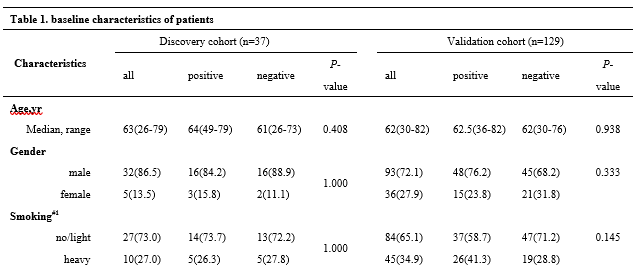
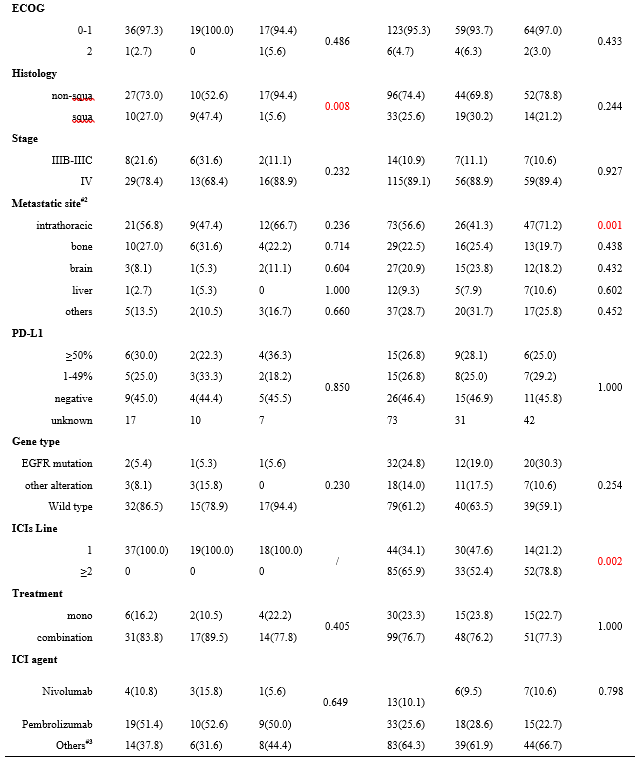
表1
2 发现集筛选5种自身抗体
前期通过在肺癌患者及健康人群中对比,筛选出了与肺癌相关性较高(敏感性>5%,特异性为93.6%)的43种自身抗体。本研究首先在发现集中检测了43种自身抗体的表达水平,结合免疫治疗疗效,将其分类为:1)正相关性抗体:即抗体阳性的人群中,疗效为部分缓解(PR)的人数是疾病进展(PD)人数的两倍及以上;2)负相关性抗体:即抗体阳性的人群中,PD的人数是PR人数的两倍及以上;3)无相关性抗体:不满足前两个条件者。在正相关性抗体组的有:Claudin2,BRCA2, HUD, P53, Annexin1, MAGE-A4, Trim21, TTC14, IMP2, GAGE7, NY-ESO-2, NY-ESO-1。在负相关性抗体组的有:ETHE1, AKAP4, PRAME, HSP105, MAGE- A3, KRT8, KRAS, RALA, FEZF1, TTC14, PRAME。然后通过结合免疫治疗PFS在12种正相关性抗体中筛选出效果最好的5种自身抗体,分别为p53, BRCA2, HUD, TRIM21 和 NY-ESO-1。考虑到单一抗体的敏感性较低(5%-20%),最后将5种自身抗体作为一组panel进行研究,任一自身抗体阳性即视为该panel阳性。
如图1所示,在发现集中,在5-TAAbs阳性人群中,PR率为47.4%,而PD率仅为15.8%。与阴性组相比,5-TAAbs阳性组患者的PFS显著延长(not reached vs. 5.32m, p=0.05, HR=0.383, 95% CI: 0.140–1.046)。

图1
3 验证集确认自身抗体疗效预测价值
在验证集中,5-TAAbs阳性与免疫治疗更好的疗效和更长的PFS相关:ORR: 44.4% vs. 13.6%, p=0.001; DCR: 84.1% vs.59.1%, p=0.002;PFS:7.6 vs. 3.3m, p<0.001, HR=0.394, 95% CI: 0.245–0.634。(见图2A,B)
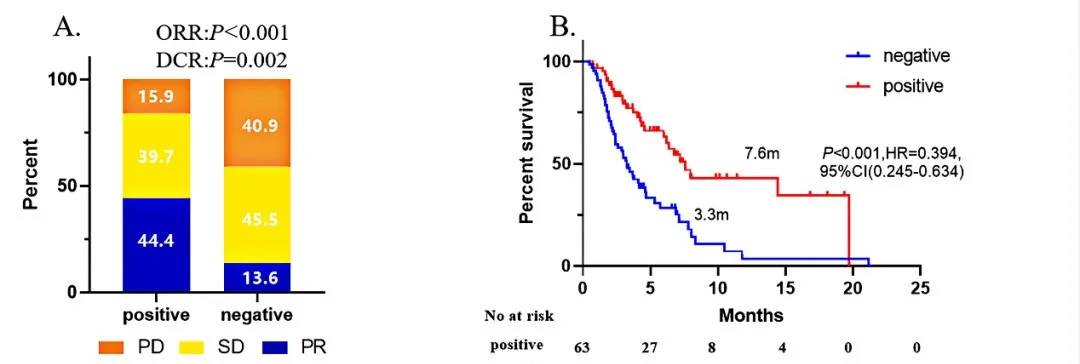
图2
亚组分析提示,无论是免疫单药治疗(ORR: 46.7% vs. 13.3%, p=0.003, PFS: 19.7 vs. 2.2m, p<0.001, HR=0.198, 95% CI: 0.076–0.511),还是免疫联合治疗(ORR: 43.8% vs. 13.7%, p=0.004, PFS: 6.7 vs. 3.7m, p=0.017, HR=0.509 95% CI: 0.303-0.857),5-TAAbs阳性均具有很好的预测价值。(见图3A,B,C,D)
但是研究结果提示5-TAAbs panel对于接受后线免疫治疗的患者意义更大(ORR: 42.7% vs. 7.7%, p=0.001, PFS: 6.2 vs. 3.0m,p=0.004, HR=0.481, 95% CI: 0.295–0.785),而对于初诊患,阳性组和阴性组的疗效和PFS并没有达到统计学差异(ORR: 46.7% vs. 35.7%, p=0.345, PFS: NR vs. 10.48m, p=0.146),可能与该人群样本量相对较少(n=44)以及联合治疗人群占比较大有关(81.8%)。(见图3E,F,G,H)

图3
此外,对于EGFR突变人群,5-TAAbs阳性组和阴性组的临床疗效和PFS没有显著性差异(ORR: 20.0% vs. 9.1%, p=0.572; DCR: 70.0% vs. 68.2%, p=1.000;PFS:6.2 vs. 3.7m, p=0.196, HR=0.527, 95% CI: 0.196–1.419)。(见图4A,B)

图4
单因素和多因素分析提示5-TAAbs panel是免疫治疗PFS的独立预测因子。(见表2)
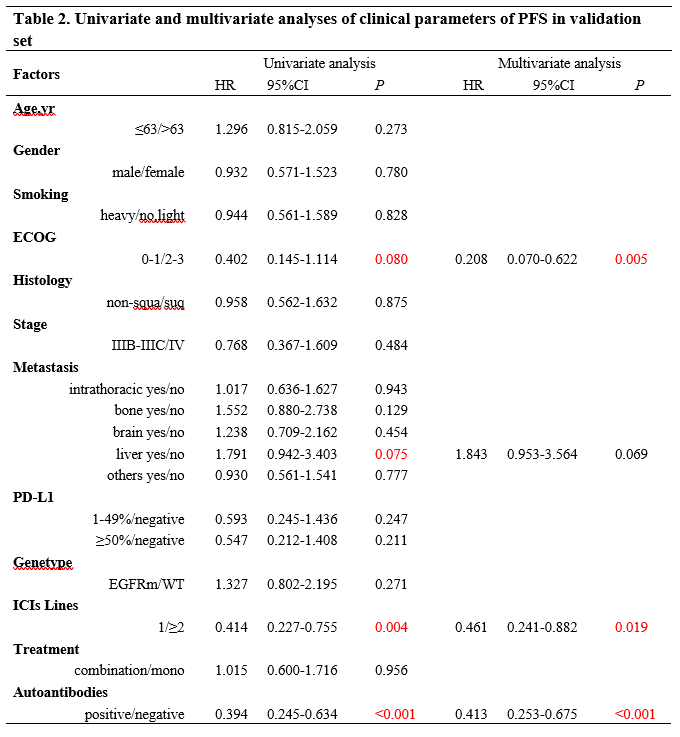
表2
4 自身抗体与免疫相关性肺炎的关系
本研究中,免疫相关性肺炎(CIP)的发生率为12.3%,中位发生时间为2.3个月。与阴性组相比,5-TAAbs阳性组的CIP发生率显著较高(20.4% vs. 5.9%, p=0.015,HR=3.504),但两组发生肺炎的级别无显著差异。(见图5C,D,E)

图5
展望
本研究在晚期肺癌人群中发现由5种自身抗体(p53, BRCA2, HUD, TRIM21 和 NY-ESO-1)组成的panel可以有效的预测免疫治疗的疗效和生存。该panel的阳性率达50%,相比其他生物标志物可以覆盖更多的人群。自身抗体水平与免疫治疗疗效相关的理论逻辑在于:首先自身抗体的阳性表达说明相对应的肿瘤相关抗原具有较高的免疫原性,但是也并非所有的肿瘤相关抗原都可以引起CD8+T细胞反应。因此,自身抗体的阳性表达反映的预先存在的体液免疫也可能是免疫治疗疗效较好的原因。
随着免疫检查点抑制剂在我国获批上市,免疫治疗大大改变了传统的肿瘤治疗策略。要想筛选出最佳获益人群,就要做到知己知彼,通过标志物了解肿瘤和自身免疫系统的状态,新型肺癌自身抗体Panel将会成为预测免疫治疗效果的可靠生物标志物。
* 参考文献:Juan Zhou, Jing Zhao,Qingzhu Jia, et al. Peripheral Blood Autoantibodies Against to Tumor-Associated Antigen Predict Clinical Outcome to Immune Checkpoint Inhibitor-Based Treatment in Advanced Non-Small Cell Lung Cancer. Front. Oncol., 16 March 2021. https://doi.org/10.3389/fonc.2021.625578
专家介绍

苏春霞
副主任医师、副教授、博士生导师;同济大学附属上海市肺科医院肿瘤科副主任;同济大学附属上海市肺科医院内科教研室副主任;中国肿瘤临床学会CSCO患教专委会副主委;中国肿瘤临床学会CSCO转化专委会副秘书长;中国肿瘤临床学会CSCO免疫治疗专委会常委;北京癌症防治学会呼吸道肿瘤药物不良反应管理专业委员会副主委;上海市抗癌协会青年理事会副理事长;上海市女医师协会肺癌专委会副主委;泛长三角胸部肿瘤联盟专委会秘书长;上海市抗癌协会肺癌分子靶向和免疫治疗专委会常委兼秘书长;《中国肿瘤临床学会CSCO 免疫检查点抑制剂临床应用指南》执笔专家;《中国肿瘤临床学会CSCO 免疫检查点抑制剂相关的毒性管理指南》执笔专家;荣获“第三届国之名医-优秀风范奖”“上海市科学技术普及奖二等奖”;“上海市科普贡献奖二等奖”“上海市杰出青年医师”等荣誉。

褚倩
教授,主任医师,博士生导师,华中科技大学同济医学院附属同济医院胸部肿瘤科副主任,中国临床肿瘤学会非小细胞肺癌专家委员会委员,中国临床肿瘤学会免疫治疗专家委员会常委;中国临床肿瘤学会患者教育专家委员会副秘书长;中国医疗保健国际交流促进会常务理事;湖北省临床肿瘤学会青年专家委员会主任委员;湖北省临床肿瘤学会免疫治疗专家委员会候任主委;湖北省免疫学会肿瘤精准治疗专业委员会候任主委。

贾罄竹
陆军军医大学新桥医院肿瘤科主治医师/讲师/博士,是国家杰青朱波教授团队骨干青年医生。主要从事肺癌相关的内科治疗与基础研究,尤其关注于肿瘤免疫学与精准诊断的转化研究方向。作为负责人主持国家自然科学青年基金1项,以第一作者/通讯作者在AdvSci,JTO,NC,PNAS等杂志发表SCI论著十余篇。
本文完
排版:Jerry


