引言
胸腔积液是呼吸领域的常见疾病,可能你会立刻联想到外伤、肿瘤、感染等等,而非常见原因引起的「乳糜胸」并不多见,把它比喻成易被忽视的「死角」并不过分。面对原因不明的肺部体征,诊治中应考虑哪些因素?当我们发现患者不仅有「乳糜胸」,还有骨质破坏,这时又该作何考虑?我们想到了一种疾病,它的死亡率很高,常用治疗方法包括手术、放疗和干扰素治疗,可疗效并不确切,那么应当如何有效治疗?……法国著名女小说家乔治·桑曾说「真理太简单了,你总是通过复杂的路线才能到达它的身边」,今天我们与大家分享的病例就是这样的「求因路线」。
病急而活检示「骨上皮样血管内皮瘤」,首次放疗后突发胸闷气急,胸腔B超示「右侧大量胸腔积液」,连抽三次胸水后查到了什么?
患者是一名25岁的男青年,平素体健,无特殊病史,否认结核病及密切接触史,否认外伤史,否认输血史,无药物过敏史。无吸烟、饮酒史,无疫区接触史。未婚,无家族遗传病史。患者于2016年8月12日因颈部疼痛伴活动障碍1月余,至广州军区总医院就诊,全身PET/CT示「枕骨、颈椎及胸椎多发溶骨性骨质破坏,伴软组织影块形成,代谢轻度增高」,于8月17日行颈椎肿物活检提示「骨上皮样血管内皮瘤」。
为进一步诊治,患者于同年9月6日致我院骨科就诊,考虑枕骨、颈椎多发肿瘤(枕骨、C1-7),因检查提示病变血供丰富,手术风险较大,建议先行放射治疗。于是,患者9月9日来到海军411医院,针对颈椎肿瘤行放疗。然而令患者及其家属猝不及防的是,就在放疗1次之后,患者突发胸闷气急,活动后加重,偶有干咳,无发热、盗汗,无咯血、胸痛,无双下肢水肿。胸腔B超示「右侧大量胸腔积液」,于9月14日予以右侧胸腔置管引流出大量血性胸水,胸水细胞学检查示「小细胞未分化癌细胞」。5天后复查胸腔B超,仍提示双侧胸腔积液。
全身PET/CT示「枕骨、颈椎及胸椎多发溶骨性骨质破坏,伴软组织影块形成,代谢轻度增高」;颈椎肿物活检提示「骨上皮样血管内皮瘤」;胸水细胞学检查示「小细胞未分化癌细胞」,平日身体完全无恙,却在不到1个月时间里连续得到了三个不好的消息,让该患者和他的家人非常难以接受。
2016年9月19日,患者为求进一步诊治来到我院呼吸科门诊,主诉「发现颈椎肿瘤1月余,胸闷气急10余天」,门诊以「胸腔积液性质待查」收入院。患者自发病以来,精神欠佳,体重无明显变化,饮食正常,二便正常,睡眠无明显异常。
一、入院检查情况:
入院后首先进行了以下体格检查:
体温36.7℃,心率80次/min,呼吸20次/min,血压110/70mmHg,SPO2 98%(吸氧4L/分),神志清楚,一般情况差,平车推入病房。全身皮肤粘膜无黄染,无瘀点、瘀斑,浅表淋巴结未触及肿大。颈椎活动受限,压痛、叩击痛阳性,颈部颈托固定。气管居中,颈静脉无怒张,胸廓无畸形,双下肺叩诊浊音,双下肺呼吸音消失。心腹查体(-)。四肢活动自如,无杵状指(趾),双下肢无水肿。神经系统查体(-)。
外院实验室检查:
全身 PET/CT(2016年8月12日于广州军区总医院):枕骨、寰椎后弓及双侧横突、颈2-7椎体多发横突、椎弓、棘突及胸2椎体右侧横突多发溶骨性骨质破坏,部分伴病理性骨折及软组织肿块影形成,代谢轻度增高,考虑骨原发病变,不除外朗格汉斯细胞组织细胞增生症可能。
颈椎 CT (2016年8月10日于广东省中山市中医院):枕骨、寰椎后弓、颈2-6棘突、颈7双侧横突多发骨质破坏,颈2-6棘突多发骨质不连续,邻近软组织肿胀,考虑中间性或恶性肿瘤。
颈椎肿瘤病理(2016年8月29日于中山大学附属肿瘤医院):病变符合血管瘤改变。
颈椎肿瘤病理(2016年8月22日于中山大学附属一院):病变符合中间型血管内皮瘤。
胸腔 B 超(2016年9月19日于海军411医院)检查提示双侧胸腔积液。胸水细胞学提示查到小细胞未分化癌细胞。
入院后完善了以下检查:
1、血检验
血常规:白细胞10.7×10^9/L↑,中性粒细胞% 84%↑,血小板 298×10^9/L,血红蛋白 157g/L
CRP:12.55(0-10mg/L)↑
血沉:58(0-15mm/h)↑
肝功能:白蛋白:36g(35-50g/L),丙氨酸氨基转移酶75(21-72U/L)↑,天门冬氨酸氨基转移酶36 (17-59U/L), r-谷氨酰基转移酶85(12-58U/L)↑
凝血:凝血酶原时间 12,2(9-13S),活化部分凝血活酶时间 33.4(20-40S),凝血酶时间24,1(14-21S)↑,纤维蛋白原 4.99(2-4.5g/L)↑,D-二聚体5620(< 550 ug/L)↑
肿瘤标志物:CA125 77.39(<35U/mL)↑,NSE、CYFRA211、CEA、CA199、鳞癌相关抗原正常
尿、粪常规、电解质、肾功能、碱性磷酸酶、乳酸脱氢酶、甲状旁腺素、降钙素、BNP、血清蛋白(IgA、IgM、IgG、IgE、 κ 、λ κ/λ )电泳、M蛋白未见明显异常,
乙肝两对半、HIV、HLA-B27阴性
2、影像学
1)胸腔镜检查(2016年9月20日)
胸腔镜检查:左侧血性胸腔积液,吸出约1000ml,胸膜未见明显异常(图1)
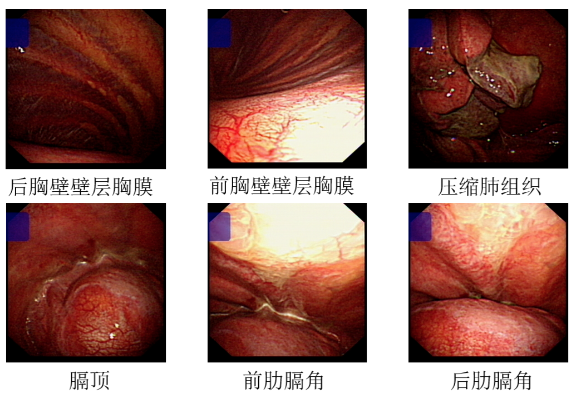
图1.胸腔镜检查
胸水常规检查:外观红色浑浊,李凡特试验阳性++,红细胞506000×10^6/ L↑,白细胞5900×10^6/ L↑,淋巴细胞65%↑,中性分叶核24%,巨噬细胞11%,见核异质细胞↑
胸水生化:白蛋白28g/ L,乳酸脱氢酶532 U/L,葡萄糖6.8mmol/L
胸水肿瘤标志物:CA125 2032 U/mL↑,CYFRA211 12.79 ug/L↑,CEA、CA199、鳞癌相关抗原正常。
三次胸水细胞学检查均未见癌细胞。
2)颈椎MRI:颈1-胸1附件与所示枕骨及周围软组织内见大片状异常信号影,边界欠清,T1WI呈低信号,T2WI呈不均匀高信号,该区部分附件缺损,增强扫描病灶呈不均匀显著强化。
3)胸部CT:双肺炎症伴双侧胸腔积液,双侧胸膜局部增厚(图2)
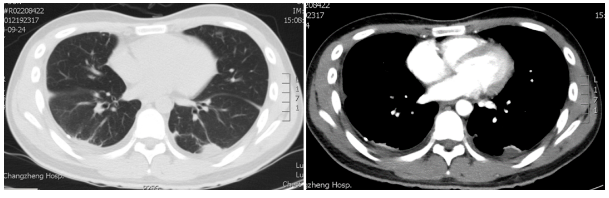
图2.肺部CT 2016年9月28日
腹部B超:未见明显异常
4)胸水(2016年9月26日 我院)
2016年9月23日,患者诉气急、胸闷加重,复查胸腔B超示左侧再次出现大量胸腔积液,予放置左侧胸腔引流管引流胸水。 2016年9月26日,左侧引流出乳糜样胸水,乳糜试验阳性。
血性胸腔积液,病理提示恶性,但多次送检胸水检查未见恶性依据,并且出现乳糜样胸水……是否遗漏线索和检测?诊断方向何在?
面对当下这种情况,患者在外院和我院均查出血性胸腔积液,外院送病理检查提示为恶性,但我院多次送检胸腔积液检查却未查见恶性依据,与此同时还出现了乳糜样胸水,究竟是何因?是否我们在诊断过程中遗漏掉了哪些重要线索?是否还有哪些检测可以辅助明确诊断?一时间似乎诊断陷入「僵局」。
仔细梳理患者的临床特点:1.症状:气急、胸闷10余天;2.体征:颈椎活动受限,压痛、叩击痛阳性,双下肺叩诊浊音,双下肺呼吸音消失,余无特殊;3.辅助检查:①胸部CT:双肺炎症伴双侧胸腔积液,双侧胸膜局部增厚;②胸腔镜检查:胸膜未见明显异常;③B超提示胸腔积液,起初为血性胸水,后为乳糜胸;PET-CT示「枕骨、颈椎及胸椎多发溶骨性骨质破坏」;④入院前胸水细胞学检查见小细胞未分化癌细胞,入院后3次胸水细胞学检查均未见癌细胞;⑤颈椎肿瘤活检病理:纤维组织增生,其中可见扩张的血管,未见细胞异型性;⑥血常规:白细胞10.7×10^9/L,中性粒细胞% 84%,CRP:12.55,血沉:58,CA125:77.39;⑦碱性磷酸酶、乳酸脱氢酶、甲状旁腺素、降钙素、BNP、血清蛋白电泳、M蛋白、HLA-B27,心电图、腹部B超未见明显异常。
您认为该患者最有可能的是什么疾病?
围绕这些特点进行诊断分析:青年男性,急性起病,双侧胸腔积液由血性变成乳糜样,颈椎肿瘤活检病理未见细胞异型性,PET-CT示「枕骨、颈椎及胸椎多发溶骨性骨质破坏」。当以乳糜性胸腔积液为切入点(图3)。
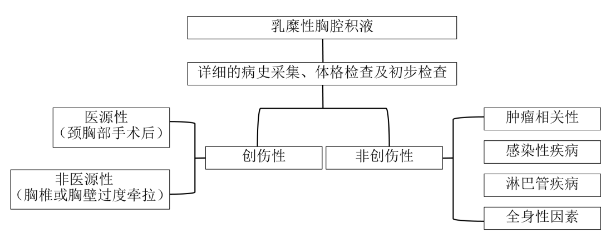
图3. 诊断分析线路图
分析如下:
1、恶性肿瘤:淋巴瘤、转移癌、Kaposi’s肉瘤。排除淋巴瘤,理由:无乏力、纳差、消瘦、盗汗及不规则发热,全身浅表淋巴结未触及肿大,胸部CT未见纵隔淋巴结肿大;不支持转移癌,理由:PET-CT无相关证据,胸腔镜检查胸膜未见明显异常,入院后三次胸水细胞学检查阴性。
2、纵隔肿瘤:畸胎瘤、主动脉瘤、胸骨后甲状腺肿。排除纵隔肿瘤,理由:PET-CT及胸部CT均未见纵隔占位。
3、感染性疾病:结核、丝虫病。结核、丝虫病均无相关证据。
4、淋巴管疾病:淋巴管瘤、Gorham病、淋巴管平滑肌瘤病。不符合淋巴管平滑肌瘤病,理由:淋巴管平滑肌瘤多见于绝经期妇女,胸部影像学可见。双肺弥漫分布的薄壁小囊肿。
5、全身性因素:甲减、系统性红斑狼疮、肝硬化、心力衰竭、肾病综合征。以上情况均无相关证据。
6、创伤性胸导管破裂。排除创伤性胸导管破裂,理由:无外伤和手术史。
可能的疾病此时浮出水面,它就是Gorham病。Gorham病又称大块骨溶解症,是一种骨质进行性吸收性疾病,是由于骨的毛细血管或淋巴管良性增生、侵蚀骨骼所致。这种疾病虽然在临床罕见,目前全球报道仅200余例,且病因和发病机制不清。该病好发于儿童和青年人,无明显遗传倾向,这一点比较符合本案例患者。Gorham病的主要临床表现为:多发性骨溶解、神经损害、骨损害附近的血管瘤或淋巴管瘤。如果侵及下位肋骨、胸椎,可导致胸导管损伤,形成大量的乳糜胸,死亡率高达53%。从临床表现看也符合本案例患者。
尤其值得注意的是,Gorham病在实验室检查时:一般无异常发现,少数可有碱性磷酸酶及嗜酸性细胞轻度增高。影像表现:一骨或多骨局部或进行性骨质破坏,无增生硬化及骨膜反应,无膨胀和溃疡性病变。病理特征:局部大块骨质溶解及脉管组织增生,无成骨或极少成骨反应,无瘤细胞。Gorham病还有一个特点,它在早期时是以血管、淋巴管增生为主,后期则以纤维组织增生为主并逐渐替代骨组织。
对于Gorham病的治疗:病变部位早期制动,避免负重,给予支具保护。药物治疗:双磷酸盐、干扰素α-2b。外科治疗:内固定术、骨水泥重建术、假体置换术。放疗:40-45Gy,1.8-2.0Gy/次。乳糜胸:胸导管结扎术、胸膜固定术、胸膜部分切除术、放疗、干扰素治疗、口服双磷酸盐。Gorham病的预后:少数患者呈自限性,大多数患者的病情呈进展性。合并胸腔积液、脊柱病变以及脏器损害的患者预后差。
综上,针对本案例患者在外院及本院目前的检查结果综合分析,我团队认为Gorham’s综合征的可能性大,颈椎肿瘤手术活检明确病理。
提示乳糜胸患者若有骨质破坏需考虑Gorham病可能?这种病手术、放疗和干扰素治疗疗效不确切,如何有效治疗?
究竟是Gorham’s综合征还是Gorham病?我们开展了多学科讨论,讨论如下:
骨肿瘤科:2016年9月26日患者全身PET-CT检查提示枕骨、颈椎及胸椎多发信号异常,考虑为肿瘤。颈椎肿瘤活检提示「骨上皮样血管内皮瘤」。我院骨科就诊考虑枕骨、颈椎多发肿瘤(枕骨、C1-7),骨肿瘤科杨再兴副教授会诊意见如下:1.进一步明确胸腔积液性质及病因。2.颈部制动,颈部保护,复查颈椎 X 线,MRI平扫+増强。3.颈椎肿瘤活检,切行复旦大学肿瘤医院进一步明确颈椎病理报告。4.待胸腔积液情况以控制稳定后联系我科行手术治疗。
病理科:2016年9月26日患者既往2次胸水细胞学未发现癌细胞,结合外院胸水细胞学提示查到小细胞未分化癌细胞及病理切片结果,请病理科会诊协助诊治。病理科蒋计生主任医师会诊意见:读中国人民解放军411医院常规涂片2张,同意外院单位诊断意见倾向小细胞未分化癌。但患者入院后未发现恶性肿瘤依据,故建议进一步复查病理。
胸外科:2016年10月8日患者全身PET-CT检查提示枕骨、颈椎及胸椎多发信号异常,考虑为肿瘤。颈椎肿瘤活检提示「骨上皮样血管内皮瘤」。我院骨科就诊考虑枕骨、颈椎多发肿瘤(枕骨、C1-7),胸外科钟镭主任医师会诊意见:1、左侧胸腔积液,乳糜胸可能,300-400/日;2、保守治疗,治疗骨肿瘤,3、胸外科随访,观察乳糜胸加重情况下考虑手术结扎胸导管。
如何诊治?团队请病理科、骨肿瘤科会诊,考虑恶性肿瘤(骨肿瘤)所致胸水可能性大,予双侧胸腔注入三氧化二砷控制胸水,白蛋白纠正低蛋白血症等对症支持治疗。患者气急、胸闷明显好转后于2016年10月9日转我院骨肿瘤科,2016年10月12日于全麻下行后路枕骨、颈椎肿瘤切除重建内固定术。术后病理:弥漫性血管瘤病。术后患者症状明显改善。
最后诊断及诊断依据:
(一)最后诊断:根据患者的临床、影像表现及多科会诊,综合诊断为Gorham病。
(二)诊断依据:1.症状:气急、胸闷10余天。青年,无家族史。2.体征:颈椎活动受限,压痛、叩击痛阳性,双下肺叩诊浊音,双下肺呼吸音消失,余无特殊。3.辅助检查:①B超提示胸腔积液,起初为血性胸水,后为乳糜胸;②PET-CT示「枕骨、颈椎及胸椎多发溶骨性骨质破坏」;③颈椎肿瘤活检病理:纤维组织增生,其中可见扩张的血管,未见细胞异型性。4.全麻下行后路枕骨、颈椎肿瘤切除重建内固定术。术后病理:弥漫性血管瘤病(图4)。
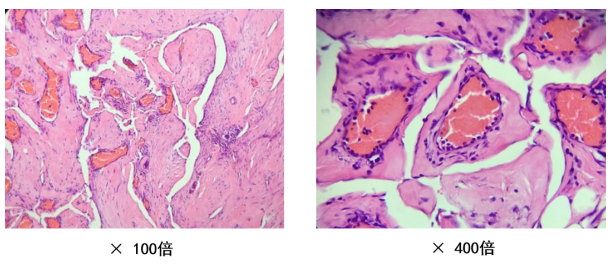
图4.颈椎肿瘤病理。骨组织溶解吸收,被血管组织及纤维结缔组织所替代,其间可见大量壁薄扩张的毛细血管,有破骨巨细胞反应,无成骨反应和钙化,无细胞异型性。
从本案例中我们得到的经验和体会如下:
1、乳糜胸常见病因为外伤、肿瘤、感染,但也可能是由其他少见原因引起。乳糜胸的患者如果有骨质破坏要考虑Gorham病的可能。
2、伴有乳糜胸的Gorham病患者死亡率很高,常用治疗方法包括手术、放疗和干扰素治疗,但疗效并不确切。本例患者胸腔注入三氧化二砷后乳糜胸明显控制。研究表明三氧化二砷可通过抑制VEGF信号通路来抑制肿瘤血管生成[1]。Gorham病是一种血管瘤样增生性疾病。因此,三氧化二砷可能对治疗Gorham病具有一定疗效。
参考文献:
[1].M.H. Yang, K.J. Chang, J.C. Zheng, H. Huang, G.Y. Sun, X.W. Zhao, B. Li, Q.Y. Xiu, Anti-angiogenic effect of arsenic trioxide in lung cancer via inhibition of endothelial cell migration, proliferation and tube formation, Oncol Lett 14(3) (2017) 3103-3109.
专家介绍

唐昊
上海长征医院(海军军医大学第二附属医院)呼吸与危重症医学科主任;中华医学会呼吸病学分会 9/10届青委会委员;中国医师协会呼吸医师分会青年委员;上海市医学会呼吸病学分会委员;上海市医学会呼吸病学分会哮喘学组副组长;上海市医师协会呼吸医师分会委员;上海市优秀学术带头人;上海市曙光学者;上海市浦江人才;上海市科技启明星。

吕游
上海长征医院(海军军医大学第二附属医院)呼吸与危重症医学科副主任医师;上海市医学会变态反应分会青年委员、中华医学会上海呼吸分会成员、欧洲过敏及变态反应学会(EAACI)会员;参与国家自然科学基金3项、上海市课题1项;主要研究方向:支气管哮喘,发表SCI 10篇,毕业论著1篇,多次参加国际大型医学学术会议(EAACI、ERS、WIRM、IES、CIA),发表会议摘要20余篇,大会报告3次并获奖。参编专著2部。2020年援鄂期间获得火神山医院“抗疫先锋”及“科研之星”,海军军医大学“抗疫先进个人”称号。

黄海
上海长征医院(海军军医大学第二附属医院)呼吸与危重症医学科主任医师,全科医学科主任;上海市医学会呼吸病学专科分会第十一届委员会委员、中国医药教育协会肺部肿瘤专业委员会会青委会委员、中国医师协会呼吸病分会中青年工作委员会委员、上海市住院医师规范化培训结业综合考核考官。主持国家、军队、省部级课题6项,近年来发表SCI论文15篇,发表各类论文50余篇。参编《内科手册》、《内科学年鉴》等专著2部。


