介入呼吸病学技术自上世纪90年代初国内首先在北京、上海、广州等地几家大医院陆续开展以来,在全国各地如雨后春笋般崛起,发展迅猛。介入呼吸病学技术是作为一名呼吸科医生必备的基本技术,它如同技工做工一样,必须对每个零构件熟悉、以及必须琢磨如何把它打磨精确,要安装到机器上不会出问题。同样,如果用一颗螺丝钉来比喻做介入的技术,把它用于一辆汽车、一架飞机、一艘火箭上,每颗螺丝钉的型号不够精准,就一定会出大问题。介入呼吸病学技术便是如此。
介入呼吸病学技术关键在于什么时候用,用到什么地方,用得恰当与否,有没有给患者造成伤害,是否给予患者最大化的获益,因此,每一步的决策正确是做介入的重中之重。
几个教训深刻的真实案例能看出什么?
正确的思路和思维是关键。举几个真实的「反面教材」,听完后大家可以思考是否得到了深刻的教训?
例1:1例良性气道狭窄。
病因是因为脑外伤进行气管插管抢救一月后逐渐出现呼吸困难,经胸部CT气管三维成像和气管镜检查诊断为气管中段纤维组织增生导致的良性狭窄。当时这名医生会装金属支架,随即就给患者装上金属支架。支架刚装上时患者的呼吸困难问题解决了,但过一两个月后,患者又出现呼吸困难,再检查时发现,这个支架完全包埋在粘膜之下,大量新的肉芽组织增生和瘢痕形成,造成气管壁再一次重度狭窄。
可能有一些相似案例的预后情况会比较好,属于上皮化的情况。因此,有些支架可以长期支撑在气管壁里,如气管软化症的患者,这样的患者可得到长期生存。但大部分气道损伤后瘢痕组织增生的患者是达不到这种预后的,不能上皮化,而支架作为一种异物,会长期反复地刺激和破坏气管壁,导致气管的二次损伤,出现大量肉芽组织增生,瘢痕组织形成,最后造成气管像麻绳一样「扭」起来,支架也难以取出。为什么?支架与气管壁融为一体,假如强行将支架取出,支气管壁就遭到破坏。这部分患者的最终结果可能因为气道梗阻而死亡。
例2:气管支气管结核 。
过去我们对气管支气管结核认识不清,是国内造成肺毁损最根本的第一大原因。 早在上世纪80年代,我们对结核极少做支气管镜,后来发现 30%-70%的肺结核都合并气管和支气管结核 ,气管支气管破坏后,气管所属的远端肺组织自然被破坏。 认识到这个问题后,才开始要求对所有诊断为肺结核的患者要做支气管镜检,早期发现气管支气管结核,才能早发现、早处理,从而达到防止毁损的目的。 当前,国内呼吸医师们的介入水平已有很大提升,镜下治疗保护了很多患者避免肺毁损,在全身抗结核治疗的同时积极开展镜下干预,让患者的气管和支气管得到了保护。 像以往那样的悲剧已很少发生。
但是,现在仍然还有一部分医生,他认为自己会装支架,一发现气管支气管狭窄,不管患者是活动期、肉芽肿期还是溃疡坏死期,只要有狭窄就装支架。这种情况的患者,最后只能选择做肺叶或全肺切除。因此,支架装得到底对不对?值得我们认真思考。
例3:因技术不熟练造成患者大出血。
尽管国内无人统计过在全国做介入手术操作过程中因技术不熟练造成患者大出血死亡的数据,但有不少家医院因此类事件曾做过大额赔偿。一些技术不熟练的医生敢上手术台,盲目操作,造成患者支气管动脉或肺动脉破裂,病人大出血死亡。有一些出血可救,但有些根本来不及救治,比如大的支气管动脉、右肺动脉主干、左肺动脉主干、右肺中间段的肺动脉主干等。这些地方一旦出血,无论选择什么样的抢救方法,对病人来说,抢救成功率几乎为零。死亡的原因主要是出血阻塞气道或因大出血休克死亡;还有一些医生,比如硬镜盲目操作造成气管断裂,有的稍一用力,直接穿透薄弱的气管,插入纵膈,还有的从咽部插到纵膈,这些都可能给病人带来危及生命的伤害。
这些都有活生生的案例。因此,我们的任务是把呼吸介入技术用到最恰当的地方,关键是在患者最需要的时候,给予患者好处,救治患者生命。诊疗思维是什么?何时用?如何保证患者安全?如何让患者最大化获益?这是做呼吸介入的根本所在。
2000年,美国学者Beamis提出「介入性肺脏病学技术」新概念,为呼吸系统疑难危重疾病诊治开辟了新途径。 何谓「呼吸介入技术」? 根据2001年ERS和ATS 定义,「呼吸介入技术」是以内窥镜为介入工具,在人体肺脏内进行操作,从而取得诊断和治疗的一组新技术。 2001年全国呼吸年会上,钟南山院士提出「向呼吸介入技术进军! 」后在王辰院士的大力推动下,我国呼吸介入技术得到快速发展。 从下图中我们可清晰浏览呼吸介入技术的应用范围。 对于呼吸系统疾病而言,没有呼吸介入技术,很多疾病无法诊断和治疗。 以肺部感染为例,最重要的是病原学诊断,诊断不清就有可能盲目使用各种抗生素。 因此,诊断,首先就要靠 介入技术的快速取到精确标本。
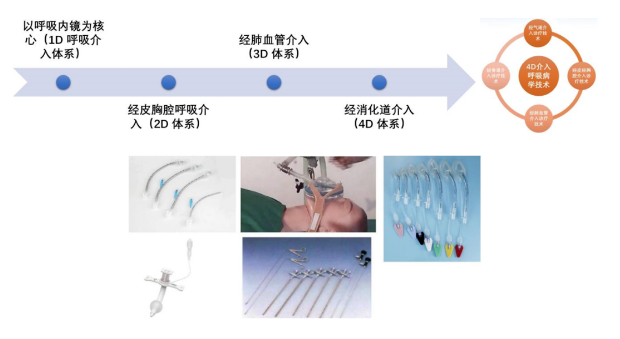
诊断的目标,是从肺、气管的远端取到标本。要取到这些标本,可依靠介入通道引导,目前临床常用的介入通道有 内镜面罩、喉罩、气管插管和气管切开、硬镜。首先要了解它们的特点:
内镜面罩的特点是适用于患者一般情况好且相对简单、耗时短、风险小的操作;喉罩的特点是容易建立,通气可靠性佳,适用范围广,是大多数复杂气道介入诊疗首选的途径,尤其对声门下病灶更为有效;气管插管和气管切开的特点是通气保障效果最佳,但不适用于气管中上段病变,且气管导管内径对操作器械有限制;硬镜的特点是使用特殊情况的操作如硅酮支架、气道Y形支架的取放、复杂异物的取出等。
在介入通道技术的引导下开展诊断技术。其中包括:气道内可见病灶取样术、中央气道外病灶取样术、肺外周病灶取样。在此我更想强调:对于镜下可见的病灶,有的可以直接取样,有的看见了也不一定要取样。因为肉眼无法看见病灶的实质,比如,一个支气管动脉瘤,粘膜有一个局部突起,看到病灶就能取吗?支气管动脉瘤的活检取样,必然造成大出血,抢救得及时、方法正确,患者可能有活的希望,抢救不好,患者可能因大出血窒息或休克死亡。因此,对气道内可见病灶的取样,一定要先对病灶进行判断,该不该取?判断清楚以后再取样。
对中央气道外的病灶,如气管、隆突、左右主支气管、中间段支气管等,这些中央气道周围的病灶如何取?现在可在CT定位下直接穿刺,或在超声镜,EBUS-TBNA找到病灶,再结合CT、超声定位取病灶;对肺外周的病灶,现在有很多种导航技术,如虚拟导航、小超声、磁导航、光学导航等,结合C臂CT联合进行外周取样。
看不到的病灶、外周的病灶要冷冻活检如何取样?可参考关于冷冻外周活检的共识,但要注意它并非A类证据
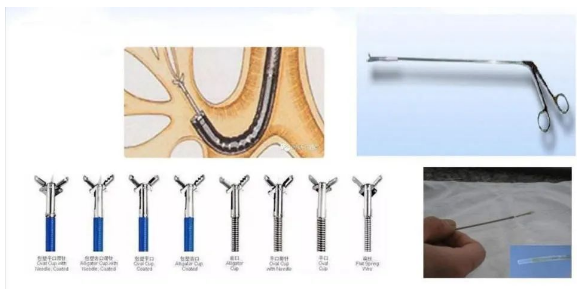
这是对气道内可见病灶看到后可直接通过活检、刷检、灌洗等方法取样。可用钳子夹,也可用冷冻活检。对于肺外周弥漫性病灶,亦可用冷冻活检。

关于冷冻活检我想强调,在气道里看见的病灶,尤其是松软的病灶,用冷冻取活检相对比较安全,且取出的病灶较大,活检的阳性率就会提高。但关键看冷冻探头大小。冷冻探头大,可获得的病灶更大。 能看到的病灶,冷冻活检取样必定会好许多,但看不到的病灶、外周病灶,冷冻活检该如何取样呢?国内由我们介入呼吸病学学组出了关于冷冻外周活检的共识。但依然要提醒大家,共识只能作为参考,不能作为绝对标准执行,因为共识非A类证据。 只有A类证据才是多中心的、前瞻性的临床研究结果。我们现在所见的专家共识,都非A类证据,只能作为参考。尤其是几位专家、个别专家提的共识,更不能作为临床诊疗依据,只能借鉴他们的个人经验。
我们在镜下看见的病灶,还要结合当前技术进展进行判断。比如:用荧光支气管镜、窄谱支气管镜可帮助我们判断病灶该不该取。
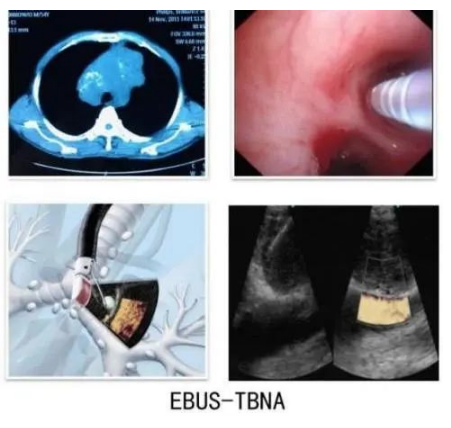
中央气道外的病灶取样主要是EBUS-TBNA技术,这项技术目前应用非常广泛,阳性率亦很高。

以上左图为中央气道外病灶的取样术,应用其他一些导航技术进行活检;右图为肺外周病灶取样术,现在用得多的,比如小超声和虚拟导航、磁导航等。
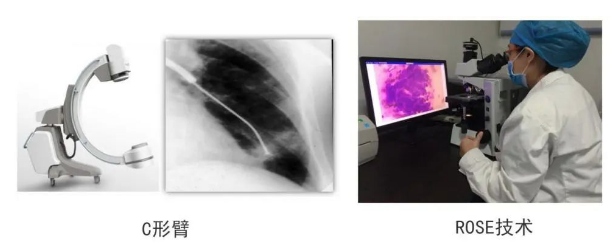
这是C形臂。无论安装大C还是中C,这些设备加导航联系起来应用,能让肺外周病灶活检的阳性率明显得到提高。目前我们将细胞学诊断用于指导穿刺诊断,现场经穿刺后直接进行细胞学检查。但细胞学检查必须要有对细胞学精通的医生,最好是在病理科工作过的医生现场看出细胞有无问题,穿刺位置准不准,他们可以帮助呼吸医生进行准确诊断,提高诊断速度和诊断准确率。
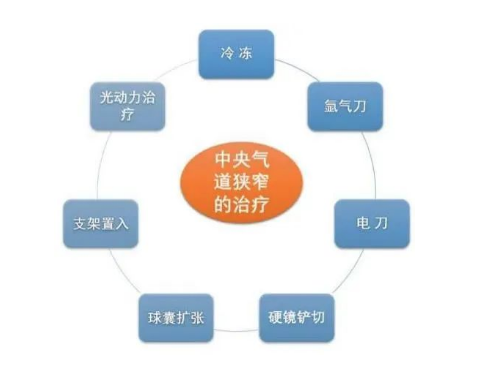
介入呼吸病学诊疗技术发展迅猛。通过镜下引导到达病灶部位,目前可用到的技术工具丰富多样,同时也在不断出现新技术。过去我们使用微波较多,最早我们使用微波技术治疗中央气道的病变,随着近几年新设备如电刀、氩气刀、冷冻、激光等技术的出现,微波逐渐被淘汰。但现在对肺外周小结节又有了微波消融这项技术,并逐步在临床中得到推广。 事实证明,过去淘汰的一些技术,可能经过创新改良后,也会起到较好的作用。

所有治疗技术、方法的应用一定是要与患者的具体情况相结合,切忌盲目行动,要严格做好术前评估和准备工作以及预防不良事件发生的预案
还想特别提醒大家,介入诊疗技术、方法的应用一定是要与患者的具体情况相结合。比如:患者气道里有一个巨大的肿瘤,造成气管严重阻塞,病人面临窒息死亡,该情况下我们可能第一步要以最快的方法打通气道,先救命,再治病!在操作过程中防止严重并发症的发生,如气道梗阻或大出血,这就要求我们必须具备: 第一,必须切下来后快速取出;第二,防止术后出血或出血后快速止血并保持气道通畅。这时要思考该如何做?首先必须全麻,因为这种患者一旦做局麻,假如出血突然窒息,立即心脏就停跳。全麻下这种可能性较小。全麻下出血,能给医生有一定的时间抢救,因为全麻下的患者通常不会突然窒息死亡;第二,如果面对巨大的肿瘤,要思考有没有把握切下来之后一次取出,一次取不出,可能会发生远端梗阻,如隆突或左右主支气管的梗阻。因此, 做好所有准备工作后再对患者进行综合性治疗,任何准备工作没做好都不能盲目行动。
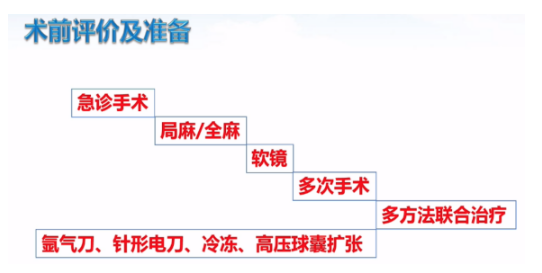
术前评价及准备非常重要,每一道程序、步骤都不能省略,要做到位,评价能否手术更重要。在此我想讲一个曾经打过官司的案例:患者是在做气管镜活检时大出血,抢救后经鉴定认为院方有责任,患者家属将院方告上法庭。责任在哪?第二次做气管镜活检术前没有做心电图。当时的情况是,患者在第一次做完气管镜后过了约2周时间,再次做气管镜时省略了心电图这个步骤。患者术中发生大出血,窒息导致心脏骤停,后经复苏抢救过来。但鉴定专家认为,患者术前就有冠心病,术前没有近期心电图,患者在术中因出血造成缺氧,缺氧导致心梗所致室颤。即便患者抢救后恢复过来再做心电图结果正常,也不能说明术前那次心电图没有问题。鉴定专家会认为漏掉这个环节是不应该的。
但实际上这个患者真正的问题出在哪?是因为对气管镜活检出血没有判断好,不应该取活检。该患者是长期慢性炎症造成的局部大量黑色素组织增生,局部支气管动脉瘤。最终,由于抢救时间过长,患者大脑缺氧,有一些后遗症。现在再回过头来分析,患者的心脏骤停并非冠心病和心梗,而是大出血窒息。但鉴定专家判断因术前没有做心电图,无法证明术前是否有冠心病或心律失常。本应是轻微责任,变成了主要责任,其结果有着天壤之别。法官认为,术前医生为什么不做心电图?做了心电图如果有问题,心梗就可以预防和避免;反之,不做心电图,患者发生心梗险些死亡,就是这个环节疏忽遗漏的原因,负主要责任。
因此,我讲这个案例就是提醒大家,术前准备和术前评价一定要坚决按规定执行,千万不能马虎,要把患者的所有资料、病史、用药情况把握得非常清楚,操作过程中想到最适当、恰当的操作办法,保证操作过程安全。医生的脑子不能迷糊,不能简单思考一个问题。所有问题被简单化处理后,最终结果可能很恶劣、很糟糕。不如把所有程序、步骤做到位,做在前。因为一旦鉴定不对,伤害的不仅是患者,还有医生和医院,事实也可能被扭曲。

本文由《呼吸界》编辑 冬雪凝 根据金发光教授讲课内容整理
专家介绍

金发光
教授,主任医师,博士生导师,现任空军军医大学第二附属医院呼吸与危重症医学科主任,唐都医院大内科主任。兼任世界内镜医师协会呼吸内镜协会副会长、内镜临床诊疗质量评价专家委员会常务委员、陕西省医学会内科学分会主任委员、呼吸结核分会名誉主任委员、中华医学会内科学分会常务委员等。


