前言
重症哮喘患者病情发作时呼吸困难明显,被迫端坐位、张口呼吸、大汗淋漓、精神高度紧张。由于患者采取被迫体位,同时伴有体液大量丢失,造成血流缓慢、血液淤积,很容易并发肺栓塞。如果哮喘病人并发肺栓塞,则呼吸困难进一步加重。此时,应用支气管扩张剂及大剂量糖皮质激素等治疗症状常常无明显改善,甚至应用机械通气缺氧症状也难以纠正。哮喘合并肺栓塞容易被误诊,延误治疗甚至危及患者生命。现报道1例如下,并结合文献对该病例进行讨论。
临床资料
患者,男,81岁。因「反复胸闷气促30余年,再发10天」于2013年6月20日入院。患者有支气管哮喘病史30余年,一直未正规诊治;10天前无明显诱因再次出现胸闷气促加重,不能平卧,自行硫酸沙丁胺醇气雾剂喷雾治疗后无好转。诊断「支气管哮喘急性发作」收住入院。
入院查体
体温36.0℃,脉搏 81次/分,呼吸 35次/分,血压 140/94mmHg,神志清楚,精神软,口唇无发绀,呼吸急促,不能讲话,颈软,气管位置居中,浅表淋巴结未触及肿大,双肺叩诊过清音,听诊呼吸音低,两肺闻及干湿啰音,心率81次/分,律齐,腹平软,无压痛、反跳痛,肝脾肋下未及肿大,双下肢不肿。
入院时实验室检查
2013年6月20日胸片显示两肺未见明显实质性病变。血常规:白细胞6.5×10^9/L,血红蛋白137g/l。电解质:K+3.39mmol/l,Na+140.9mmol/l,Cl-107.7mmol/l,Ca2+2.10mmol/l。血气分析:PH7.411,PO2:180mmHg,PCO2:37.4mmHg,BE:-0.5mmol/l,BNP:182.6pg/ml。
诊疗过程
入院后予头孢哌酮舒巴坦针(可倍)抗感染,辅以雾化平喘、化痰等对症处理。6月21日凌晨出现胸闷气促加重,端坐张口呼吸,伴大汗淋漓,呼吸频率35次,两肺广泛哮鸣音,急诊血气PH7.084,PaO2:78.9mmHg,PCO2:77mmHg,BE:-6.7mmol/l,考虑支气管哮喘持续状态,立即气管插管接有创呼吸机辅助呼吸,同时予甲强龙抗炎、补液营养支持等对症处理,后患者症状逐渐改善,肺部哮鸣音减少,6月25日予气管拔管。但拔管后患者一直感胸闷,两次查血D-二聚体偏高,考虑是否存在肺栓塞可能,7月3日CTPA提示慢支、肺气肿征象,右肺中叶小结节。两侧胸腔少量积液,CTA示双侧肺动脉主干及右侧上、中、下叶肺动脉,左侧上叶肺动脉栓塞(图25-1)。彩超:双下肢所测动脉少许微小粥样斑块。诊断「肺栓塞」明确,予低分子肝素皮下注射及华法令片口服,同时监测凝血功能,治疗后病情逐渐好转,7月18日复查肺动脉CT未见明显异常,7月19日予带华法令出院,嘱其门诊监测凝血功能等指标。
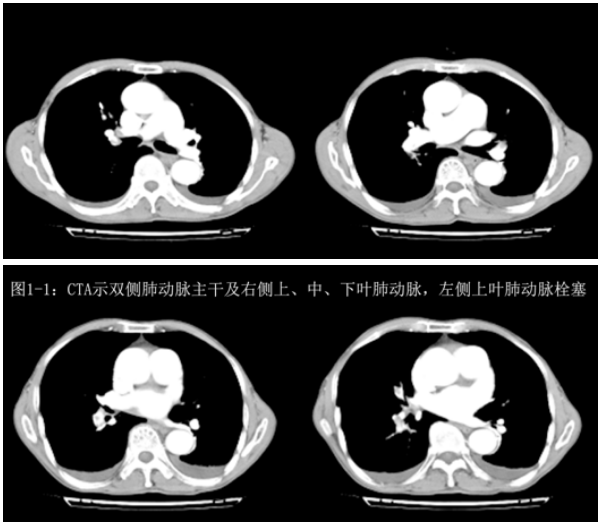
【图】CTA示双侧肺动脉主干及右侧上、中、下叶肺动脉,左侧上叶肺动脉栓塞
讨论
急性肺栓塞(acute pulmonary thromboembolism,APTE)是由于内源性或外源性的栓子堵塞肺动脉主干或分支,引起肺循环障碍的综合征,在心血管疾病中排第三,年发病率100/10万~200/10万,是临床常见的危重症之一 [1],其主要原因是深静脉血栓形成(deep venous thrombosis,DVT)的发病率高。肺栓塞(pulmonary thromboembolism, PTE)的临床常见症状为呼吸困难、胸闷、胸痛、晕厥、烦躁不安、惊恐、咯血等呼吸及心血管系统症状,常伴随其他疾病如恶性肿瘤、糖尿病、肺部基础疾病等发生,由于其缺乏特异性的症状,临床上误诊及漏诊率高。
本例患者为81岁老年男性,既往有30余年哮喘病史,因再发胸闷气促10天入院,入院后第二天病情加重,呈端坐位张口呼吸,伴大汗淋漓,呼吸频率增快,两肺可及广泛哮鸣音,动脉血气提示Ⅱ型呼吸衰竭,为典型重症哮喘表现,结合既往哮喘病史,重症哮喘诊断基本明确;经积极抗炎、平喘及机械通气后气喘好转,肺部体征不明显,但胸闷现象持续存在,无法用单纯哮喘解释,且两次查血D-二聚体偏高,考虑是否存在肺栓塞可能,故而完善CTPA后明确诊断。此类以胸闷为唯一症状、伴随哮喘急性发作而发生的肺栓塞患者并不少见,但因其临床表现与单纯哮喘患者相比无特异性,临床上常被漏诊或误诊,故而相关临床报道甚少。有研究表明,美国每年发生致死性深静脉血栓及肺栓塞患者约29.64万例,其中60%的患者被漏诊或误诊,只有7%的患者得到及时与正确治疗[2]。而报道称PTE患者早期诊断和规范治疗病死率可由12.5%降至4.5%[3]。因此,这就要求临床医师对PTE病因及危险因素提高认识,早期诊断,正确治疗。
PTE发病原因主要是存在血流动力学及血液流变学的改变,如血液缓慢、粘稠、血液淤积、血管内皮损伤等,其危险因素包括易栓倾向和获得性危险因素。其中获得性危险因素包括高龄、肥胖、下肢手术、动脉疾病、深静脉血栓病史、急性感染、真性红细胞增多症、活动受限、避孕药以及激素替代治疗等。有研究表明,哮喘患者发生PTE的风险是非哮喘患者的3.24倍[4],其可能机制有:1.哮喘患者由于喘息症状反复发作,慢性缺氧,继发红细胞增多,血液粘稠;喘息症状发作时被迫坐位、张口呼吸、大汗淋漓等,使得体液进一步丢失,血流更加缓慢、淤滞[5];2.反复感染,电解质、酸碱代谢失衡等造成细胞代谢紊乱、血管内皮损伤诱发血栓形成;3.哮喘患者存在氧化与抗氧化失衡[6]、氧化应激[7]引起组织损伤等;上述三种因素综合作用,从而诱发PTE的发生。此外,哮喘患者,尤其是重症患者,常需连续使用高剂量的糖皮质激素。最新的研究表明,糖皮质激素可使VTE[8]和PTE的风险增加[9]。而在本例中,患者高龄,哮喘病史较长且未规范治疗,急性发作时长时间端坐位喘息、张口呼吸、大汗淋漓等造成血液粘稠、血流缓慢,再加上感染、酸碱失衡及糖皮质激素使用等多因素存在,从而诱发了PTE的发生。
PTE患者由于栓塞引起气道痉挛,肺顺应性下降,肺水肿导致低氧血症,由于严重的通气/血流比例失调,一般治疗效果差;而栓子本身可释放5-羟色胺、缓激肽、组胺致气道痉挛加重哮喘。因此,哮喘患者一旦发生PTE喘憋症状进一步加重,常规使用平喘药物症状难以控制,且症状常被掩盖,造成误诊、漏诊,给患者造成生命威胁。因此,哮喘患者发作期如症状控制不理想应及时想到发生PTE的可能,应尽早行CTPA检查,目前CTPA检查仍然是诊断PTE的金标准。
其他辅助检查对鉴别哮喘是否合并PTE有一定意义。研究报道称70%的下肢DVT患者会发生PTE[10]。当怀疑PTE时,临床首选双下肢静脉超声检查,当哮喘患者经超声检出DVT对寻找PTE的成因和发病危险因素有着肯定价值。心电图呈SⅠQⅢTⅢ综合征,是PTE患者经典心电图特征,对是否合并PTE有重要参考意义。D-二聚体是交联纤维蛋白在纤溶系统作用下的特异性降解产物,发生PTE时,体内的纤溶系统被激活,外周血D-二聚体水平可显著升高,对于排除和提示肺栓塞均有重要作用,但其诊断PTE的特异性随着年龄的增长而稳步下降。新指南推荐,对D-二聚体在年龄>50岁的人群中,需进行年龄校正,即测定值+年龄×10,代替以往500μg/L的临界值,排除PTE的可能性由6.4%升至29.7%[11]。因此对于发生DVT或PTE的高风险患者,D-二聚体仍是首选的检测指标。
综上所述,哮喘患者为肺栓塞的高发人群,当哮喘患者存在以下危险因素:既往高龄、肥胖、VTE病史、近期手术史、恶性肿瘤史、长期卧床≥7天时更易并发PTE。哮喘合并PTE患者的临床表现无特异性,临床上以哮喘患者出现晕厥、休克、难以纠正的胸闷,体检发现双下肢非对称肿胀,一般治疗后低氧血症难以纠正,心电图出现SⅠQⅢTⅢ综合征,血浆D-二聚体水平升高等,需警惕是否合并PTE的发生,应进一步合理安排CTPA检查确诊。
参考文献
[1] Konstantinides SV, Torbicki A, Agnelli G. et al. 2014 ESC guidelines on the diagnosis and management of acute pulmonary embolism. Eur Heart J. 2014 Nov 14; 35(43):3033-69
[2] Heit, JA, Cohen AT, Anderson FA. Estimated annual number of incident and recurrent,non-fatal venous thromboembolism(VTE)events in the US.Blood, 2005, 106: 267A
[3] 蔡柏蔷,李龙芸.协和呼吸病学[M].北京:中国协和医科大学出版社, 2005: 1009
[4] Chung WS, Lin CL, Ho FM, et al. Asthma increases pulmonary thromboembolism risk: a nationwide population cohort study. Eur Respir J 2014, 43: 801–807
[5] Majoor CJ, Kamphuisen PW, Zwinderman AH, et al. Risk of deep vein thrombosis and pulmonary embolism in asthma. Eur Respir J 2013,42: 655–661
[6] Ruprai RK. Plasma oxidant–antioxidants status in asthma and its correlation with pulmonary function tests. Indian J Physiol Pharmacol 2011,55: 281–287
[7] Martinez M, Cuker A, Mills A, et al. Nitrated fibrinogen is a biomarker of oxidative stress in venous thromboembolism. Free Radic Biol Med 2012,53: 230–236
[8] Johannesdottir SA, Horva´th-Puho´ E, Dekkers OM, et al. Use of glucocorticoids and risk of venous thromboembolism: a nationwide population-based case-control study. JAMA Intern Med 2013, 173: 743–752
[9] Stuijver DJ, Majoor CJ, van Zaane B, et al. Use of oral glucocorticoids and the risk of pulmonary embolism: a population-based case-control study. Chest, 2013, 143: 1337–1342
[10] Gunen H, Gulbas G,In E,etal. Venous thromboemboli and exacerbations of COPD [J]. Eur Respir J, 2010, 35(6): 1243-1248
[11] Konstantinides SV, Torbicki A,Agnelli G, et al. 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism: The Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC) Endorsed by the European Respiratory Society (ERS)[J]. Eur Heart J, 2014, 29. pii: ehu283
本文完
作者:崔恩海、华锋 - 浙江大学湖州医院 湖州市中心医院 湖州市呼吸病研究所
本文转载自订阅号「重症与康复」(ID:CriticalAndRehabCare)



