
这位患者是一名59岁男性,上海人,已退休,罹患急性白血病近3年,反复接受多次化疗,但病情依旧反复,2018年3月骨髓再现29%原始细胞,提示全面复发。本次收住入院拟进行挽救化疗序贯单倍体造血干细胞移植。
移植前10天
开始发热,伴轻度畏寒,无咳嗽、咳痰、胸痛、胸闷等不适,血常规示WBC 0.2×10^9/L,RBC 2.1×10^12/L,Hgb 70g/L,PLT 23×10^9/L,患者进入骨髓抑制阶段,给予亚胺培南西司他丁钠抗感染治疗……
3天后
发热无好转,联合利奈唑胺广谱经验性治疗,降钙素原、血培养等感染指标均为阴性,发热逐渐好转。
移植后5天
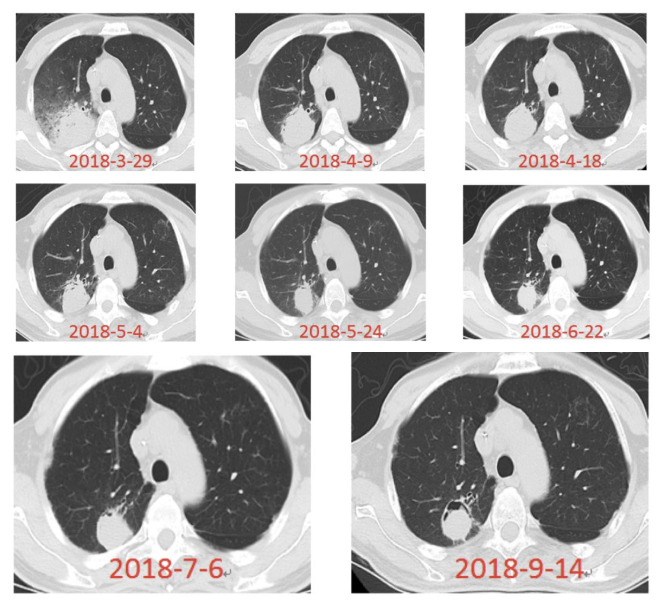
再次发热,伴畏寒、头痛、口腔黏膜炎、呕吐、腹泻等新发症状,咳嗽少痰,抗生素调整为头孢哌酮-舒巴坦钠联合替加环素(当时同病区有多药耐药肺炎克雷伯杆菌检出),停用利奈唑胺,同时改变原预防真菌用药(口服氟康唑)为卡泊芬净静脉滴注进行经验性抗真菌治疗,胸部CT平扫(2018-3-29)发现:右肺上叶大片渗出、实变灶,当时血、痰细菌及真菌培养均无阳性发现,痰涂片找抗酸杆菌阴性,血GM试验阴性,呼吸道病原体九联检包括肺支原体、衣原体、流感病毒、副流感病毒等均阴性,一周以来降钙素原持续增高为2~3ng/ml。
结合患者长期化疗免疫低下以及处于造血干细胞移植粒缺期等宿主背景、肺部病变影像学实变特征,临床考虑侵袭性肺曲霉病可能最大,因其感染病变范围较大,且患者尚未达到骨髓植入全血细胞依旧减少,预估此类患者感染进展迅速,建议实施伏立康唑联合卡泊芬净的二联用药,抢先抗真菌治疗。呼吸科会诊建议等待患者外周血进一步恢复后进行肺泡灌洗等有创操作,以减少严重出血等操作风险。
抗感染10天后
再行CT发现:感染病灶边界清晰化,范围明显缩小,考虑抗真菌治疗有效,继续原方案控制感染。
此时患者造血干细胞已开始植入,粒细胞、血小板等计数稳步上升,立即进行了支气管镜检查,镜下支气管通畅,未见新生物,右上叶后段分泌物较多,粘膜轻度充血水肿。进一步右肺上叶后段进入超声探头,可见片状中高不均质回声病灶约2cm,局部予以刷检及活检。刷检涂片及灌洗液培养未有阳性发现,但灌洗液GM试验结果增高达到5.244,灌洗液及活检组织经高通量测序回示:曲霉属,检出序列数分别为470和7503。抗感染治疗6周后病灶体积显著缩小,患者顺利出舱,序贯伏立康唑口服,门诊继续随访。
讨论要点
1、曲霉感染与宿主免疫的关系?侵袭性肺曲霉病肺泡灌洗液GM试验的敏感特异性如何?是否优于血清GM结果?高通量基因测序的报告怎样解读?持续存在的残余感染灶如何处理?
2、肺曲霉病有哪些影像学改变?曲霉感染具备嗜血管特征,影像学上有何特征性变化?如何早期识别气道侵袭阶段的肺曲霉?
3、血液病/恶性肿瘤患者侵袭性肺曲霉病的治疗用药选择?如何根据PK/PD优化抗真菌治疗?
讨论与点评
呼吸科 李君杰
曲霉感染类型与宿主免疫状态有关,侵袭性肺曲霉病多发生于高度免疫抑制宿主,亚急性侵袭性肺曲霉病多发生于中度免疫抑制宿主,而慢性肺曲霉病多发于轻度及无免疫抑制宿主。变应性支气管肺曲霉病及非侵袭性曲霉病多发于免疫正常宿主。
国外多部指南建议血清GM及BAL GM试验作为诊断血液系统恶性肿瘤及HSCT患者中侵袭性曲霉病的精确诊断标志物,其敏感度约70%。而在非血液系统恶性肿瘤患者(如实体器官移植及慢性肉芽肿性疾病)、非粒缺患者、ICU患者及接受抗霉菌治疗的患者中,血清GM敏感性显著下降, 强烈推荐行BALF GM试验。
曲霉PCR及高通量测序(NGS)方法常用于血及BALF检测,具有较好的敏感率。但BALF中检测到的曲霉菌很难鉴别为定植菌还是感染菌,需结合患者临床表现、BALF GM结果及多次测序结果综合判断。另外,由于目前缺乏标准化检测方法及通过临床验证的商业化试剂盒,不推荐在常规临床实践中应用曲霉基因检测方法。
推荐IPA的疗程至少持续6~12周,具体疗程取决于免疫抑制的程度和时长、感染部位和疾病改善的证据。本例患者治疗14周时临床及实验室指标皆改善,但肺内病灶未完全吸收,建议继续抗真菌治疗,检测肺内病灶,若治疗6~12月后肺内病灶仍未完全吸收,可进一步性BALF GM及肺穿刺活检找曲霉菌,若无曲霉菌现症感染依据,可考虑停药,反之建议继续抗真菌治疗。
放射科 李若坤
影像学上,肺曲霉菌病通常分为4型:曲霉菌球(Aspergilloma)、变应性支气管肺曲霉菌病(Allergic Bronchopulmonary Aspergillosis,ABPA)、血管侵袭性曲霉菌病(Angio-Invasive Aspergillosis)和气道侵袭性曲霉菌病(Airway-Invasive Aspergillosis)。前两者多见于免疫正常人群,后两者多见于免疫抑制状态患者。
肺曲霉菌球是曲霉菌在在原有空腔中定植(如结核、结节病、肺气肿、肺气囊、支扩等所致空洞),无肺组织侵犯,上叶多见,影像上表现为实性软组织密度,可随位置移动,可见「新月征」(Crescent sign),是由曲菌球、空洞内气体和空洞勾勒出的新月样间隙,具较为特异的征象。
ABPA多见于哮喘或囊性纤维化患者,可见中心区域的支气管囊状扩张,上叶多件,管腔内因黏液潴留而呈Y形、V形或指套征。
血管侵袭性曲霉菌病几乎只见于免疫抑制状态人群,尤其是伴有严重中性粒细胞缺乏者(WBC < 500),高危因素包括骨髓移植、血液系统恶性肿瘤、大剂量皮质激素治疗、Cushing综合征、再生障碍性贫血等。
病理上常继发肺组织缺血性坏死和出血性梗死。影像学上表现为肺内斑片影、实变影、结节影或者磨玻璃密度影。「晕征」是特异性征象,表现为实变或结节周边的磨玻璃密度影,代表出血性梗死。恢复期也可出现为「新月征」。对于一些免疫抑制状态相对较轻的患者(如基础肺病、慢性消耗性疾病、糖尿病、酗酒等),影像学上可表现为慢性进展性叶/段实变或空洞。
气道侵袭性曲霉菌病可以伴或不伴血管侵袭性曲霉菌病,病理上可见气道基底膜存在曲霉菌,临床上表现为急性气管-支气管炎、细支气管炎、支气管肺炎等。影像学上可见支气管管壁增厚、沿支气管血管束分布的斑片影和磨玻璃密度影。
药师 方洁
近年来深部真菌病发病率呈持续上升趋势,此与机体免疫功能受损机会增多有关,由于深部真菌病患者病情严重,常危及生命,因此有效控制真菌感染具有重要临床意义。本例患者使用了伏立康唑和卡泊芬净治疗曲霉菌感染,临床效果良好。
卡泊芬净为棘白菌素类抗真菌药物,通过抑制丝状真菌和酵母细胞壁的(1,3)-β-D-葡聚糖的合成而杀灭真菌,因人体细胞无细胞壁,因此该类药物毒性较小,已成为临床治疗深部真菌感染的重要药物,口服不能吸收,只能静脉给药,呈线性动力学特征。棘白菌素类对念珠菌为杀菌剂,对曲霉为抑菌剂,为浓度依赖性且具有较长PAFE(抗真菌后效应)的药物。
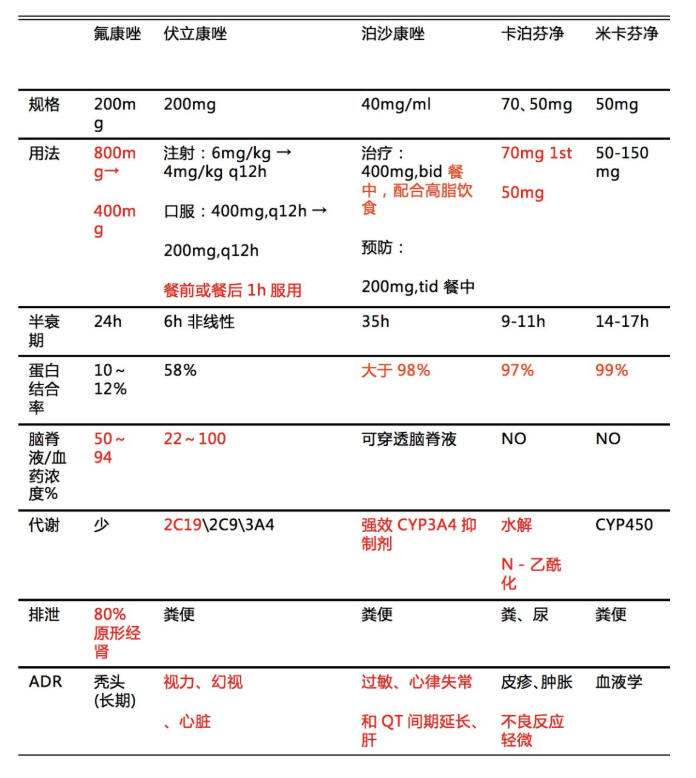
伏立康唑为三唑类抗真菌药物,主要通过抑制细胞色素P450酶介导的14α-甾醇去甲基化,抑制真菌细胞膜上麦角固醇生物合成,从而破坏真菌细胞膜的完整性,达到抑制真菌生长的目的,但对人体细胞膜胆固醇合成无影响。三唑类属于时间依赖性且PAFE较长的药物。常用抗真菌药物的重要参数见下表。
周敏主任点评
这是一例侵袭性肺曲霉病患者,诊断时往往需结合患者的宿主免疫状态来判断,此例是造血干细胞移植过程中并发,在血液恶性肿瘤疾病中很常见。
除此之外,我们呼吸科发现该病可以发生于许多不同的职业,如油漆工、建筑工、菜市场商贩等,可能与他们长期劳作的工作环境有关,在机体抵抗力下降时定植也有可能演变为侵袭性感染。
曲霉感染为一个动态过程,其诊断也随着微生物、影像学等依据逐渐的明晰而层次分明,GM试验是我们常用的检测与随访指标,特异性高,但有时还是未免假阳性的可能,如此例患者血清GM始终阴性,但肺泡灌洗液中GM很高,这也符合疾病进展规律,肺曲霉感染早期处于气道侵袭阶段尚未累及血管,且患者从移植开始就接受真菌预防治疗及后来的经验性治疗,致使两种标本GM结果截然不同;曲霉感染有噬血管特征,后期侵犯血管时血清GM阳性再次增高。二代测序具有非常高的敏感度,但BALF中检测到的曲霉菌并不能排除定植的可能,也不构成确诊肺曲霉的依据,还需结合临床表现、BALF GM及多次测序结果综合判断。
该患者明确诊断方向后,及时采取抗曲霉抢先治疗联合用药,在获得最终病理依据之前即获得明显疗效,治疗上并未耽搁,最终通过呼吸科介入检查获得充分依据而确诊。
经过半年治疗,目前影像学上仍有残留感染灶,虽然患者已无任何临床症状,但还是建议继续抗真菌治疗。我们曾遇到类似患者,宿主免疫状态优于本例患者情况,但过早停止用药还是造成了日后残留病灶的复燃,尽管各大指南均有关于疗程的推荐,但基于宿主背景不同仍有许多差异。鉴于该患者的情况必须坚持足疗程,根据最新影像已出现新月征,后期随访中需提醒患者注意在病灶吸收过程中可能出现咯血等症状,必要时求助胸外科手术介入,以避免发生严重出血。
另外,若患者感染后出现严重喘息等症状,往往与曲菌引起的变态反应有关,可通过IgE水平等检测来评估,治疗上可以适当加用小剂量激素缓解症状。
作者介绍



