推荐语
中年女性咳嗽发热数周,期间自行服用止咳药、前往当地医院治疗无明显成效……胸部CT示双肺多发片状影,病灶为何好转后再次加重?最初的治疗思路是否正确?为何直播间开始有观众「质疑」病理的诊断意义?这位患者最终成功诊治,专家说值得进一步思考的问题有哪些?
患者,女,43岁。 职业:仓库管理员;2018年6月2日入院。
主诉:咳嗽3周,发热2周。
现病史:
2018年5月10日,患者劳累后出现咳嗽、咳少许黄白粘痰,无发热、盗汗、咯血、胸闷、气促等,自行口服止咳药物后无好转。
5月19日,开始出现发热,Tmax 38.7℃,伴畏寒,偶有寒战。遂至当地医院就诊,查WBC 6.8×10^9/L,NE 78.7%↑,hs-CRP 72.29mg/L↑,PCT(-),甲流病毒抗原(-)。胸部CT提示两肺多发浸润影,右肺为主。当地医院先后予阿莫西林克拉维酸、哌拉西林他唑巴坦抗感染,并予止咳化痰、解痉平喘等治疗。患者仍有咳嗽、咳黄痰,体温无明显下降。
5月30日,复查CT病灶无明显吸收。
6月2日,为进一步诊治至我院急诊就诊,查WBC 8.73X10^9/L,NE 81.8%,CRP>90.0mg/L,PCT 0.07ng/mL,CA125 61.7U/mL。予头孢美唑、莫西沙星抗感染治疗。现为进一步诊治收入我科。
病程中精神可,胃纳夜眠可,二便如常,体重无明显变化。
既往史:有慢性胃炎史,余无殊。
个人史:自诉起病前曾至发霉环境。余无殊。
婚育史、月经史、家族史:无殊。
体格检查:
T:36.7℃ P:88 次/分 R:18 次/分 BP:110 / 70mmHg
SpO2 95%(未吸氧)神清,呼吸平稳,自主体位,查体合作。全身皮肤未见皮疹,全身浅表淋巴结未及肿大,气管居中,胸廓无畸形,双肺呼吸音粗,右肺散在少许湿啰音,心率88bpm,律齐,腹部平软,肝脾肋下未及,四肢脊柱无畸形。
辅助检查:
2018-5-19 外院血常规:WBC 6.8×10^9/L,NE 78.7%,
2018-5-19 外院 hs-CRP 72.29mg/L↑,PCT(-),甲流病毒抗原(-)。
2018-6-2 本院血常规:WBC 8.73X10^9/L,NE 81.8%,
2018-6-2 CRP>90.0mg/L,PCT 0.07ng/mL,CA125 61.7U/mL
胸部影像学检查:
2018-5-20 外院胸部CT:

2018-5-30(抗感染治疗后):
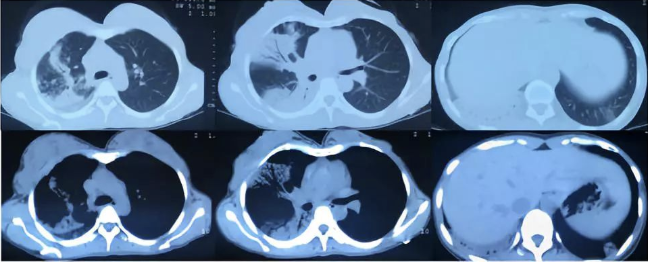
总结病例特点
中年女性,既往体健。本次亚急性起病,起病前有劳累、曾到过发霉的仓库;临床表现为咳嗽咳痰3周,发热2周,伴畏寒,无明显呼吸困难,无盗汗、咯血。外院抗感染治疗10天症状无好转。
查体:SpO2 95%(不吸氧),神清,呼吸平稳,消瘦,右肺听诊闻及少许湿啰音。
辅检:N%、CRP升高,胸部CT提示两肺多发斑片实变影,右肺为著。
初步诊断与鉴别诊断
诊断需考虑感染性病变(CAP、肺部真菌感染、肺结核)与非感染性病变(肿瘤性病变、结缔组织疾病、间质性病变等)。结合患者临床特点,暂有的辅检结果,优先考虑CAP;同时需完善相关检查排除肺结核、血管炎、机化性肺炎等。
治疗方案选择
患者按CAP初始抗感染治疗效果不好;可从无反应性肺炎方面考虑,包括治疗不足(初始治疗未覆盖病原体,或病原体耐药);少见病原体感染;肺炎合并症;非感染性病变。经综合考虑暂予升级抗生素,同时进一步检查明确有无少见病原体,及非感染病变存在。
入院后予以美罗培南1.0 q12h抗感染治疗,同时辅以止咳化痰等治疗。
入院后的辅助检查:
血常规:WBC 8.73×10^9/L,NE 81.8%,LY 7.7%。
炎症指标:CRP>90mg/L,PCT 0.07ng/ml,ESR74mm/h
血气分析:pH 7.49,PaCO2 28mmHg,PaO2 80mmHg,AB 21.3mmol/L,SB 24.1mmol/L,BE -1,SaO2 97%(未吸氧)
生化:肝肾功能、电解质:K+ 3.4mmol/L,白蛋白27g/l,余正常范围。
出凝血:纤维蛋白原843mg/dl,D二聚体1.81mg/L
微生物:呼吸道9联检(-),隐球菌荚膜抗原定性检测(-),G试验(-),T-SPOT A抗原1/B抗原6,HIV抗体(-),梅毒特异性抗体(-)
肿瘤标志物:CA125 61.7U/ml,AFP、CEA、CA19-9、NSE均正常
自身抗体:抗核抗体 着丝点1:1000,抗着丝点抗体(+),其余阴性
细胞免疫:B淋巴细胞CD19 5.1%,T淋巴细胞CD3 88.2%,Th淋巴细胞CD4 40.8%,Ts淋巴细胞CD8 45.8%,CD4/CD8 0.9,自然杀伤细胞(CD56+16) 5.9%
尿常规:蛋白+,红细胞± 尿蛋白定量:0.38g/24h(0-0.15g/24h)
自身抗体:抗核抗体 着丝点1:1000,抗着丝点抗体(+),其余阴性
特定蛋白:IgG 9.31g/L,IgG4 0.37g/L,IgA 1.25g/L,IgM 0.78g/L,IgE 80IU/mL,C3 1.46g/L,C4 0.30g/L,总补体测定: 47.0IU/mL
肿瘤指标:CA125 61.7U/ml,AFP、CEA、CA19-9、NSE均正常
2018-6-6胸部CT:
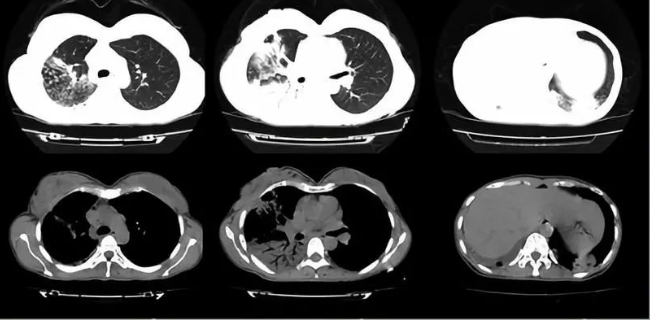
2018-6-6支气管镜:
镜下见各支气管腔通畅,粘膜光滑,未见新生物;于中间支气管灌入生理盐水20ml,回收液送细菌、真菌及结核涂片和培养。外周超声结合透视引导下达右下叶背段阴影处行TBLB并刷检。
微生物检查:冲洗液、肺组织、刷检、咳出物均为阴性;
组织病理(右下肺背段):穿刺组织细支气管粘膜下水肿,可见中性粒细胞及少量淋巴细胞浸润,肺泡腔内充满纤维素性渗出物,及大量肺泡巨噬细胞,肺泡间隔少量粒细胞及淋巴细胞浸润,肺泡上皮轻度增生,肺泡间隔纤维组织轻度增生,部分小血管内膜增厚。
免疫组化:CK{pan}(上皮+),CD68{KP1}(组织细胞+)
特殊染色:未查见阳性菌:PAS(-),抗酸(-),六胺银(-),网染(网状纤维+)
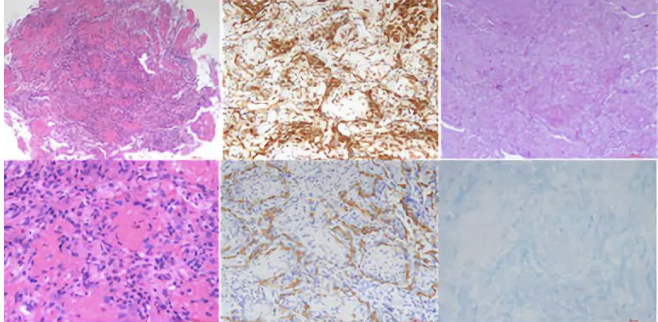
病程中患者诉口干、眼干症状较明显;故完善相关检查:
颌下腺、腮腺、颏下腺:彩超正常。唾液腺现象:唾液腺摄取和分泌功能正常
Schirmer试验、角膜染色:考虑干眼症。
入院经治疗后,患者无发热,但咳嗽加重,有活动后胸闷气促。复查胸部CT提示病变较前进展。
2018年6月14日 胸部CT(美罗培南1.0 q12h;6-2~6-14):
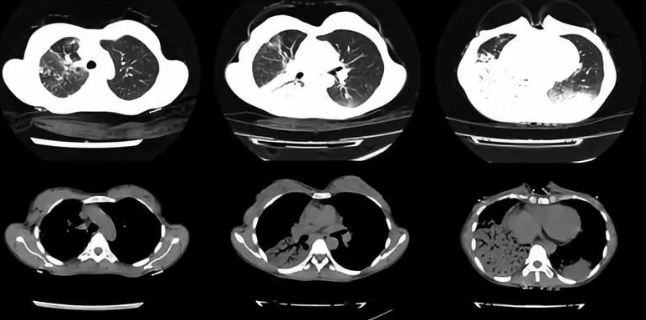
修正诊断
AFOP
结合患者的临床症状,影像学特点,病理结果;我们查阅相关文献,并经过科内讨论,最终考虑急性纤维素性机化性肺炎(AFOP)。是特发性AFOP,还是继发性AFOP有待进一步观察验证。
调整治疗
6月14日开始:继续美罗培南1g q12h ivgtt抗感染+甲强龙40mg q12h ivgtt×6天;
6月20日开始:停用美罗培南;继续甲强龙40mg qd ivgtt×12天;
患者症状好转,复查胸部CT影像学较前吸收,故还用强的松30mg qd 口服治疗。
2018年6月26日 胸部CT(糖皮质激素治疗后):

2018年8月3日,患者门诊随访时,胸部CT提示右肺尖病灶较前(6-26)增多,两下肺炎症较前片改善。
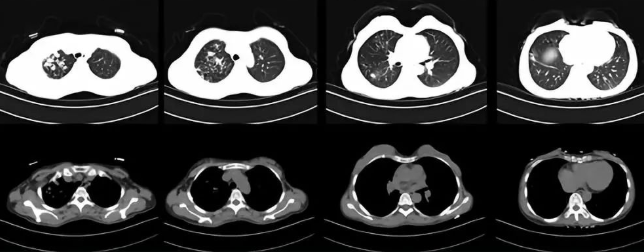
病情变化原因分析
1、AFOP诊断是否有误?
该患者临床症状、影像学特点及辅助检查,病理特点均符合AFOP,且激素治疗后双下肺病灶明确吸收;故考虑诊断不存在错误。
2、激素减量过程中复发?
虽然是在激素减量过程中,但患者双下肺吸收良好,仅仅右上肺病灶加重,且病灶影像学特点不一致;故不考虑激素减量后复发。
3、合并感染?
长期应用糖皮质激素的患者,可导致免疫力下降,容易合并感染。结合患者右上肺多发、多形性病灶(片状影、小叶中心性肺结节、树芽征),需考虑结核杆菌感染可能大,须与细菌、真菌感染鉴别,需进一步检查以明确诊断。
第二次入院完善检查
血常规:WBC 7.38×10^9/L,NE 91.9%,LY 3.9%。
炎症指标:CRP2mg/L,PCT 0.07ng/ml,ESR 20mm/h
生化:肝肾功能、电解质:正常。微生物: T-SPOT A抗原9/B抗原32.
自身抗体:抗核抗体 着丝点1:100,抗着丝点抗体(+),其余阴性
细胞免疫:B淋巴细胞CD19 11.1%,T淋巴细胞CD3 80.3%,Th淋巴细胞CD4 20.%,Ts淋巴细胞CD8 58.7%,CD4/CD8 0.3.
2018年8月9日复查支气管镜:
于右上叶尖段灌入生理盐水20ml,回收液送细菌、真菌及结核菌涂片和培养。透视引导下于右上叶尖段阴影处行TBLB及刷检。
冲洗液行厚涂片找抗酸杆菌3+;组织病理未见典型坏死性肉芽肿,但抗酸染色阳性。随后冲洗液和组织培养结果显示分枝杆菌培养: 阳性;结核分枝杆菌复合群特异性抗原MPB64: 阳性。结核PCR亦为阳性。

目前诊断
1、继发性肺结核
2、AFOP
结核与AFOP的相关性分析
是肺结核继发AFOP,还是AFOP使用激素后出现肺结核;亦或是肺结核与AFOP独立存在,是其他原因诱发AFOP?专家们进行了精彩分析,详见点评总结。
下一步治疗方案的调整
根据患者影像学及支气管镜检查结果,现活动后肺结核诊断明确,应积极抗结核治疗。因患者CD4T淋巴细胞明显降低,CD4/CD8 0.3;提示细胞免疫功能低下;继续使用激素不利于结核治疗。且患者双下肺病灶基本完全吸收,考虑AFOP控制可,故暂停用激素,单用抗结核治疗,定期随访胸部CT。
专家点评总结
影像科 张兴伟副主任医师
学员读片总体规范性尚好,对于肺部病变的特点进行了较充分的描述,而且能够注意到纵隔窗关注淋巴结及胸腔积液、胸膜增厚等情况。该患者6月6日影像学特点是双肺多发斑片状实变影、磨玻璃影、结节影等多形性病变、可见支气管充气征、树芽征。总体倾向于感染性病变,结合患者有发霉物体接触史,需警惕真菌感染;同时不排除多种病原体混合感染。6月14日,胸部CT提示右上肺尖段部分病灶增多,部分病灶吸收;双下肺实变较前明显;病变总体较前加重,且有游走性。8-3胸部CT提示双下肺实变影明显吸收;但右上肺病灶进展,以斑片状阴影,结节影,小叶中心性结节和树芽征为特点,纵膈窗部分病灶见可疑钙化,结合患者病史需考虑结核感染。
风湿科 陈慧勇副主任医师
该患者ANA着丝点1:1000,抗着丝点抗体+;但ANA对于结缔组织病诊断敏感性高、特异性不高;在感染,肿瘤性病变也会升高。引起ANA升高的结缔组织病,常见的有CREST综合征,SLE、干燥综合征,系统性硬化等。该患者虽然ANA高,但结缔组织病特异性抗体阴性。患者有干眼症状,但同位素试验阴性,SS-A、SS-B阴性,暂不考虑干燥综合征,考虑继发性干眼。综合分析目前结缔组织病依据不足。
CD4T细胞下降,存在感染、药物、酗酒、肝硬化、特发性等多种可能因素。感染引起CD4T细胞下降,多见于病毒感染,该患者目前症状及辅检没有充分依据。结合患者长期糖皮质激素使用,可诱导淋巴细胞凋亡,进而导致CD4T细胞下降。
病理科 纪元主任
首次气管镜病理提示染色见肺泡腔内充满嗜伊红的纤维素性渗出物,肺泡间隔轻度增宽,肺泡间隔少量粒细胞及淋巴细胞浸润,肺泡上皮轻度增生,肺泡间隔纤维组织轻度增生。肺泡腔内有巨噬细胞,但未形成肉芽肿结节,肺泡腔内亦未见成纤维细胞,无透明膜形成等。特殊染色PAS,抗酸、六胺银均为阴性,排除真菌、结核感染。结合患者临床-影像学特点,符合AFOP诊断。AFOP与OP的病理鉴别在于,AFOP为肺泡腔内纤维蛋白球形成,超过50%肺泡区域;肺泡管和细支气管内见疏松结缔组织。OP为肺泡和细支气管中成纤维细胞、肌成纤维细胞、疏松结缔基质、胶原组成的肉芽组织栓。
第二次活检病理提示肺泡及支气管壁组织,支气管粘膜下间质较多淋巴细胞、浆细胞浸润,纤维组织增生,肺泡间隔纤维母细胞增生,呈炎症性病变。抗酸染色见阳性菌,倾向结核;进一步NGS、ddPCR明确结核分枝杆菌。结核感染为什么病理未见肉芽肿形成及坏死,考虑与患者长期糖皮质激素使用有关。
微生物室 周春妹副主任技师
冲洗液抗酸杆菌涂片阳性,提示分枝杆菌感染,但涂片不能明确分枝杆菌类型。进一步完善冲洗液及肺组织培养,均提示分枝杆菌生长。支气管镜冲洗液、肺活检组织相对无菌,且冲洗液与肺组织结果一直,故排除污染,检测结果可信。MPB64是结核分枝杆菌复合群特异性抗原,NTM基本不存在该抗原;故目前结核分枝杆菌感染明确。
呼吸与危重症医学科 王葆青主任医师
激素治疗后右上肺病变进展,结合影像学特点及病理、组织培养结果,结核感染明确。因患者起病初T-SPOT基本正常,且激素治疗后病变部位,与起病初部位不一致;综合考虑激素治疗后,免疫抑制,导致潜在结核复发或继发结核感染。
呼吸与危重症医学科 金美玲主任医师
该患者临床症状、影像学特点,病理结果均符合AFOP诊断。AFOP分为特发性和继发性。进一步病因的诊断,对于治疗和预后至关重要。该患者虽然ANA阳性,但综合考虑结缔组织病依据不足,暂不考虑结缔组织相关AFOP。结合患者起病初的发热、咳嗽咳痰、炎症指标偏高,需考虑感染性病变诱发AFOP;有待进一步检查及随访。胸部CT见右上叶及中叶存在多发小结节及树芽征,可能原发存在,亦可能是实变吸收过程的遗留,需要动态随访症状及影像学变化,必要时进一步检查。
呼吸与危重症医学科 李华茵主任医师
T-spot存在一定的假阳性及假阴性,故不能用于临床确诊或排除活动性结核,只能用于结核的辅助诊断。患者前期影像学显示右上肺小结节一直存在,但T-spot不高,激素应用后右上肺多形性病灶明显增多,T-SPOT升高,综合考虑结核为激素应用后,免疫力低下,导致的继发性结核感染。
呼吸与危重症医学科 陈雪华副主任医师
激素应用后右上肺病灶进展,抗酸涂片阳性,冲洗液、组织培养提示结核分枝杆菌生长,NGS、ddPCR也提示结核分枝杆菌,故该患者右上肺病灶结核感染明确,类型属于继发性肺结核。该患者激素使用前,右上肺即可见典型小叶中心肺结节、树芽征;应考虑分枝杆菌感染,后续激素应用导致免疫力低下,结核感染快速进展。T-SPOT只能用于结核感染的辅助诊断,阴性不能完全排除结核。第一次气管镜未找到结核菌,与患者冲洗及活检部位有关,遗憾的是初次未行上叶冲洗及活检。
本患者倾向于继发性AFOP。结核感染可以诱发机体变态反应,进而导致AFOP;亦有可能结核与AFOP起病初均存在,但是由其他病因比如病毒感染、药物因素、结缔组织病等所致AFOP。诱发AFOP的确切病因,有待进一步检查及随访观察。
关于明确结核感染后的,激素使用问题。因为该患者相对症状较轻,且激素治疗后病灶吸收快,2周内下肺病灶基本吸收。且患者CD4细胞明显下降,免疫低下,如继续激素使用,对结核治疗不利。故建议停用激素,单用抗结核治疗。随访症状及影像学变化,如实变及磨玻璃影加重,可再次加用激素。
呼吸与危重症医学科 何礼贤主任医师
本患者初始拟诊CAP,按指南抗感染治疗后病情无好转。三级医院CAP按指南治疗成功率约为50%。欧洲报道CAP抗感染3d后,可达到临床稳定约为40%。该患者初始治疗无效后,按照无反应性肺炎的流程及时全面的处理;通过病理结果,结合临床-影像学特点,明确AFOP;进而开始激素治疗。AFOP是少见病例,国内报道十余例,国际上截止2016年报道100余例。其临床特点与COP相似,但病理特征不一致。
激素使用后,出现病情变化,最终右上肺诊断继发性肺结核。是结核继发AFOP,还是激素应用导致肺结核?从文献报道来看,AFOP主要继发于病毒、真菌感染,有不动杆菌感染继发AFOP报道,但罕有结核继发AFOP报道。仅有国内1例报道过结核病,病理上见AFOP表型。该患者前期右上肺有小结节及树芽征,但病原学阴性,并不能明确起病初结核感染。该患者长期应用激素,且CD4细胞下降,故容易出现激素应用后结核,以内源性感染为主,少见新发外源性结核感染。
本病例前期诊治比较顺利,思路正确。后期及时发现病情变化时,及时诊断及处理。总体而言,通过本病例我们学习了无反应肺炎的处理流程,AFOP的诊治等相关内容,对临床工作有很大启发。
呼吸与危重症医学科 宋元林主任医师
感谢所有PCCM学员对病例的充分准备,以及各位专家的精彩点评。通过该病例,我们对无反应性肺炎的处理,AFOP的诊断与治疗有了进一步的认识;治疗过程中及时发现病情变化,通过全面检查,明确结核感染,并及时调整治疗,总体上这是成功治疗病例,有很多方面值得学习与借鉴。
需要强调的是右上肺病情反复时,当时炎性指标如CRP、ESR均正常,且无气促,无发热,影像学特征与前面不一致;故不考虑AFOP复发。该患者第二次TBLB时,组织病理未见坏死性肉芽肿的典型结核表现,如果抗酸染色阴性,而组织培养结果未出时,我们如何诊断和治疗?该患者是亚急性的临床类型,如何是急性起病的类型,临床上如何快速准确的诊断与治疗?虽然本病例成功诊治,但很多问题值得我们进一步思考。
作者介绍

感谢正大天晴药业集团
对本季PCCM疑难病例讨论直播的支持


