摘要
B群β溶血链球菌(Group B streptococcus,GBS)又称无乳链球菌(Streptococcus agalactiae),是一种可引起人和动物发生严重感染的病原菌。自20世纪70年代以来,有报道称GBS是侵入性新生儿感染的致病菌,可引起新生儿肺炎、脑膜炎乃至脓毒症等严重的感染性疾病[1]。在西方国家,GBS是引起产妇和新生儿感染的最常见致病菌,是间接导致发达国家围生儿死亡的主要原因[2]。近年来研究显示,我国GBS感染有上升趋势,在临床上引起感染的比例不可忽视[3]。现将一例GBS感染所致的新生儿肺炎、脓毒症病例分享如下。
病史概要
患儿,男,12+小时足月儿,顺产,胎龄39+4周,以「呻吟、气促2小时」入院。出生体重3055g,羊水清亮,量500ml,胎盘正常。2+小时前,患儿阵阵哭吵伴呻吟,吸吮力稍差,吞咽不协调,偶有干呕。予以洗胃,洗出胃液干净,无咖啡渣及胆汁样物质。2+小时以来,经洗胃对症处理后,患儿仍不停呻吟,呕吐2次,为未消化奶瓣,呼吸稍促,欠规则,氧饱和度维持在88%-90%之间,反应稍差,哭声欠响亮。无吐沫、尖叫、抽搐及双目凝视。已开奶,胎便已解,初尿已排。以「新生儿肺炎」收入新生儿科。患儿母亲孕期产检均正常。
检查
T:36.5℃,R:60次/分,P:122次/分,发育正常,营养一般,精神、反应差。头颅外观无畸形,前囟平、软,约2x2cm。面色欠红润,唇周微绀,可见鼻扇,无三凹征。双肺呼吸音粗,可闻及中细湿罗音。心律齐,心音稍低。肌张力正常。神经反射检查:觅食、吸吮、握持、拥抱反射均减弱。
实验室辅助检查(2月8日)
血常规:WBC:2.25×109/L↓,RBC:3.96×1012/L↓,NEU%:56.5%,NEU:1.27×109/L↓,LYM%:38.6%,LYM:0.87×109/L↓,MON:0.08×109/L↓,CRP:5.93mg/L,PCT:23.44ng/mL↑
血气分析:PH:7.309↓,PaCO2:35.4mmHg,PaO2:87.5mmHg,HCO3-:17.8mmol/L↓,SO2:98.1%,c-Lac(乳酸): 8.1mmol/L↑
生化检查:肝功能:AST:108.1U/L↑,GGT:130.0U/L↑,LDH:762U/L↑,TP:48.1g/L↓,ALB:35.0g/L↓,PA:71.0g/L↓,GLB:13.1g/L↓,余正常。
心肌酶谱:CK:575.0U/L↑,CK-MB:91.0U/L↑,α-HB:591.0U/L↑,肾功能、电解质检查正常。
TORCH检查:HCMV-IgM,TOX-IgM,RV-IgM,HSV1-IgM,HSV2-IgM全阴性。
凝血功能、大便常规、尿常规检查均未见明显异常。
胸部(DR)正位示新生儿肺炎征象,如图1。
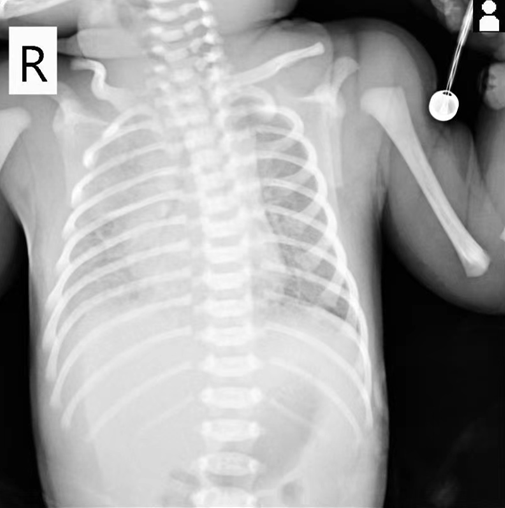
图1:胸部DR
诊疗经过
入院诊断
新生儿肺炎、心肌损害、新生儿脓毒症?化脓性脑膜炎?
入院后马上予经验抗微生物治疗:青霉素30万单位静滴bid联合头孢他啶0.15g静滴bid抗感染治疗。同时送检微生物检测标本。
2月8日微生物学实验室收到吸痰(培养+药敏)标本1个、血需氧培养(左右上肢各1瓶)标本2个、脑脊液(培养+药敏)标本1个。分子实验室收到耳后(腋下)皮肤拭子GBS筛查(PCR)标本1个。2月13日收到患儿母亲阴道(直肠)拭子GBS筛查(PCR)标本1个。
痰培养+药敏检验,标本涂片革兰染色见少量白细胞,偶见鳞状上皮细胞,偶见革兰阳性球菌、成双排列,如图2。标本接种血琼脂培养基和嗜血杆菌巧克力琼脂培养基,置于10%CO2培养箱培养24小时后,血琼脂培养基可见少量白色、湿润、中等大小、有小β溶血的可疑菌落生长,如图3。对该可疑菌落行革兰染色,为革兰阳性球菌、部分呈链状排列,如图4。同时用血琼脂培养基转种该菌,培养48小时,菌落呈白色、湿润、中等大小、有小β溶血,如图5。该菌触酶试验阴性,使用珠海迪尔96STREP肠球菌/链球菌鉴定卡,于2月11日经DL-96Ⅱ细菌测定系统鉴定为无乳链球菌(鉴定率:99.9%)。CAMP试验阳性(左侧为ATCC29213,右侧为ATCC25923,中间为待检菌株),如图6。

图2:痰革兰染色(×1000)
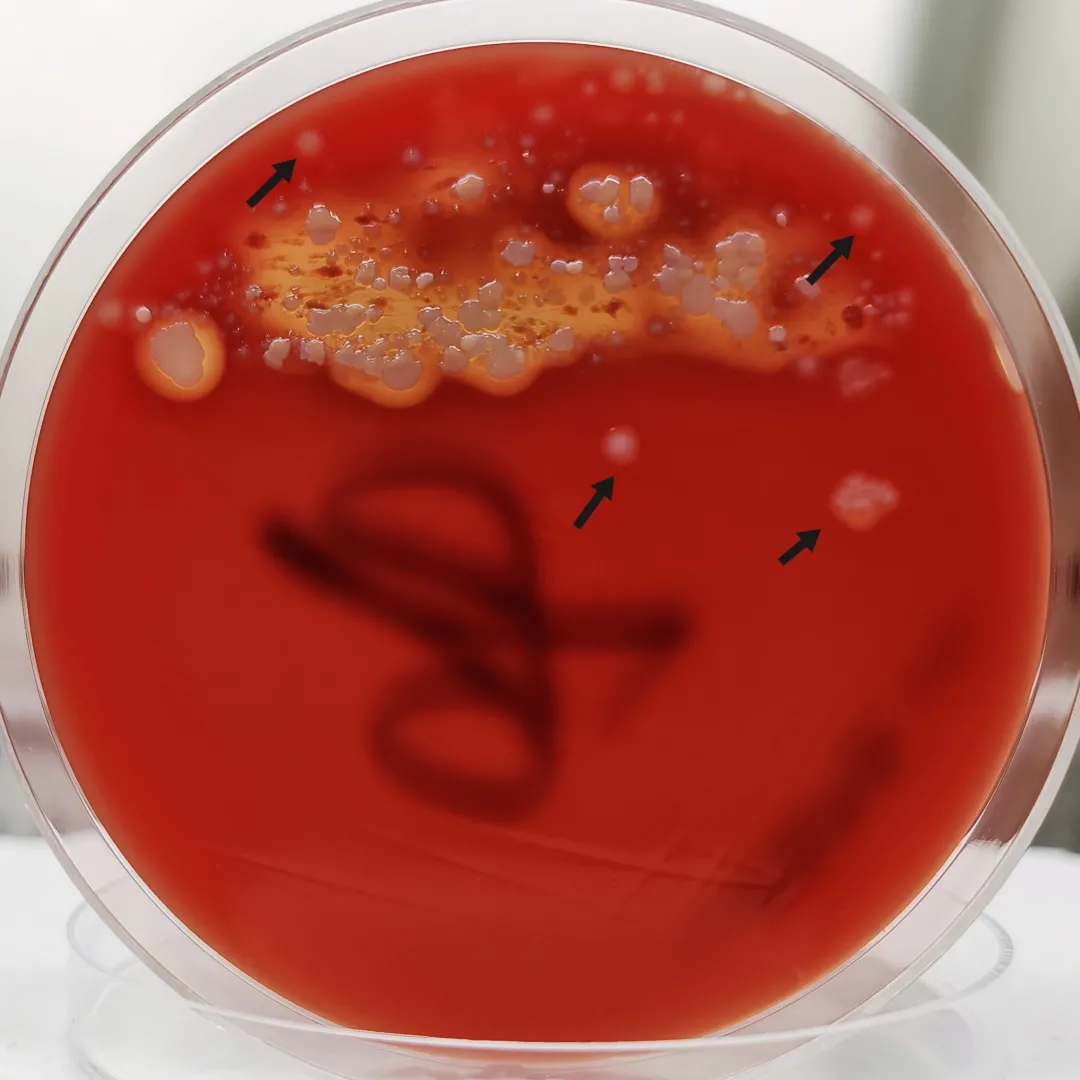
图3:痰培养24小时,→可疑菌落
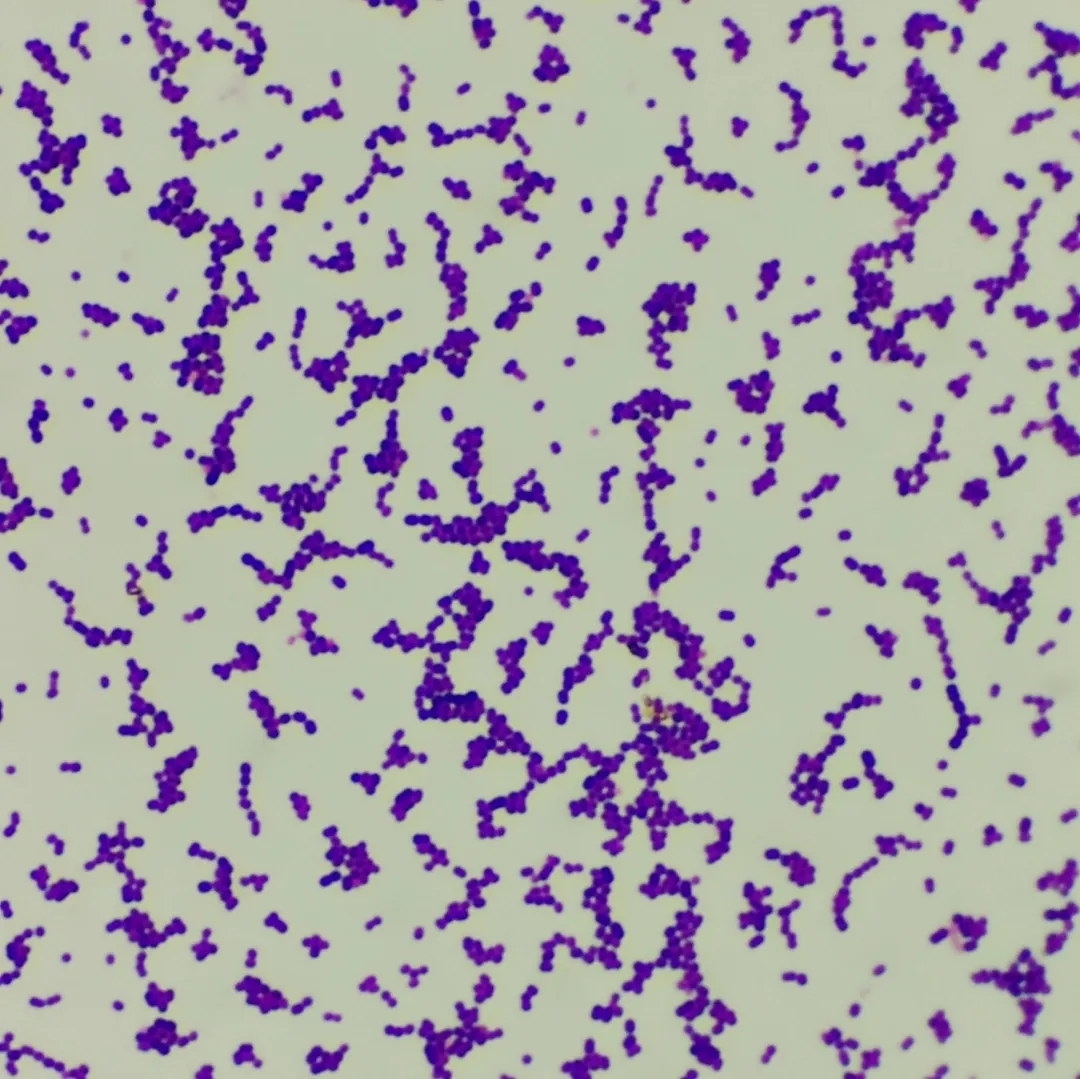
图4:可疑菌落革兰染色(×1000)
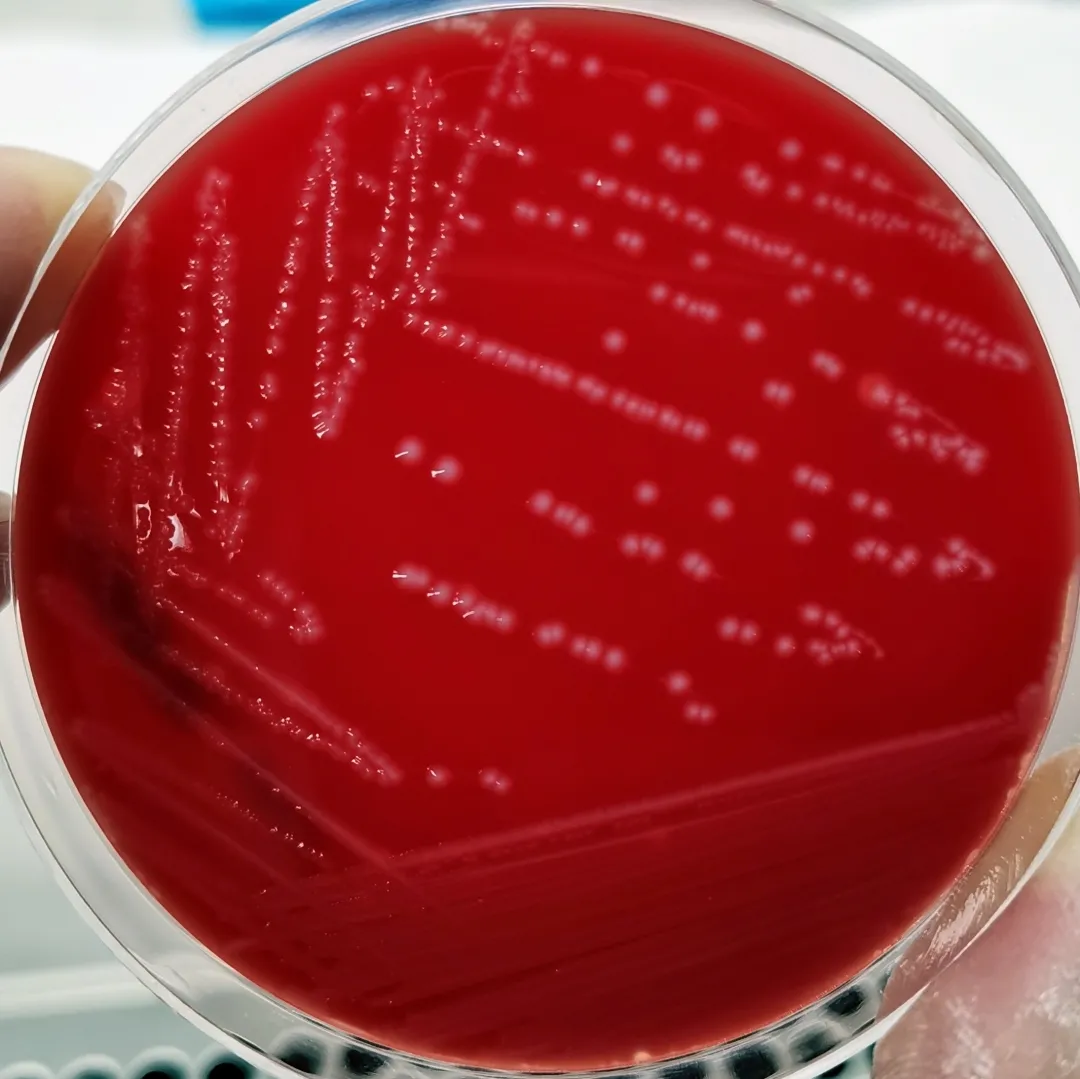
图5:可疑菌落转种,培养48小时
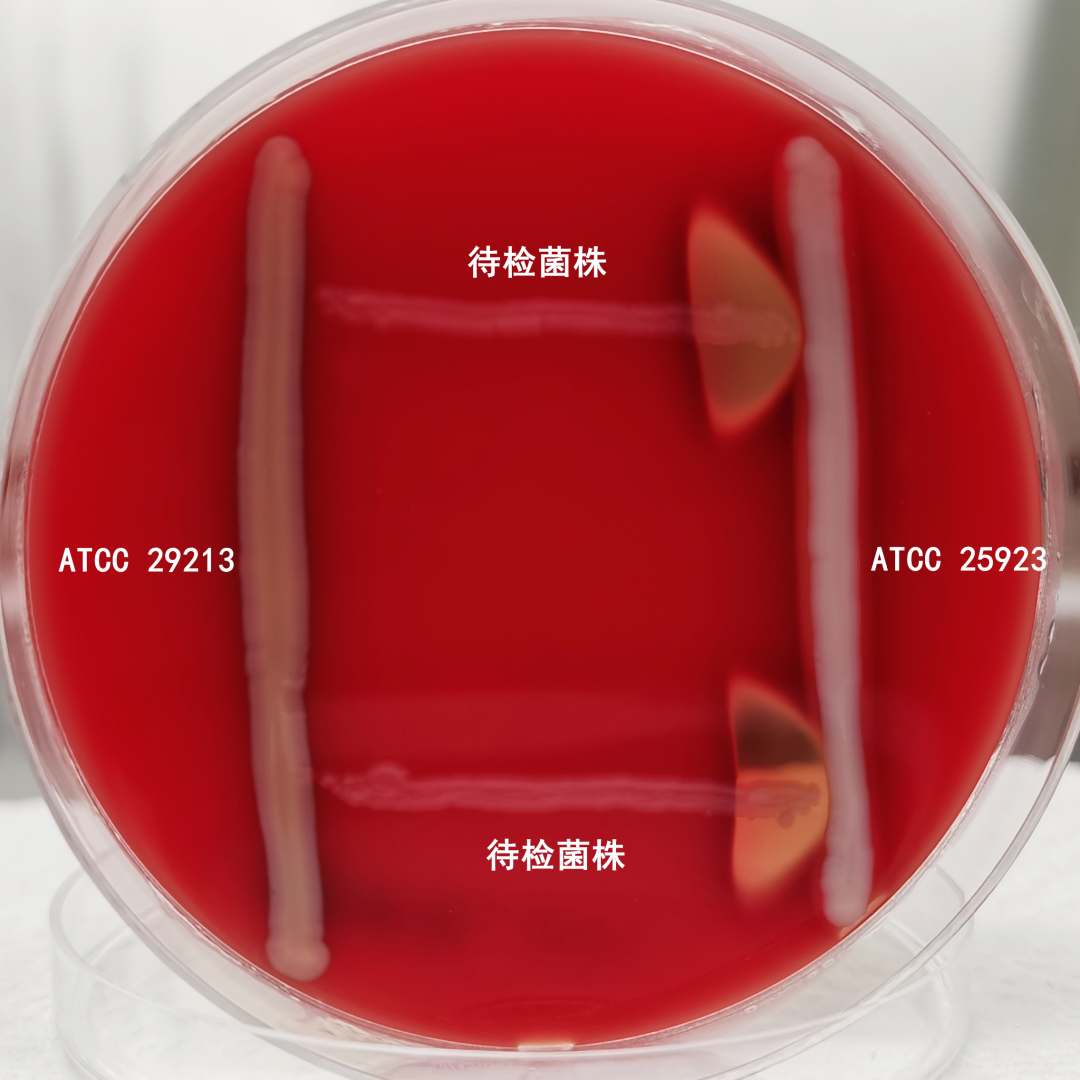
图6:CAMP试验阳性
血需氧培养检验结果:双侧标本均报阳性,左侧肢体抽血报阳时间8.5小时,右侧肢体抽血报阳时间9.1小时,如图7。抽取血培养瓶培养液涂片革兰染色见革兰阳性球菌,呈链状排列,如图8。即刻抽取培养液转种于血琼脂培养基,置于10%CO2培养箱培养。同时行直接CAMP试验(左侧为ATCC29213,右侧为ATCC25923,中间为血培养瓶培养液),结果为阳性,如图9。转种培养24小时后用珠海迪尔96STREP肠球菌/链球菌鉴定卡,于2月11日经DL-96Ⅱ细菌测定系统鉴定为无乳链球菌(鉴定率:99.9%)。
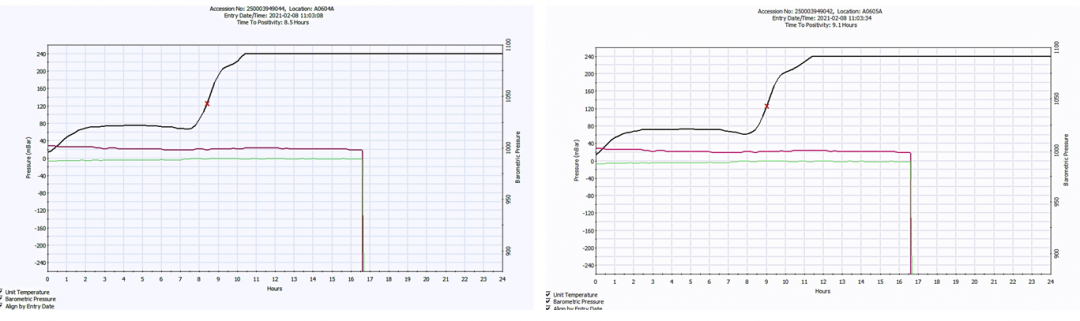
左侧肢体抽血报阳时间:8.5h
右侧肢体抽血报阳时间:9.1h
图7
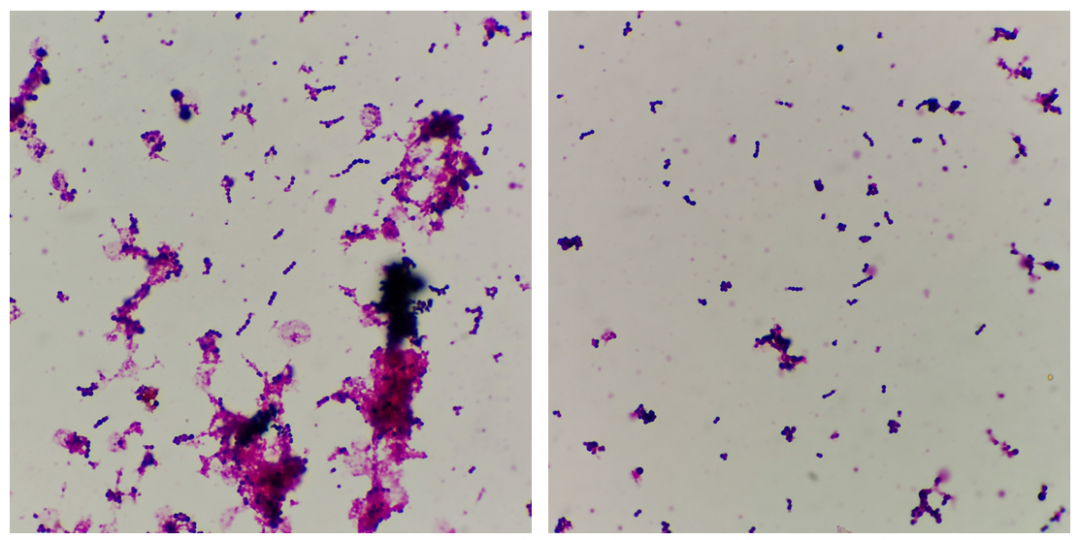
血培养左侧 革兰染色(×1000)
血培养右侧 革兰染色(×1000)
图8
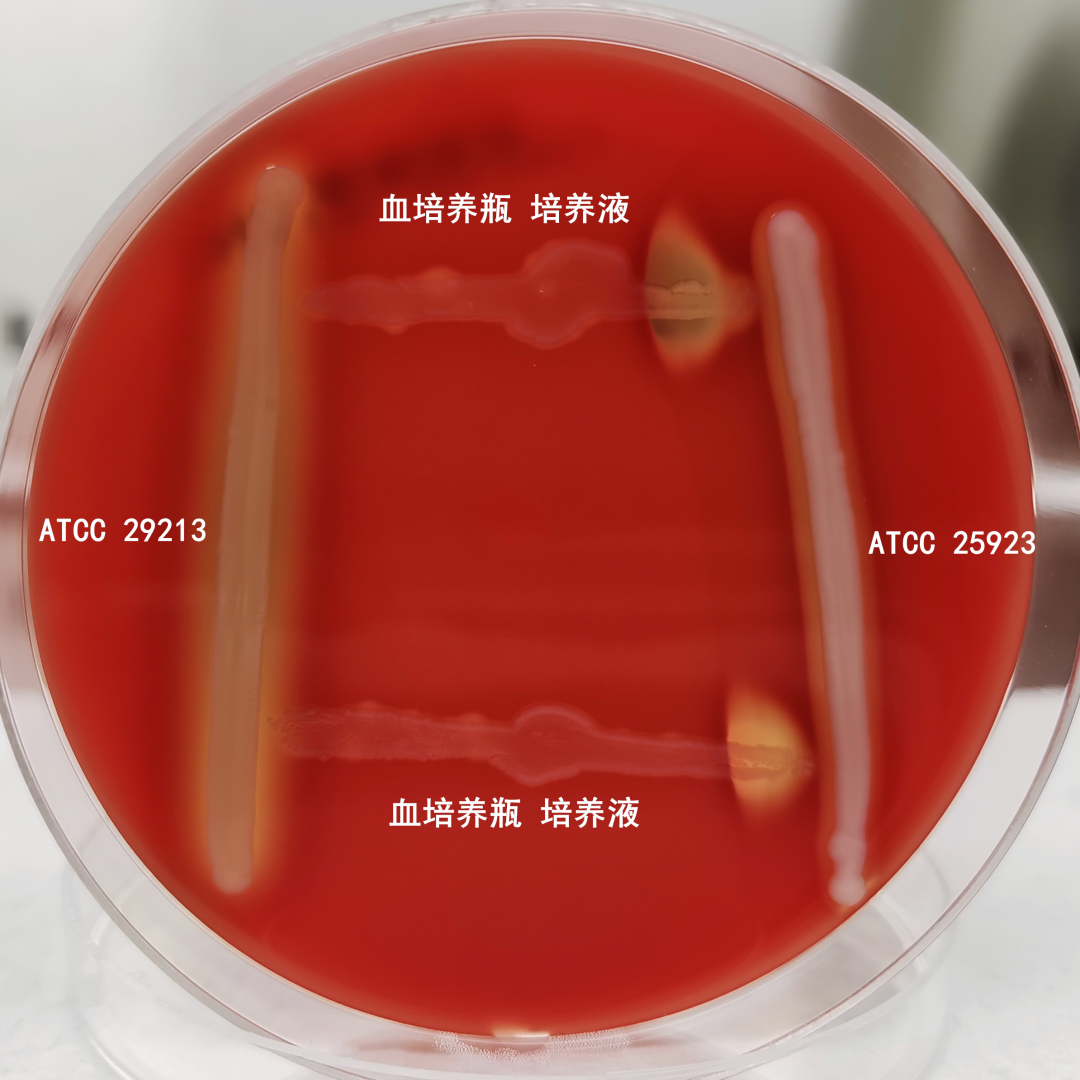
图9:直接CAMP试验阳性
脑脊液培养检验,脑脊液标本1mL接种于血培养需氧瓶,培养5天无细菌生长。
2月9日,检测耳后(腋下)皮肤拭子GBS(PCR)报告:阳性。
2月14日,检测患儿母亲阴道(直肠)拭子GBS(PCR)报告:阳性。
药物敏感性试验:用微量稀释法测定最低抑菌浓度(MIC),按照美国临床和实验室标准化协会(CLSI)推荐的M100标准文件进行耐药性判断。结果为:青霉素、万古霉素、左氧氟沙星、利奈唑胺、美罗培南、氨苄西林、头孢曲松敏感。克林霉素、红霉素、四环素耐药。
根据微生物学检验结果,可明确诊断患儿肺炎及菌血症由GBS感染所致。同时结合《中国严重脓毒症症/脓毒性休克治疗指南(2014)》,患儿白细胞2.25×109/L(<4×109/L),PCT:23.44ng/mL,2月10日检测CRP: 49.27 mg/L,高乳酸血症,可诊断患儿为脓毒症。依据药敏结果,2月12日抗感染治疗由青霉素联合头孢他啶两联经验性抗感染治疗调整为青霉素30万单位静滴bid单药治疗。经过14天治疗,患儿治愈出院。期间在2月15日复查痰培养未检出致病菌,血培养阴性。复查胸部DR,炎症病灶较之前明显减少,如图10。炎症相关指标,如血白细胞(WBC)、CRP、PCT恢复正常,如图11。
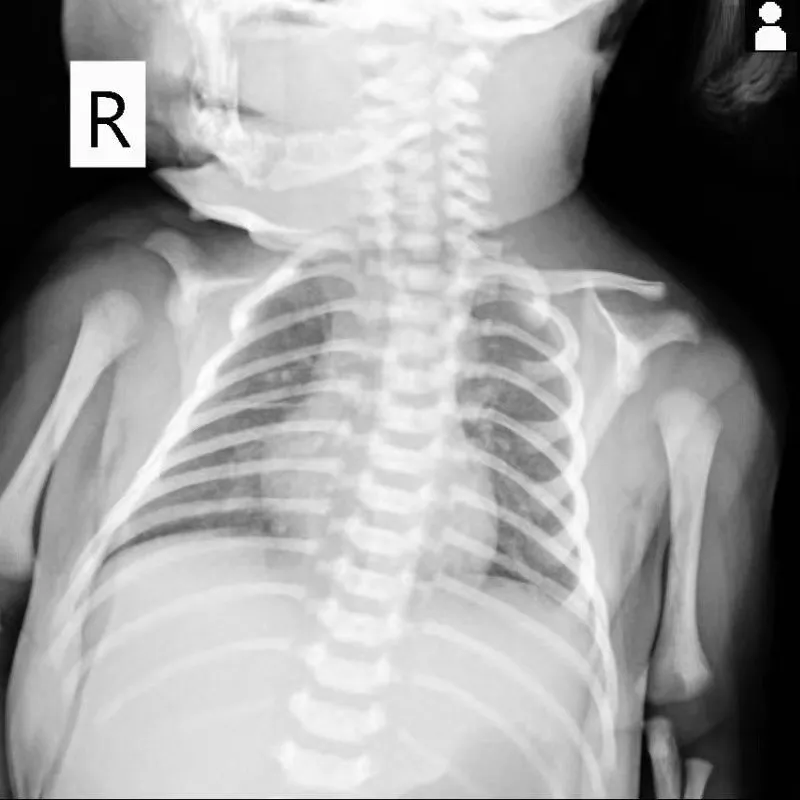
图10:复查胸部DR
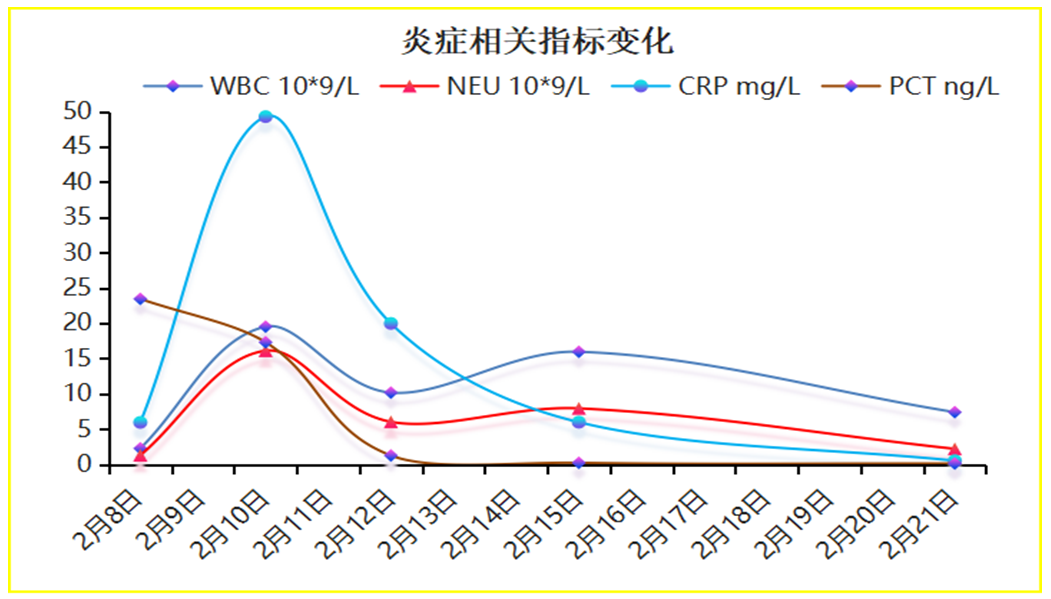
图11
案例总结
患儿实验室检查WBC降低、PCT升高、CRP升高(出生6-24h龄<5mg/L)、血c-Lac(乳酸)升高,结合胸部(DR)示新生儿肺炎征象。可初步诊断患儿血流感染和肺部感染。临床及时送检血培养和痰培养,培养并鉴定为GBS,为患儿最终明确诊断提供了病原学证据。青霉素是治疗GBS感染的首选药物。因此,临床正确及时的选用青霉素进行经验性抗感染治疗和后期结合药敏结果足疗程规范化治疗,是患儿良好预后的关键。GBS的分离鉴定并不困难,但本案例中,笔者认为血培养报阳后直接CAMP试验这一做法值得推广。在临床工作中,若为新生儿血培养报阳,涂片染色为革兰阳性球菌,且(或)呈链状排列。这时要高度怀疑GBS的感染,在对血培养进行转种培养的同时,建议加做直接CAMP试验。可为GBS感染的早期诊断和后续鉴定提供帮助。
GBS是引起新生儿侵袭性感染的主要病原菌,可导致新生儿肺炎、败血症及脑膜炎/脑炎,造成新生儿死亡或神经系统后遗症[4]。GBS感染根据患儿年龄分为两种类型[5]。生后一周内感染为早发感染型,平均发病时间为生后20小时,多因生产过程中从有GBS定植的母亲生殖道获得。早发感染的新生儿基本均有血流感染、1/3到一半可有肺炎和/或呼吸窘迫综合征表现、1/3表现为脑膜炎。生后第2周至3个月内的感染为迟发感染型。致病菌可在分娩时(同早发感染)获得,也可在产后从与有细菌定植的母亲、育儿员或其他来源的接触获得。脑膜炎是迟发感染最常见的表现形式,在大多数情况下与Ⅲ型荚膜GBS菌株有关。
GBS在母亲定植是患儿感染的高危因素。对35-37孕周的孕妇做阴道下端/直肠拭子GBS筛查并做相应处理,对于降低GBS感染率至关重要。2010年美国CDC制定颁布了《围产期B群链球菌病预防指南》、2017年英国皇家妇产科医师学院(RCOG)发布了《新生儿早发型B群链球菌病预防指南》、2020年1月美国妇产科医师协会(ACOG)发布了《预防新生儿早发型B群链球菌病:ACOG委员会共识》。这些指南和共识的预防策略核心是,产前GBS筛查与产时抗生素干预(IAP),即GBS筛查阳性,分娩时给予预防性使用抗生素(以氨苄西林或青霉素为主),从而降低新生儿早发型感染[6]。
本案例为早发感染型,母体GBS定植是最可能的感染来源。但追问患儿母亲,述产前曾行GBS筛查、结果为阴性。本次为患儿母亲行阴道(直肠)拭子GBS检测(PCR),为阳性结果。而标本采集部位和手法、检测方法、采集当时阴道和直肠菌群情况等,均影响GBS筛查的结果。因此,产前筛查阴性的新生儿,如出现感染表现时、仍应做GBS相关检查并及时处理,以免漏诊。
参考文献
[1] 王辉等译.(美)詹姆斯H.约根森,(美)迈克尔A.普发勒.临床微生物学手册[M],第11版.北京:中华医学电子音像出版社,2017.6.
[2] 刘泽滨等.无乳链球菌的研究现状及进展[J].检验医学与临床杂志,2016,13(14):2057-2058.
[3] Dagnew AF, Marianne C, Dube Q ,et al. Cunnington,QueeDube. Variation in Reported Neonatal Group B Streptococcal Disease Incidence in Developing Countries[J]. Clin Infect Dis,2012,55(1):91-102.
[4] Edmond KM, Kortsalioudaki C. Scott. et al. Group B streptococcal disease in infants aged younger than 3 months: systematic review and meta-analysis [J].Lancet,2012,379(9815):547-556.
[5] 胡必杰,潘珏,高晓东主译.(美)丹尼斯 L.卡斯珀,(美)安东尼 S.福西.哈里森感染病学[M].上海:上海科学技术出版社,2019.5.
[6] Verani JR, McGee L, Schrag SJ, et al. Prevention of Perinatal Group B Streptococcal Disease Revised Guidelines from CDC,2010[J]. MMWR Morb Mortal Wkly Rep,2010,59(RR-10):1-36.
作者:龙宪川、王坤、李国兰 - 重庆市永川区儿童医院检验科;审校:黄金伟、赵鸿
本文转载自订阅号「京港感染论坛」(ID:PIDMIC)
原链接戳:【病例讨论】新生儿侵袭性感染的重要"杀手"B群β溶血链球菌感染病例
本文完
排版:Jerry


