第五部分 妊娠篇
一、2019年《欧洲急性肺栓塞诊断和治疗指南》
妊娠期肺栓塞的流行病学和高危因素
急性肺栓塞(PE)仍然是高收入国家孕产妇死亡的主要原因之一。与同龄的非孕妇相比,孕妇的静脉血栓栓塞症(VTE)风险更高,妊娠期间 VTE 风险逐渐增加,并在产褥期达到高峰。如存在额外的 VTE 风险因素(包括体外受精),妊娠相关风险进一步增加。其他重要和常见的危险因素包括既往 VTE、肥胖、合并症、死胎、先兆子痫、产后出血,以及剖宫产;因此,孕产妇进行 VTE 风险评估是必要的。
妊娠期肺栓塞的诊断
临床预测标准与D-二聚体
因为PE症状经常与正常妊娠的症状重叠,故妊娠期PE的诊断极其具有挑战。确诊PE中女性发病率很低,仅在2%~7%。然而孕期D-二聚体水平会持续升高,并且在孕晚期约1/4的孕妇D-二聚体水平会超过VTE的阴性预测值水平。一项关于441名急诊入院怀疑PE的孕妇的多国前瞻性研究提示:基于临床可能性、D-二聚体、下肢静脉超声(CUS)和CT肺动脉造影(CTPA)的诊断方法可以安全地除外妊娠期PE。在该研究中,D-二聚体阴性能排除11.7%的392名GENEVA评分为非高危的孕妇,而在孕晚期这个比例降低到了4.2%。
影像检查
使用现代成像技术,母体和胎儿的辐射暴露都很低。对于V / Q显像和CTPA,胎儿辐射剂量远低于可引起胎儿辐射并发症相关的阈值。过去,据报道CTPA会导致乳房高辐射; 但是,CT技术已经发展,现有技术可以在不影响图像质量的情况下减少辐射,包括减少扫描的解剖覆盖范围,减少千伏数,使用迭代重建技术,和减少对比监测组件。因此,现代CTPA成像技术可以将CTPA母体乳房的辐射量降低至3-4mGy的中位剂量。现代CTPA技术对母体患癌症风险的影响可以忽略不计;因此,为避免母体患癌风险避免CTPA检查是不合理的。
正如回顾性研究所示,正常灌注扫描和CTPA正常对于排除妊娠期PE同样安全。然而灌注扫描和CTPA完成后仍然有4%-33% 患者不能确诊,特别是在孕晚期。
V/Q显像对胎儿和母体辐射低,在妊娠期PE诊断方面具有前景,然而,在将其广泛纳入诊断流程之前,需要进一步评估该方法。对于MRA,钆造影剂对胎儿的长期影响尚不清楚,同时在非妊娠的患者中,MRA图像质量不高,并且扫描结果存在较高不确定,因此,目前不推荐使用该技术诊断或排除妊娠期间的PE。常规肺血管造影涉及胎儿的极高辐射暴露(2.2±3.7 mSv),应避免在妊娠期间使用。
PE的过度诊断是一个潜在风险,可能对孕妇产生重大的终身影响,包括分娩时出血的风险、抑制雌激素的反应以及影响未来妊娠期间血栓预防。 因此,避免妊娠期PE过度诊断与不漏诊PE同样重要。
妊娠期和产后6周内可疑肺栓塞患者的诊断检查和处理

CTPA =CT肺动脉造影;CUS =加压静脉超声;DVT =深静脉血栓形成;LMWH =低分子量肝素;PE =肺栓塞。
妊娠期PE的治疗
LMWH是妊娠期PE的首选治疗方法。与VKAs和NOAC相比,LMWH不会透过胎盘,因此不会出现胎儿出血或畸形的风险。此外,虽然UFH在妊娠期间也是安全的,但LMWH具有更稳定的药代动力学特点和可能实行的风险评估。尽管没有RCT研究评估LMWH在妊娠期间治疗PE的最佳剂量,但目前公布的数据与非孕期患者类似,可以基于孕早期体重qd或bid使用。对于大多数在妊娠期间接受LMWH治疗的患者,仍不确定使用血浆抗Xa因子活性的连续测量来指导给药是否能带来临床益处。重要的是要记住:(i)LMWH具有可预测的药代动力学特征,(ii)缺乏血浆抗Xa因子活性水平的数据,以及(iii)检测本身具有局限性。此外,没有关于妊娠期间LMWH基于体重频繁调整剂量的临床益处与危害的数据。因此,可以针对特定的高风险情况保留血浆抗Xa因子活性监测。
UFH的使用与肝素诱导的血小板减少和骨质疏松有关。目前还不能确定使用LMWH是否也与骨质疏松相关。
如果有LMWH过敏或不良反应可考虑使用磺达肝癸钠。对LMWH的反应虽然缺乏可靠的数据,但仍有少量可以穿过胎盘。VKAs可以穿过胎盘,并且在孕早期与胚胎病明确相关,在妊娠晚期使用VKA可导致胎儿和新生儿出血,以及胎盘早剥,华法林可能与胎儿中枢神经系统异常有关。NOAC在妊娠期妇女中禁忌。
需要特别注意生产的管理。对于接受治疗量LMWH的女性,应与多学科团队合作,对计划分娩进行详细地考虑,以避免在足量抗凝时自发分娩的风险。在抗凝治疗的孕妇中,局部麻醉后脊髓血肿的发生率尚不清楚。如果考虑对接受治疗量LMWH的妇女进行局部镇痛,则LMWH剂量至少已经≥24小时,才进行插入脊柱或硬膜外针头操作。
在高风险情况下,例如在近期患PE的患者中,建议在分娩前将LMWH转换为UFH≥36 h。UFH泵入应在预期分娩前4-6小时停止,并且在局部麻醉前APTT复查正常(即不延长)。
产后重新启动LMWH的最佳时间数据有限,具体时间将取决于分娩方式和多学科团队评估血栓形成与出血风险。直到移除硬膜外置管≥4 h才可以给予LMWH, 关于时间和剂量应该考虑硬膜外置管是否是创伤性的,并考虑到女性的风险特征。例如,硬膜外导管移除4小时后,可以考虑给予临时的预防量LMWH(剖宫产后),并且在预防量和治疗量应用期间允许间隔≥8-12小时。建议产科医生,麻醉师和内科医师之间密切合作。
抗凝治疗应在产后6周以上开始,并且在3个月内维持小剂量。LMWH和华法林可以用于哺乳的母亲;NOACs不推荐。
围产期高风险,危及生命的PE是一种罕见但可能致死的事件。最近的一项系统评价包括127例妊娠期(以及产后6周)接受溶栓,取栓术和/或ECMO治疗的重症PE患者。在高危和中危的PE病例中23%的女性有心脏骤停,溶栓和外科血栓切除术后报告的生存率分别为94%和86%。然而,这些高生存率可能有报告偏倚。溶栓后在妊娠期和产褥期分别有18%和58%的患者出现大出血。最后,溶栓和取栓术后12%和20%的患者分别发生胎儿死亡。溶栓除了用于危及生命的PE外,不应在围产期用于治疗PE。通常,UFH用于高风险PE的急性期治疗。
尽管下腔静脉滤器与非妊娠的患者适应证相似,但在妊娠期应用的经验不足,手术风险可能增加。
妊娠期多学科PE管理团队
一个由多学科组成的团队合作,应为包括PE在内的心血管疾病女性规划产前、生产时和产后护理途径。该团队中尽可能多的成员应具备在孕期和产后管理PE的专业知识。
羊水栓塞
羊水栓塞(AFE)是一种发生在孕期或分娩过程中的罕见疾病。它仍然是高收入国家孕产妇直接死亡的重要原因之一。AFE的诊断具有挑战性,主要是临床排除诊断。意识到AFE,及时诊断和积极的生命支持至关重要。AFE的特征是突发性心血管或呼吸系统衰竭,常伴有弥散性血管内凝血,孕期或产后报道的发病率约为每10万个产妇27个,每10万次分娩的死亡率为0.5-6。不同报告中死亡率各不相同,有的报告中死亡率可高达60%以上,反映了诊断的挑战和AFE的罕见性。最近的文献表明,AFE的危险因素可能包括已存在的心脏、脑血管和肾脏疾病,前置胎盘,羊水过多,死胎,绒毛膜炎,高血压,阴道助产和剖宫产。AFE起病急骤,来势凶险,其管理往往是支持性的。正确判别AFE后及时解除肺动脉高压、积极治疗过敏性休克、纠正DIC,保护重要脏器功能,进行识别和诊断后的高质量急诊护理,对AFE来说是非常重要的,所以相关医疗及护理人员应加强此方面的学习。
诊断肺栓塞程序中辐射剂量估测
(基于各种参考文献)
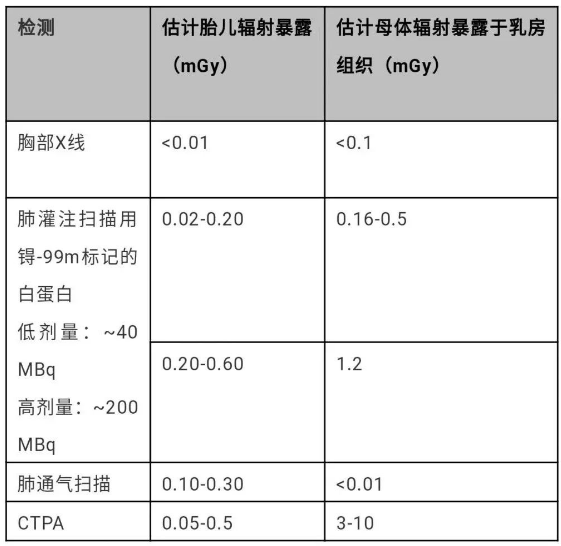
CTPA =CT肺动脉造影;mGy = milligray;MBq = megabecquerel;PE =肺栓塞。
妊娠合并PE的推荐意见
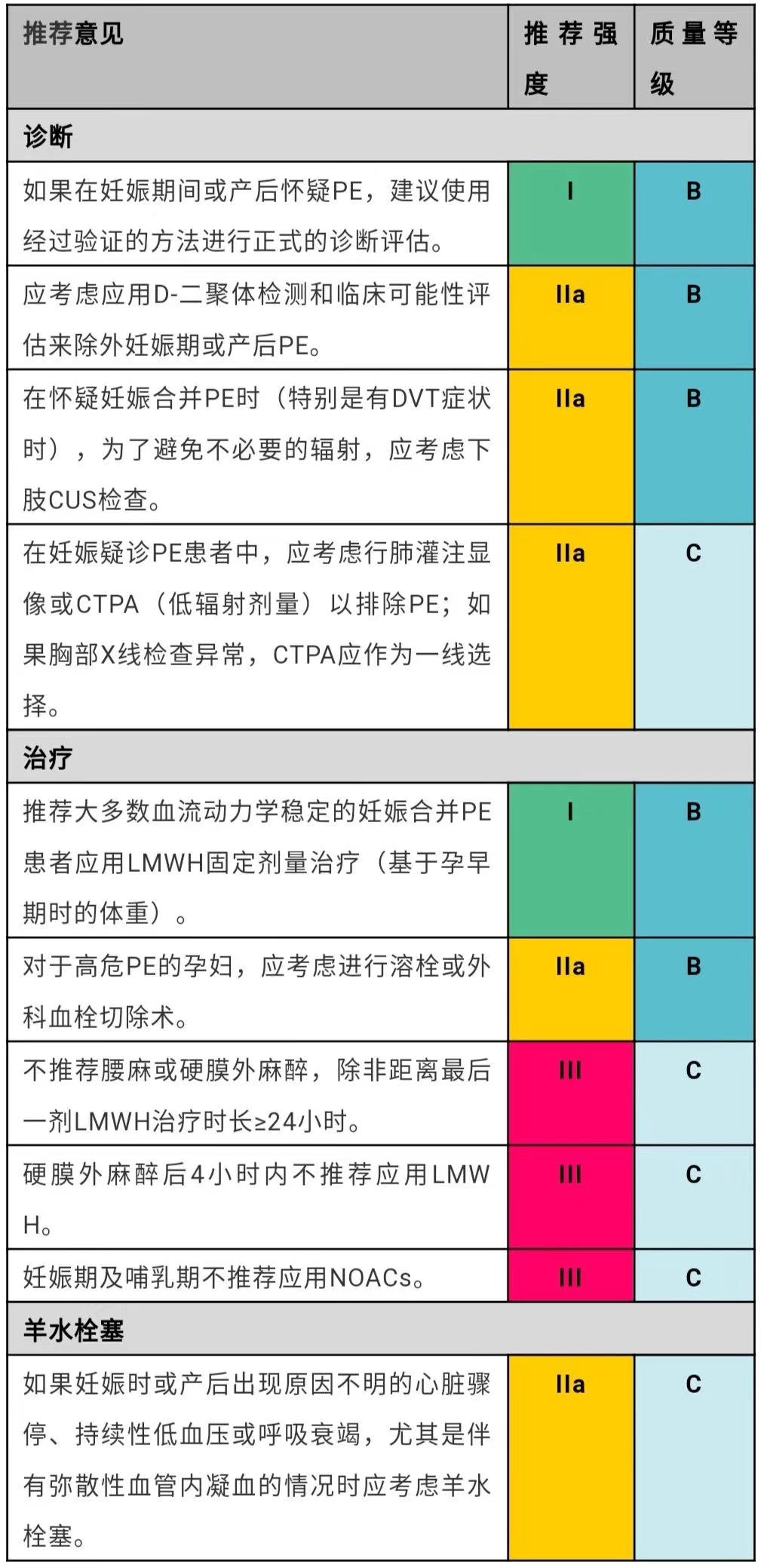
CTPA=CT肺动脉造影;CUS=加压静脉超声;DVT=深静脉血栓形成;LMWH=低分子量肝素;NOACs=非维生素K拮抗性口服抗凝剂;PE=肺栓塞。
二、2018年《中国肺血栓栓塞症诊治和预防指南》
【推荐意见】
1、妊娠期,如果疑诊急性PTE:
(1)建议进行D-二聚体检测,若阴性可基本除外急性PTE【2C】;
(2)建议行下肢CUS检查,一旦确诊DVT,即可按照VTE进行处理【2C】;
(3)如下肢CUS检查阴性,临床仍高度怀疑PTE,建议行肺V/Q显像【2C】。
2、妊娠合并急性PTE的治疗:
(1)妊娠期间抗凝药物首选LMWH【1B】。产后建议切换为华法林【2B】;
(2)溶栓治疗仅限用于危及生命的高危PTE【2C】。
【推荐意见说明】
对于疑诊急性PTE的妊娠妇女,需要平衡潜在的致死性风险和放射暴露带来的损伤。肺V/Q显像和CTPA对胎儿的放射暴露为1~2 mSv,但CTPA对孕妇乳腺组织的放射暴露高达10~70 mSv,为肺V/Q显像的35倍,会增加孕妇的乳腺癌风险。此外,CTPA检查所需要的碘造影剂可以诱发胎儿甲状腺功能减低,所以诊断妊娠合并PTE优先选择肺V/Q显像。
三、要点对比

参考文献
[1] Henriksson P, Westerlund E, Wallen H, Brandt L, Hovatta O, Ekbom A. . Incidence of pulmonary and venous thromboembolism in pregnancies after . in vitro fertilisation: cross sectional study. BMJ 2013;346:e8632.
[2] Righini M, Robert-Ebadi H, Elias A, Sanchez O, Le Moigne E, Schmidt J, Le Gall . C, Cornuz J, Aujesky D, Roy PM, Chauleur C, Rutschmann OT, Poletti PA, Le . Gal G; CT-PE-Pregnancy Group. Diagnosis of pulmonary embolism during preg- . nancy: a multicenter prospective management outcome study. Ann Intern Med . 2018;169:766-773.
[3] van der Pol LM, Tromeur C, Bistervels IM, Ni Ainle F, van Bemmel T, Bertoletti . L, Couturaud F, van Dooren YPA, Elias A, Faber LM, Hofstee HMA, van der . Hulle T, Kruip M, Maignan M, Mairuhu ATA, Middeldorp S, Nijkeuter M, Roy . PM, Sanchez O, Schmidt J, Ten Wolde M, Klok FA, Huisman MV; Artemis Study . Investigators. Pregnancy-adapted YEARS algorithm for diagnosis of suspected pulmonary embolism. N Engl J Med 2019;380:1139-1149.
[4] Armstrong L , Gleeson F , Mackillop L , et al. Survey of UK imaging practice for the investigation of pulmonary embolism in pregnancy[J]. Clinical Radiology, 2017:S0009926017301745.
[5] Fong A , Chau C T , Pan D , et al. Amniotic fluid embolism: antepartum, intrapartum and demographic factors[J]. The Journal of Maternal-Fetal & Neonatal Medicine, 2015, 28(7):793-798.
[6] Fitzpatrick K , Tuffnell D , Kurinczuk J , et al. Incidence, risk factors, management and outcomes of amniotic-fluid embolism: a population-based cohort and nested case-control study[J]. BJOG: An International Journal of Obstetrics & Gynaecology, 2016, 123(1):100-109.
[7] 中华医学会呼吸病学分会肺栓塞与肺血管病学组, 中国医师协会呼吸医师分会肺栓塞与肺血管病工作委员会, 全国肺栓塞与肺血管病防治协作组. 肺血栓栓塞症诊治与预防指南[J]. 中华医学杂志, 2018(14):1060-1087.
[8] 张竹, 王增慧, 高倩. 2018版中国《肺血栓栓塞症诊治与预防指南》解读之四:特殊情况下肺血栓栓塞症的处理[J]. 中国实用内科杂志, 2018, 38(11):49-53+110.
本文完
编译人员:王静、邵翔;审校:高倩、翟振国、瞿红
本文转载自订阅号「中日肺血管病多学科会诊平台」
原链接戳:传承、更新与交融:2019版ESC《急性肺栓塞诊断和治疗指南》与2018版CTS《肺血栓栓塞症诊治和预防指南》的精萃解读之五


