
导语
肺结节患病率接近1个亿,5~10%肺结节为肺癌。在早期阶段发现肺癌、阻止肺癌的发展,对病人的治疗、转归非常重要。那临床怎样发现肺结节是肺癌,如何筛查?筛查出来如何达到不误诊、不漏诊、不延误诊断?靠医生人工阅片已经不能满足现代人的需求,现代人工智能能否提高医生的诊断水平和效率?
究其详情,如何应用人工智能在肺结节中进行诊断、分型并早期筛查出肺癌,达到早诊早治的目的呢?
人工智能来筛查肺结节是时代需求吗?
无论男性还是女性,肺癌占所有肿瘤死因的第一位。
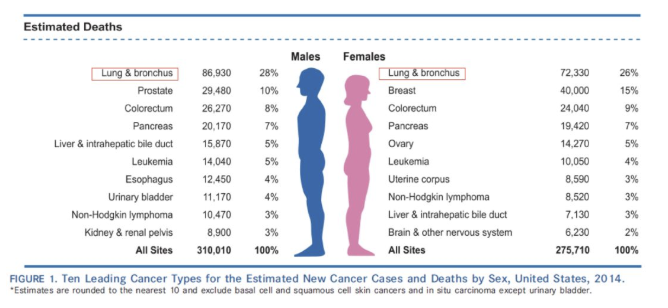
女性发病率最高的不是肺癌,而是乳腺癌,但死亡率最高的是肺癌。男性发病率和死亡率第一位的都是肺癌。因此肺癌的威胁更应该受到重视,我们男女都应该重视肺癌。
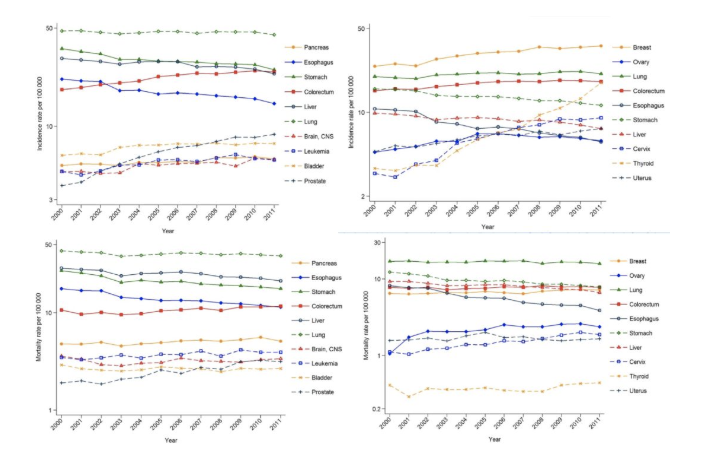
【图】上排:2000~2011年男性癌症发病率、2000~2011年女性癌症发病率
下排:2000~2011年男性癌症死亡率、2000~2011女性癌症死亡率
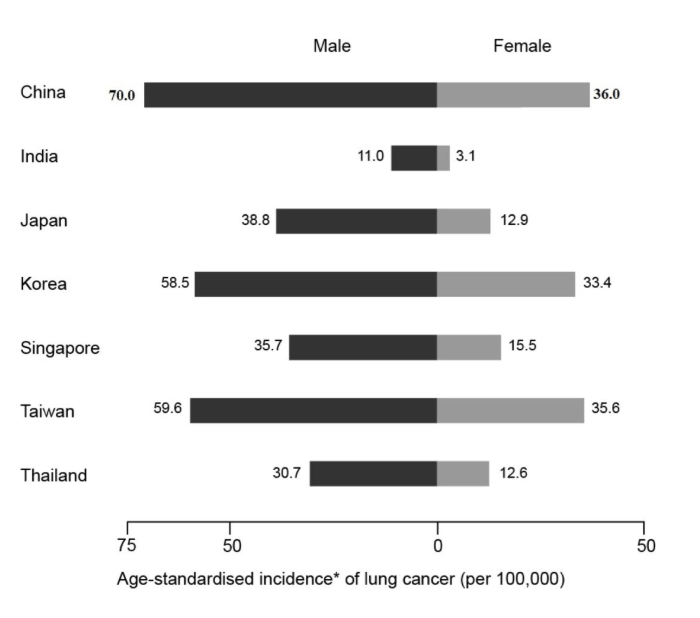
中国男性肺癌的发病率达到了70/10万,女性达到了36/10万,这个是2011年时候的数据,现在男性发病率已经不是原来的73万,超过了83万。这样在亚洲所有的国家和地区之中,中国的肺癌无论是男女发病都是首位。
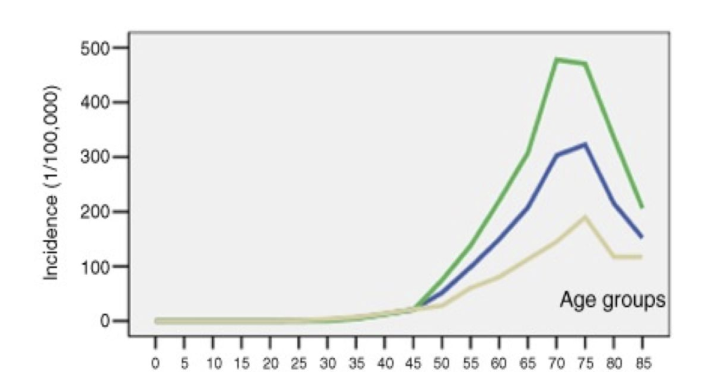
这是来自河北石家庄在Thorac Cancer上发表的文章,男性70岁的年龄肺癌发病率接近了500/10万,什么概念呢?这是世界之最。
怎么解决这个问题?特别是早诊、早治,肺结节中肺癌的发病率是80多万,肺结节患病率接近1个亿,5~10%肺结节为肺癌,在这个阶段发现肺癌、阻止肺癌的发展,对病人来说是非常重要的。那临床怎么发现肺结节为肺癌,如何筛查,筛查出来如何不误诊、不漏诊、不延误诊断,这是相当大的工作量。不但工作量大,还要求提高手工业作坊式诊疗模式,医生为国家甚至国际标准的现代化流程作出贡献,怎么能达到呢?靠我们人工阅片,不能满足现代人的需求,那如何同时提高医生的诊断水平和效率,那就需要人工智能(Artificial Intelligence,AI)。
AI由人制造出来的机器所表现出来的智能。我们把它分成两类,一类是弱人工智能,一类是强人工智能。「弱人工智能」(Narrow AI)是能够与人一样,甚至比人更好地执行特定任务的技术。「强人工智能」(General AI),它不仅有和我们人类一样的感知和思考能力,并且它的这种能力比我们还要强大很多,就好像一个超人一样。并且它的这种能力可以比人类强大,变成超人工智能,但现在不是所有的想法都能达到,我相信将来能达到。
正因为如此,中国的人工智能已经按照国家的发展战略,《新一代人工智能发展规划通知》 :2020年:人工智能将达到世界同步水平;2025年:人工智能理论重大突破,部分技术应用达到较高水平;2030年:人工智能理论和应用总体达到行业较高水平,成为世界主要人工智能创新中心。
基于CT影像的无创病理诊断系统
(iPathology)在肺早期腺癌中的应用
背景
这个系统对肺腺癌进行亚型的分类,我们研究该系统CT的影像诊断。Travis WD等研究结果发现,结节中实性成分比值与病变的侵润成分有密切的关系。
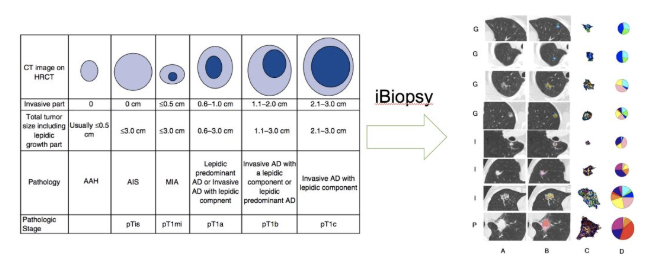
方法
在中山医院,我们收集了195个病人,术后病理做了亚型分类,经过计算机处理,PNIFS多维度特征提取,以及诊断有效性,包括AUC、PRS、ROC,不仅能分辨出是否为肺癌,还能分辨出亚型,如原位腺癌、微浸润腺癌、非典型瘤样增生。
肺腺癌结节CT
2014~2016,n=195(1757s)
术后病理亚型
AAH/AIS/MIA/IAC
6/43/43/114
计算机处理
肺结节影像特征集(PNIFS)
多维度特征提取,R-SVM
诊断有效性:
AUC,PRS,ROC
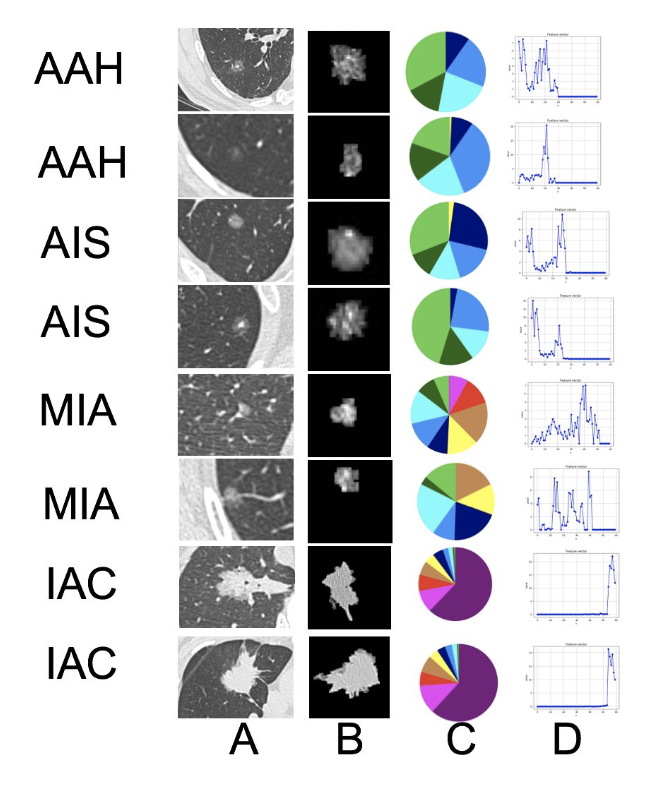
(A) 肺结节原始CT轴状位断层;
(B)肺结节三维重建;
(C)肺结密度特征分布饼状图;
(D)肺结节向量特征可视化曲线图; AAH,非典型腺瘤样增生;AIS,原位腺癌;MIA,微浸润腺癌;IAC,浸润性腺癌。
这样达到原始数据库的处理标准化流程和病理亚型分类,标准化数据库的流程就是这样,肺癌常规的影像,它可以对CT诊断的数据进行像素单元细分,应用数字可视化方法进行分配,最后我们通过第一步构建一个参考的标准,第二步通过病理亚型确诊,第三步判别肺结节的风险。
1.原始CT数据库
(层厚<=1mm)
复旦大学附属
中山医院
2.预处理
图像分割
•肺间质部分
•肺结节部分
3.标准化数据库
特征提取(无监督聚类)
•图像单元数据库
•距离矩阵标记的图像数据库(10维)
•多向量的CT密度分布特征(60维)
4.病理亚型匹配
AAH, AIS, MIA, IAC
•机器分类模型(支持向量机,SVM)
5.分类
结节风险
我们研发的iPathology,准确性可达85%~95% 。在ATS上获过奖。
iPathology系统提供了一种无创的基于CT影像分析的肺腺癌结节的分类方法,包括 AAH,AIS,MIA 和 IAC四种亚型。
我们的研究结果提示iPathology系统可以在不久的将来为肺结节的精准治疗提供诊断的依据。
基于深度卷积神经网络技术的人工智能肺结节筛查和诊断系统在中美人群中的应用
筛查:深度学习
诊断:影像组学 vs. DCNN
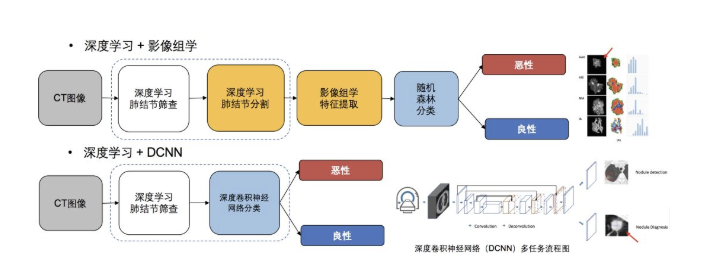
影像组学可以提供我们用于诊断的重要特征,但是深度学习具有更高的准确性。
以下是我们测试和训练的数据集。
LIDC测试数据集: 92 scans,总结节数:254,恶性结节数:62,良性结节数:192 。
中山训练数据集:452 scans,总结节数:2,141 ,恶性结节数:267,良性结节数:1,874 。
中山测试数据集:51 scans,总结节数:210,恶性结节数:36,良性结节数:174。
与美国人群相比,中国人群的肺结节偏小,毛玻璃样结节GGO更多。美国和中国的数据集中肺结节的分布情况存在明显差异。
在中国数据集中小于8mm的肺结节所占的比例显著大于美国数据集;在中国数据集中GGO占相当大的比例,而在美国数据集中GGO非常罕见。
在美国数据集中训练的AI模型不适合运用于中国肺结节人群,在中国数据集重新训练后,肺结节筛查的敏感性显著提升。
模型-随机森林:
在96项已知特征中筛选出最重要和最不重要的影像组学特征
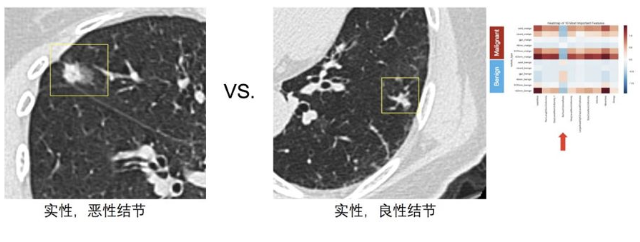
实性,恶性结节:数值越低代表更规整(球形)的形状;
实性,良性结节:在热图分析中,恶性实性结节更倾向球形,而良性结节较少呈现球形。
mGGO,恶性结节:GLN是衡量图像中灰度密度值的变异性,数值越低代表灰度密度值越均一;
mGGO,良性结节:在热图分析中,恶性混合性GGO的灰度密度值的变异较大,而在良性结节中GLN数值较低。
训练数据集:在美国数据集中,AI模型在诊断恶性结节时具有较高的敏感性,但假阳性率较高,一些良性结节被判断为恶性结节;
测试数据集:通过在中国数据集的重新训练之后,AI模型的假阳性率显著减少,同时诊断的敏感性和特异性大大提高。
小结:
• 在中美肺结节人群中存在明显差异肺结节的特征分布。
• 人工智能(AI)技术,例如深度卷积神经网络(DCNN)系统为肺结节筛查和早期诊断提供了一个有效途径 。
• DCNN AI 系统通过深度学习的改良和重新训练可以把诊断肺结节的AUC提高至0.986。
参考文献
[1] CA CANCER J CLIN 2014;64:9–22
[2] CA Cancer J Clin 2016;
[3] Bai, et al. S0012-3692(16)01308-8 10.1016/j.chest.2016.02.650
[4]Thorac Cancer. 2016 Mar; 7(2): 238–245.
[5] Parkin DM, et al. CA Cancer J clin 1999;49.33-64
[6] Travis WD, Brambilla E, Burke AP, et al. Lyon 2015
[7] F Maldonado, F Duan, SM Raghunath, et al. AJRCCM 2015
[8]Le VB, Yang DW, et al. Computer Methods and Programs in Biomedicine, 2018,160:141-151.
[9] Le VB, Yang DW, et al. Journal of Medical Imaging and Health Informatics, 2017,7(8):1753-1758.
[10] Armato SG 3rd, et al. Med Phys. 2011 Feb;38(2):915-31.
[11] van Griethuysen, etc. Cancer Research, 77(21), e104–e107.
专家介绍



