病例简介
患者,女,29岁。职业:个体户;2019-5-17入院。
主诉:咳嗽伴痰血半月余,胸痛8天。
现病史
2019年5月1日患者无明显诱因下出现咳嗽咳痰,少许白粘痰,偶有痰中带血,无低热盗汗、无纳差乏力,无胸闷胸痛、无气促等,自服止咳药物后无好转。5月5日至当地医院就诊,查胸部CT提示肺弥漫性病变,予抗感染化痰等治疗。5月9日出现右侧胸痛,伴活动后气促,咳嗽咳痰及痰中带血无加重,无发热,当地医院复查胸部CT提示右侧气胸,压缩60%,双肺弥漫性囊性病变;予胸腔闭式引流后,气促改善不明显。5月13日来我院急诊,查血常规:RBC 4.85*10^12/L,Hb 144g/L,WBC 11.28*10^12/L,CRP:21.9mg/L;胸部正位片:气胸引流术后改变,双肺炎症机会大,右侧少量胸腔积液;现为进一步诊治收入我科。
病程中精神可,胃纳夜眠可,二便如常,体重无明显变化。
既往史:否认高血压、糖尿病、心脏病等疾病史,否认传染病史,否认过敏史,否认手术外伤史,否认过敏史。预防接种随社会。
个人史:生长于原籍,否认抽烟、喝酒等不良嗜好,否认疫区驻留史,否认毒物、放射性物质接触史。
婚育史:已婚,已育1女,配偶及女儿体健。
家族史:否认家族遗传病史,否认家族肿瘤病史。
体格检查
T:36.0 ℃ P:98 次/分 R:20 次/分 BP:124 / 87mmHg
SpO2 95%(未吸氧)神清,静息时气平,自主体位,查体合作。全身皮肤未见皮疹,全身浅表淋巴结未及肿大。胸廓无畸形,右上肺叩诊鼓音,左肺叩诊清音;右肺呼吸音低,左肺呼吸音粗,未及明显干湿啰音,心率98bpm,律齐,腹部隆软,可见紫纹;肝脾肋下未及,四肢脊柱无畸形,双下肢无浮肿。
辅助检查
血常规:RBC 4.85*10^12/L,Hb 144g/L,WBC 11.28*10^12/L
炎症指标:CRP 21.9mg/L,PCT 0.09ng/mL
生化:TB 23.9μmol/L,ALT/AST 47/46U/L,SCr 64μmol/L,电解质正常。
出凝血:PT11.8s,APTT29.9s,INR 1.08,D二聚体0.97mg/L
心脏标志物:cTnT 0.008ng/ml,pro-BNP 13.4pg/mL
微生物:呼吸道九联检、支原体抗体、隐球菌荚膜抗原、G试验(-)
自身抗体:抗核抗体 1:100,其余阴性
血气分析:PH7.4,PCO2 46mmHg,PO2 74mmHg,SO2 95%(未吸氧)
肿瘤指标:CEA、CA125、CA199、SCC、NSE、CYFRA211等均正常。
胸部影像学检查
2019-5-13我院胸片
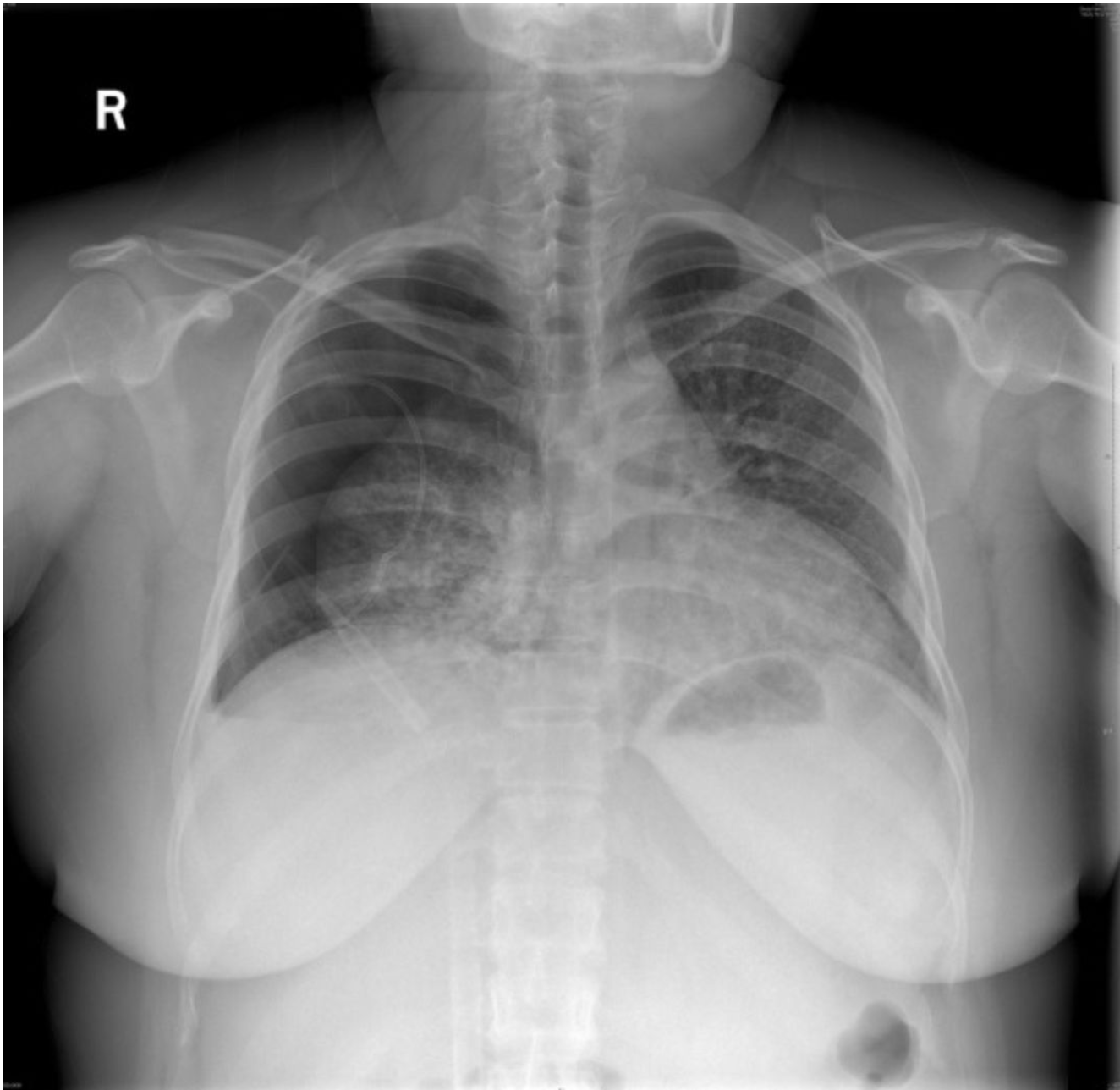
2019-5-14我院胸部CT平扫
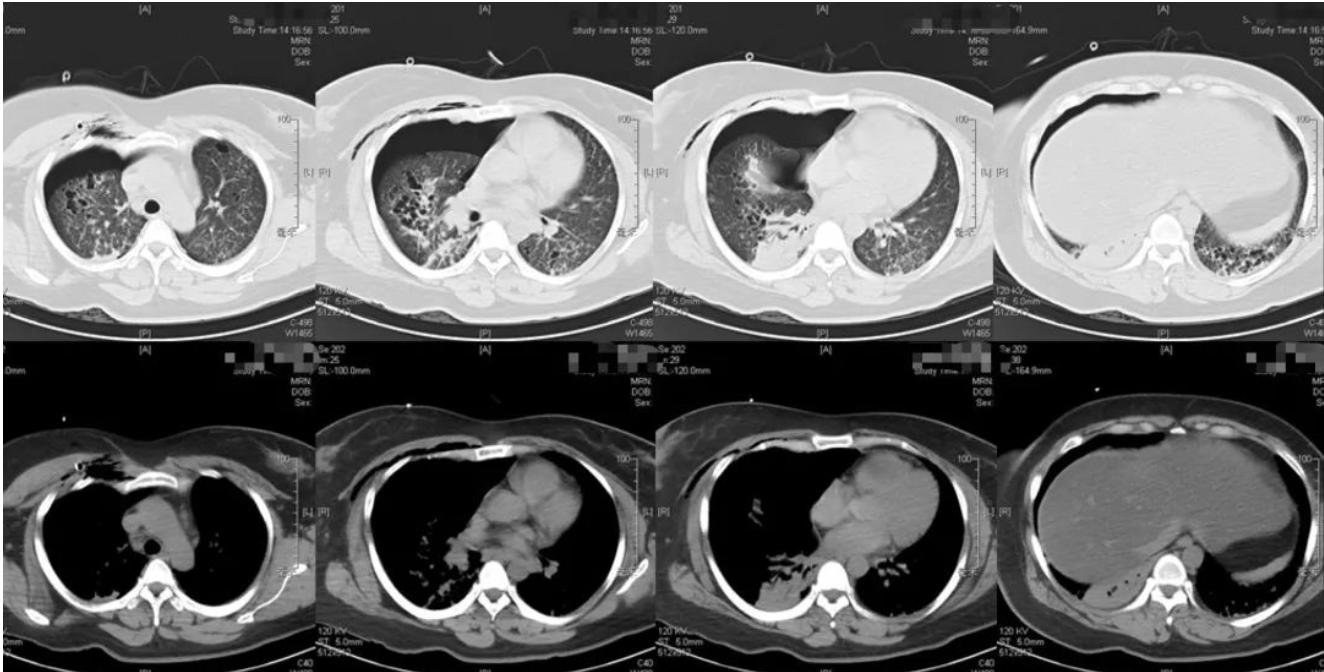
初步诊断
1.气胸
2.双肺弥漫性病变
3.肺部感染
肺部弥漫性囊泡样病变,如何鉴别?
患者青年女性,因「咳嗽、咳痰、咯血半月余,胸痛8天」入院,急性起病,逐渐加重,胸部CT提示右侧气胸,双肺相对弥漫分布的气囊与结节,沿气管血管束分布,右下肺实变。肺部弥漫性囊泡样疾病,需要考虑肺淋巴管平滑肌瘤病(LAM)、BHD综合征、肺朗格汉斯组织细胞增生症(PLCH)、淋巴细胞性间质性肺炎(LIP)、感染性疾病如耶氏肺孢子菌肺炎(PCP)等疾病。LAM一般常见于育龄期女性,影像学以弥漫均匀分布的薄壁囊泡为主要表现,此例患者为年轻女性,肺部多发囊泡,需要考虑LAM,但囊泡不是薄壁,分布不均匀,形状不规则,不符合LAM的典型表现。PLCH一般多见于吸烟患者,影像学以奇形怪状的沿支气管血管束分布的囊泡样改变为特点,吸烟患者一般以上叶及中叶病变为主,不累及肋膈角,多系统病变患者可以累及肋膈角,本例需考虑PLCH可能。BHD综合征肺部表现为多发薄壁囊肿,形状不规则,多于基底部、外周、沿纵隔分布,其他系统表现可合并皮疹、肾肿瘤等,可有家族史,本例患者无BHD家族史,需进一步排查其他器官有无病变。LIP常有肺部多发囊泡改变,一般合并自身免疫性疾病,该患者需进一步完善自身抗体等风湿免疫相关指标,协助诊断。此外,还需考虑PCP、金葡菌感染等感染性疾病。PCP多见于免疫抑制宿主,可以有多发性肺气囊的表现,该患者无发热,无免疫抑制病史,目前考虑可能性不大。
初始治疗
1、抗感染:头孢美唑2g bid ivgtt;
2、继续留置胸腔闭式引流;
3、补液,维持水电解质平衡等支持治疗。
入院后辅助检查
2019-05-15实验室检查:
血常规:RBC 4.02*10^12/L,Hb 117g/L,WBC 6.52*10^9/L
肝功能:TB 8.9μmol/L,ALT/AST 28/33U/L
肾功能:SCr 57μmol/L
炎症标记物:CRP 74.4mg/L (↑)PCT 0.07ng/mL
D-二聚体:0.98mg/L (↑)
自身抗体:ANA 1:100 (↑) ,其余正常
5-16胸片
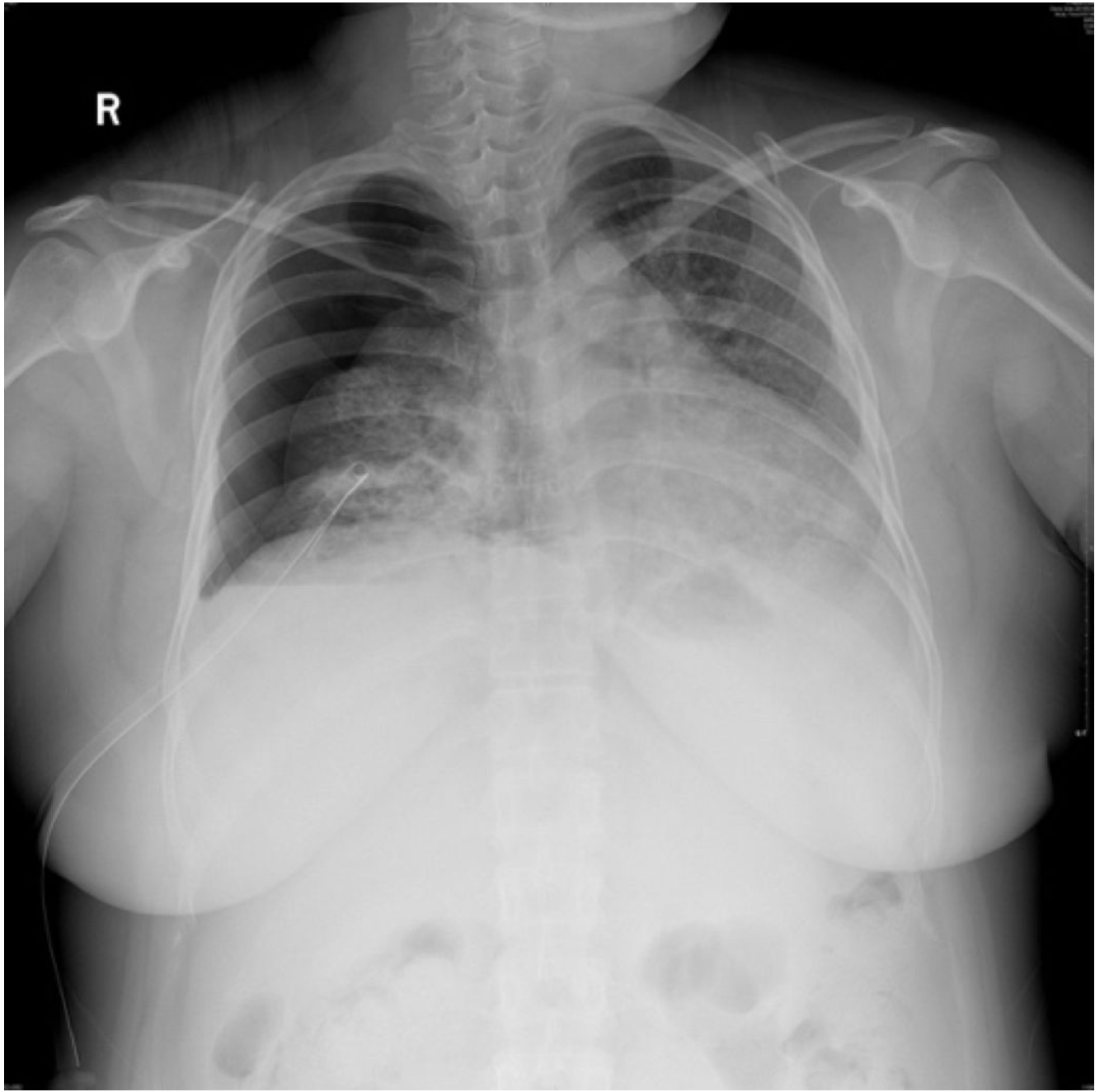
5-17胸部LDCT
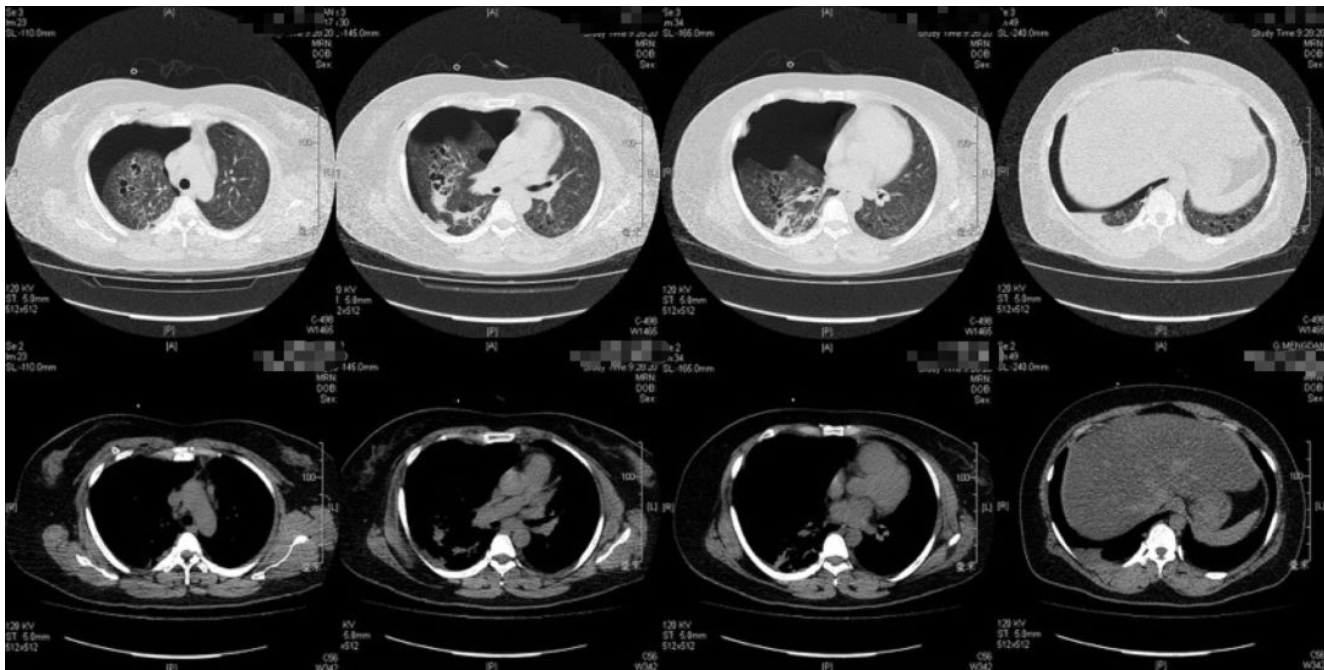
补充病史
2015-2:口干、多饮、多尿;
2015-5:停经,曾服用黄体酮治疗,月经可来,现自行停用;
2015-7:当地查头颅MRI,诊断为脑垂体柄肿瘤、中枢性尿崩症;
2015-10:上海某医院行γ刀治疗,术后症状未缓解,予去氨加压素口服,尿量明显减少,口干症状明显改善;
后每半年定期随访垂体病变无明显变化,未监测激素水平变化,现每日去氨加压素共0.25mg(0.05mg/次,在6、10、15、18及21时分次服用)口服。
进一步辅助检查
2019-05-19实验室检查:
血常规:RBC 4.36*10^12/L,Hb 129g/L,WBC 6.98*10^9/L
尿、粪常规:正常
肝功能:TB 9.1μmol/L,ALT/AST 37/40U(↑)/L
肾功能:SCr 53μmol/L
电解质:Na 142mmol/L,K 4.3mmol/L,Cl 104mmol/L,Ca 2.32mmol/L,P 1.78mmol/L,Mg 0.82mmol/L
炎症标记物:CRP 23.7mg/L (↑),PCT:0.10ng/mL
D-二聚体:2.09mg/L (↑)
心脏标志物:cTnT <0.003ng/ml,pro-BNP 5.1pg/mL
呼吸道九联检、支原体抗体、隐球菌荚膜抗原、G试验、HIV(-)
LDH 257U/L (↑)
免疫球蛋白:IgG 7.53g/L,IgA 1.08g/L,IgM 1.02g/L,IgE <10g/L,IgG4 0.35g/L
补体:C3 1.61g/L(↑) ,C4 0.36g/L,总补体 63.7IU/mL
α1-抗胰蛋白酶:1.54g/L
静脉血糖:5.2mmol/L,HbA1c 5.5%
血脂:TG 2.02mmol/L (↑) ,HDL 0.49mmol/L(↓),Lp(a) 667mg/L (↑)
ACTH:28.9pg/ml(8时),9.1pg/ml(16时),14.1pg/ml(0时)
皮质醇:78.0nmol/L(8时),38.7nmol/L(↓)(16时),18.5nmol/L(↓)(0时)
甲状腺功能:T3 1.6nmol/L,T4 66.5nmol/L,FT3 4.0pmol/L,FT4 9.4pmol/L(↓),TSH 4.850uIU/mL (↑) ,TG 259ng/mL (↑) ,TGAb <10.0IU/mL,TPOAb <9.0IU/mL,TRAb <0.8IU/L
性激素:LH <0.3mIU/ml,FSH 1.7mIU/ml,PRL 1104.0mIU/L (↑) ,E2 <18.4pmol/L
2019-5-20辅助检查:
甲状腺、腹部及妇科B超:甲状腺双侧叶实质占位——考虑良性病变;子宫偏小,其余正常
心超:正常,LVEF 71%,肺动脉压力 30mmHg
垂体平扫+增强MRI:垂体柄结节样强化灶,部分空蝶鞍
骨扫描:全身骨骼平面显像未见明显异常
2019-5-21胸片:
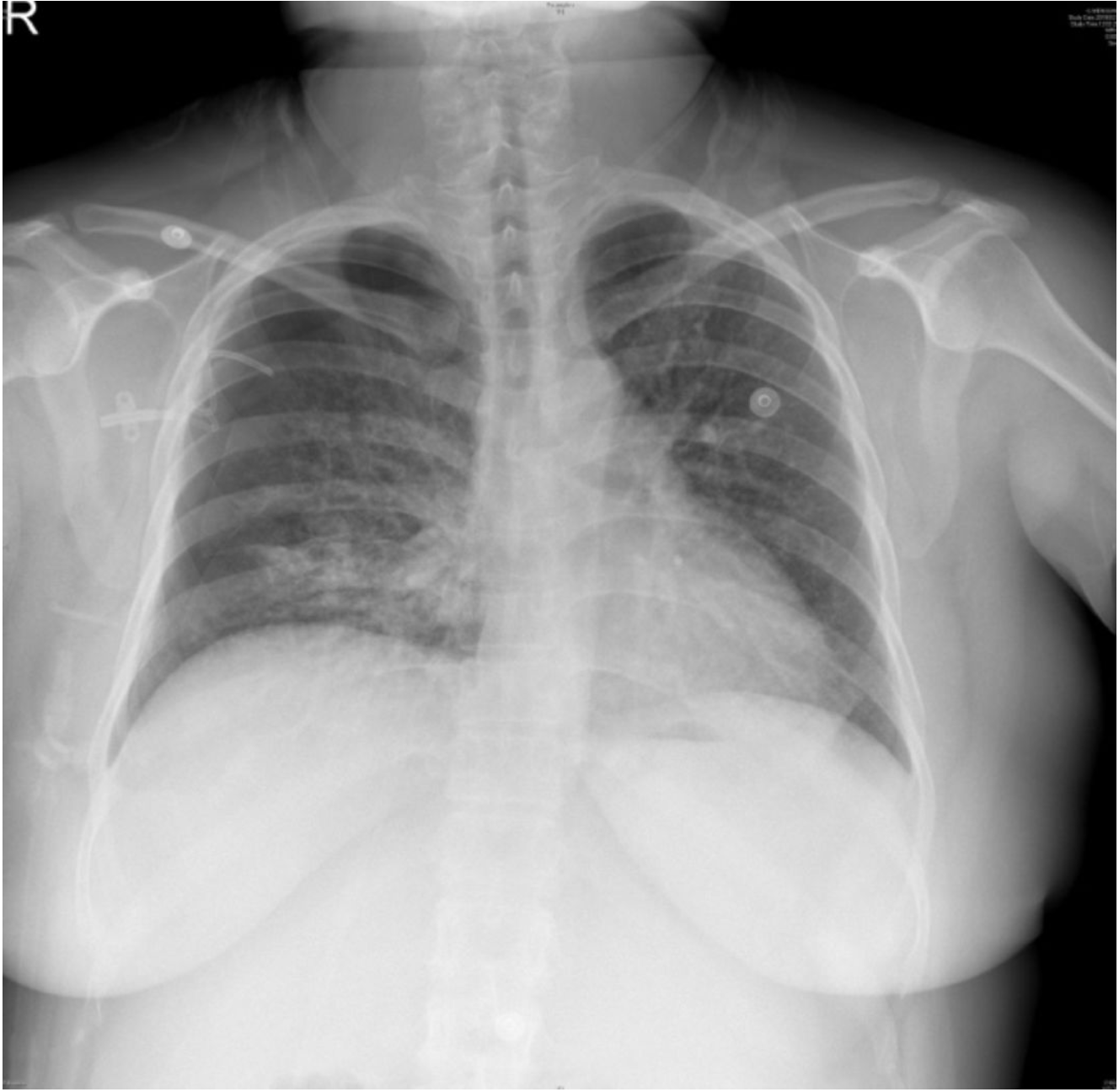
更正诊断
1.右侧气胸
2.双肺弥漫性病变
3.肺部感染
4.垂体肿瘤
5.中枢性尿崩症
6.肥胖症
7.停经
治疗方案调整
1、抗感染:头孢唑肟3g bid ivgtt(5-17下午起);
2、激素替代治疗:氢化可的松100mg q12h(5-20下午起),100mg q8h(5-22上午起),继续目前去氨加压素口服治疗方案;
3、对症支持治疗:营养支持、雾化吸入、抗凝、护胃、维持水电解质平衡
4、因气胸胸腔闭式引流疗效不佳,2019-05-22全麻下行胸腔镜下右侧大泡切除术
病理
(右肺大泡)参考免疫组化结果,符合朗格汉斯组织细胞增生症。
免疫组化:S-100(部分+),CD1a(+),Langerin(+),CD68{KP1}(少量+),Ki-67(50%阳性),CK7(上皮+),TTF-1(上皮+),CD15(散在+),HLA-DR(部分+),PLAP(-),CD45RO(部分+),Lysozyme(个别+),B-raf V600E(-),LCA(+)。
基因检测:B-raf基因第15外显子未检测到突变。
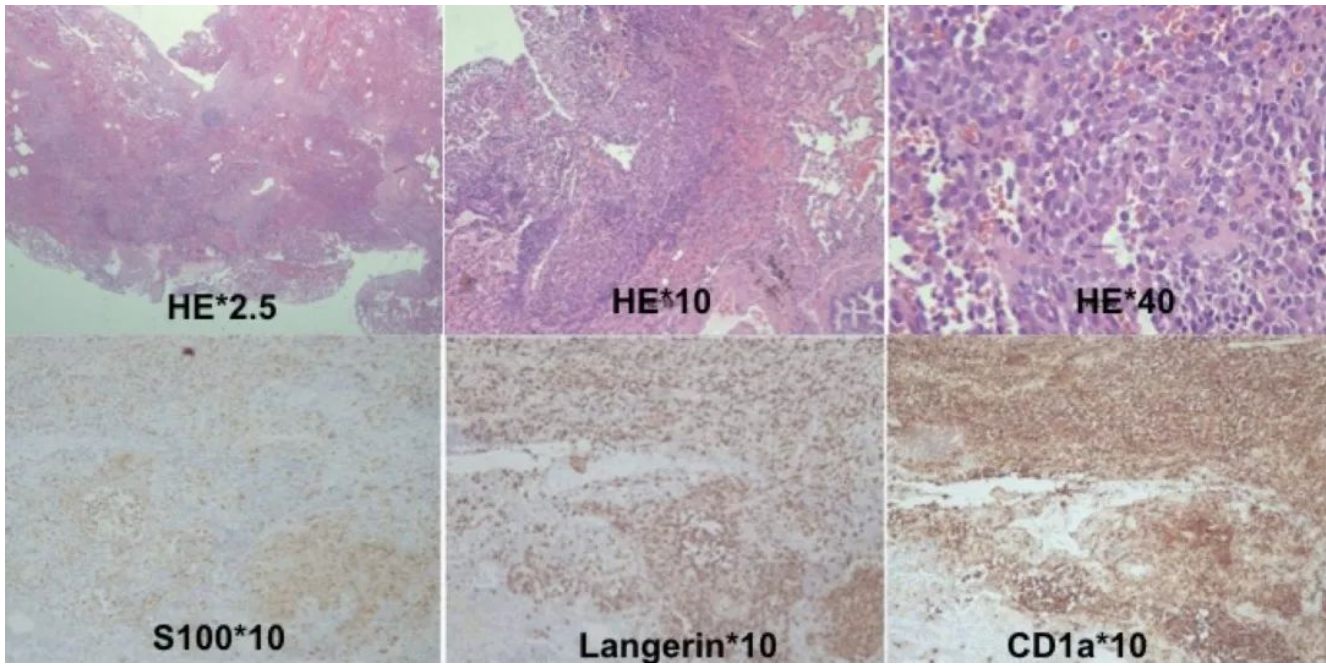
最终诊断
朗格汉斯组织细胞增生症(肺、垂体)
病情变化
2019-05-23凌晨1时,患者出现畏寒、高热、头痛、恶心、胸闷、心悸等不适;查体见胸腔置管通畅,体温39.2摄氏度,SpO2 93%(4L/min),血压 143/95mmHg,心率123次/分,呼吸26次/分,双肺呼吸音弱,未闻及干湿啰音。
2019-05-23床旁胸片:
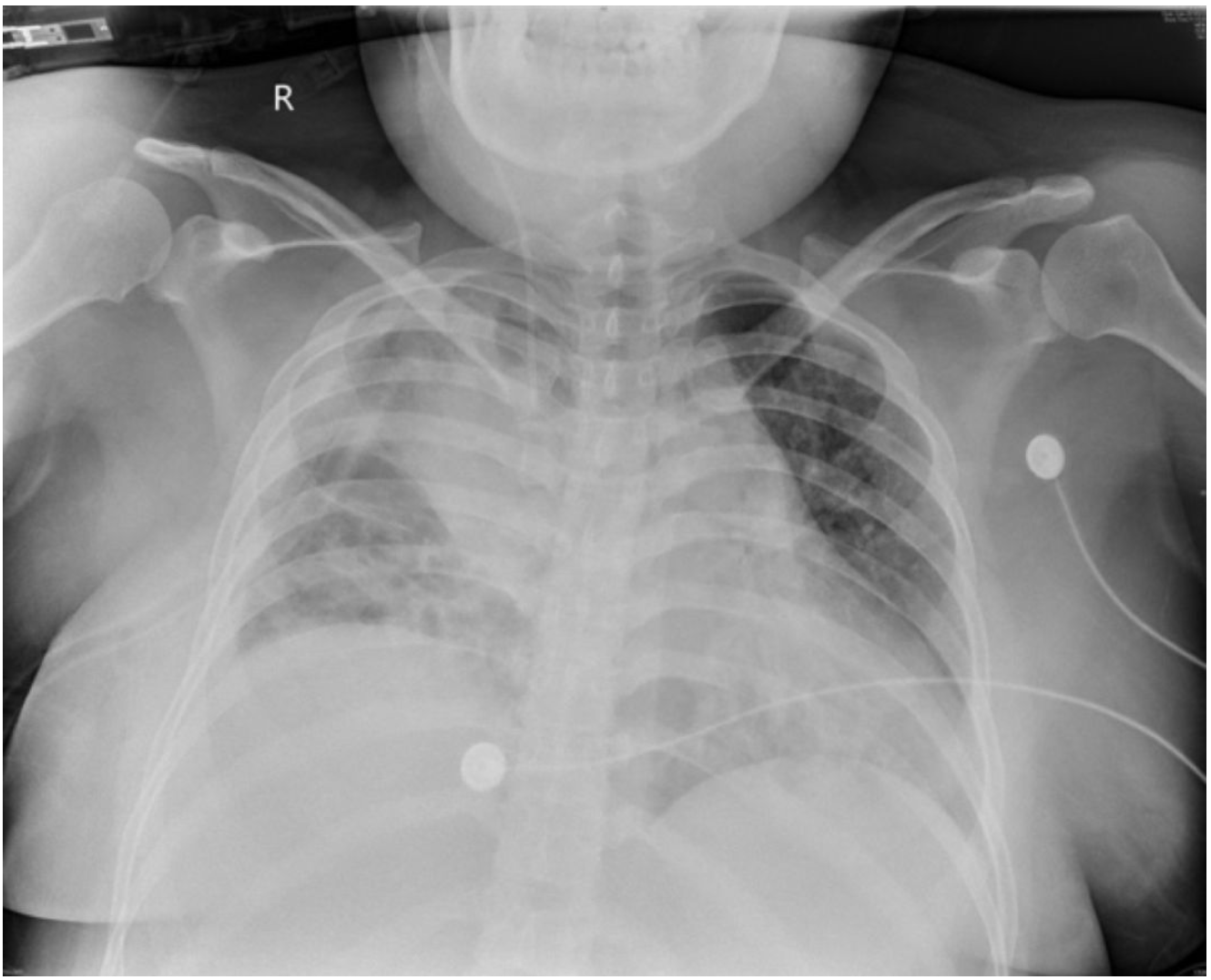
实验室检查:
检查日期:2019-05-23
血常规:RBC 5.06*10^12/L,Hb 147g/L,WBC 19.59*10^9/L (↑)
肝功能:TB 11.7μmol/L,ALT/AST 53/40U/L (↑)
肾功能:SCr 58μmol/L
CRP:42.2mg/L (↑)
D-二聚体:2.18mg/L (↑)
乳酸:4.05mmol/L (↑)
心脏标志物:cTnT 0.007ng/ml,pro-BNP 215.2pg/mL (↑)
血气分析(鼻导管4L/min):pH 7.37,PaCO2 50mmHg (↑) ,PaO2 55mmHg(↓),BE 3.6
BG:10.9mmol/L (↑)
促肾上腺皮质激素:9.3pg/ml
皮质醇:695nmol/L(↑)
甲状腺功能:FT3 2.6pmol/L (↓),FT4 9.5pmol/L(↓),TSH 1.490uIU/mL (↑)
治疗方案再调整
1、抗感染治疗方案:美罗培南1g ivgtt q8h+莫西沙星0.4g ivgtt qd(5-23至5-31)
2、激素替代治疗方案:遵内分泌科会诊意见,氢化可的松100mg ivgtt q8h(5-23凌晨起),q12h(5-26至5-31),醋酸可的松片 25mg po bid(6-1起),优甲乐 25ug po qd(5-28起),去氨加压素维持术前剂量
3、对症支持治疗:营养支持、雾化吸入、抗凝、护胃、维持水电解质平衡
转归及后续治疗
1、治疗后患者体温平,复查CT提示气胸吸收,2019-05-26拔除胸腔闭式引流管,2019-06-06出院;
2、出院后至外院血液科继续诊治,目前已完成6周期阿糖胞苷单药化疗;
3、目前有活动耐量受限(一次爬2层楼),无其他不适主诉,未再出现气胸,去氨加压素现减量至0.1mg/日,尿量约5000ml/日。
2019-05-31胸部CT:
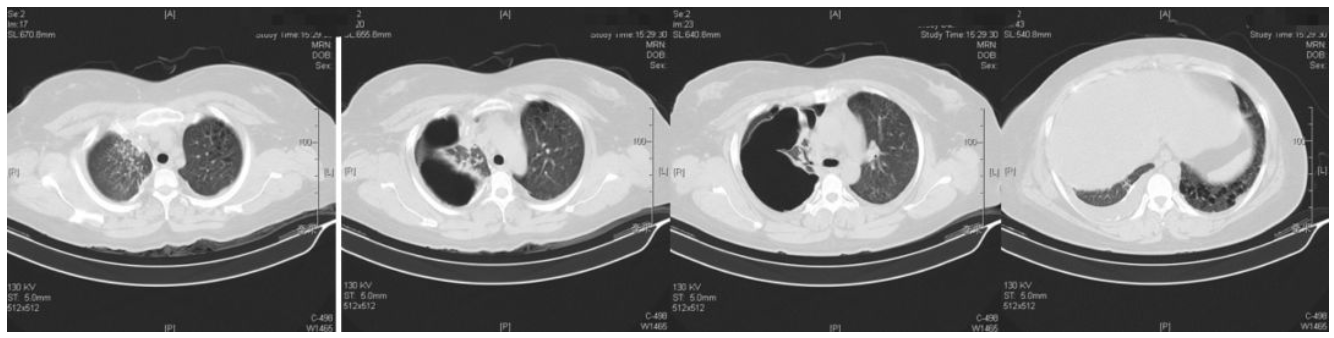
专家点评
金美玲教授
本病例的鉴别诊断主要强调的是弥漫性囊泡样改变的鉴别,要关注各类囊泡样疾病的特点。LAM的囊泡一般为弥漫均匀的薄壁囊泡,与本例不同,但因患者为育龄期女性,因此要考虑与LAM鉴别,同时要关注全身其他系统的问题。LIP也是较常见的有囊泡改变的疾病,但是特别强调,LIP多发生于自身免疫系统疾病患者,特别是年轻女性要注意排查风湿免疫指标,比如干燥综合征相关的指标检测及病史的询问。BHD等其他一些疾病也要考虑到。
鉴别诊断要强调全身特征,本例患者肥胖、尿崩症、垂体肿瘤等,对鉴别诊断有很大意义。弥漫性囊泡病变的鉴别,不要动不动强调病理。LAM无病理也可以诊断,这个病人肺部有奇形怪状的气囊,合并垂体肿瘤,已经高度提示LCH,因为正好巧合气胸需要外科手术治疗,因此行胸腔镜活检明确了病理诊断。病理固然重要,但仔细的问病史和查体更重要。
张新主任医师
本次PCCM病例讨论学员准备充分,讨论合理,希望下次可以更完美。
鉴别诊断不一定要罗列很多,鉴别的要点一定要准确,要抓住疾病特点,比如LAM要强调薄壁、弥漫,而BHD是综合征,一定会合并皮肤、肾脏等其他系统的病变。关于病理活检,囊性病变一般不轻易做肺穿刺,因为引起气胸的风险非常大,而且本例患者本来就合并气胸。但因为气胸引流效果不佳,考虑手术治疗,则可以同时进行活检。本例患者除了肺部病变,还有垂体受累,因此在病理诊断之外,已强烈提示LCH的诊断。
提醒一下年轻医生,少见病不能仅仅依据影像学特征来鉴别,要抓住哪些改变是有特征性的,有鉴别诊断价值的。如果多个环节的线索共同指向同一疾病,则可高度怀疑。本例患者的影像学表现其实不是很典型。囊性病变,随着不同病程,可以有磨玻璃影、实变、结节等不同表现,有一定的演化过程,可以帮助我们更好地理解影像学的表现。
王葆青教授
鉴别诊断主要是LCH和LAM的鉴别,确诊均需要病理。那怎么选择活检的方式和部位?LCH可以局限于肺部,也可以累及其他部位,因此一开始的病史询问其实是缺陷的。患者肥胖,腹部有紫纹,要注意是否有合并垂体的病变。此外还要关注是否有皮肤病变。如有皮肤病变,则可以进行皮肤活检。如垂体有病变,也可进行垂体的活检,但本例患者已行γ刀治疗,故不能选取。如有骨病变,也可进行骨活检。本例患者气胸治疗效果不佳,有外科手术指征,因此可以在处理气胸的同时进行活检。
顾宇彤教授
临床分析时抓住囊泡样病变的主线的同时,不要忽略细节。患者最初的CT提示右下肺实变,抗感染治疗后有吸收,后来抗感染治疗方案的调整依据是什么,应该再讨论一下。
放射科张兴伟副主任医师
本例患者的胸部CT主要表现为两肺相对弥漫分布的怪异的气囊和结节,气囊为薄壁,以中上肺分布为主,沿支气管血管束分布,符合LCH细胞沿支气管分布的特点,并且有可能会引起支气管阻塞,类似活瓣样的作用,因此囊腔的形状怪异。胸腔镜术后的CT表现,可能是局部阻塞牵拉引起疱的加重,也可能是胸膜粘连后局限性的气胸的表现。
病理科卢韶华主任医师
在本例患者肺大泡切除的HE染色标本中,可以在低倍镜下见到大泡、实性改变及出血,实性部分基本为实变,围绕支气管生长,在支气管周围可见成片实性生长的细胞巢,为病变细胞。高倍镜下可见成片的嗜酸性粒细胞及胞浆呈淡伊红色且核异型性不大的组织样细胞,细胞核可见咖啡豆样核沟。LCH与LAM不同,这些病变细胞与支气管壁伴随,而不是在囊腔周围分布。LCH也称嗜酸性肉芽肿,常伴大量嗜酸粒细胞浸润。结合本例患者影像学表现及病理特点,首先考虑为LCH。进一步行免疫组化,提示S-100(部分+),CD1a(+),Langerin(+),这是诊断LCH必备的3个指标。LCH还往往有B-raf V600E突变,但本例患者为阴性。因此,本例患者诊断为LCH明确。
何礼贤教授
LCH是少见病,我曾经见过一例,反复气胸伴尿崩症,当时虽然没有病理依据,但仍按照LCH来诊断。LCH因为比较少见,常常会想不到,因此看到弥漫性囊性疾病,要考虑到LCH。PCP主要是见于免疫抑制宿主,可以发生多发性肺气囊,一般两上肺为主。另外也要考虑到肺腺样囊性癌等疾病。关于LCH的预后,与是否多器官受累,有无吸烟史等很多因素都相关。本例患者已合并垂体病变,已经不是局限性病变,预后会受到影响。据报道,部分病例不治疗可以自行恢复,部分患者应用激素会有一定疗效。但对于这例病人,需要进一步的观察今后的情况。发生呼吸衰竭的病人还可以考虑肺移植,但需要注意移植后仍有复发的可能。这例患者目前还没有到肺移植的程度。此外,还有个别报道提出可应用造血干细胞移植治疗LCH。
宋元林教授
这次病例讨论选择的病例很好,各位学员总结资料较全,分析思路清晰,各位专家点评精彩到位。有时候对于疾病的诊断,首先考虑像什么,不像什么。可以通过以下三种方法:1)确认与排除相结合:比如免疫抑制宿主肺部弥漫性磨玻璃影合并圆形气囊,需要考虑PCP,本病例不符合上述特点,可基本排除;LAM一般为薄壁弥漫气囊,本例不太像,而PLCH和BHD很像;2)影像与病理相结合:LCH为组织细胞增生引起,推测囊壁为不规则,形状怪异,而不会表现为与LAM、PCP一样的薄壁充气的圆形气囊,因此可以结合疾病的病理特点来推测影像学表现;3)局部与整体相结合:比如LCH可以累及肺、皮肤、垂体等多种器官,如果患者有多系统受累,就需要重点考虑全身性疾病。而肿瘤性疾病,一般少有累及多系统,因此可以排除。另外,本例患者后续的病情加重,首先考虑感染,但感染本身也会引起垂体危象、甲状腺危象等情况,因此需要抗感染的同时补充相应的内分泌激素。
作者介绍
 朱亦淳
朱亦淳
复旦大学附属中山医院呼吸与危重医学科住院医师,PCCM专科培训学员(第三年)
本文完
编辑:《呼吸界》Jerry
未经许可,请勿转载
特别鸣谢
瀚晖制药有限公司
点击「阅读原文」,可进入《呼吸界》直播间参与回看。


