推荐语
昨晚,第二期PCCM疑难病例讨论吸引了几千呼吸人的关注。为吸引更多的呼吸人参与讨论,主讲者在层层递进的讨论过程中,分六个阶段特设投票环节,助力了线下观众与现场PCCM学员的热烈讨论、各抒己见。
针对这位已因出血无法控制而继发凝血功能异常、DIC、失血性休克、多脏器功能受损的35岁女患者,直播现场专家及观众为何都说相比最终的诊断结果,应更在乎诊疗过程?在激素使用剂量、ECOM指征、改善氧合等方面,线上线下进行了哪些多角度多方面的讨论?
病情的扑朔迷离使现场专家和同行都连连称难,而王辰院士的最后点评引发了大家热烈感叹,王辰院士做了怎样透彻清晰地分析,使线下参与病例分析的医生赞叹为「大师级点评」?敬请关注。
(王辰院士点评视频可在本文末尾处查看)
35岁女性,职员,主因「四肢皮疹4月,肌无力2月,呼吸困难伴发热3天」于2017年12月21日入院。
4月前诊断为皮肌炎(Jo-1阳性),予甲强龙1000mg×3d冲击治疗2次,并口服甲氨蝶呤+环孢素+白芍总苷治疗。
激素及免疫抑制剂应用情况见下表:

2017-12-20
总结病例特点
青年女性,急性起病。基础病为皮肌炎(Jo-1阳性),大剂量激素冲击+三种免疫抑制剂治疗过程中。此次主要表现为高热、进行性加重的呼吸困难,干咳为主,RR 33次/分,口唇紫绀。实验室检查提示淋巴细胞计数极低,白细胞、中性粒细胞百分比轻度增高,PCT不高,CT表现为沿气道分布的斑片影及GGO,胸膜下不受累。头孢类抗生素治疗效果不佳。
针对免疫抑制患者合并呼吸衰竭的诊治可总结为三方面:
1、呼吸衰竭病因鉴别——此为首要任务,因为它决定了我们下一步的治疗方向;
2、呼吸支持策略的选择;
3、其他脏器功能的监测与支持。
首先,病因的鉴别应从感染和非感染两方面鉴别
感染方面除了想到常见社区获得性肺炎的致病菌外,也应考虑到机会性致病菌的可能,如PCP、CMV、曲霉菌等;非感染方面应首先除外原发病肺受累的情况,也应考虑机化性肺炎、左心功能不全、药物性肺损伤、弥漫性肺泡出血等。
至于如何鉴别,应结合临床症状及基本实验室检查判断,如患者痰性状如何,黄色、白色或者无痰,稀薄或拉丝;有无原发病加重的临床表现,如新发皮疹、关节肿痛、血尿加重、肌力下降等;此外,也应明确患者原发病的治疗情况,呼吸衰竭是发生在大剂量激素及免疫抑制剂治疗过程中,亦或是激素减量过程中也有很重要的鉴别意义。除临床症状外,一些实验室检查也非常必要,如风湿免疫相关指标:ESR、CRP、自身抗体、Kl-6、Fet、肌炎抗体谱等,免疫状态评估:免疫球蛋白+补体、淋巴细胞亚群;其中气管镜及CT在鉴别感染及非感染方面尤为重要,如无明显禁忌需尽早完成;最后,若经上述检查仍不能区分病因,可行肺活检明确。
根据上述线索我们认为此患者呼吸衰竭的主要原因为感染,可能的病原学不除外PCP、CMV、流感病毒等,因此初始抗感染治疗暂选择泰能+万古霉素+磺胺+更昔洛韦。
重要实验室检查结果回报: 血常规:WBC 11.2×10^9/L,NEUT 10.81×10^9/L ,LY 0.23×10^9/L;PCT 0.25ng/ml;淋巴细胞亚群:N 170个/μL、CD4+ 43个/μL、CD8+ 38个/μL、NK 11个/μL;气管镜镜下粘膜轻度充血水肿,可见少量白色泡沫样分泌物,BALF PCP核酸(+)、CMV核酸(+)、EBV核酸(+),余病原学均阴性,因此降级抗感染药物为头孢他啶+磺胺+更昔洛韦。
除抗感染治疗外,对于免疫抑制合并呼吸衰竭的患者而言,更重要的是纠正免疫抑制状态,包括停用免疫抑制剂,继续甲强龙40mg静点治疗原发病,另外辅以胸腺肽及丙球增强细胞及体液免疫。
下一步将讨论呼吸支持策略选择
患者入ICU时的通气、氧合情况:T 39.4℃,HR 126次/分,RR 33次/分,BP 126/71mmHg,SpO2(面罩10L/min)60%。查体:神清,有自主咳嗽能力,痰量不多;喘憋貌,口唇发绀,言语不成句,张口呼吸,双肺背部可闻及细湿啰音,呼气末可闻及少许干啰音。氧合指数(PFR)约105mmHg。胸片提示双肺弥漫性渗出影。处理措施:1、降低氧耗,具体措施包括冰毯、吲哚美辛栓、赖氨匹林降温,艾司洛尔持续泵入控制心室率,丙泊酚+右美托咪定持续镇静镇痛;2、选择合适的呼吸支持方式。
一、首先选择何种呼吸支持方式?
首先,继续增加面罩的氧流量并无提高吸氧浓度的作用,且此种吸氧方式不利于气道的温湿化,因此不选用。经鼻高流量与NPPV在轻中度ARDS中的应用指征存在较大重叠,HFNC气道温湿化效果较好,且呼气末存在一定水平正压,约5~6mmHg,但此患者呼吸频率快,张口呼吸明显,因此呼气末正压效果可能被削弱;此外,患者PFR仅105mmHg,临床评估偏重,因此我们并未将HFNC作为首选。至于IPPV,在免疫抑制合并呼吸衰竭患者中,IPPV存活率低,仅6.7%~50%,因此并不作为首选,一般是在优化NPPV设置且无效的基础上才考虑使用。ECMO为终极呼吸支持手段,其经济负担重,并发症较多,一般是作为传统机械通气及补救性通气策略无效的前提下才考虑应用。因此对于此患者,考虑到其基础免疫抑制状态,氧合水平、神志、咳嗽咳痰能力的评估,首先选用NPPV,选用S/T模式。
NPPV试用1小时后,患者胸腹矛盾呼吸及辅助呼吸肌参与的情况并未改善,RR 35~44次/分,SpO2 85%~91%,复查血气(FiO2 1.0): pH 7.35,PaCO2 45mmHg,PaO2 68mmHg,HCO3- 23.4mmol/L,lac 1.7mmol/L。试用2小时后上述情况进一步恶化,复查血气:pH 7.28,PaCO2 57.8mmHg,PaO2 33mmHg,HCO3- 26.1mmol/L,lac 2.8mmol/L。
对于I型呼衰NPPV失败会增加低氧所致的呼吸心跳骤停风险,进而增加病死率,因此NPPV失败后我们立即转换为IPPV。IPPV参数设置:PC 16cmH2O,PEEP 10cmH2O,RR 20次/分,FiO2 1.0,监测HR 121次/分,RR 20次/分(无自主呼吸),BP 88/40mmHg,插管后15min复查ABG,PFR仅53mmHg,仍存在持续低氧血症。
二、针对ARDS的持续低氧,如何处理?
我们的选择包括:增加PEEP水平、肺复张(RM),其目的均为肺泡开放,并维持肺泡开放状态从而改善氧合;俯卧位通气通气(PPV)可改善V/Q,对于具有重力依赖区分布的病变效果好,并有改善痰液引流的作用,此患者病变分布并非典型的重力依赖表现,且存在一定程度的循环不稳定,需要应用NE维持血压;另外患者腹胀较明显,PPV可能降低胸壁及呼吸系统顺应性;至于高频震荡通气(HFOV),用于此类患者可改善氧合并且降低气压伤风险,但HFOV存在的最大问题即痰液引流;因PCP、CMV治疗疗程较长,后期可能合并其他感染可能性,此时HFOV无法行痰液引流。此时由于RM等补救性通气策略暂未应用,且免疫抑制患者ECMO后血流感染风险大,因此暂不积极考虑ECMO。
我们选择行RM,PEEP 30cmH2O,PC 10cmH2O,持续2min后,以氧合导向的PEEP滴定法选择合适的PEEP,最终滴定至14cmH2O,SpO2可维持于90~92%,复查ABG较前明显改善(PFR 83mmHg)。
RM后4小时,患者SpO2再次下降,SpO2 92%→80~85%,RR较前增快,30~40次/分,无明显人机对抗,PFR降至67mmHg。
三、下一步是否行ECMO支持:
因考虑到重度ARDS早期肌松剂可能降低病死率,我们加深镇静镇痛,并加用肌松剂,但氧合改善不明显。因PCP气压伤风险高,目前PEEP水平较高,为防止气压伤,我们并未再次RM或增高PEEP,PPV对非重力依赖区病变的氧合改善有限,HFOV存在痰液引流障碍,因此最终直接选择VV-ECMO支持。
关于免疫抑制患者ECMO支持的循证医学依据,有研究显示此类患者远期预后欠佳,6月存活率9.1%~40.7%,最重要的死亡原因为感染,包括肺部感染、导管相关性感染约占77%。因此,对于此类患者,在无原发病加重证据,传统机械通气策略无效时可选用ECMO。
ECMO后机械通气参数设置应采用「肺休息」及「防止肺泡塌陷」的策略,降低PC、FiO2、RR水平,维持适当高水平PEEP防止肺泡塌陷。
四、是否行清醒ECMO?
患者ECMO支持过程中,患者出现VAP及VILI(纵隔气肿),因此我们考虑是否可行清醒ECMO,拔除气管插管并去除正压支持,此外此患者神志清,配合好,咳嗽、咳痰能力尚可,此时ECMO运行正常,因此我们在ECMO支持后第16天拔除气管插管(2018-1-8),复查CT(2018-1-9)提示双肺大面积实变影。因肺部病变未好转,继续ECMO治疗等待肺组织修复。
第三,我们简要讨论了关于SOP的诊断和治疗
2018年1月29日患者感染控制好,原发病改善,再次复查CT提示双肺仍有较大面积实变影合并牵拉性支气管扩张,双肺听诊爆裂音,不除外SOP,因此予甲强龙120mg静点5天,继之以40mg维持。8天后(2018-2-5)复查CT实变影较前明显吸收。
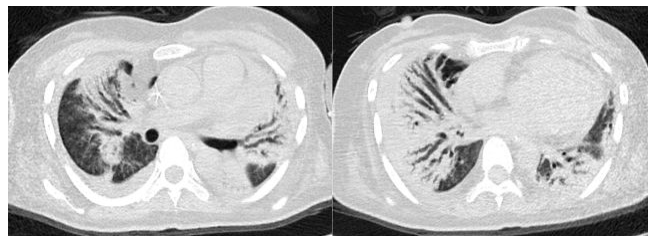
(2018-01-29)
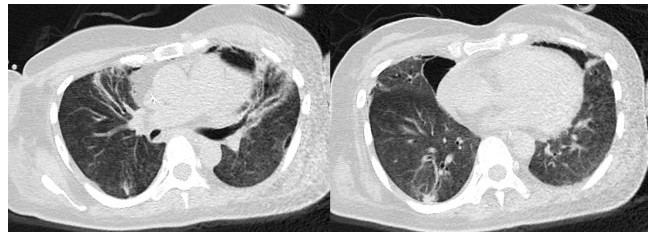
(2018-02-05)
2018年2月8日起夹闭ECMO气源,评估是否可撤离ECMO。28小时后复查血气分析:pH 7.46,PaCO2 41.9mmHg,PaO2 110mmHg,HCO3- 29.6mmol/L,Lac 2.5mmol/L,基本可考虑撤离ECMO。但因存在纵隔气肿,为使肺脏继续休息,加快气压伤吸收,继续ECMO支持。
最后,我们讨论患者死亡原因
我们认为患者最终因弥漫性肺泡出血(DAH)死亡,虽然各位学员对DAH诊断存在疑问,认为仍需完善尿常规、含铁血黄素、补体等其他检查明确,但我们仍按DAH处理,除停用肝素抗凝,予鱼精蛋白中和,升级抗生素,对症输血、补充凝血因子外,予甲强龙120mg治疗。但患者最终因出血无法控制继发凝血功能异常、DIC、失血性休克、多脏器功能受损去世。考虑出血原因,也应分为感染及非感染,非感染因素首先根据凝血指标除外了抗凝过度;出血前用药简单,药物相关因素也不予考虑;此外皮肌炎引起DAH的报道较少;分析出血前后感染指标变化,WBC、PCT均有升高,虽无病原学依据,不除外感染加重导致DAH可能性。
大咖发言总结
● 谢晟主任医师分析影像学表现:
影像学有助于区分感染与非感染性疾病。此患者的特点表现为中心型GGO分布,小叶中心型结节、小叶间隔增厚,均为PCP、CMV的典型特点,因此倾向于感染。另外,间质性肺疾病胸膜下不受累的情况少见,仅有少部分机化性肺炎及AIP可出现实变及胸膜下不受累的情况,而上述类型在皮肌炎肺间质受累的表现中较为少见。
● 卢昕主任医师针对原发病肺受累及感染进行了鉴别:
此患者为Jo-1阳性皮肌炎,此类型皮肌炎对激素敏感,很少出现在激素治疗过程中加重的情况,但减量过程中易复发;此外,因影像学胸膜下不受累,而表现为弥漫GGO及斑片影;因此考虑原发病累及肺间质的可能性不大。针对基础存在风湿免疫病应用激素+免疫抑制剂后合并肺部感染的患者,基本原则是在判断原发病非活动的前提下将激素+免疫抑制剂减量。此患者应用的三种免疫抑制剂均为非细胞毒性药物,此患者免疫抑制状态实则为大剂量激素冲击造成,因此对于此患者最为重要的治疗时减少激素用量,从而改善免疫抑制状态。
● 代华平主任医师对肺泡出血的原因进行了分析:
肺泡出血原因尚不不清除,凝血功能基本在目标范围,不能用抗凝过度解释;有无皮肌炎本身导致的肺损伤或皮肌炎累及肺小血管,及正压通气导致的肺损伤,及有无其他脏器功能障碍,如心功能不全导致的肥胖水肿、出血的表现均可能作为肺泡出血可能的原因。代老师也提出,此患者为免疫抑制患者,前期无创支持是否可通过优化参数设置等方式继续应用无创,从而避免后期IPPV造成的呼吸机相关性肺损伤及VAP也非常值得探讨。
王辰院士总结性发言
1、肺部阴影的原因分析: 皮肌炎的肺内表现?单纯感染?皮肌炎合并肺部感染?根据发病过程、重度的疫抑制状态、症状、较为典型的影像学表现,后期病原学证实,应为感染为主,病原学推测可能为PCP、CMV、EBV或其他病毒感染,也不除外非典型病原体等混合感染。但也不能完全除外实变影的背景下隐藏的间质改变,但胸膜下不受累在间质性肺疾病中较少见。
2、呼吸支持技术的选择: 重度免疫抑制患者,神志清楚、气道保护能力好,因此同意首选无创。但当患者神志差,痰量明显增加时需要及时转化为有创,但对于如此重度免疫抑制患者使用有创需要慎之又慎,因为多项研究证实,IPPV合并VAP会增加病死率。此病人ECMO指征偏晚,若早期可能会避免IPPV,虽然ECMO可能合并血流感染,但血流感染较VAP来说容易避免。因此王院长建议充分应用NPPV,若因病情中氧合仍无法维持,可在NPPV的基础上加用ECMO支持。若患者已经插管,此时应注意呼吸机参数的精细化设置,注重参数条件的细节,如选择自主呼吸/控制通气模式如何选择,吸气流速、触发灵密度如何设置;对于镇静镇痛肌松在此类患者中的应用指征及实施也应明确及规范;此外,IPPV还应注重气道管理,应用集束化措施预防VAP。关于RM,此患者的影像学类似于PAP表现,而非典型ARDS表现,因此RM效果存疑;至于PPV适用于病变符合重力依赖区分布的患者。ECMO后IPPV参数设置问题:压力和容量如何平衡才能保证肺休息,又保证肺泡不塌陷,具体措施包括控制压力水平、下调FiO 2
(0.6以下) 及RR,但也应维持一定的容量,防止肺泡塌陷。VAP的防控应贯穿气管插管始终,动态监测体温、白细胞、PCT、病原学,尤其是新发病毒感染。
3、关于感染继发SOP的问题,我们也应有高度的重视,除了抗感染治疗无效,影像学提示实变伴牵拉性支扩外,最重要的体征为爆裂音,爆裂音可作为一诊断依据。至于激素的用量也应根据患者基础免疫抑制状态、病程长短选择,对于此患者不宜应用过大剂量,同意目前剂量(甲强龙120mg*3d),且疗程可能不宜过长。激素治疗过程中注意密切监测淋巴细胞计数,而有时候即便淋巴细胞计数正常,也不能除外淋巴细胞功能异常导致免疫抑制的情况。
4、弥漫性肺泡出血的原因: 最多见的为病毒感染,有无免疫抑制基础上潜在感染复燃的可能性,如CMV、流感病毒或其他病毒,因此应动态监测病毒核酸,甚至病毒载量。若尸检成功或穿刺进行肺组织病原检测为更为有利的依据。
最后,王辰院士再次肯定了PCCM病例讨论的形式,让我们学会有思维、有根据的分析病情,指导治疗,而非跟着感觉走,一切都应有proof of concept 或data/evidence based的意识。呼吸病与危重症均需全面掌握,呼吸科医师为掌握最全面的内科医师,两条腿走路才能对病人进行更好地救治及照护。
王辰院士点评视频请戳:
建议在Wi-Fi环境下观看
作者介绍

点击文末「阅读原文」可回看本次直播


