小细胞肺癌的治疗在过去十几年的发展历程中很受局限,大多数患者一旦确诊,约70%已发展为广泛期,治疗上唯有以全身化疗为主。小细胞肺癌广泛期涉及远处转移,初诊就发现有脑转移、肝转移的不在少数,一旦出现转移后,患者生存期更短(尤以肝转移为甚)。有些患者对药物使用不同程度受限(源于肝酶关系)。对于一诊为小细胞肺癌广泛期的患者,无论患者亦或是医生,都会感到失望,因为这些患者没有办法从手术中获益。因此,小细胞肺癌往往在诊断之初就足以使医患双方陷入困境。对于这部分患者,如果年龄尚算年轻,身体基本状况尚算良好,我们仍坚持要进行化疗,以观后效。

小细胞肺癌往往在诊断之初就足以使医患双方陷入困境……他的OS仅约11个月,对这种病例医生常常感到十分无奈
小细胞肺癌在广泛期尽管ORR颇高,用一线EC或EP方案可获取较好的缓解率,甚至有的可达到CR、PR,但这种效果十分短暂。如:用依托泊苷+卡铂治疗,患者3周以后(20天左右)复查,发现病灶有大范围缩小,此时患者及其家属会「欢呼雀跃,对医生千感万谢」,实际上,医生心里很「悲凉」。因为大家非常清楚它太容易复发。有些患者不到3个月病情就复发,一旦复发二线治疗效果极差。
对于这些患者,在治疗药物上可选择的按照指南上推荐有拓扑替康,它放在二线治疗ORR实际上只有百分之二十左右。但由于它能够改善患者生活质量,相对于喉返神经受累的声音沙哑,以及吞咽困难,均有一定作用,因此FDA才批准它用于二线治疗。
由于拓扑替康不可及,我们临床上基本用伊立替康。伊立替康具有「顽固腹泻」的副作用,应当查基因型,查明患者是否属于容易出现腹泻的类型。其他的二线方案,如:紫杉醇;目前的新剂型白蛋白结合型紫杉醇;氨柔比星,这些都是可选方案。但这些方案治疗ORR占比也只有百分之二三十左右。
以上就是小细胞肺癌在广泛期治疗上面临的一种困境。一旦一线复发之后,二线治疗的这几个药效果都并不好,总体OS超不过1年。
临床中我们遇到的病例,对于那些缓解率特别好的,治疗6个周期后病灶已经回缩得很小的,对一些很年轻的患者、全身没有远处转移灶,或者有远处转移灶但控制得不错的,这时就需要做局部巩固治疗,如胸部放疗。先分享几个病例:
病例1
该患者系黑龙江籍一位38岁男性患者,患者为「现代农民」身份,是家中主要劳动力。患者原本身体非常结实,因腹痛就医。考虑到患者平时喜欢喝酒、吃烤肉串,胰酶检测结果偏高,当地医院判断其有胰腺炎的可能性,遂按照胰腺炎,用奥曲肽和PPI等抑酸药治疗。效果不好,胰酶下降不明显。在当地进一步做腹部CT扫描,发现膈肌顶部位置有一部分胸腔有占位,遂做胸部CT,发现中央型肺癌。
患者于2019年1月来到北京,进入我院治疗。首先用气管镜活检,结合其已有胰腺转移,且有多发骨转移,诊断为广泛期小细胞肺癌。用EC方案进行化疗。化疗时患者的胰酶、血淀粉酶、尿淀粉酶均偏高,但一般状况良好,考虑三项指标偏高为胰腺转移造成,化疗后胰酶恢复正常。治疗1个周期后原发病灶明显缩小,6个周期后患者副反应不重。
由于患者体质较壮实,加之我们加用过止吐药,按照化药的恶心、呕吐指南原则处理,整个化疗过程非常顺利。复查胰腺时做了全身PET-CT,胰腺没有高摄取,说明胰腺病灶缓解得非常好,几乎没有残留,只在胸部残留一点病灶,遂进行胸部巩固放疗。
放疗做完接近3个月的时间,患者称腹部疼痛。直接查B超,发现胰腺肿瘤标志物又超高。打个比方:患者第一次入院时ProGRP>5000,出院时(6个化疗完成)全部恢复正常,符合前面所讲的「小细胞肺癌对EC、EP方案特别敏感,有些甚至能够达到CR、PR」。该患者在前期出院时已达到PR,后续又进行积极治疗。但一线化疗完成之后他又复发了,他这种情况就属于「难治性小细胞肺癌」。这样的病例对于医生而言感到非常无奈。
往往这种再次复发的患者,就像身体打开了「多米诺骨牌」的开关,进展相当迅速,包括全身疼痛感、腹水、颈部淋巴结转移……PS评分3分,后期只能卧床,生命力急剧下降。由于患者年轻,我们给他进行了二线化疗,用紫杉醇。因为患者前期治疗花费巨大,家中失去主要劳动力,经济十分困难,患者及其家属只能选择紫杉醇这种比较便宜的方案。打伊立替康无效,换紫杉醇似乎有效,但1个疗程后照样进展,肿瘤标志物明确。最后,患者只能选择回家,在当地医院进行「对症支持治疗」。患者整个OS仅约11个月。患者于2019年11月回家,未能挺过12月。
这样的病例不仅对患者家属打击大,对医生的打击同样大。医生的无奈可能更早,因为医生更清楚地知道广泛期小细胞肺癌的预后较差。
她的上腔静脉压迫综合征非常厉害,脸肿、头胀,只能在脚上输液……一旦出现有症状脑转移生存期非常短
病例2
该患者是一名50岁女性,诊断广泛期小细胞肺癌。她的上腔静脉压迫综合征非常厉害,脸肿、头胀,化疗之后,上腔静脉被包得死死的,只能在脚上输液。化疗几次之后效果很好,颈部淋巴结目测就能看见在明显缩小。复查CT,纵膈淋巴结也明显缩小。由于这种患者的病灶存在对大血管的压迫,她容易长血栓,因此治疗上还要用小剂量低分子肝素抗凝。患者前期治疗效果非常好,行动无异于正常健康人,甚至还能帮忙照顾自己女儿。化疗6个周期之后,几乎胸部病灶已经观察不到。考虑其尚算年轻,进行全面复查后,我们建议她做「预防性脑照射」。
局限期小细胞肺癌患者做预防性脑照射是非常推荐的,但对于广泛期小细胞肺癌患者而言,假如胸部病灶缓解得非常好,全身远处无转移,医生也会建议患者做脑照射。
这名患者平日喜爱斗地主、打麻将等娱乐活动,称自己在网上查过信息说「做了脑照射人会变傻」,坚持不做脑照射。后来我们只能通过微信、电话联系,反复叮嘱患者在当地复查,做头颅增强核磁。基本上每2个月嘱咐其做一次。而患者在之后第4个月时,出现步态不稳症状,我们考虑有脑转移,患者再来我院就医,观察到面部鼻唇沟明显变浅,流涎,讲话口齿不清,单侧肢体肌力差,需要旁人扶。后患者做了全脑放疗,状况有所改善。但是,一旦出现这种有症状脑转移的患者,生存期很短。所以这就是小细胞肺癌的局限性,一线治疗效果非常好,但很容易复发。该患者最后也只能进行维持治疗。
即便就算当初她谨遵医嘱,按照我们的建议进行了预防性脑照射,只能说可能不会进展、复发得那么快,也不会太乐观。广泛期小细胞肺癌就是恶性度高、进展快,随时可能在别处又转移,这就是它的特点。
他做完「预防性脑照射」半年后四肢乏力,查出脊膜转移……转移病灶致膈神经受累,又累及膈肌运动导致肺不张,最后连化疗都打不了
病例3
该患者为50多岁男性,诊断为局限期小细胞肺癌。
他有长期吸烟史,性格内向,我们判断可能因为他的一个外孙出生就有肌无力的遗传病,从小只能被抱着,在轮椅上生活,自打有这个外孙后他就更内向,不爱讲话,精神层面压力巨大,导致抽更多的烟,免疫抑制。
患者进行了同步放化疗,也按照要求做了预防性脑照射,定期随诊观察。每过2个月查一次胸部CT或增强CT,包括头颅增强核磁,再隔2个月做一次B超。大概在患者脑照射完成近1年时,其儿子打电话称他出现乏力症状,患者自感四肢均乏力,胳膊、腿都要靠人扶,描述「两个胳膊和腿似乎就像在身上挂着,且乏力越来越厉害」,患者还出现小便困难,遂来我院住院检查。
实际上患者已在当地医院做了两次头颅核磁,起初怀疑有脑转移,但增强头颅核磁未见脑转移灶。随着后来症状的逐渐加重,患者肚脐以下感觉消失。我们给患者做了颈椎、胸椎、腰椎核磁,发现脊膜上有些地方好像有很小的结节。一度怀疑患者是否有小细胞肺癌抗体介导的副肿瘤综合征,如:Hu Ri Yo,包括Lambet-Eaton综合征,这些都有肌无力的表现。还做了腰穿,脑积液、血液里都查了Hu Ri Yo,全部正常。只在脑积液里可见核异质细胞,这是在协和医院查的,且脑积液里的细胞分类是淋巴细胞为主,占90%。因此,结合患者颈椎、胸椎、腰椎核磁,怀疑他有脊膜转移。
对患者采取了积极的治疗,再次用依托泊苷和卡铂化疗,对于他来讲这两个药是可行的。再后来,我们要给他打化疗的时候,他表示「总感觉呼吸困难」,并且患者突然间发烧。听诊发现右下肺呼吸音低,照床旁胸片发现右下肺不张,做床旁气管镜,发现有很多痰。
其实,病人在来我院复查时,胸部并没有病灶,没有明显进展。但是什么原因造成右下肺不张呢?因为患者有二便失禁,我们考虑由于颈椎脊膜上有结节,是否损伤了膈神经,导致神经受累,累及膈肌运动。之后对患者做了B超,发现患者右侧膈肌根本不动。因此,患者的肺张不开,有痰堵住,即便是发烧也打不了化疗。最后患者只能回家,其家属对我们说,「好在我们终于知道是什么原因了才出现这一系列症状的」。患者回家后住当地医院ICU勉强维持治疗,于去年年底去世。
这3个病例告诉我们,小细胞肺癌是一个复杂的病,各方面因素无法预期和确定,医生往往是治得了胸,治不了脑,治得了脑,治不了远处转移、骨转移。小细胞肺癌在我们眼里就像一个「恶」魔,总结它的特点就是:恶性度高、复发转移快,一线ORR虽然好,但OS不长。它就像「一锤子买卖」,并且这「一锤子买卖」还经常做不好。因此,医生大多对小细胞肺癌感到无奈,在临床上也特别不爱讲小细胞肺癌的患者。
小细胞肺癌对EP、EC方案非常有效,但之后非常容易选择出一个突破口,肿瘤又沿着这个方向去增殖……近几十年来化疗药上、靶向治疗上并无突破
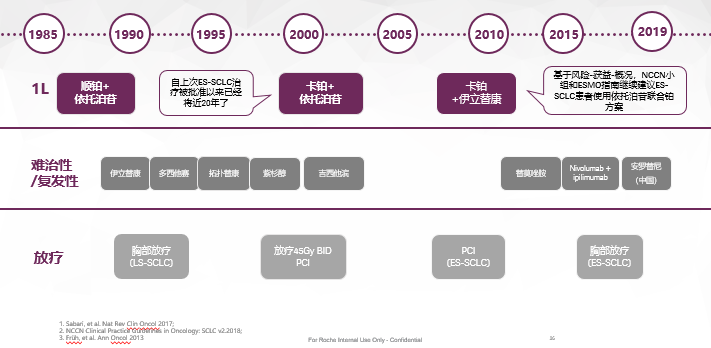
对于小细胞肺癌的患者的治疗探索中,小细胞肺癌很容易耐药,比如:它对EP、EC方案非常有效,之后非常容易选择出一个突破口,肿瘤又沿着这个方向去增殖,它还可以长。
小细胞肺癌这几十年大概有40多项临床实验,涉及了60多种药物,几乎就没什么进展,最后变成了广泛期的化疗,以全身治疗为主。如果能达到CR或者是PR的在一线治疗中,患者又比较年轻,可以加上脑预放;如果胸部病灶达到大的PR,患者又比较年轻,全身没有转移。那么,我们可以做胸部的一个巩固治疗,但也就仅此而已。我们在化疗药上并没有更多的突破,如氨柔比星这些所谓新的在小细胞肺癌的药物,也没有突飞猛进的进展。并且关键是没有能阻止它耐药的药物,患者不能够有长生存的获益,因此就不能写进指南。
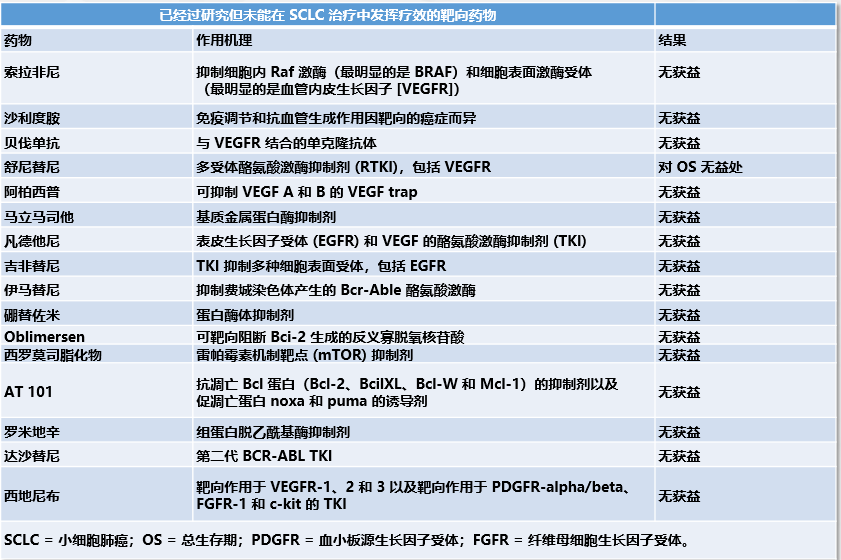
小细胞肺癌在靶向治疗方面是没有突破的,从基因来讲,它就是TP53抑癌基因,它还有突变,还有RB1,基本没有药物,即便靶向药也不行。像PARP抑制剂,虽说它在机理上,有些小细胞肺癌PARP抑制剂可能有效,然而在大规模临床实验中,可能它不容易取得效果。

美国国家癌症局将SCLC定义为「顽固性、高度侵袭性肿瘤」, 疗效上的微小突破可带来巨大临床获益,都有可能被认定为突破性疗法。
年长的老师常说「以前和肺癌患者做不到1年的朋友」……非小细胞肺癌OS能「跨年」,而小细胞肺癌在一线用EC方案加阿替利珠单抗首次OS突破1年,意义更为重大
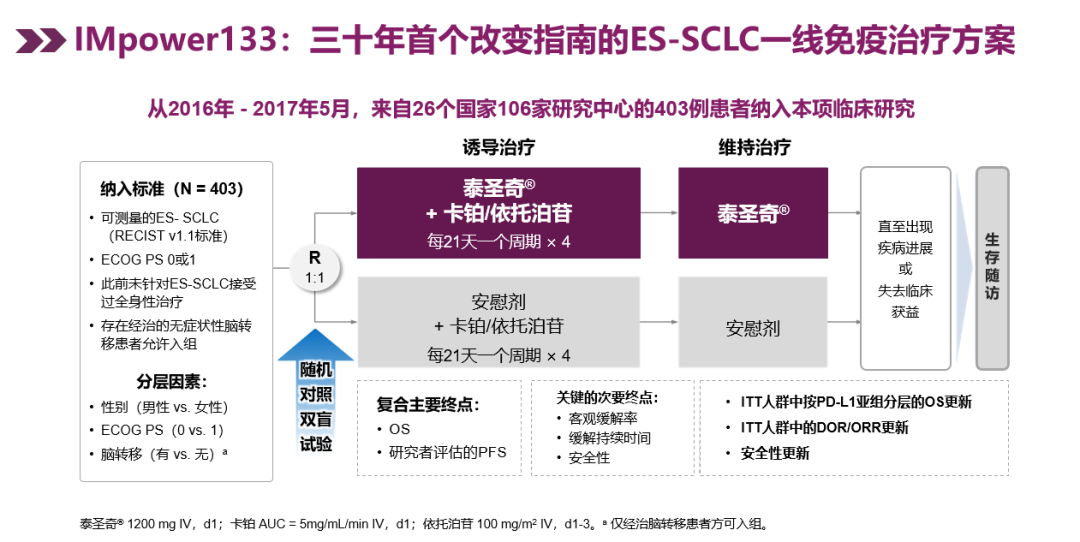
我们说小细胞肺癌进入免疫治疗新时代,这又被视为是一个重大突破。为什么这么说?IMpower133研究,这种全球、多中心、安慰剂,双盲对照的研究取得PFS和OS的双阳性结果,是第一个取得双阳性结果的研究,这的确是一个「突破」,改变了以前小细胞肺癌只有放化疗的现状,也真正是标志着它进入了免疫治疗时代。
非小细胞肺癌中,原来拿ECOG 1594做研究,不管是多西他赛联合铂还是紫杉醇联合铂,亦或是吉西他滨联合铂,即便如此最后发现不管怎么治,晚期的非小细胞肺癌患者OS就是8个月,就是个瓶颈。而
ECOG 4599让非小细胞肺癌患者的OS突破了1年。将非小细胞肺癌分成鳞癌、腺癌,驱动基因阴性的腺癌,用培美曲塞化疗,鳞癌用吉西他滨化疗,这样的话就做到了「四驾马车」做不到的事情,这就是重大突破,非小细胞肺癌OS跨年。
一些老师经常说,「以前和肺癌的患者就做不到1年的朋友」,言下之意正如此,在没有免疫药和没有靶向药的时候,全是悲情的故事。
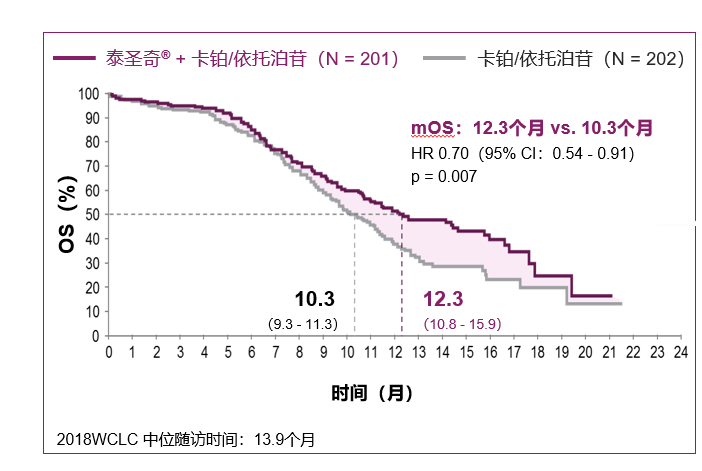
广泛期小细胞肺癌中,IMpower133研究在一线治疗时期用 EC方案加上阿替利珠单抗,4周期之后,再用阿替利珠单抗去维持,三十年来在广泛期小细胞肺癌首个OS超过一年。
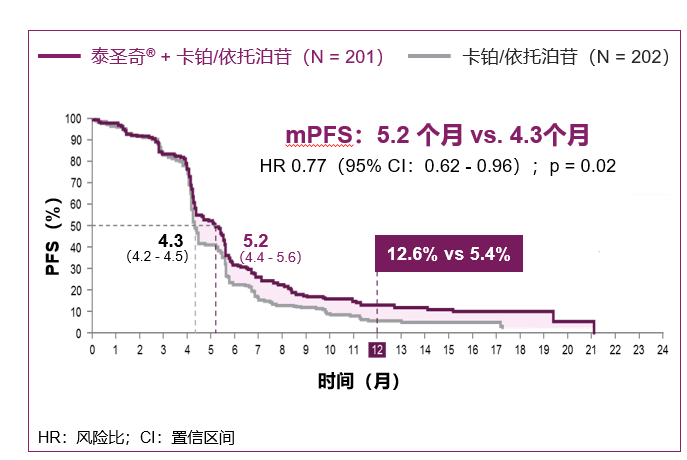
双阳性终点中的另外一个研究者评估的PFS,一年的无进展生存率实现了翻倍。
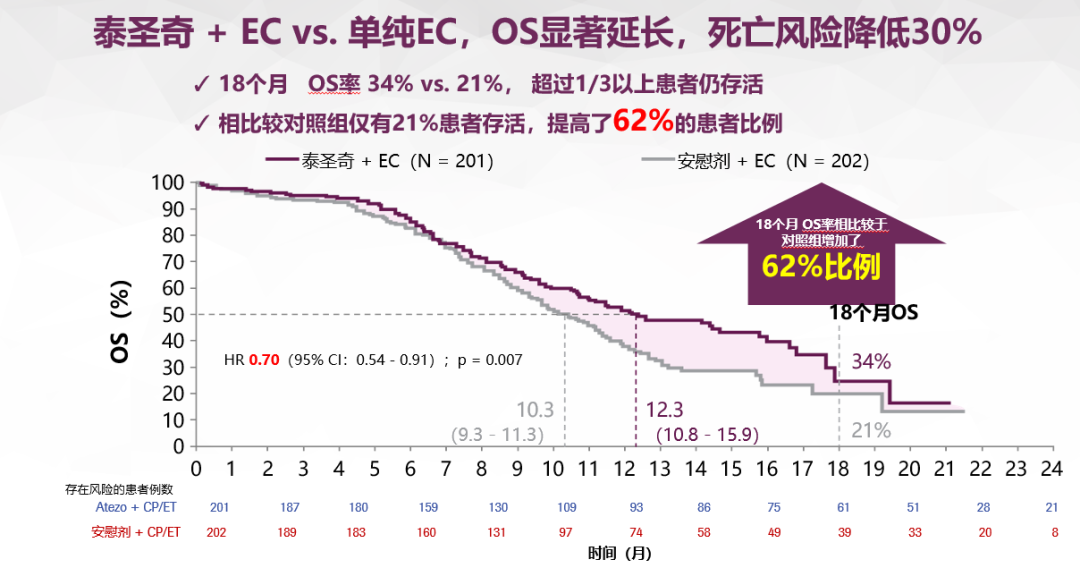
另外我们看到,18个月的时候OS率还有30%多,相当于1/3的人,在一年半的时候还活着。这是很好的效果,也符合免疫治疗我们主要看其长生存效应的结果。先延长OS,将来还有可能等来更新的治疗,有可能能够延缓患者的生存期,所以我认为意义非常重大。
对于小细胞肺癌患者一定要尽早使用免疫抑制剂,小细胞肺癌患者非常容易快速进展,首先免疫治疗,它的起效或者它的特点就是慢。所以说你把它用在维持治疗上对于小细胞肺癌这种,打了化疗还进展,那么说明肿瘤微环境更抑制。那么可能这时候你用免疫治疗,搞不好就用到二线上去了。这时候免疫治疗的效果也不好,在患者状态最好的时候,与化疗联合使用,然后维持治疗,持续改造肿瘤的微环境。
PD-L1抑制剂进入临床我会推荐,但会对患者做好免疫治疗相关的筛查,尽量避免其副作用……与PD-1相比,PD-L1的不良反应较轻
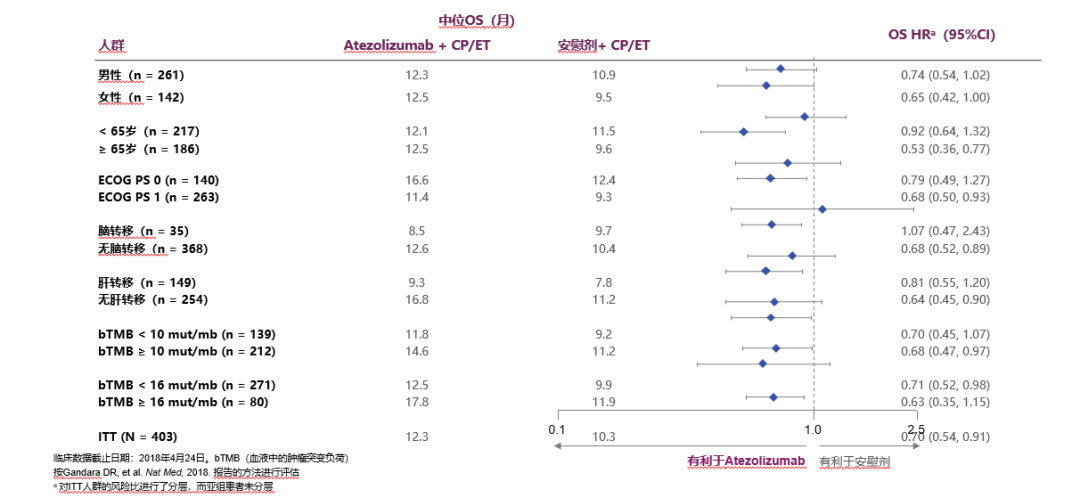
从IMpower133研究的亚组分析去看,无论患者的年纪,如果经济条件能够允许的话,我都会去给患者推荐这种治疗方式,因为这是一个重大突破。
如非肝转移的亚组的确不错,os延长了近半年,这绝对是个更大的突破了,在非小细胞肺癌里也是个难得的数据了;
但是如果说病人有肝转移,又比较年轻,我在沟通清楚不良反应之后,同样会推荐他进行免疫治疗,因为同样也可能会从免疫治疗中获益。
我们也常常遇到患者前来询问有没有更好的药物,阿替利珠单抗的PD-L1抑制剂没有在中国上市时,2018年WCLC上公布了这个结果,在欧洲、美国获批之后,就有患者前来咨询。现在的患者及其家属学习能力很强,他们基于学习各种媒体的科普知识,随时掌握新药的动态,我想他们的接受程度应该是不错的。
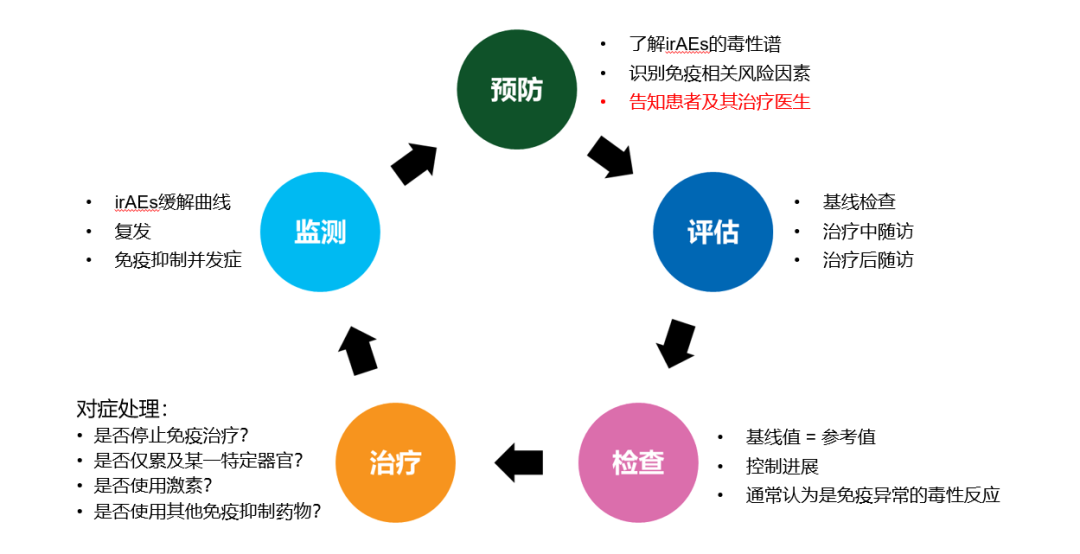
但是对于小细胞肺癌免疫治疗的人群筛选我们还要注意,这些人需要做与免疫治疗相关的筛查,这比单纯打化疗筛查项目更多一些,我可能会去关注他的自身抗体,比如甲状腺抗体,包括他的基础病,有没有冠心病、有没有心脏搭桥、有没有放支架等等,还要询问患者有没有例如银屑病、内分泌等基础病。因为免疫治疗是有一些副作用的。
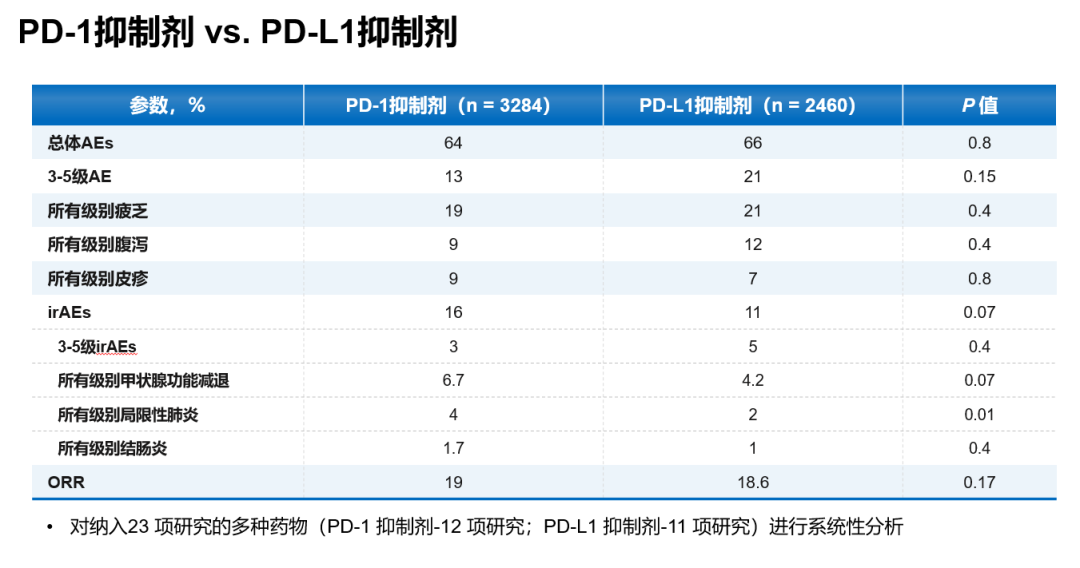
还要说明一点,阿替利珠单抗作为一个PD-L1抑制剂,它与PD-1抑制剂又有不一样的地方,它阻断的是PD-L1,但同时它还保持了PD-L2,PD-L2可以和PD-1结合,这样的话它应该保持着一定的宿主(或机体)的自稳性,因此它的不良反应我认为比PD-1的副作用会稍少一些,完全性更好一些。对PD-1治疗非小细胞肺癌的应用上我们叫安全可控,对于PD-L1可能毒性更小,基于在前面又有了1年多对于PD-1抑制剂的应用经验,我认为它的应用不会很难。
作为一名呼吸医生,我认为无论小细胞肺癌也好,非小细胞肺癌也好,它们首先都是肺癌,都发生在肺上。得肺癌这些患者大部分跟吸烟有相关,或者说跟他们由于呼吸道可吸入的有害物质造成的这种慢性疾病有关。肺癌是肺纤维化的患者合并肺癌的多,反过来看,由于吸烟的肺癌患者合并慢阻肺的多,所以呼吸科大夫在治疗上更会去关注他们呼吸道的基础疾病,比如慢阻肺,我们会更关注患者的肺功能。
以我们病房为例,无论是小细胞肺癌患者还是非小细胞肺癌患者,他们打化疗的时候,我一定会把他有没有合并慢阻肺排查清楚。有慢阻肺的按照他的ABCD分组,先给予充分的治疗,这样的话更能够让他把化疗顺利进行下来。有的病人表示打完化疗太乏力了,但有些不见得是化疗导致的,也有可能化疗后由于感冒引起的COPD,表现为乏力、呼吸困难,这与化疗药无关。在这些细节方面需要予以鉴别说明。
对于免疫治疗,那么这种新的医疗模式,可以说跟化疗完全不一样的这种治疗模式,而且又容易在肺癌患者出现肺毒性,那么呼吸科大夫一定要发挥自己的长处,比如在激素的使用上,应用糖皮质激素,仅次于免疫科大夫。比如在应用支气管镜,像支气管镜肺泡灌洗,那么非常简单的一个技术在鉴别到底是感染引起的肺炎还是肿瘤进展,都有自己的优势。
专家介绍

杨萌
中日友好医院呼吸中心肺癌病房主诊医师,日本金泽医科大学进修,日本千叶大学附属病院胸外科进修,北京肿瘤学会肺癌专业委员会委员,中国医药教育协会肿瘤化学治疗专业委员会委员,北京医学奖励基金会肺癌青委会委员,北京医学会呼吸病学分会肺癌学组委员,首医肿瘤学系肺癌青年学组委员,北京肿瘤防治研究会内镜分委会委员。


