非常高兴有机会和大家在《呼吸界》交流。大家先思考一个问题,当临床医生碰到一个病人,这个病人为什么会出现症状?这是因为机体的功能发生了改变,而功能取决于结构,所以结构改变会引起功能改变,功能改变就会出现相应的临床症状。我今天和大家交流的主题是COVID-19肺部病理改变及其对呼吸功能可能的影响。
呼吸系统的主要功能是气体交换,气体交换功能是如何完成的?
结构是功能的基础,结构改变会引起功能改变,功能改变会引起机体异常,机体异常表现出来症状和体征,这就是临床表现。
知道正常现象才可能知道异常现象,我们对一切异常的判断都是建立在与正常相比的基础之上。了解新冠肺炎会引起哪些肺部病理改变之前,先简单复习一下气管、支气管及肺部的正常组织学结构。
一、气管、支气管及肺正常组织学结构
从胸腔开始,气体的交换需要导气部和呼吸部。导气部包括气管-主支气管-叶支气管-段支气管-小支气管-细支气管(管径约1mm)-终末细支气管这七个结构,导气部负责传递空气;呼吸部包括呼吸性细支气管-肺泡管-肺泡囊-肺泡这四部分,呼吸部进行气体交换。气管和主支气管是肺外导气部,从叶支气管开始一直到终末细支气管是肺内导气部。

肺小叶(肺的单位结构)包括细支气管-终末细支气管-呼吸性细支气管-肺泡管-肺泡囊-肺泡这六种结构。小叶性肺炎是以细支气管为中心的化脓性炎症。
气管和主支气管的结构(三层)
1、黏膜层
黏膜层的成分包括两大部分:上皮:纤毛细胞、杯状细胞、基底细胞、刷细胞、小颗粒细胞;固有层:疏松结缔组织,这是取得营养支持上皮的作用。
2、黏膜下层
主要成分是疏松结缔组织,其中有气管腺。气管腺有浆液腺和黏液腺,气道需要湿润,浆液腺分泌液体;气道需要一层保护层,这个保护层就是黏液的屏障,由气管、支气管分泌的黏液细胞构成,包括腺体和黏膜层的杯状细胞分泌的黏液共同汇合在气道表面,起到一种保护的作用。
3、外膜层
外膜层有气管软骨,在气管软骨的后部有个缺口,它属于透明软骨,由疏松结缔组织和弹性纤维连接游离的透明软骨环;气管后壁软骨环缺口由弹力纤维、平滑肌连接,其中有气管腺体。
随着支气管的分支,管腔变细、变薄,三层分界逐渐不明显;环状软骨越来越不完整,变为不规则的软骨片,而平滑肌纤维逐渐增多。
显微镜下的形态
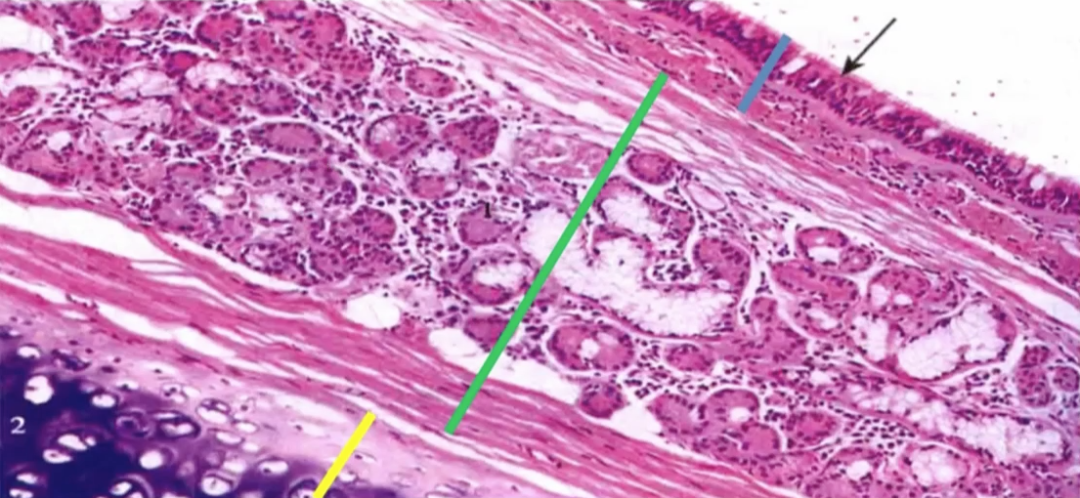
这三种结构分为三种颜色的线,蓝线是黏膜层,有黏膜的上皮和黏膜的固有层,黏膜上皮里面有五种细胞;绿线是黏膜下层,大量的管状结构和泡状结构是气管腺体,包括浆液腺和黏液腺;黄线是外膜层,左下角深蓝色的部分是气管软骨环。
黏膜层上皮放大的模式图
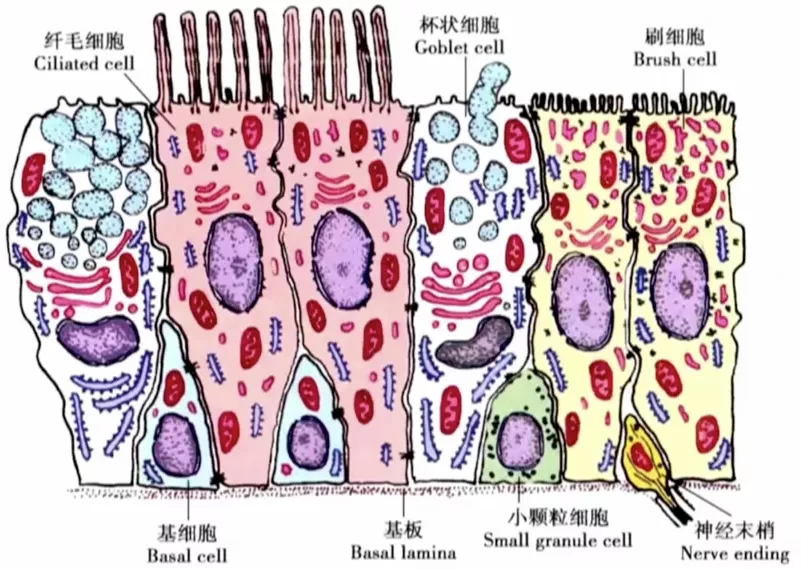
纤毛柱状上皮细胞具有清洁的作用,纤毛快速地摆动可以把气管里的黏液分泌物不停地向咽部摆动。
杯状细胞可以分泌黏液,与气管腺体分泌的黏液相互配合,在气道表面形成一层很薄的黏液保护层叫做黏液屏障。黏液屏障可以吸附我们吸入空气里面的微尘颗粒、细菌,溶解有害气体(比如空气中的二氧化硫),由纤毛柱状上皮细胞不停地摆动,把分泌的带有有害的颗粒或者有毒气体的分泌物摆向咽部,然后排出。
到目前为止,刷细胞的功能还不太清楚,有人发现它与神经末梢有接触,所以认为刷细胞可能起到感受信号传递给机体的作用。
小颗粒细胞属于神经内分泌细胞,在正常情况下,小颗粒细胞分泌激素(比如五羟色胺),它的生理作用是调节气道平滑肌的收缩功能,另外调节腺体的分泌。
在呼吸道的基底细胞是一种干细胞,纤毛柱状上皮细胞、刷细胞、杯状细胞、小颗粒细胞不停地进行新老交替,完成功能会死去,有新的细胞增生出来,基底细胞的功能就是可以变成这四种细胞的任何一种细胞,所以基底细胞被认为是干细胞。当有炎症刺激的时候,基底细胞可能不沿着正常的方向分化,有可能变成鳞状上皮,所以呼吸道的上皮受到炎症刺激以后,会发生鳞状化生,在鳞状化生的基础上可能会发生鳞状细胞癌。我们理解这些正常的情况对于判断异常情况很有帮助。
肺的呼吸部
肺的呼吸部参与气体交换,包括呼吸性细支气管-肺泡管-肺泡囊-肺泡这四种结构。
呼吸性细支气管与2~3个肺泡管相连,表面衬覆单层纤毛细胞和分泌细胞(Clara cell)。呼吸性细支气管衬覆的纤毛细胞很少,主要的细胞是分泌细胞,就像我们在临床上碰到的不典型腺瘤样增生、原位腺癌和部分腺癌是来自于分泌细胞。另外,上皮外是平滑肌和弹性纤维。
肺泡管上面是呼吸性细支气管,下面是肺泡,肺泡管与20~60个肺泡相连,表面衬覆单层立方或扁平上皮,上皮外有平滑肌和弹性纤维。
肺泡囊与肺泡管相通,是若干个肺泡的共同开口形成的囊腔,一般是几个肺泡。肺泡囊没有表面,全部都是开口,所以它没有内层上皮。
肺泡开口与呼吸性细支气管、肺泡管、肺泡囊相连,相邻肺泡之间的结缔组织称为肺泡隔,又称为肺泡壁。成人每侧肺内有3~4亿个肺泡。
要了解这些结构是因为它们对气体交换都很重要,所以说「知道正常才有可能知道异常」。
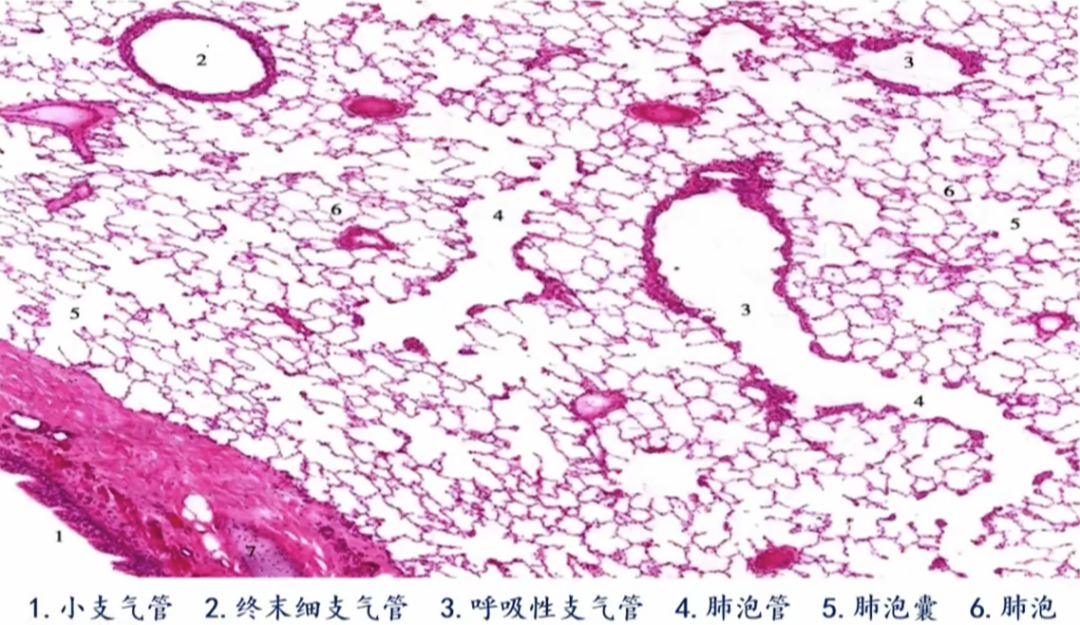
显微镜下正常的肺部结构
正常肺泡的组织学结构
肺泡内衬上皮
肺泡内有两种上皮,一种是Ⅰ型肺泡细胞,另一种是Ⅱ型肺泡细胞。
Ⅰ型肺泡细胞的功能是参与构成「气-血屏障」,是气体交换的部位。扁平状,约覆盖肺泡95%的表面积,无再生能力,损伤后由Ⅱ型肺泡细胞增殖、分化补充。
Ⅱ型肺泡细胞为立方或圆形,核圆,胞浆少,呈泡沫状,散在于Ⅰ型肺泡细胞之间;约覆盖肺泡5%的表面积。分泌表面活性物质,调节肺泡表面张力。有分裂、增殖并分化为Ⅰ型肺泡细胞的潜能。
注意:Ⅰ型肺泡细胞具有气体交换的能力,Ⅱ型肺泡细胞不具有气体交换的功能;Ⅰ型肺泡细胞无再生能力,Ⅱ型肺泡细胞有再生能力。如果Ⅰ型肺泡细胞损伤,由Ⅱ型肺泡细胞覆盖原来Ⅰ型肺泡细胞的地方,从而丧失气体交换的功能。所以,了解正常的结构非常重要。
肺泡隔
是指相邻肺泡间薄层结缔组织,内有连续的毛细血管网和丰富的弹性纤维,毛细血管网和肺泡壁相贴。薄层结缔组织和毛细血管是两种重要的成分,这两种成分参与气体交换,一旦损伤,会影响气体交换的功能。
肺泡孔
是相邻肺泡间气体流通的小孔;1个肺泡壁上有1个或数个肺泡孔。
气-血屏障
通过6层结构进行气体交换:肺泡表面液体-Ⅰ型肺泡细胞与基底膜-薄层结缔组织-毛细血管基底膜-连续内皮细胞。如果这些结构破坏会影响气体交换的功能。
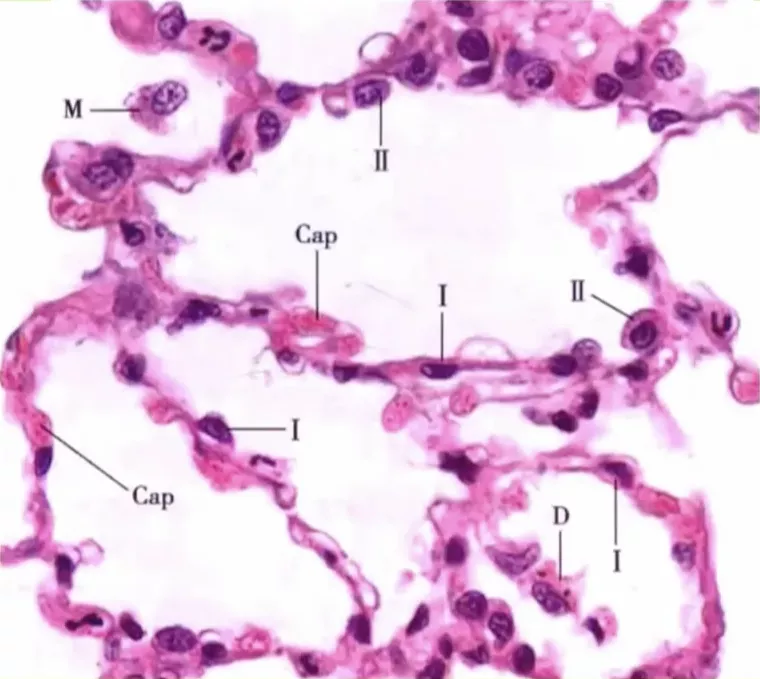
肺泡在显微镜下放大的图像
Ⅱ型肺泡细胞呈立方状,Ⅰ型肺泡细胞呈扁平状,肺泡隔里面有毛细血管,无法看清薄层结缔组织,因为太薄了,即使在显微镜下放大400倍,也看不清楚。
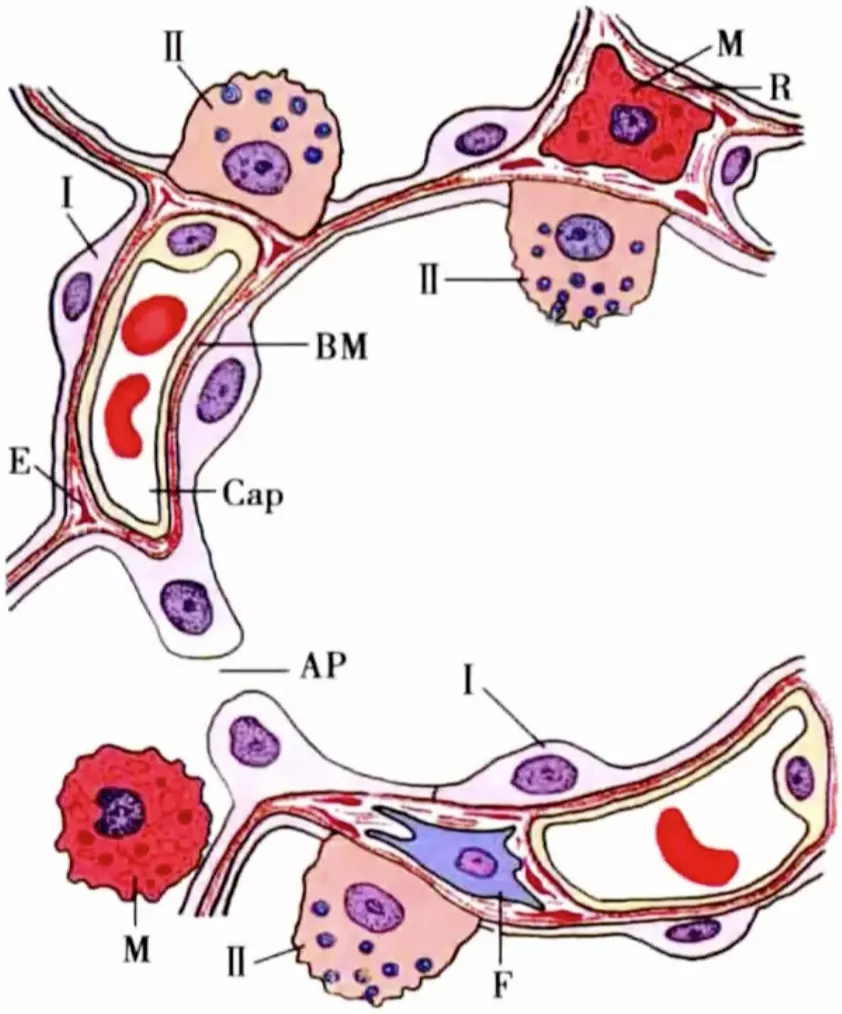
肺泡的模式图
二、COVID-19病理变化
今天的话题主要围绕COVID-19这种传染病,我认为我们要从四方面认识传染病。第一,是什么病原微生物引起的疾病?即病原体;第二,病原体是如何进入人体的?即传播途径;第三,病原体进入人体后发生什么?即发病机制及病理变化;第四,患了该病后的结局如何?即转归(预后)。
新冠肺炎的病原体是冠状病毒;传播途径主要为呼吸道,也可以通过消化道传播;对发病机制了解甚微,不太清楚;新冠肺炎的感染属于病原微生物的感染,病原微生物的感染引起的病理变化是炎症,炎症的病理变化包括渗出、变质、增生,但是新冠肺炎引起的炎症与普通性病原微生物引起的炎症不同;对于转归(预后),临床医生更加了解,不再多说。
刚开始大家都不知道新冠肺炎能够引起肺部以及身体其他部位怎样的病理变化,为了更加了解新冠肺炎,在国家卫健委的组织下决定对新冠肺炎尸体解剖。我们医院(上海交通大学医学院附属瑞金医院)有幸参与新冠肺炎的尸体解剖,在2月16日下午3点左右接到通知,2月17日8点乘坐高铁出发去武汉。下图是我们在2月17日在上海站出发时拍摄的照片,整个车厢里边没有其他人,只有我们六位医生和列车的工作人员,其中有三位是瑞金医院病理科的医生,有一位是瑞金医院 B超室的医生,还有两位是上海交通大学医学院病理学教研室的老师。

到达武汉以后,我们和卞修武院士的团队回合,共同开展新冠肺炎的尸体解剖工作。汇合以后,我们重温入党誓言,要把光荣的任务完成好。

接下来我介绍的工作都是我们的团队和卞修武院士的团队共同完成,这是团队的劳动成果。

我们一共做了二十几例的尸体解剖,在解剖之前,要对遗体默哀片刻,表示对死者的尊重和感谢,以及对死者家属的感谢。
COVID-19肺部病理改变
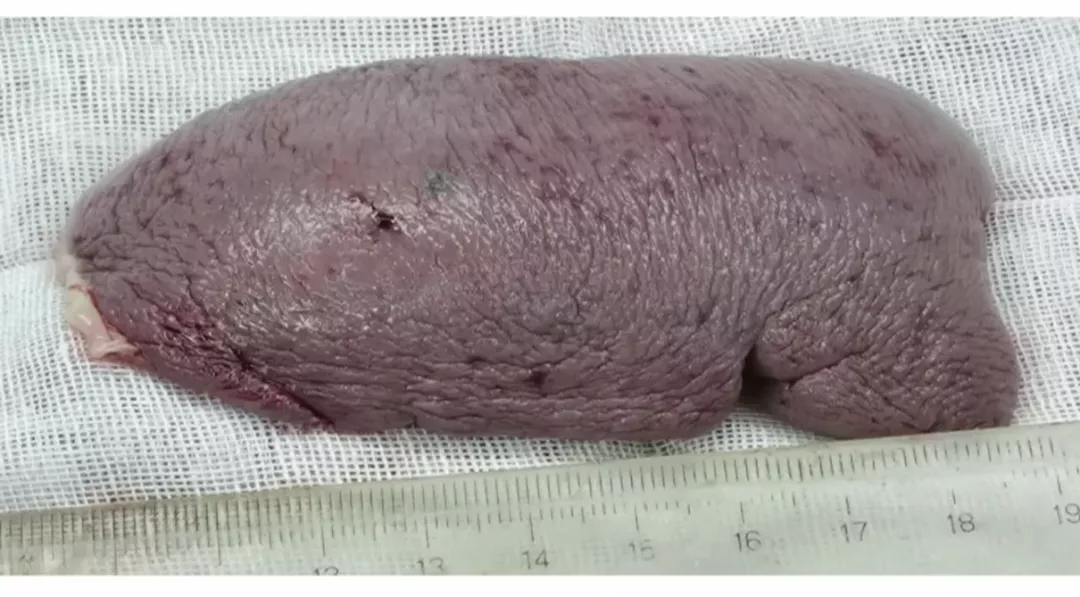
大部分新冠肺炎尸体解剖所取出的肺像脾脏,看起来不像肺,脏层胸膜是皱缩的,表面胸膜的皱缩应该是肺组织的萎缩。
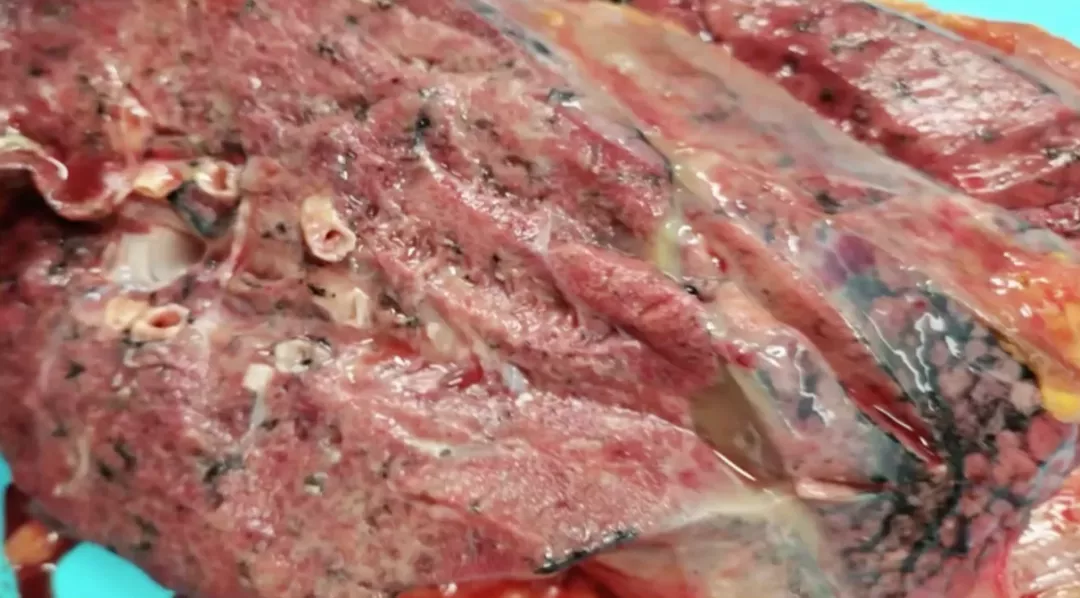
切开肺部以后,发现颜色和正常的肺有所不同,有点苍白,而正常的肺是褐色的。肺部发白的原因是结构发生了变化,在显微镜下可以看到纤维组织增生。
光镜所见
在光学显微镜下制成病理切片,病理切片样的形态是什么样?下图是我在带着大家一起看显微镜下的病理改变的照片。

COVID-19肺部病理变化包括哪些?
渗出包括这几方面:肺泡腔内多量巨噬细胞渗出、浆液性和浆液纤维素性渗出,肺泡腔面可有透明膜形成;可伴有肺泡腔内出血。
变质指炎症局部组织发生变性和坏死,对于新冠肺炎而言,会发生肺泡弥漫性毁损,肺泡上皮损伤,支气管上皮损伤。变质属于损伤,哪里有损伤,哪里就有修复,增生用来修复。
增生包括这几方面:Ⅱ型肺泡上皮不同程度增生,因为Ⅰ型肺泡上皮损伤以后没有再生能力,需要Ⅱ型肺泡上皮来修复;纤维组织增生,肺内的结构就会发生明显改变,纤维组织增生包括肺泡内纤维组织增生(肺泡肉质变)、肺泡壁内纤维组织增生(肺泡壁增宽)、肺组织纤维化(肺实变),增生会带来肺部很严重的改变,不可逆的损伤。
1、渗出性病变
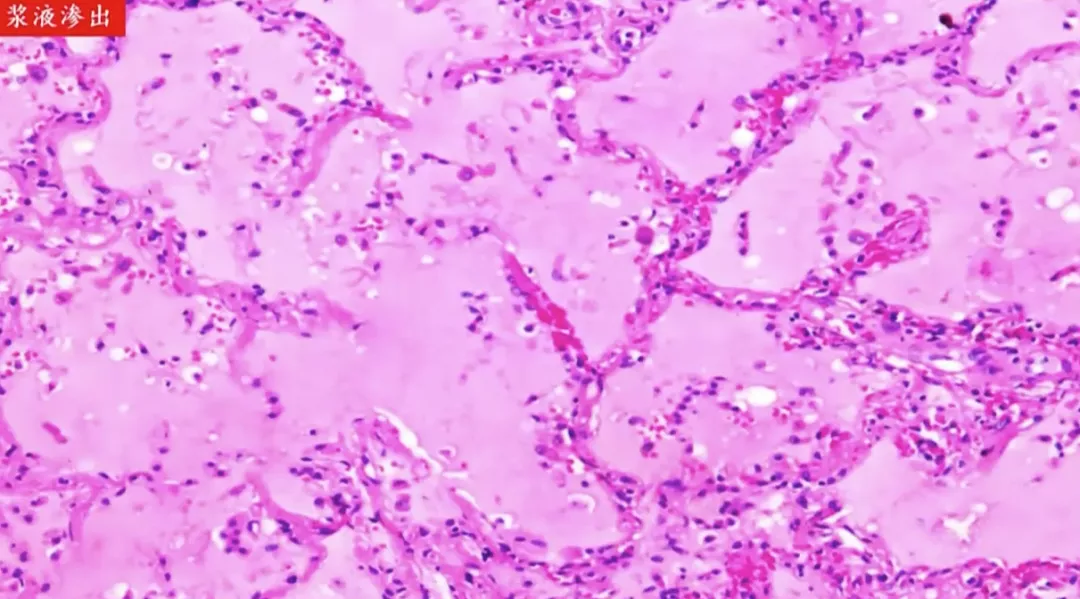
上图为浆液渗出,有肺泡壁、肺泡腔。正常情况下,肺泡腔里面是气体,偏红色的是液体,有液体充满肺泡腔,气体根本无法进来,结构发生改变。
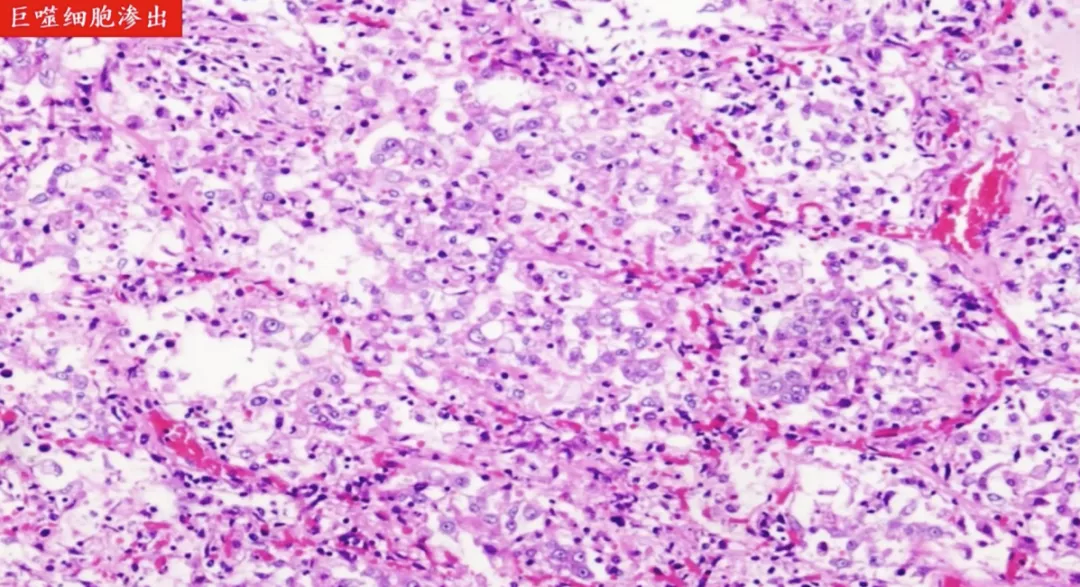
上图为巨噬细胞渗出,肺泡腔里有巨噬细胞。我做第一例尸体解剖的时候,就看到新冠肺炎的肺部炎症与普通的炎症不一样,有大量的巨噬细胞渗出,当时我预感到巨噬细胞在新冠肺炎的治疗过程中会起到非常重要的作用。现在经初步研究发现,巨噬细胞的确介导了严重的损伤。
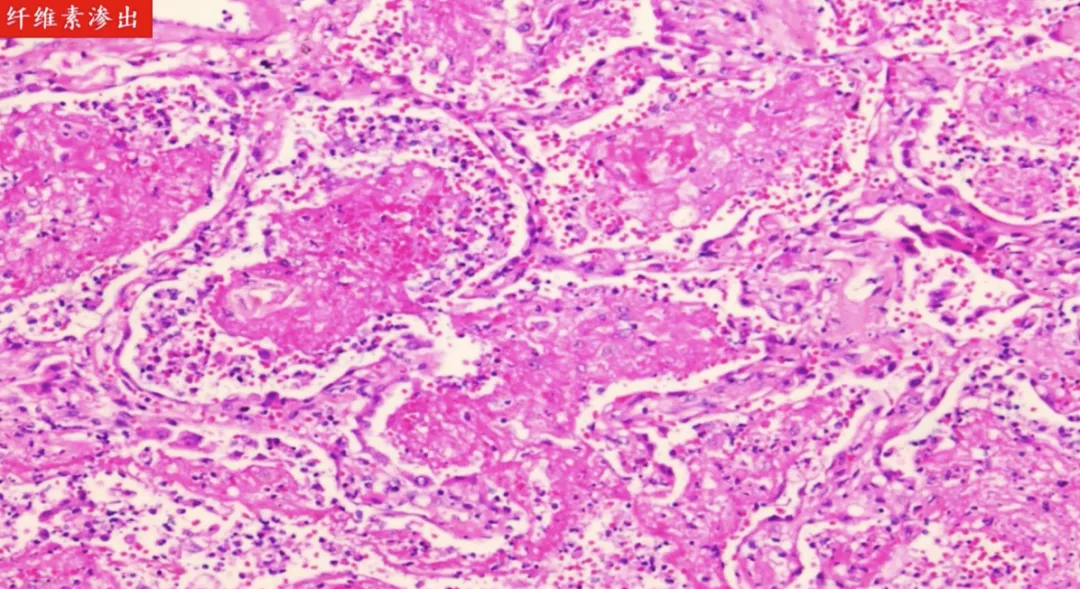
上图为纤维素渗出。肺泡腔里粉红色的是纤维蛋白渗出,纤维素通过肺泡孔相连,如果纤维素不能被完全吸收,纤维组织有可能长进去,这个肺泡就有肉芽组织填充,称为肺泡肉质变。
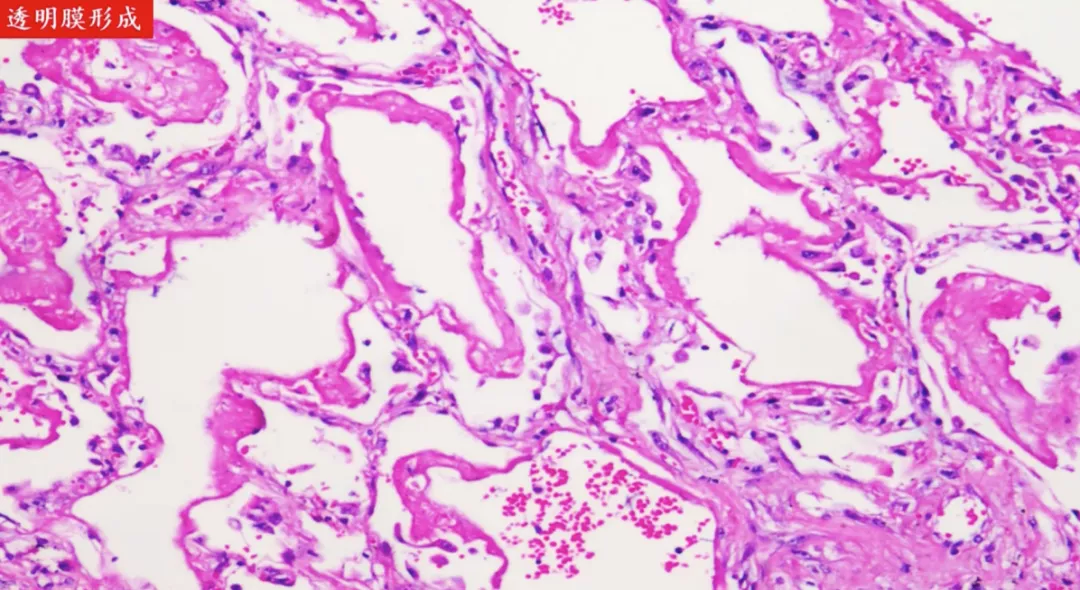
纤维素相互融合变成薄膜覆盖在肺泡表面,称为透明膜。透明膜的形成严重影响气体交换。
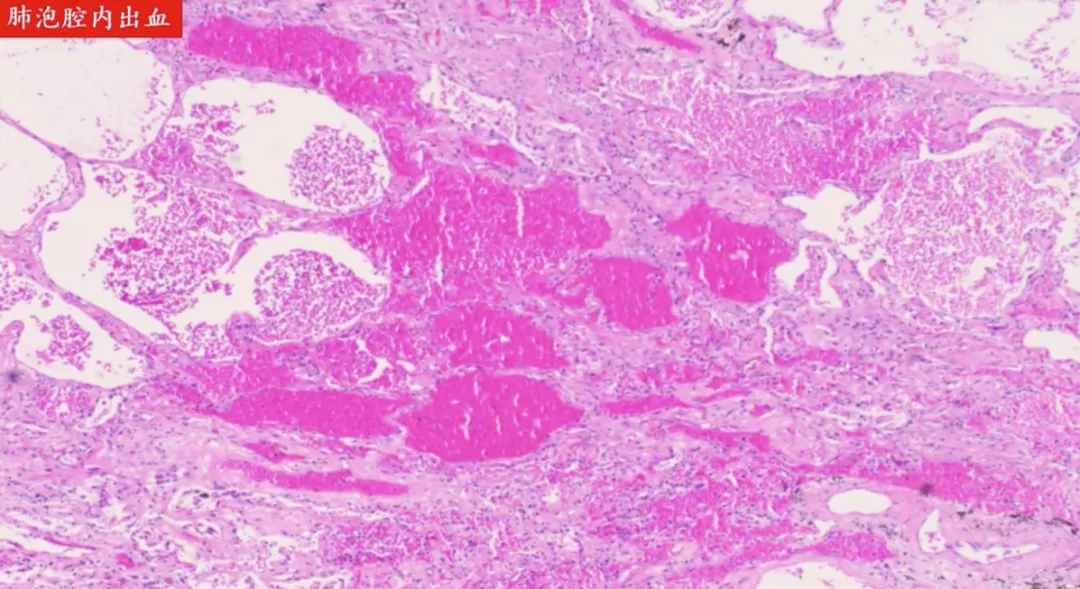
渗出性病变包括以上几种,另外肺泡腔内可能继发出血。有红细胞显露出来,红细胞从心血管腔内移除到管壁外的过程称为出血。出血包括破裂性出血和漏出性出血两种类型,这应该属于漏出性出血。肺泡腔里面有红细胞,红色的是密度更高的肺泡腔内出血,这里的肺已经发生实变。
2、变质性病变
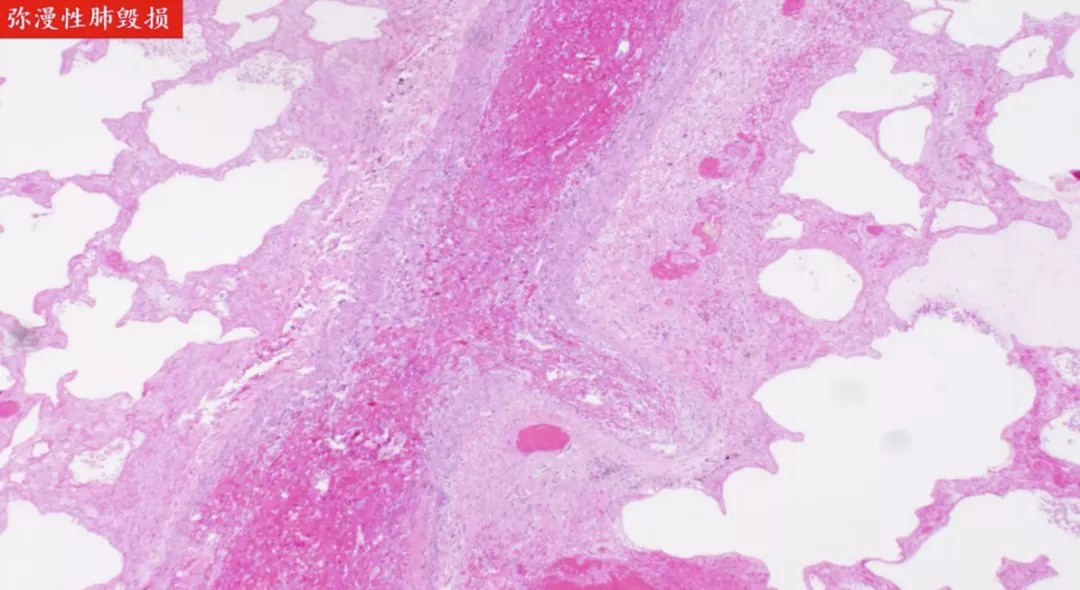
上图为弥慢性肺毁损。肺泡腔里边几乎没有细胞成分,只有个别的炎细胞,这是因为所有的细胞都发生了坏死。
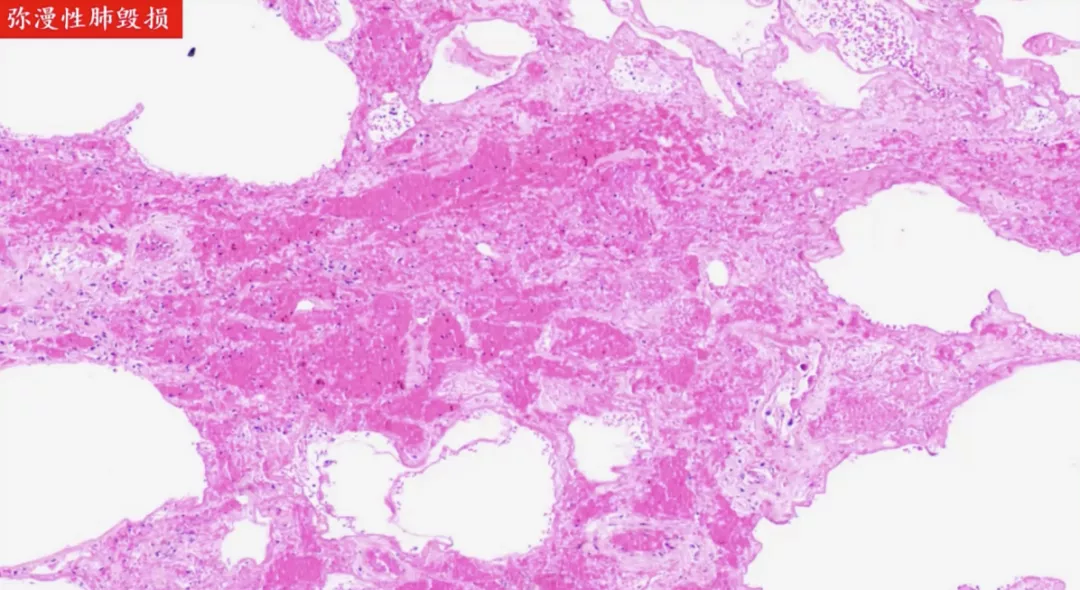
一般情况下会发生比较多的炎症反应,但是对于新冠肺炎而言,它的病灶内很少有淋巴细胞反应。我们做了20多例新冠肺炎尸体解剖,在不继发其他细菌感染的情况下,很少有淋巴细胞浸润。所以我们认为在新冠肺炎中,不知道通过什么机制抑制了免疫功能,在临床上进行外周血检查会发现白细胞较低,现在还不清楚这个机制。

上图为肺泡上皮的免疫组化标记。肺泡腔面在正常情况下有完整的肺泡上皮覆盖,这个肺泡腔面已经全部没有肺泡上皮。
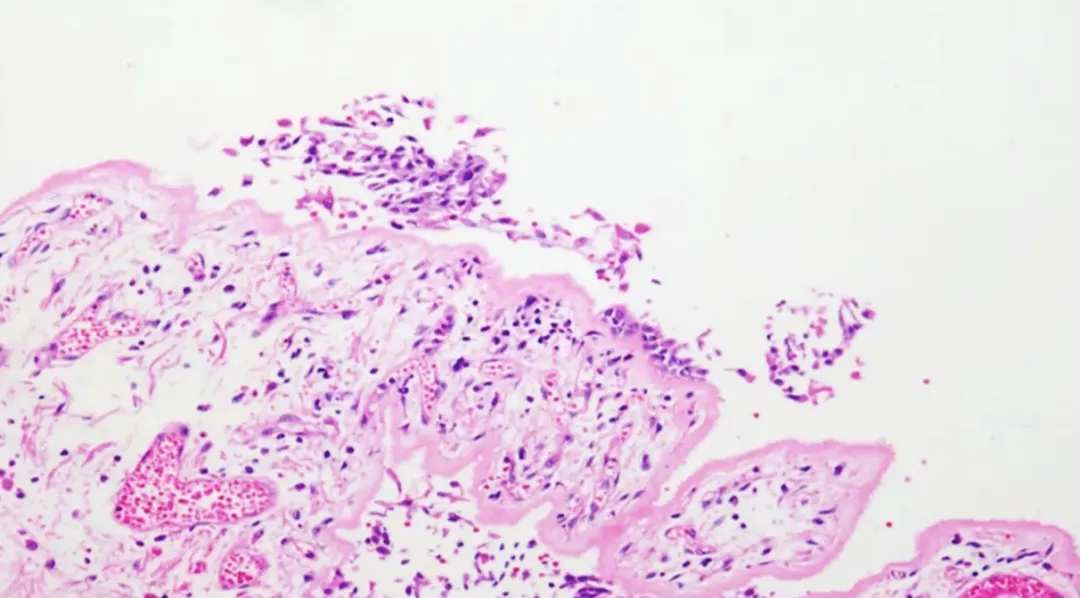
上图为支气管的改变。支气管黏膜上皮发生改变,黏膜上皮脱落。黏膜上皮内有五种细胞,其中有一种细胞是纤毛柱状上皮,具有清洁空气、排痰的功能,当纤毛柱状上皮脱落以后,不能有效排痰。
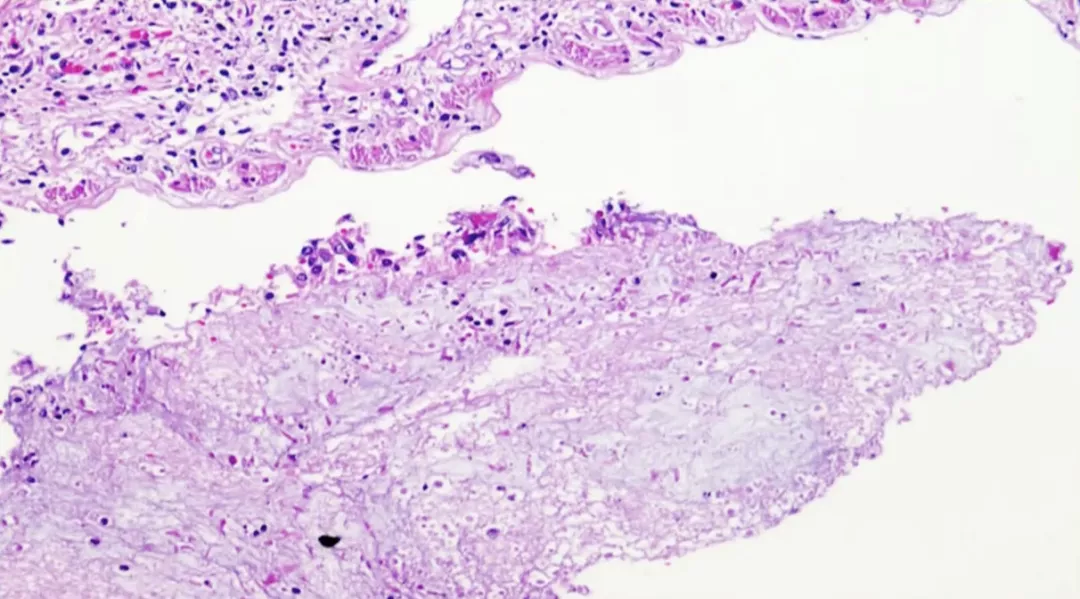
正常情况下是覆盖黏膜上皮,但是黏膜上皮脱落了,脱落的黏膜上皮和黏液混在一起形成黏液栓。对于新冠肺炎来说,由于支气管上皮破坏会导致引流不畅,引起痰栓的形成,从而引起气道通气不畅,甚至阻塞,导致通气障碍。
3、增生性病变
增生就会发生不可逆的变化。
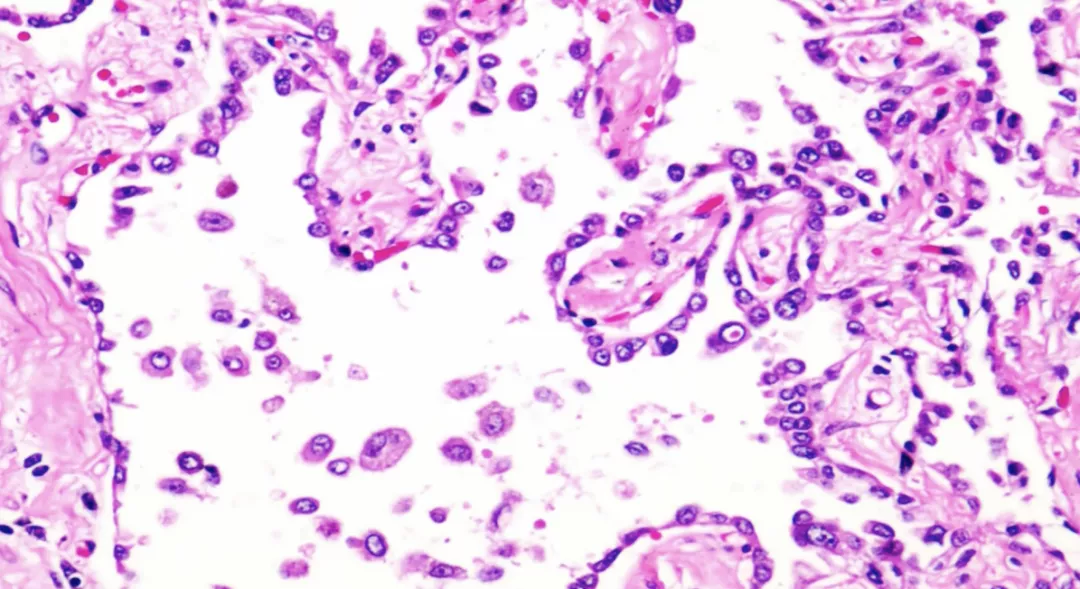
肺泡壁变厚就是纤维组织增生,正常情况下Ⅰ型肺泡细胞覆盖肺泡表面95%,Ⅰ型肺泡细胞参与气体交换,Ⅱ型肺泡细胞没有气体交换功能。由于Ⅰ型肺泡细胞损伤且没有再生能力,Ⅱ型肺泡细胞增生填充了Ⅰ型肺泡细胞的空间,所以Ⅱ型肺泡细胞增生覆盖了肺泡的表面,即使有气体进来,也无法进行气体交换,上图为Ⅱ型肺泡细胞的增生。
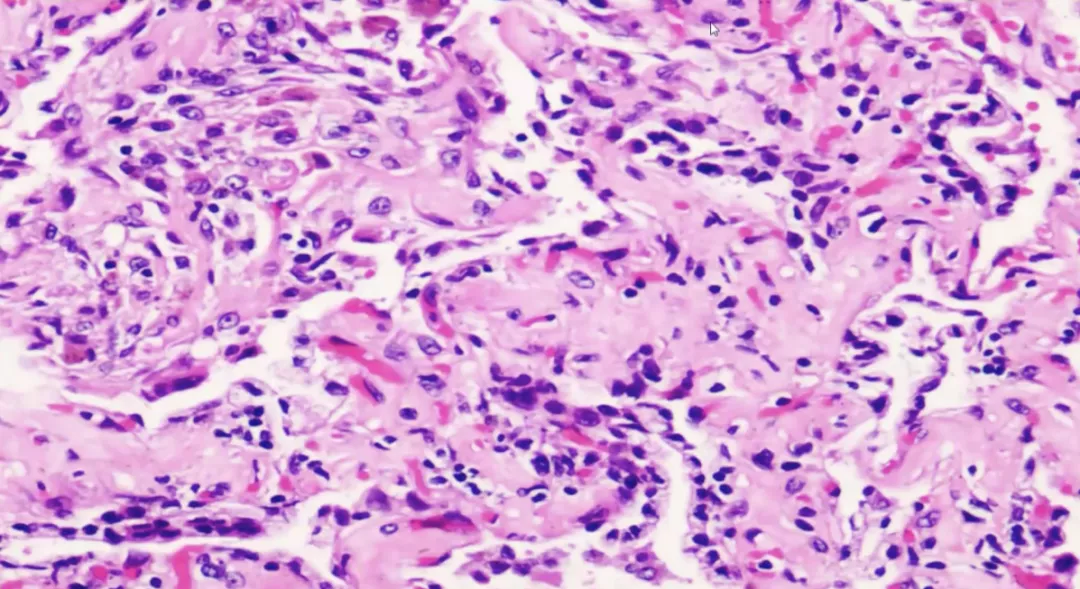
上图为纤维组织增生,有上皮细胞。
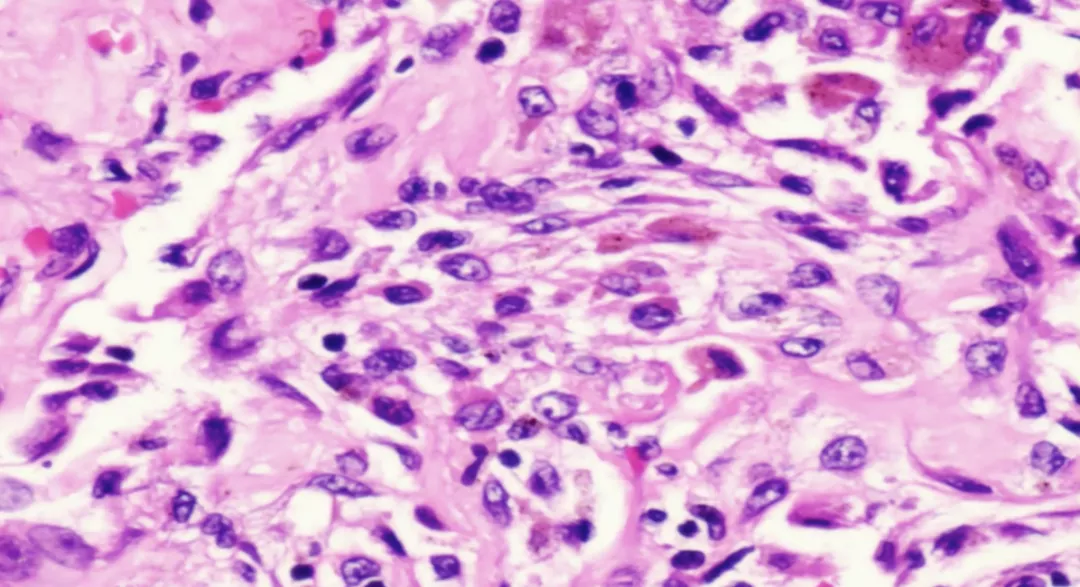
当我带到年轻的病理医生看这种病理切片的时候,会进一步放大,这些都是上皮细胞。在武汉的时候,一位年轻的病理医生询问我,这个病理看上去像癌,我告诉他这不是癌,这就是新冠肺炎导致的一种反应性的Ⅱ型肺泡细胞的不典型增生,这种不典型增生不是肿瘤性的,而是修复性的。这张图就是高倍镜下的Ⅱ型肺泡细胞的增生和纤维组织增生,淋巴细胞非常少。
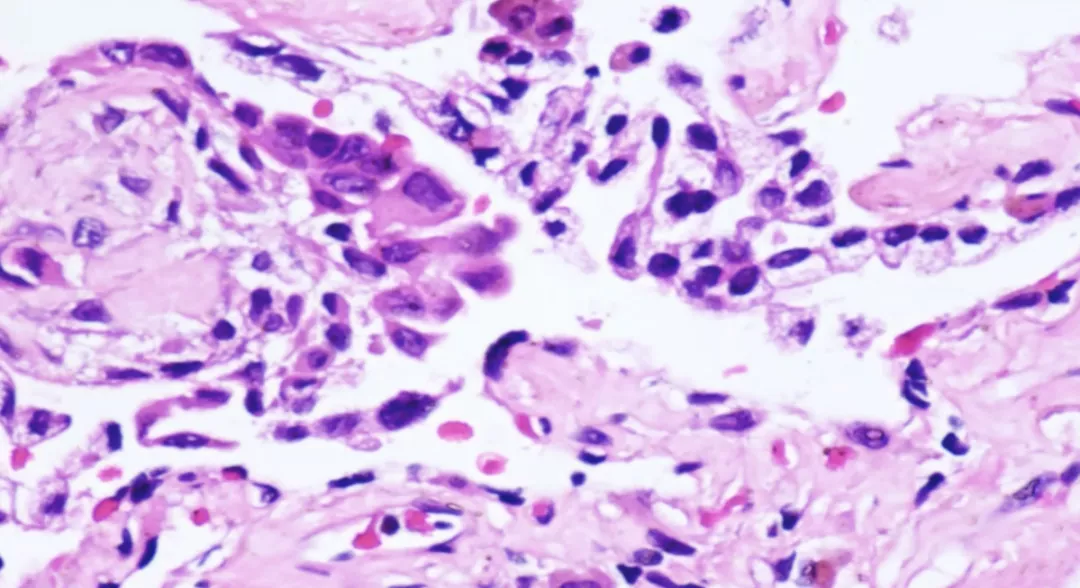
上图的上皮增生有点像癌,很像肿瘤。我在做尸体解剖前看到一篇文章,文章提到原来有一个患者因为发烧去医院去拍CT,发现肺上有个阴影,切下来是肺癌,经检查等手段发现是新冠肺炎,这篇文章报道的最终结论是这个患者既有肺癌又患有新冠肺炎。我对此表示怀疑,可能是新冠肺炎导致的肺泡上皮的不典型增生,把肺泡上皮的不典型增生误诊是肺腺癌。
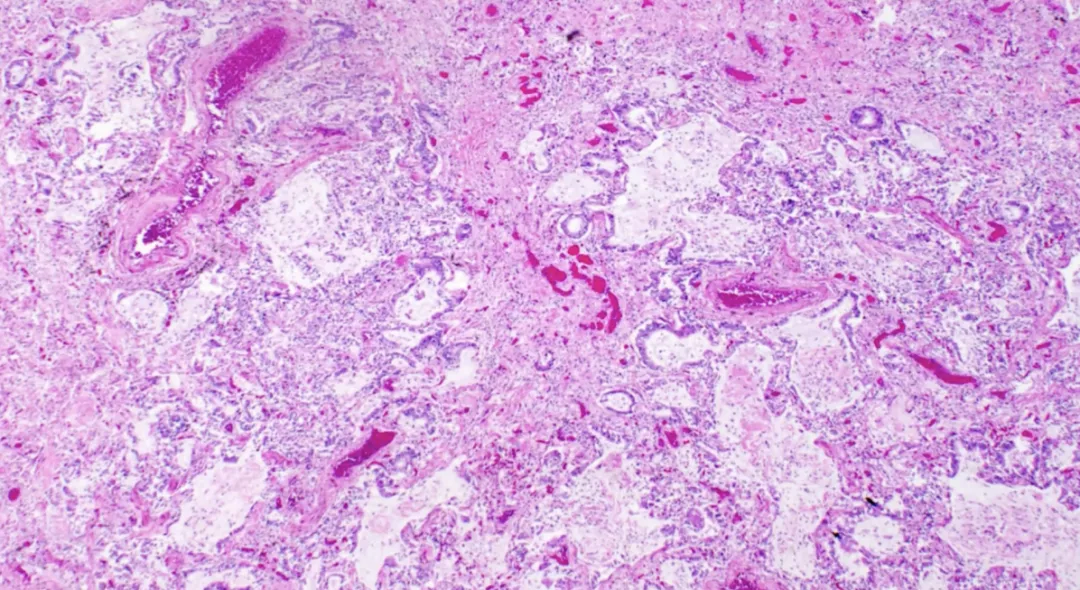
如果不告诉你上图为新冠肺炎的病理,很多病理医生可能都认为是肺腺癌,其实这是新冠肺炎导致的一种支气管腺体以及肺泡上皮的增生。
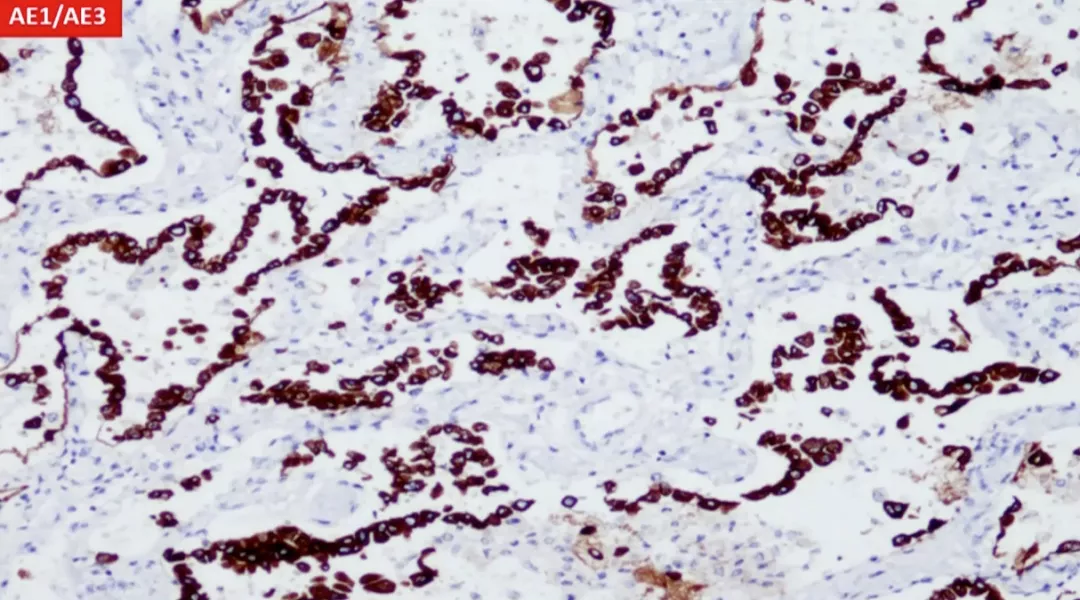
做免疫组化,这些上皮都是阳性的,从形态上看是立方形,是Ⅱ型肺泡细胞。Ⅱ型肺泡细胞很多,很像肿瘤。
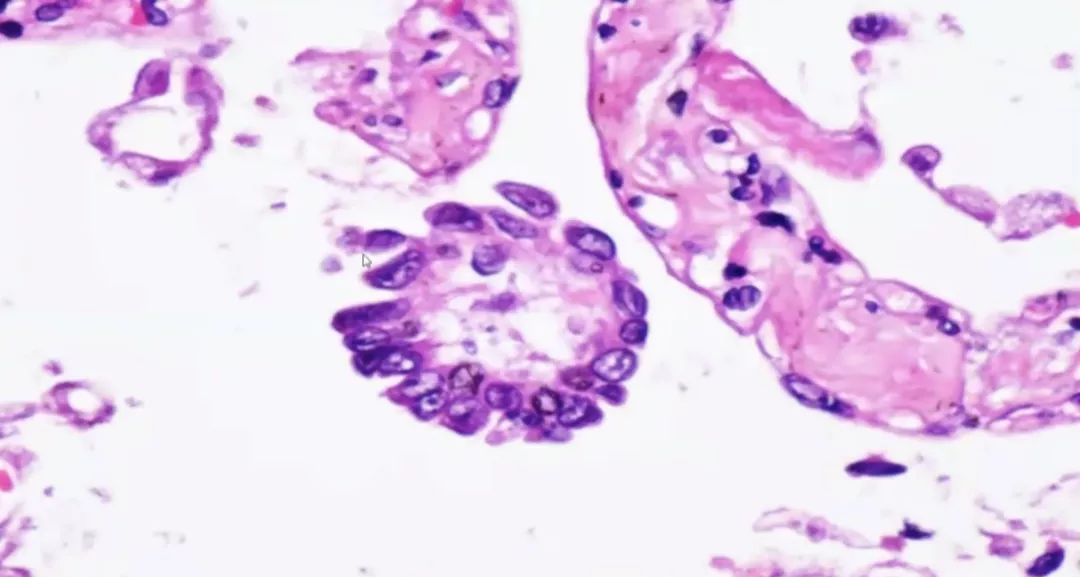
呈乳头状增生,非常像腺癌的乳突亚型。
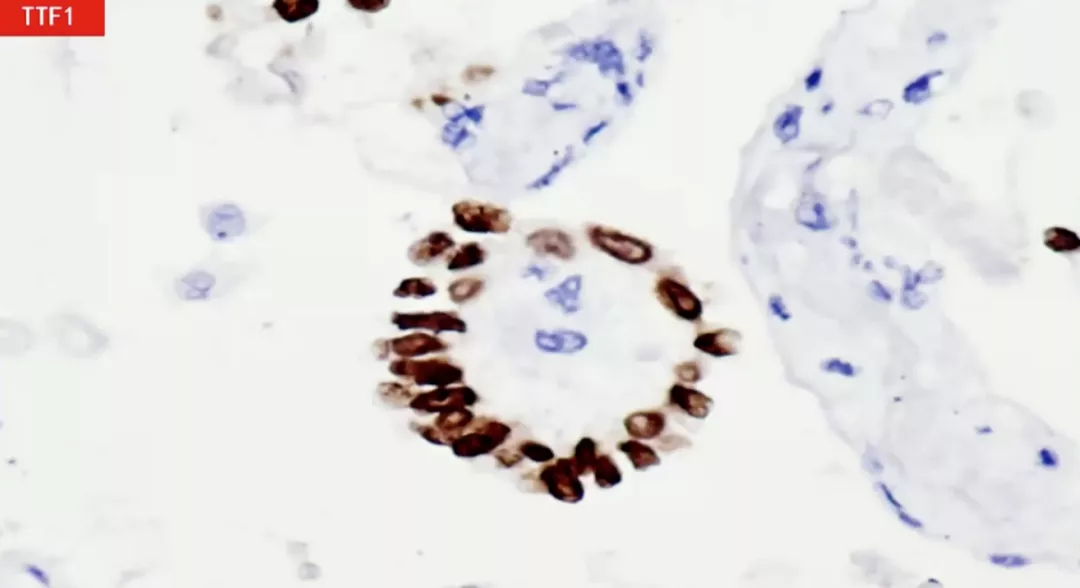
做免疫组化,Ⅱ型肺泡细胞是否增生,TTF1为阳性。
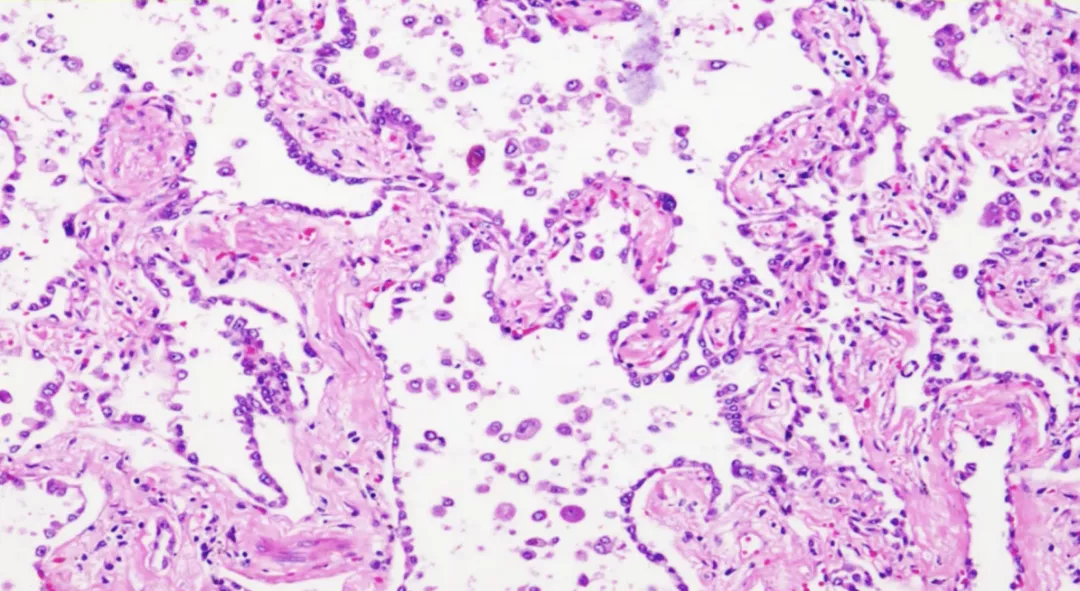
肺泡间隔很宽,即使有气体进入,也不能进行气体交换。第一,表面被Ⅱ型肺泡细胞覆盖;第二,肺泡间隔纤维组织增宽。正常情况下,肺泡壁很薄的纤维结缔组织参与气体交换,现在纤维组织增宽,已经不能进行气体交换。
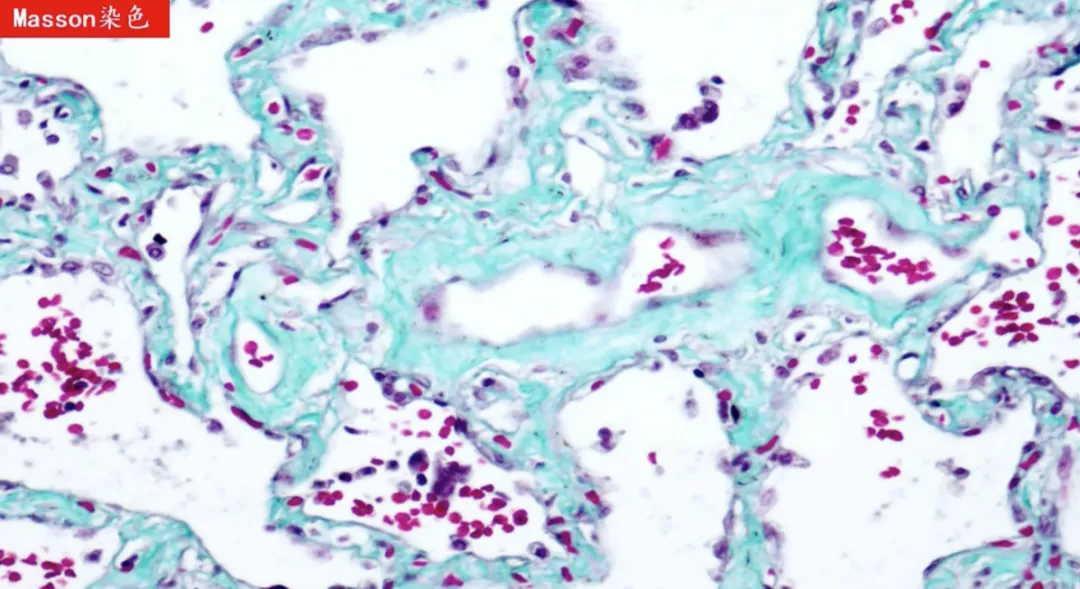
做纤维组织的Masson染色,纤维组织被染成淡绿色,纤维组织增生导致肺泡间隔增宽。淡绿色的这种染色应该是胶原纤维。由此可知,肺泡间隔由纤维结缔组织增生。
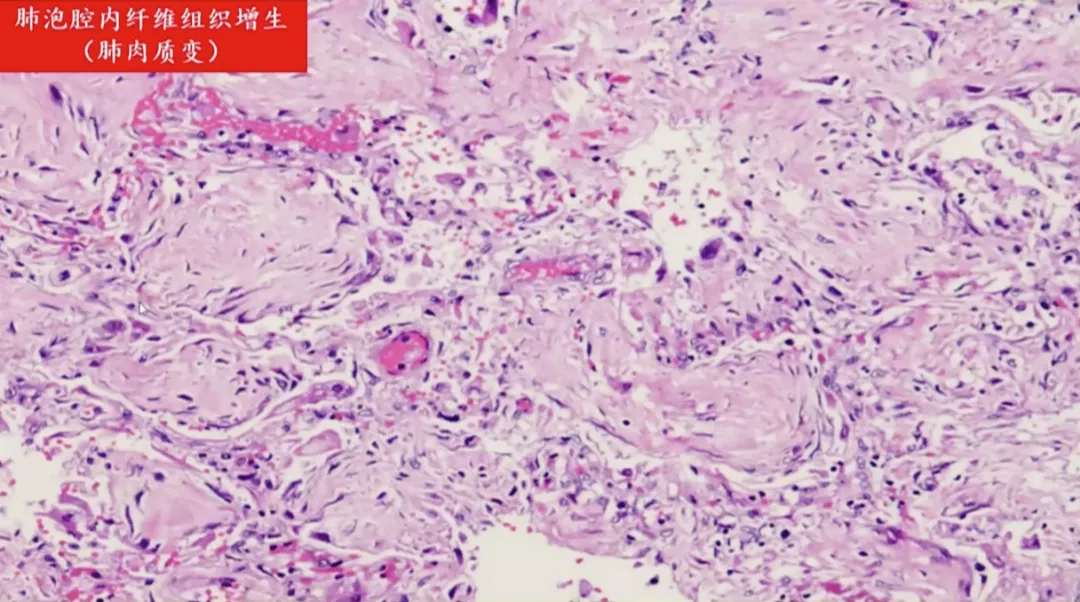
肺泡的轮廓还在,肺泡腔内被纤维组织填充,本来是气体,现在由肉芽组织取代,由纤维组织填充了本来的空间,称为肺泡的肉质变。
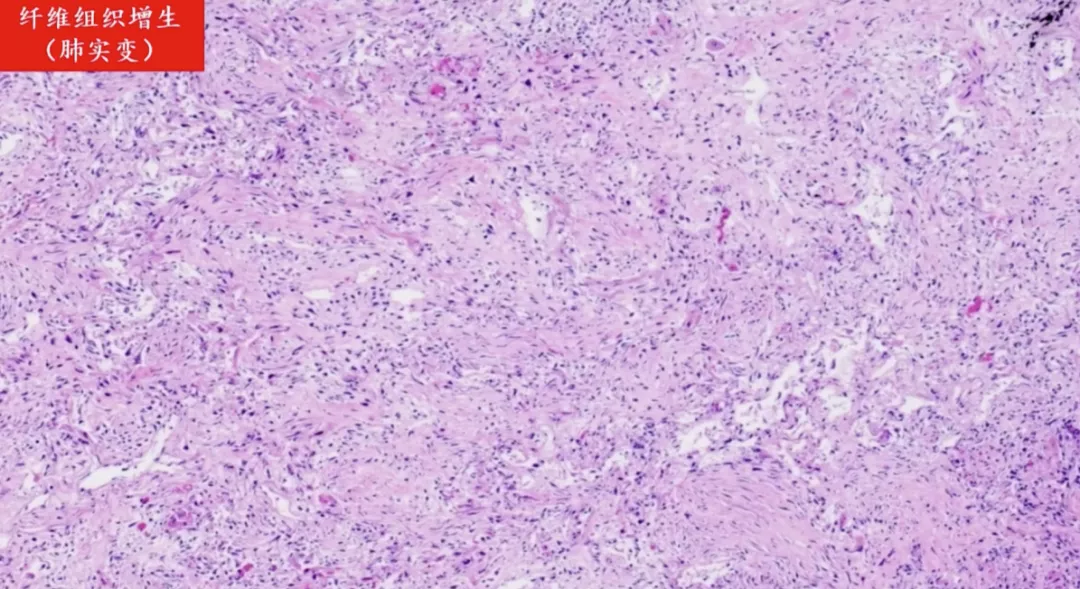
如果肺泡结构完全被破坏,称为肺实变。看不出一点肺的成分,完全由纤维结缔组织取代。这些增生都是不可逆的,使用任何药物都没有作用。
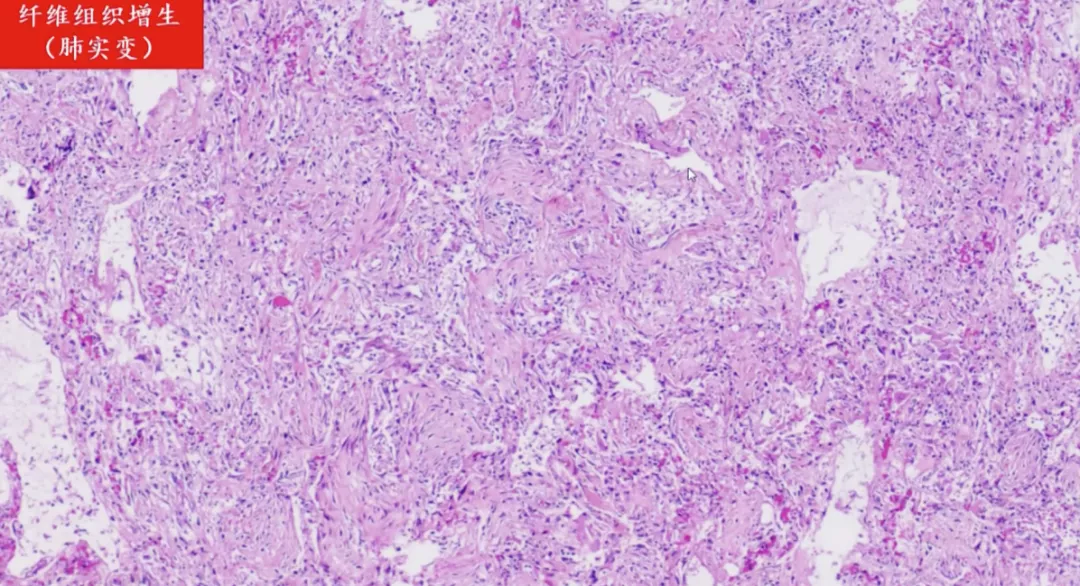
上图为另外一个视野,有残存的肺泡,完全没有肺泡的结构,由纤维组织取代。
4、继发性病变
> 支气管
由于支气管上皮不同程度损伤,包括纤毛柱状上皮脱落、纤毛脱失、鳞状上皮化生;小气道黏液腺体分泌亢进,腔内可有黏液性分泌物潴留,甚至有黏液栓形成,黏液栓会引起导气障碍。
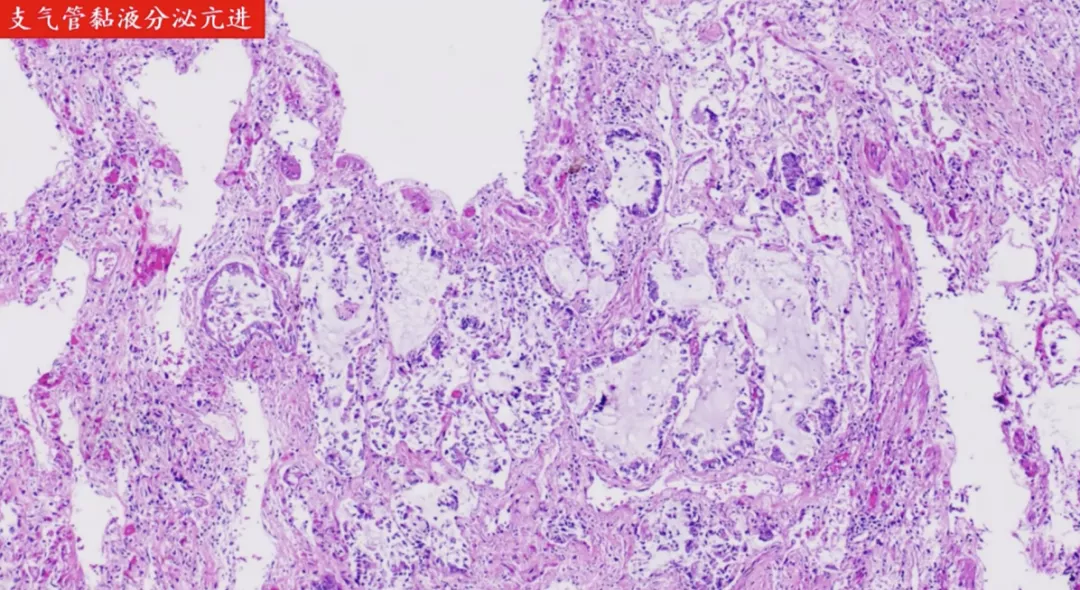
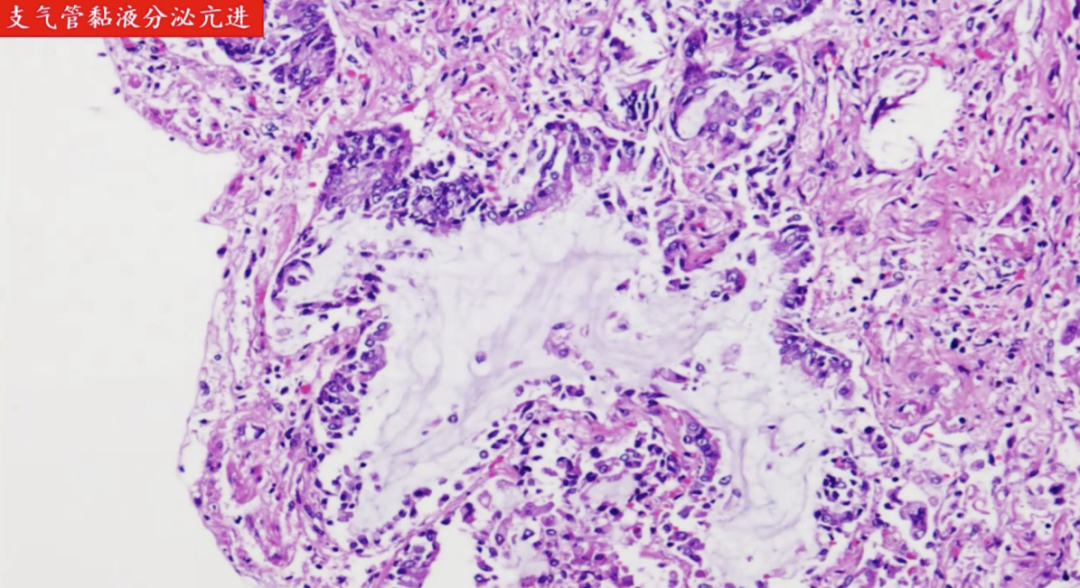
支气管壁上的黏液腺体在炎症的刺激下增生,分泌亢进,这些都是分泌大量的黏液,这些黏液无法排出,在肺内存留会引起通气障碍。
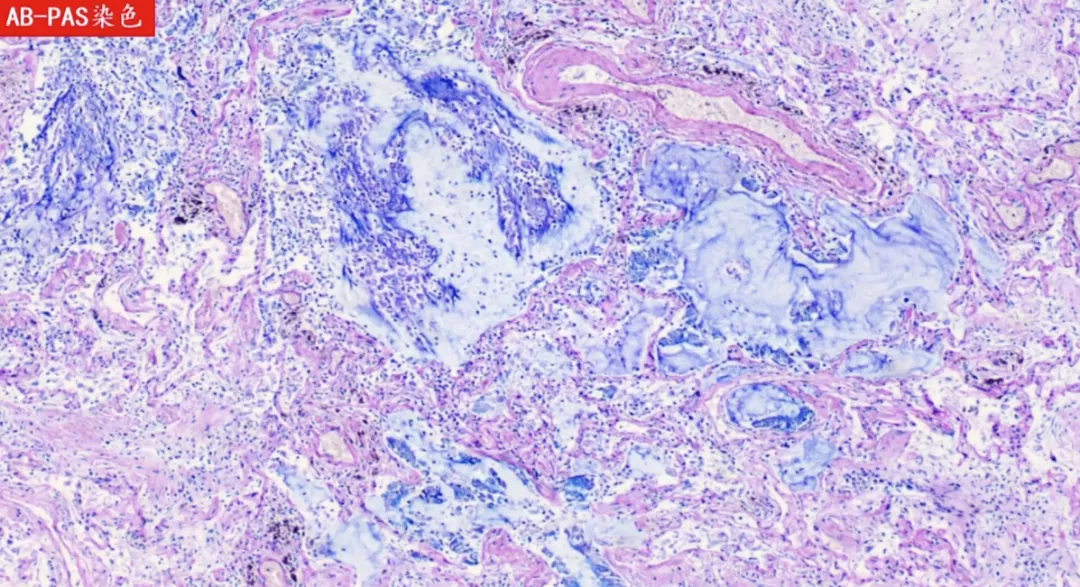
怎么知道是不是黏液腺体呢?使用AB-PAS染色,蓝色的都是黏液,正常情况下不会有这么多的黏液。
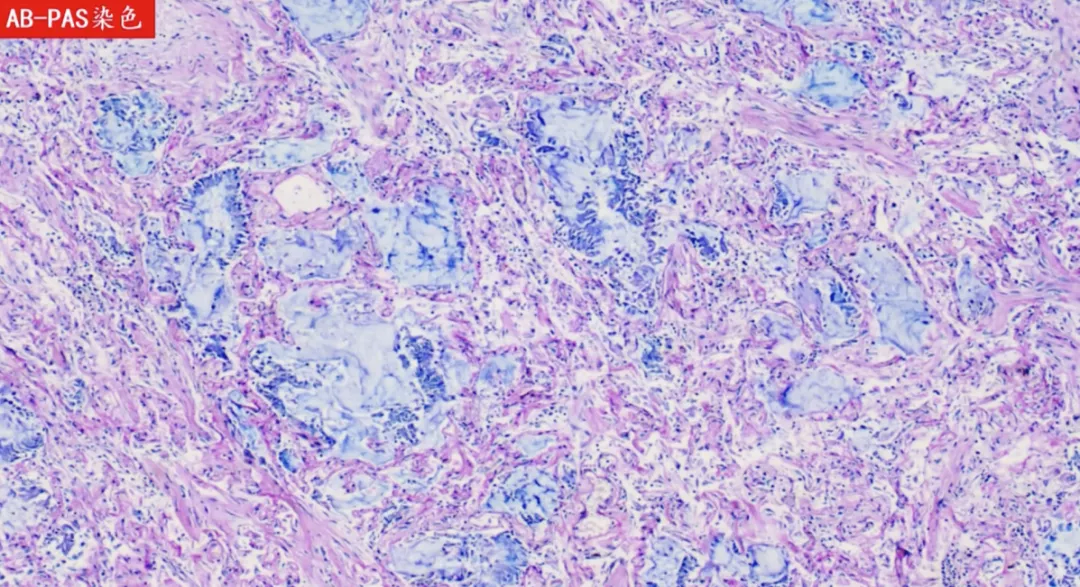
上图为另外一个病例,到处都是黏液,这些黏液排不出来会引起阻塞。
> 继发其他病原微生物感染
可继发细菌感染,表现为病灶内可见以中性粒细胞为主的炎细胞浸润;可继发真菌感染,表现为病灶内可见真菌菌丝/孢子。
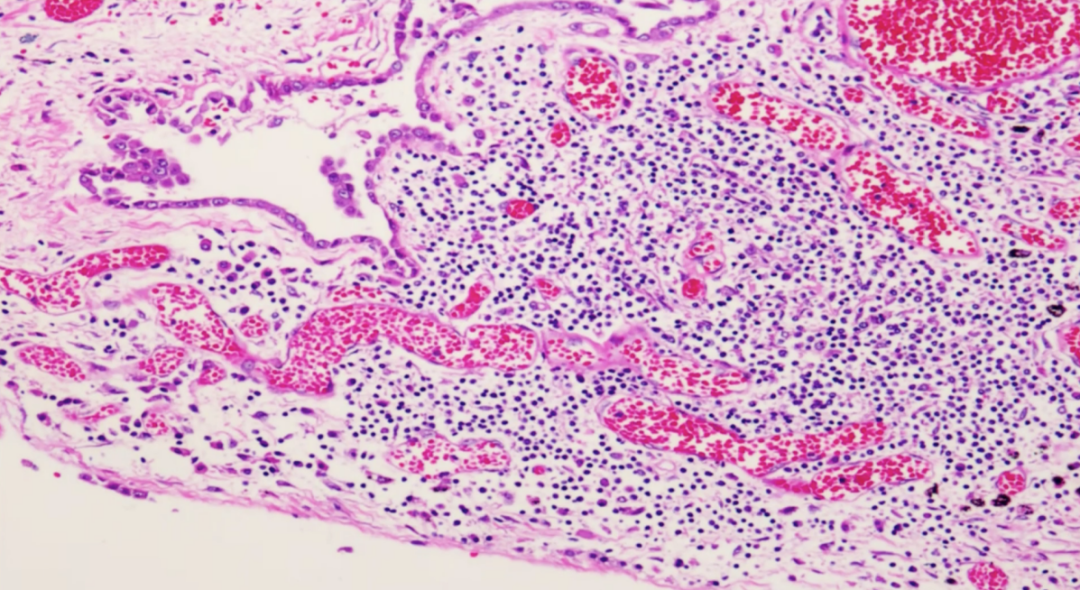
上图有炎细胞、淋巴细胞、中性粒细胞,根据这些炎细胞的种类,可以判断是继发其他细菌感染,而不是新冠病毒的感染。如果不继发其他细菌的感染,在新冠肺炎的病灶内仅有少数的淋巴细胞浸润。
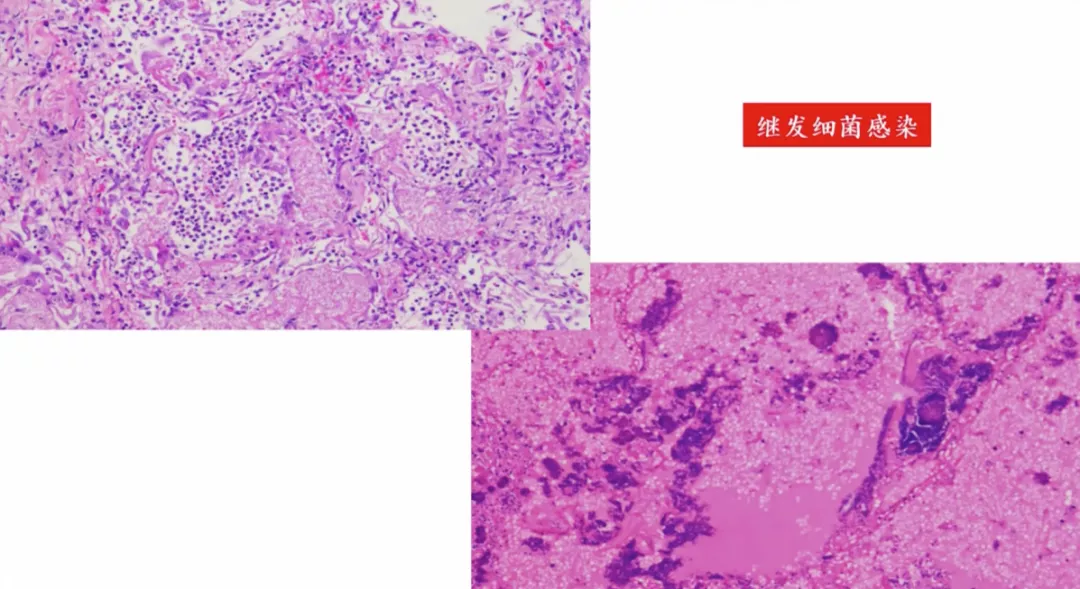
紫色的部分都是细菌的菌落,有炎细胞的浸润、中性粒细胞的浸润、淋巴细胞的浸润。如果不继发细菌感染的时候,没有这些中性粒细胞出现。
5、继发血栓形成
血栓的形成不仅在肺,身体所有的部位都有可能继发血栓形成。对于新冠肺炎而言,血栓形成的概率比较高,我们几乎在每个病例都能看到血栓形成。
临床病理联系
这些病理改变会引起怎样的功能改变,功能改变又会引起怎样的临床表现?
结构改变
结构改变会引起通气功能和换气功能改变。结构改变包括呼吸道上皮损伤、小气道分泌物储留/黏液栓形成;肺泡腔内渗出物;肺泡肉质变;肺实变;肺泡腔内出血,这些结构的改变会引起通气功能障碍。Ⅰ型肺泡上皮(参与气体交换)损伤;Ⅱ型肺泡上皮增生;透明膜形成;肺泡毁损;肺泡壁内纤维组织增生,这些结构的改变又会引起换气功能障碍。在通气功能障碍和换气功能障碍的共同作用下引起新冠病人的呼吸困难。
三、新冠病毒是如何致病的?
新冠病毒侵入肺部以后,不在肺泡腔内致病,那么新冠病毒如何致病呢?它要进入机体的什么细胞或者组织?
COVID-19发病机制初步探讨
新冠病毒如何侵入细胞?
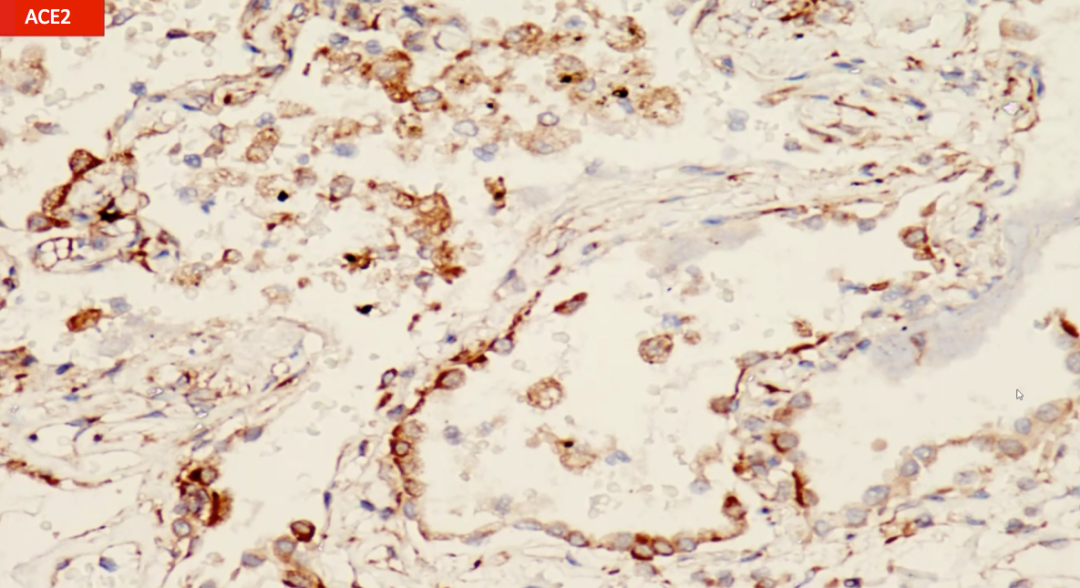
病毒侵入细胞要有配体和受体,也就是说要有细胞表面的受体和病毒的配体结合才能侵入。病毒需要的配体是ACE2,肺内什么细胞含有ACE2呢?我们做了免疫组化,肺泡上皮是阳性的,肺泡腔里面的巨噬细胞是阳性的,也就是说肺泡上皮和巨噬细胞都有ACE2抗体,新冠病毒可以侵入。
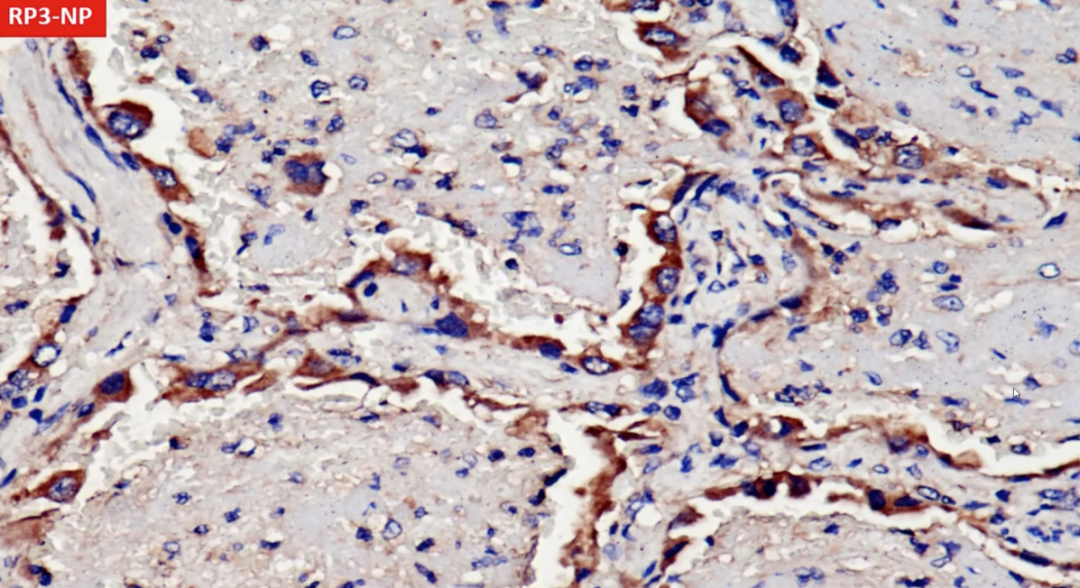
病毒是否进入肺泡上皮,我们使用RP3-NP检测新冠病毒,这是新冠病毒的抗体。肺泡上皮包浆是阳性的,巨噬细胞也是阳性的。刚才看到在肺泡上皮和巨噬细胞中有ACE2配体,通过免疫组化证实在肺泡上皮内和巨噬细胞的胞浆内发现了新冠病毒。
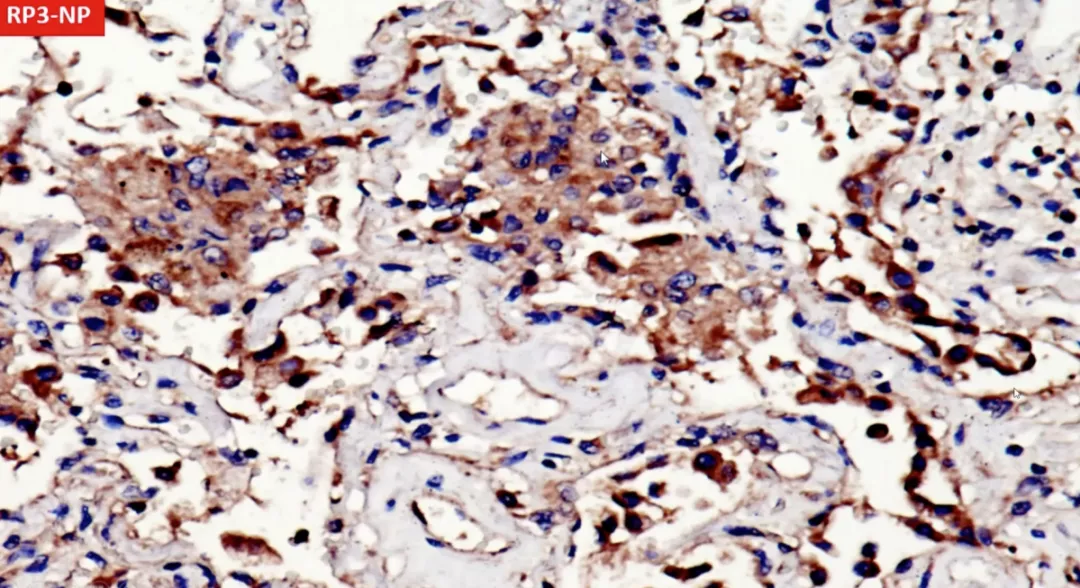
巨噬细胞和肺泡上皮都是阳性。
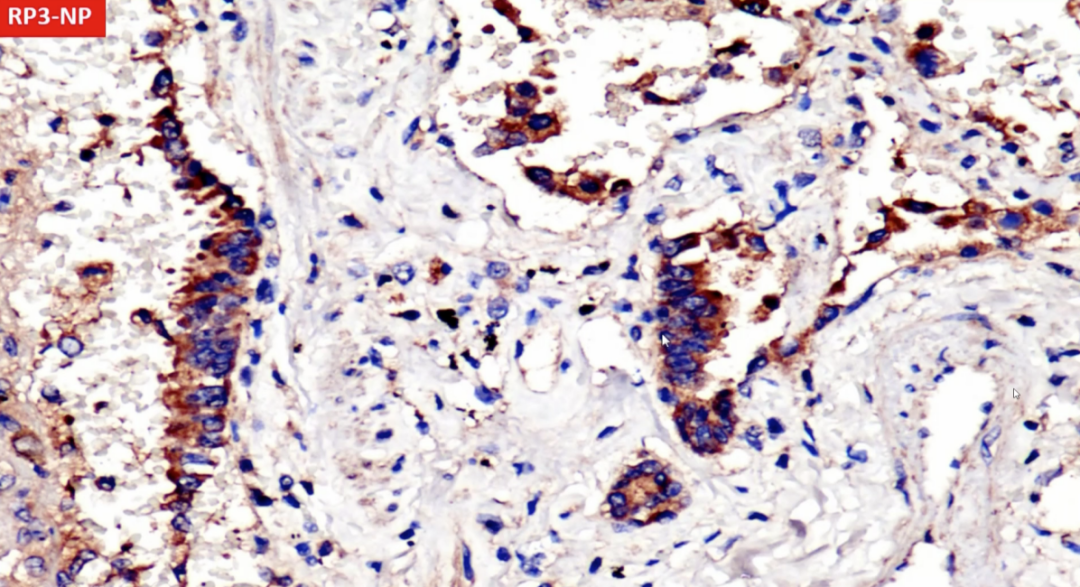
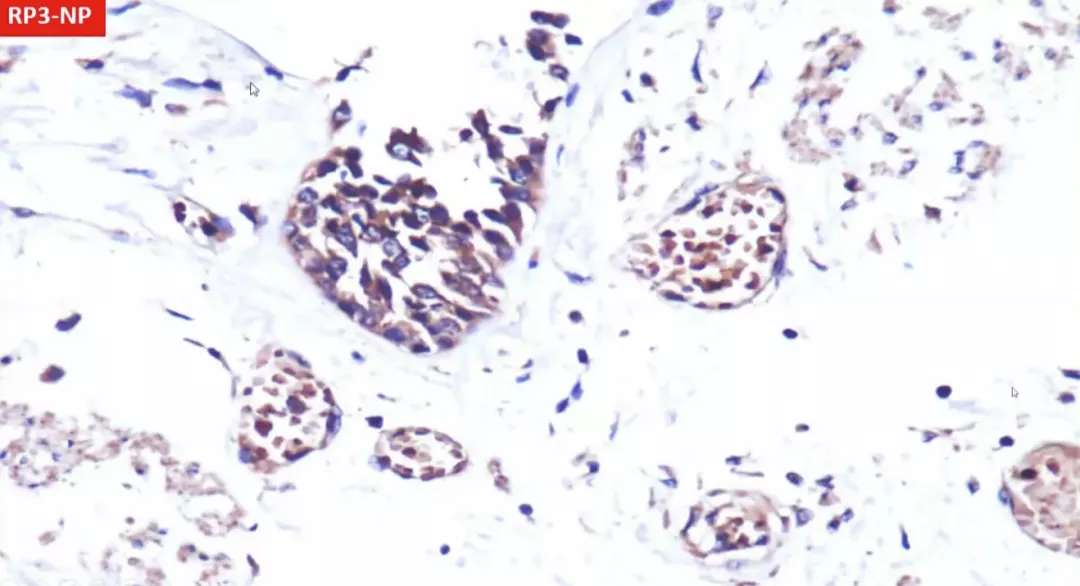
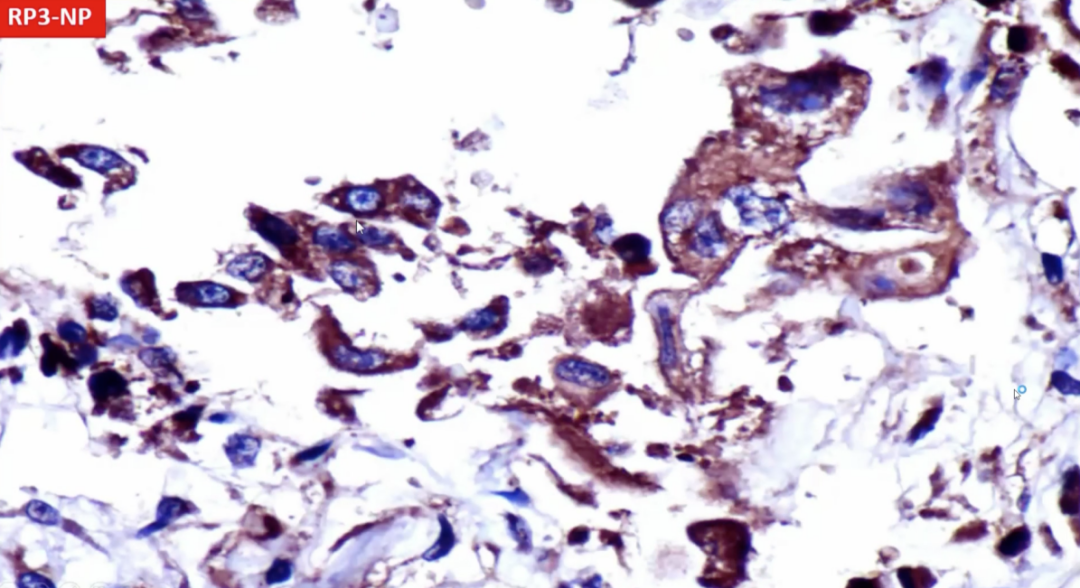
以上三张图片均为支气管上皮,有ACE2配体,新冠病毒也能侵入。
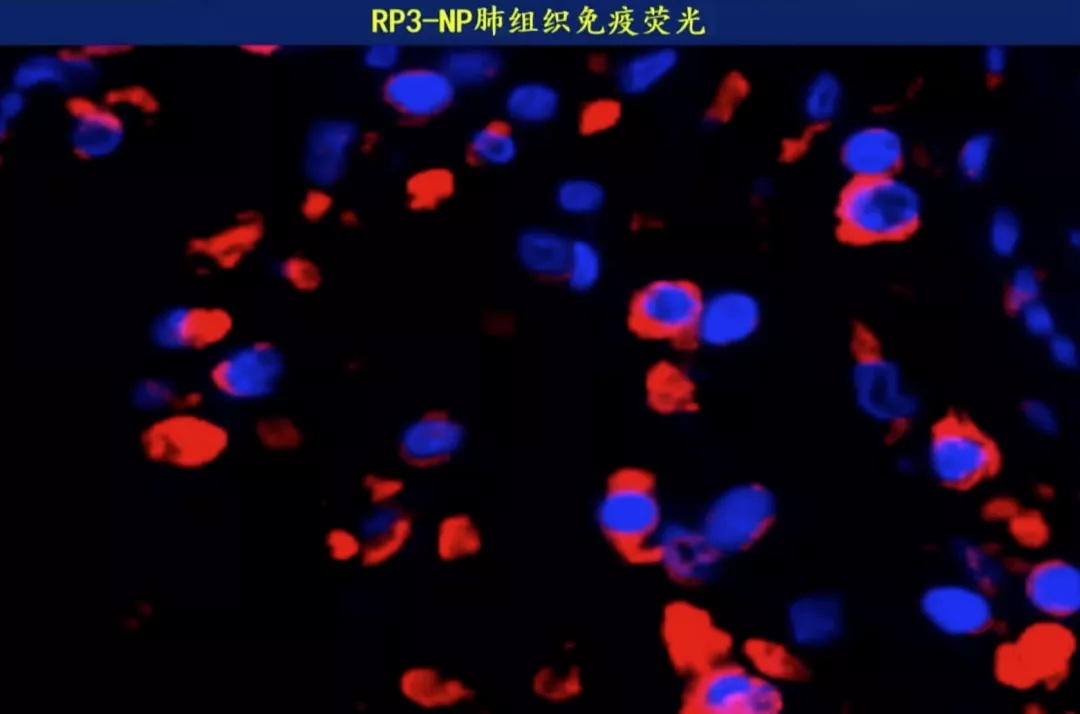
上图为荧光免疫组化。荧光代表有新冠病毒存在,肺泡上皮、巨噬细胞的胞浆内都有新冠病毒存在。
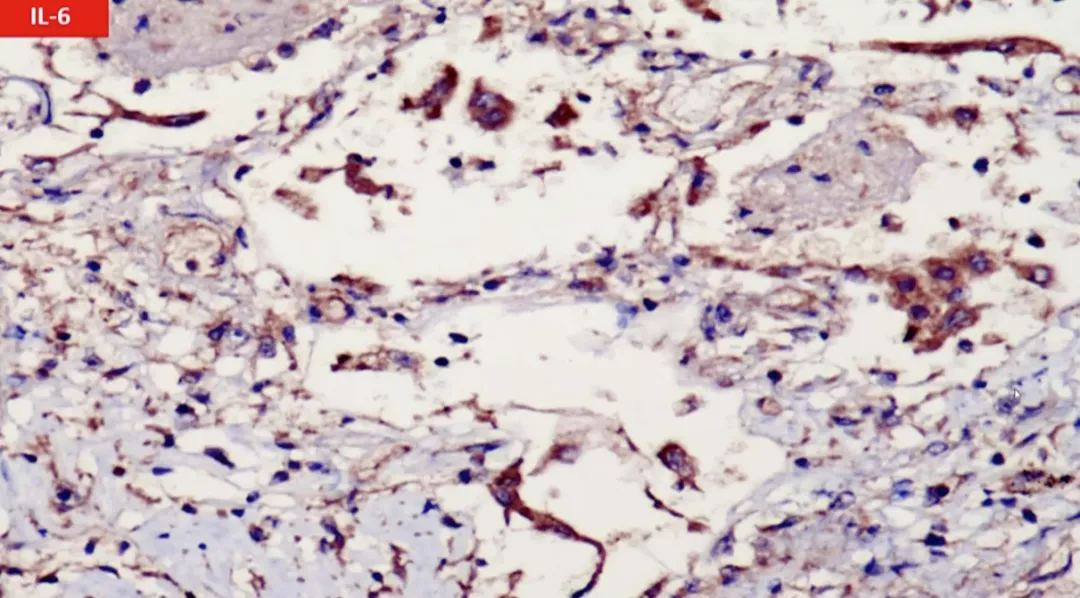
因此,我们初步探讨新冠病毒进入肺内后,首先侵入肺泡上皮细胞,然后引来巨噬细胞,新冠病毒又可以进入巨噬细胞的包浆里面,巨噬细胞开始释放细胞因子。我们检测出释放的细胞因子的白细胞介素-6比较高,用白细胞介素-6抗体,上图中巨噬细胞的胞浆是阳性的。
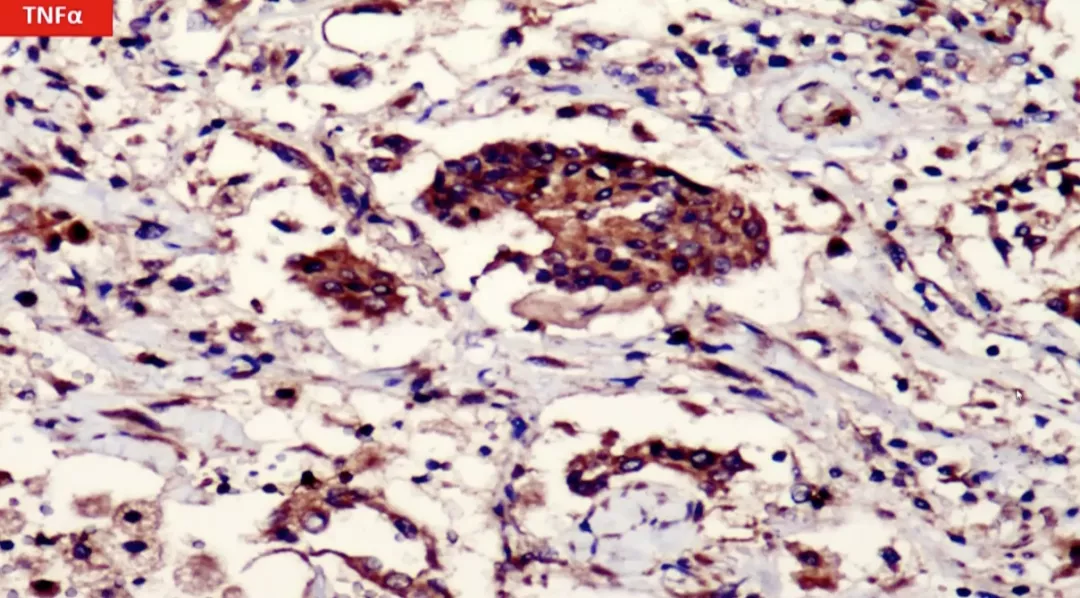
肿瘤坏死因子在巨噬细胞中也有很多是阳性的。
我们初步探讨新冠病毒如何致病的结论如下:新冠病毒首先到达肺泡腔内以后,进入肺内上皮细胞,肺内上皮细胞被感染以后,机体吸引巨噬细胞,巨噬细胞反应释放大量炎症因子,介导了这种炎症的过度损伤,所谓的炎症风暴带来一系列机体的变化。

我们进行了相关研究,在《EBIOMEDICIN》发表了这篇文章,上图是这篇文章的校样。
四、小结
新冠肺炎肺部主要病理变化是属于炎症的范畴,包括渗出、变质、增生。肺内的结构改变影响了通气和换气功能。巨噬细胞介导的「炎症风暴」引起的过度损伤可能是新冠肺炎主要的发病机制之一,也就是由巨噬细胞扮演了很重要的介导作用。
答疑讨论
王一民:您介绍的20多例尸体解剖的病人,从发病到死亡的时间平均大概是多长时间?有什么差别吗?比如A病人发病很快去世,B病人的病程很漫长,他们的病理改变是否存在差别?
王朝夫:存在差别。炎症的过程是渗出、变质、增生,现在还没有对每例尸体解剖进行病程长短与病理改变的具体联系的分析,但是根据我们对炎症的理解,应该是病程长,增生会比较明显,病程初期是以渗出为主的病变,接下来才是变质,变质就代表损伤,哪里有损伤哪里有修复,主要是靠纤维来进行修复。
一般来说,新冠肺炎死者的病程都比较长。我们也碰到过病程比较短的病人,有的病人有基础病变,比如有一例病人是新冠肺炎继发心肌梗死,病程就比较短,尸体解剖的结果就是肺内的渗出性病变较多,而增生性病变较少。
王一民:您刚才讲到新冠病毒直接侵犯肺泡上皮细胞,吞噬细胞会有聚集的表现。新冠病毒是直接攻击了巨噬细胞,还是巨噬细胞主动去保护机体,想包含新冠病毒,您如何看待这个问题?
王朝夫:目前新冠肺炎的发病机制还不太清楚。在正常情况下,肺泡腔内没有什么巨噬细胞,如果出现巨噬细胞就是在病理的状态下。刚开始,正常的健康人呼吸了带有新冠病毒的空气后,新冠病毒首先进入肺泡腔,接触的是肺泡上皮,当肺泡上皮感染以后会引起机体的炎症反应。不同的病原体会吸引不同的炎症细胞,靠趋化因子来吸引不同的炎症细胞。比如,结核病的病灶内以巨噬细胞为主,没有中性粒细胞,因为结核杆菌感染以后不释放中性粒细胞的趋化因子,所以没有中性粒细胞过来。而新冠病毒感染了肺泡上皮以后,应该是炎症病灶释放了巨噬细胞的趋化因子,趋化作用以后到达炎症病灶,它起到防御的功能。但是由于巨噬表面有ACE2配体,所以新冠病毒也可以进入巨噬细胞内,巨噬细胞可能无法把新冠病毒杀死。我们推测新冠病毒可能在巨噬细胞内继续生长繁殖,使病毒由少变多,然后再播散到全身。
王一民:我们越来越多了解到COVID-19是一种全身性疾病,除了肺脏损伤外,您能否给临床医生提一些有关其他器官损伤的建议,如何去了解其他器官受到新冠病毒的影响的一些特征?
王朝夫:根据我们进行尸体解剖发现,新冠肺炎引起的病理变化可以概括为这几大方面,第一,主要的病理变化是肺部;第二,免疫功能的抑制,具体是什么抑制还不清楚;第三,影响凝血的状态,这是主要的三大基本病理变化。另外,在尸体解剖中发现其他器官不同的改变,比如心脏,一般情况下心肌受损,心肌变性,新冠病毒还可以继发心肌梗死,但不是每例病都会这样,我们可以肯定经尸体解剖发现心肌存在不同程度的变性。另外,我们在胃肠道、男性的睾丸发现了新冠病毒。所以,新冠病毒侵入机体后,首先感染肺部,然后播散到全身,引起致命的病理变化主要是肺部,其次是免疫系统功能的降低,还可能继发血凝状态的改变,会引起血栓形成,甚至DIC形成。
王一民:我们最早认识的病毒性肺炎是2003年的SARS,后来了解流感,包括季节性流感、甲型H1N1流感等、H7N9禽流感。您也会了解这些病毒性肺炎的相关特征,能不能结合以往的经验和这次的COVID-19,简单介绍一下不同类型的病毒性肺炎在病理上除了刚才您提到的吞噬细胞特别明显,而淋巴细胞比较少的特征之外,还有什么能够让我们所了解和熟悉的?
王朝夫:我没做过流感尸体解剖,没有直接参与SARS尸体解剖,但是我知道一些基本病理变化。流感、SARS、新冠肺炎都是病毒感染,病毒感染引起的病理变化和细菌感染不同。新冠病毒感染引起的病理变化引来的炎细胞主要是巨噬细胞,但是在新冠肺炎引起的巨噬细胞反应的量应该比SARS多。SARS的主要病理变化是有广泛的透明膜形成,而在新冠肺炎中引起的病理变化是可以有透明膜形成,但不够广泛,有些新冠肺炎的病例,我就没看到有透明膜形成,也就是说透明膜形成不是致病的主要病理改变。它们有相似之处,即病毒感染的共同之处。不同之处在于各有各的特点,新冠肺炎是以渗出和变质为主,变质是广泛的肺损伤,肺泡壁坏死、肺泡上皮坏死、支气管上皮坏死,新冠病毒会破坏这些结构。而SARS侵犯肺部的病理改变主要是有巨噬细胞渗出、纤维素渗出,以透明膜形成较多为特点。所以说它们有相似之处,也有不同之处。
王一民:线上的医生们对吞噬细胞、淋巴细胞与病毒之间的关系非常感兴趣。在这方面能否给大家一些借鉴,做哪些工作可以让我们更深入了解新冠病毒、吞噬细胞、淋巴细胞之间的关系?
王朝夫:现在我们发现新冠病毒对肺部的直接损伤,但是没有发现新冠病毒通过什么对免疫系统进行损伤。我们推测有可能是两方面,第一种可能性,新冠病毒感染后可能直接杀死淋巴细胞,但是我们没看到证据;第二种可能性,可能在更高的层次上,新冠病毒抑制淋巴细胞的转化。现在我们也不清楚,根据我们的理解,客观上肯定是免疫功能低下,淋巴细胞减少,本来存在的淋巴细胞是被消耗了还是被杀死了?为什么不能得到有效的补充?是不是在淋巴细胞转化这个层面上被抑制了?如果大家想研究可以从两方面研究,第一,新冠病毒与淋巴细胞有没有杀伤和被杀伤的关系;第二,新冠病毒侵入机体后,是否导致淋巴细胞转化的功能被抑制,这仅仅是我的初步判断。
专家介绍

王朝夫
教授,主任医师,博士生导师,上海交通大学医学院附属瑞金医院病理科主任。任上海医师协会病理科医师分会副会长,上海市医学会病理学专业委员会委员,《诊断学理论与实践杂志》副主编,《临床与实验病理学杂志》编委等职务。擅长肿瘤病理诊断,尤其是淋巴造血系统肿瘤、泌尿系统肿瘤及骨和软组织肿瘤的病理诊断。

王一民
中日医院呼吸与危重症医学科主治医师,中国医师协会呼吸分会青年委员会委员,中国医疗保健国际交流促进会临床微生物与感染分会青委副主委。


