在临床诊治中,我们常常提及「时机」,所谓的时机其实就是「时间」和「机会」。我们临床医师应该及时发现重症与危重症患者,并抓住机会及时进行侵入性诊治措施干预,从而达到改善患者预后的目的。
梳理一下在呼吸危重症救治中常用的侵入性诊疗手段,诊断方面常用的有气管镜下气道内分泌物抽吸、保护毛刷、肺泡灌洗、肺活检,但由于新冠肺炎的传染风险,其诊断主要依赖于鼻咽拭子的核酸检测,上述技术在实际中运用并不多。在重型及危重型COVID-19的救治中,关键还是呼吸功能的支持治疗——包括鼻导管或面罩给氧、经鼻高流量吸氧(HFNC)、无创正压通气(NIPPV)、有创机械通气乃至体外膜肺氧合(ECMO)治疗成了这次新冠疫情中大家关注的焦点。
究竟在什么时机选择恰当的呼吸支持手段特别是侵袭性手段呢?首先应该关注疾病严重度的分层,参照第七版新型冠状病毒肺炎诊疗方案。
COVID-19的临床分型
轻型是指临床症状轻微,影像学未见肺炎表现。普通型是具有发热、呼吸道等症状,影像学可见肺炎表现但无呼吸功能不全,这两型一般并不需要侵袭性诊治手段,本文主要关注重型和危重型,其分层依据主要围绕「呼吸功能」,包括呼吸频率、氧饱和度、氧合指数等。
重型,符合下列任何一条:
1、呼吸窘迫,RR≥30次/分;
2、静息状态下,指氧饱和度≤93%;
3、动脉血氧分压(PaO2)/吸氧浓度(FiO2)≤300mmHg (1mmHg=0.133kPa)。
-高海拔(海拔超过 1000 米)地区因根据以下公式对 PaO2/FiO2 进行校正:PaO2/FiO2 x [大气压(mmHg)/760]
-胸部影像学显示 24-48 小时内病灶明显进展 >50% 者按重型管理。
危重型,符合以下情况之一者:
1、呼吸衰竭,且需要机械通气;
2、出现休克;
3、合并其他器官功能衰竭需ICU监护治疗。
重型和危重型之间存在动态的演变过程,我们需要特别关注预警其转变的一些指标,以便抓住时机及时干预,在《新型冠状病毒肺炎诊疗方案》第七版中提出成人重型、危重型临床预警指标有:
1. 外周血淋巴细胞进行性下降;
2. 外周血炎症因子如IL-6、C反应蛋白进行性上升;
3. 乳酸进行性升高;
4. 肺内病变在短期内迅速进展。
一旦出现上述指标,临床医师就应该及时采取相应的干预措施,否则可能就会贻误时机。上述指标也反映了重型、危重型COVID-19绝不仅限于呼吸系统。
COVID-19是一种全身性疾病,几乎所有的系统都可能受到累及
在疫情早期,我们认为患者的病变主要集中在肺部,命名也是「肺炎」,随着对SARS-CoV-2病毒发病机制研究的不断深入,目前已经明确COVID-19是一种全身性疾病,2020年7月10日,《 Nature Medicine 》发文显示,呼吸、血液、心血管、肾脏、胃肠道、内分泌、神经、皮肤等几乎所有的系统都可能受到累及,而几乎所有的重症危重症患者均出现了多系统受累的证据。
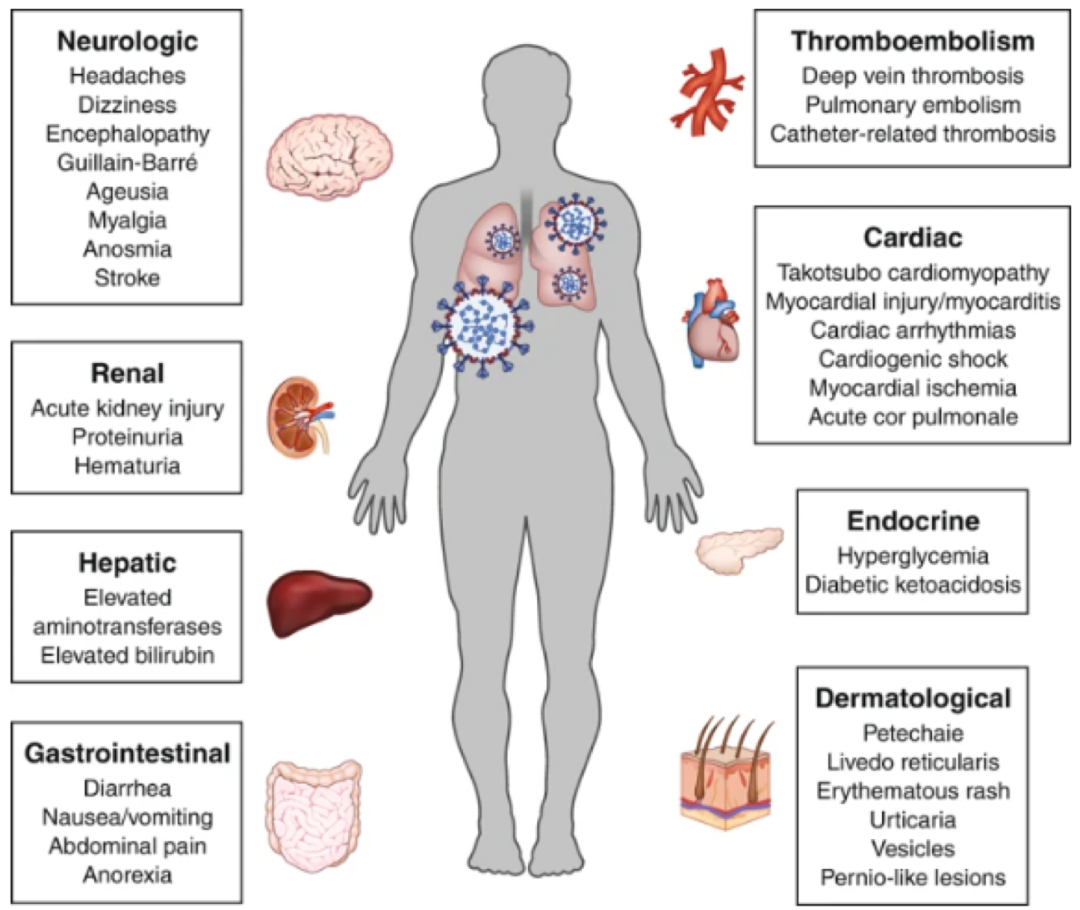
现有研究已经证实SARS-CoV-2通过其表面的刺突蛋白与ACE2相结合,在TMPRSS2的存在下进入宿主细胞。
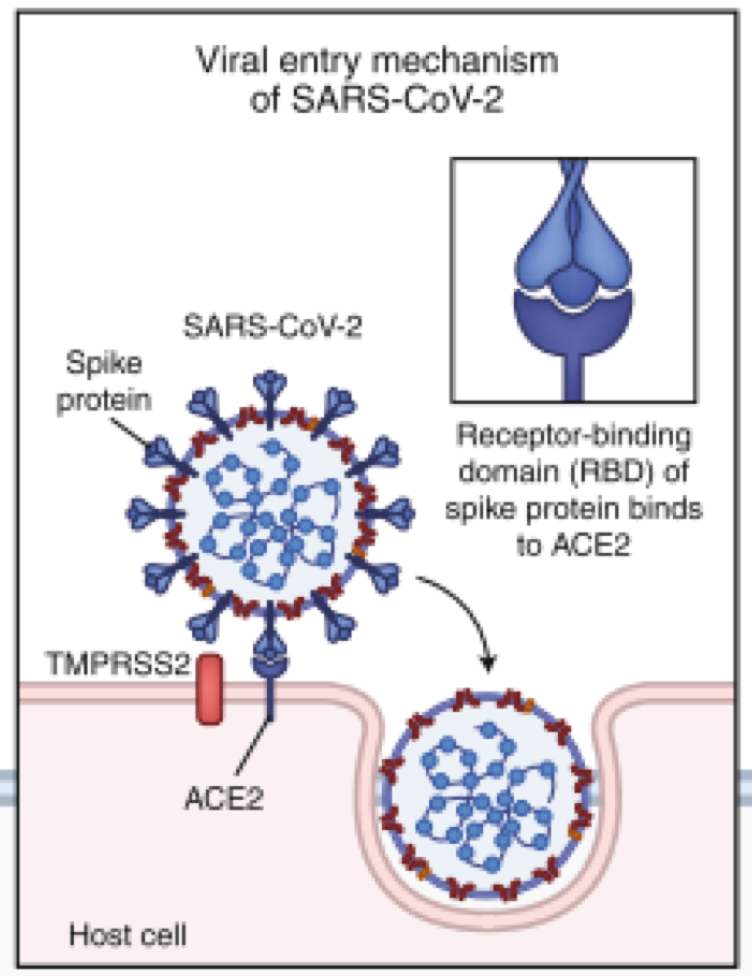
而人体血管、肾脏、肠道和呼吸道的内皮细胞都有大量的ACE2,因此病毒可以直接通过这些受体来感染相应组织和系统。ACE2在不同组织的表达水平见下图所示。
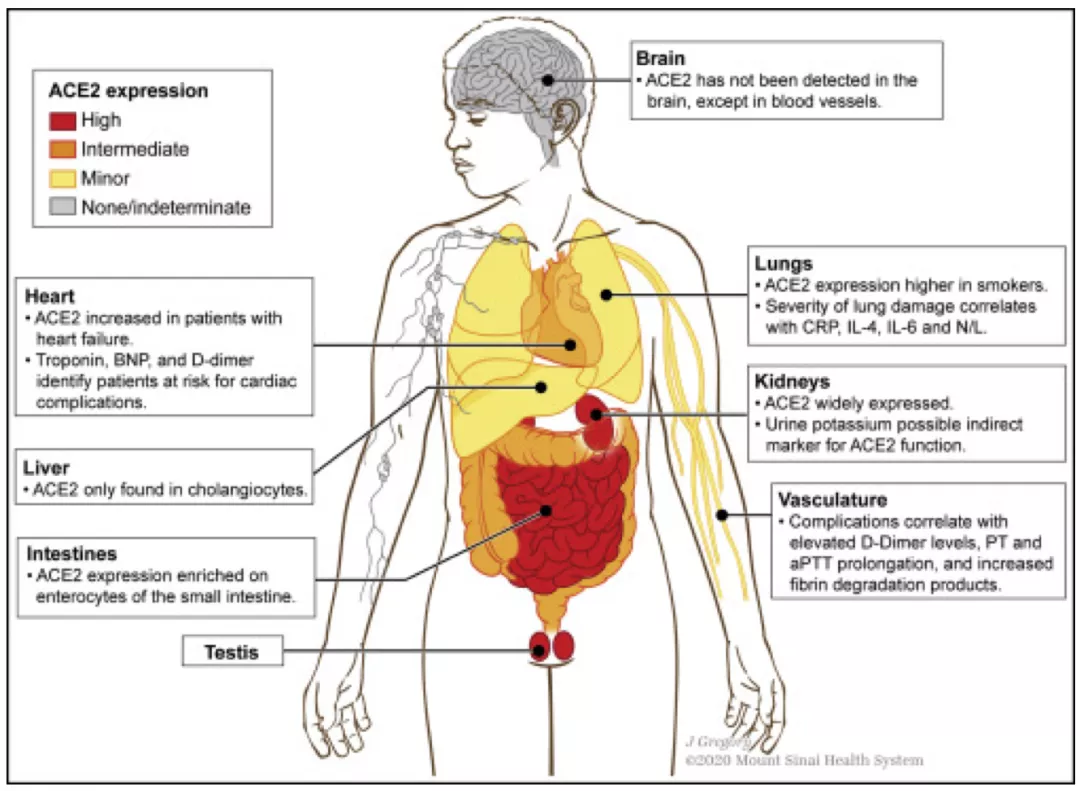
图中颜色越红的地方,ACE2的表达水平越高。相对而言,肺部并不算是最高的,肾脏、心肌、血管内皮细胞、性腺、胃肠道(尤其是小肠粘膜),这些部位都可能有很高的表达水平。而出现多系统受累的患者往往就已经是重症了。
SARS-CoV-2可能的发病机制提示关注相关生物标记物变化可以预测重症化
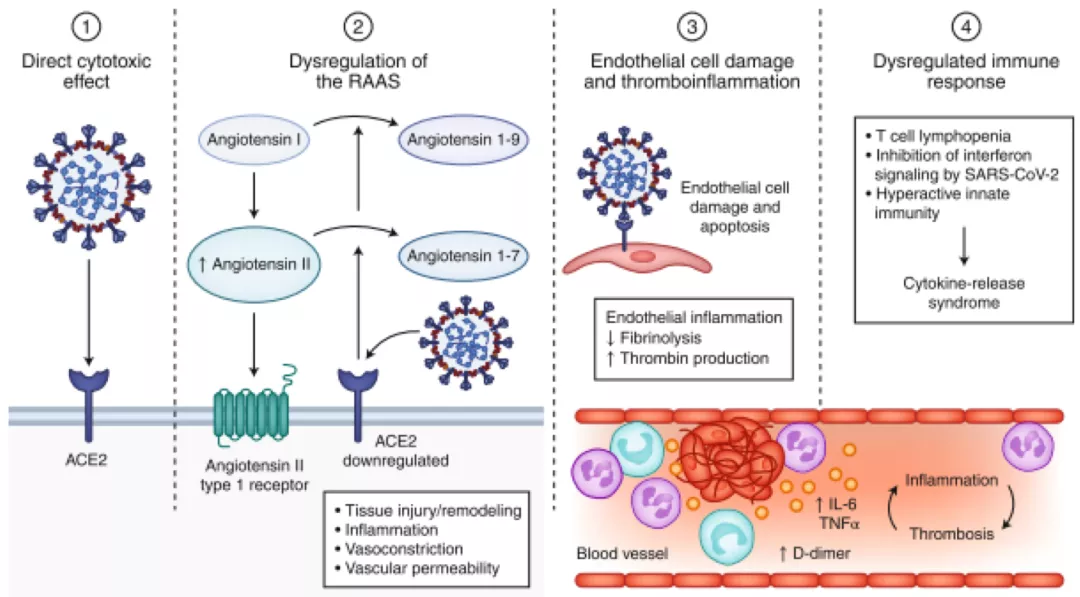
SARS-CoV-2可能有以下四个发病机制:1)病毒直接介导的细胞损伤;2)病毒通过相关的ACE2下调导致RAAS失调,从而导致血管紧张素 I 和 II 的转化减少;3)内皮细胞损伤和血栓性炎症;4)病毒抑制干扰素信号传导,T细胞淋巴消耗,产生促炎细胞因子,特别是IL-6和TNFα,导致免疫反应失调和过度炎症。这些损伤机制可能不会单独出现,当患者同时出现后两种情况时,就更可能出现重症、危重症,因此所谓要抓住时机,就要找到能提示血管内皮损伤和免疫炎症反应等关键指标,因为等到临床发现重要脏器功能衰竭的表现时可能就贻误时机了。
现有的研究显示,血液系统表现是比较便于监测的
淋巴细胞减少症是细胞免疫受损的标志,在严重的新冠肺炎患者中,CD4+T细胞和CD8+T细胞都大量减少。
SARS-CoV-2的入侵可使机体出现炎性细胞因子风暴,其中白细胞增多(尤其是中性粒细胞增多)被认为是感染SARS-CoV-2的高炎症反应的结果。
在感染的早期阶段,血液中D-二聚体和纤维蛋白原的异常高水平反映了过度的炎症。
中国和荷兰的重症监护室(ICU)首次报告了高达30%的患者出现血栓性并发症,在多个小型研究中,对患有新冠肺炎的危重病人进行常规的血栓性疾病筛查,结果显示,尽管有血栓预防措施,但这些患者的血栓性并发症发生率依然很高,从69%到85%不等。而且当感染SARS-CoV-2后,ACE2在内皮细胞中的表达增加,这可能会延续内皮炎症的恶性循环,促进血栓性炎症。
处理对策:根据国际止血和血栓学会的临时指南,建议在新冠肺炎患者住院期间进行白细胞计数、D-二聚体、凝血酶时间、纤维蛋白原等的检测,炎性标记物动态变化助于预测住院患者的临床结果和治疗反应:
心血管系统表现也值得关注,一些新冠重症患者可能会出现猝死
在疫情早期有一些并非重症患者出现猝死,让重症救护人员感到很困惑,是不是因为观察不及时还是治疗中有什么疏忽?其实由于ACE2在心血管组织中高表达,包括心肌细胞、成纤维细胞、内皮细胞和平滑肌细胞,故SARS-CoV-2可以直接损伤心血管组织;心肌损伤也有可能来自细胞因子风暴,表现为 IL-6、铁蛋白、LDH 和D-二聚体水平升高。SARS-CoV-2可引起直接的心血管并发症和间接的心血管后遗症,包括心肌损伤、急性冠状动脉综合征(ACS)、心肌病、急性肺心病、心律失常、心源性休克、血栓性并发症等。一项研究发现,当住院患者肌钙蛋白升高的频率和幅度较大时,病情严重性的几率就越大。在一项对中国武汉138例患者的研究中,17%的普通住院患者和44%的ICU患者发生心律失常。
死亡和存活患者住院期间
TnT和NT-proBNP水平的动态变化差异
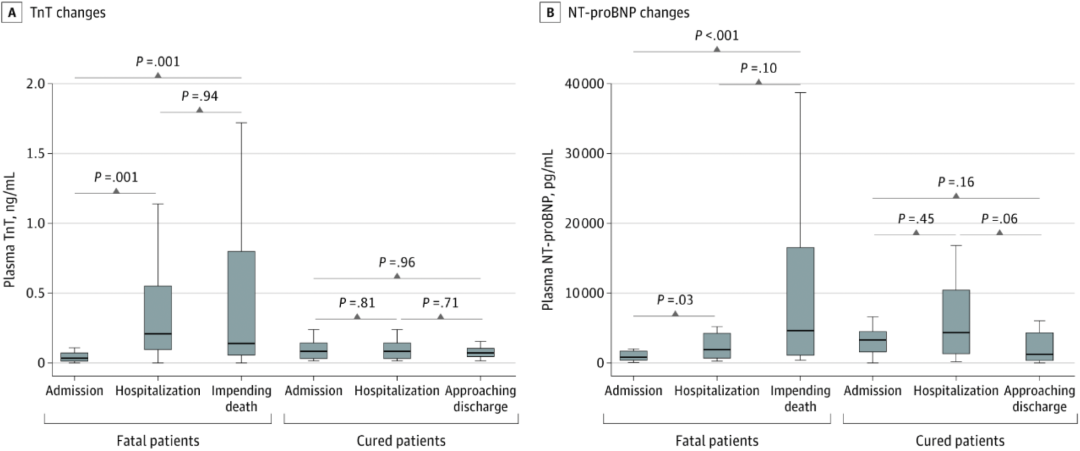
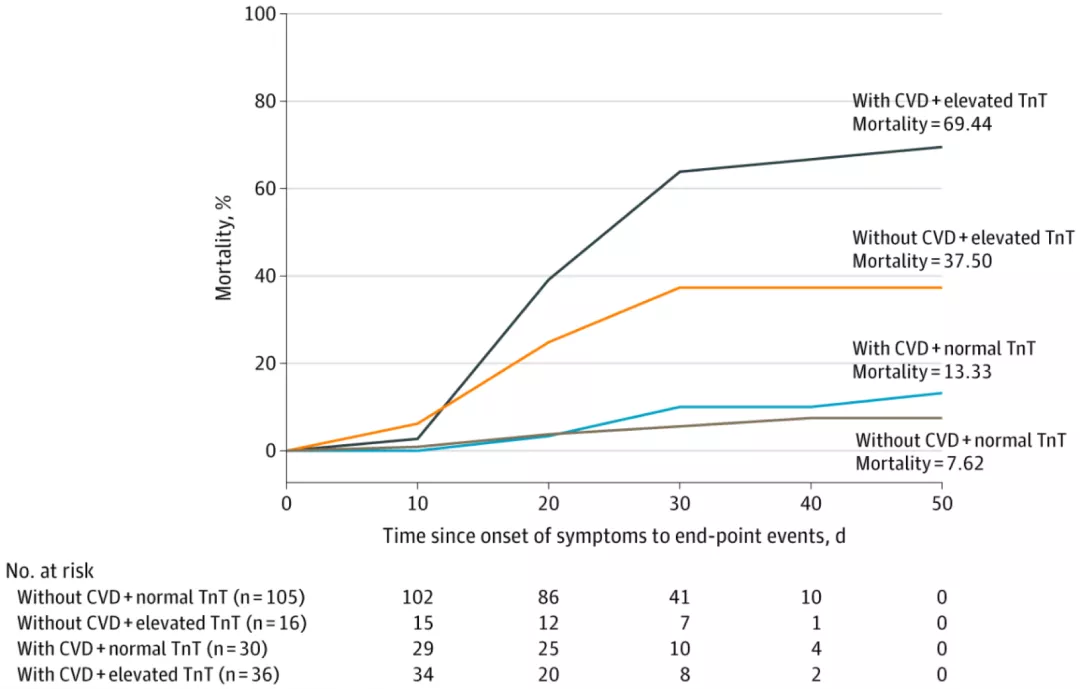
研究显示因COVID-19死亡患者住院后TnT和NT-proBNP水平明显高于治愈出院的患者,且既往有心血管疾病的患者出现TnT升高时死亡率高于无心血管疾病伴TnT升高的患者。
处理对策:对同时接受可延长QTc药物治疗的中高危患者进行心电图或遥测监测,在高危患者中考虑纤维蛋白溶解治疗,加强非侵入性血流动力学评估,检测乳酸、肌钙蛋白和β-三肽浓度,指导液体复苏、血管活性物质和机械循环支持。
在肾脏系统表现方面,急性肾损伤(AKI)也是新冠肺炎常见的并发症
据报道中国新冠肺炎住院患者AKI的发生率从0.5%到29%不等。一项来自三级教学医院701例新冠肺炎患者的研究,入院时出现蛋白尿者为43.9%、血尿26.7%、肌酐升高14.4%、尿素氮升高13.1%、GFR下降13.1%、AKI发生率5.1%。美国新冠肺炎住院患者的AKI发生率更高,纽约市医院系统对近5,500名新冠肺炎入院患者进行研究,发现有37%的患者发生AKI,其中14%的患者需要透析。在这项研究中,约有三分之一的患者在入院后24小时内被诊断为AKI。纽约市的另外一项研究中,257名入住ICU的患者中,31%接受了肾脏替代疗法(RRT)。此外,近半数的新冠肺炎患者有血尿的报道,新冠肺炎的危重病人中,蛋白尿的报道高达87%。新冠肺炎患者在终末期时,被诊断为肾病患者和需要肾移植者也越来越多。因此,临床医生应提高重症新冠肺炎患者对肾脏疾病的认识。 所有COVID-19患者入院时均应进行尿液分析和蛋白与肌酐比值的分析。
我们习惯于将COVID-19为新冠「肺炎」,但有些患者初始可能是以胃肠道系统表现为主
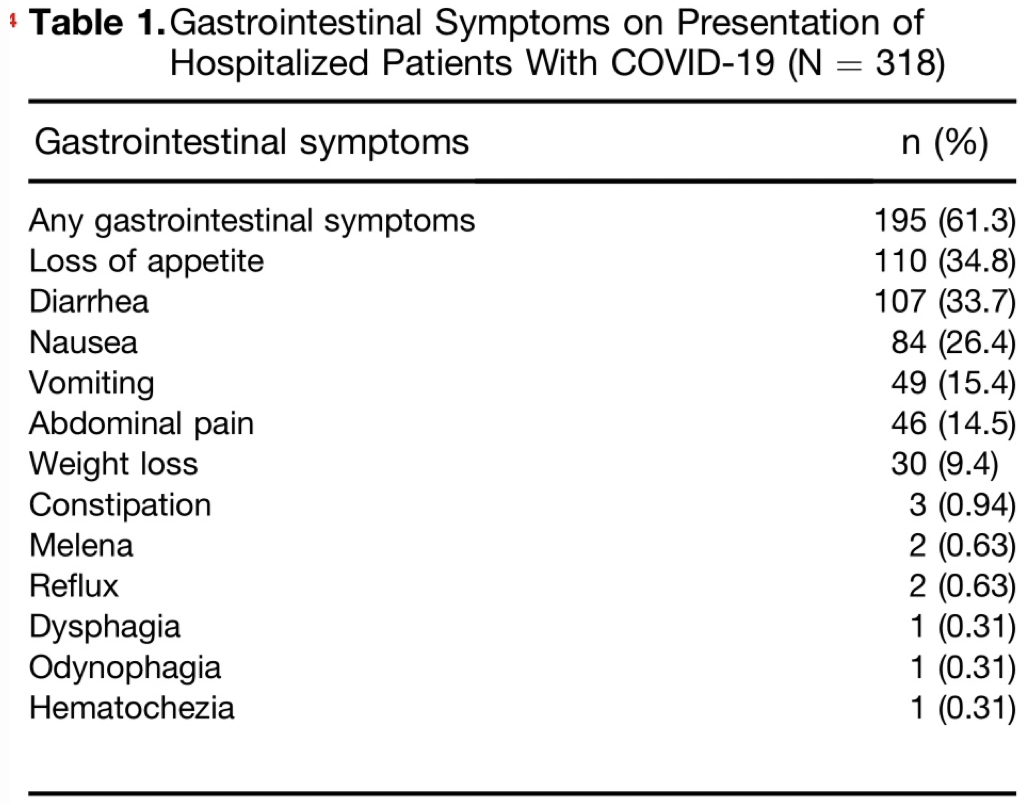
研究显示COVID-19患者胃肠道表现的发生率从12%到61%不等。
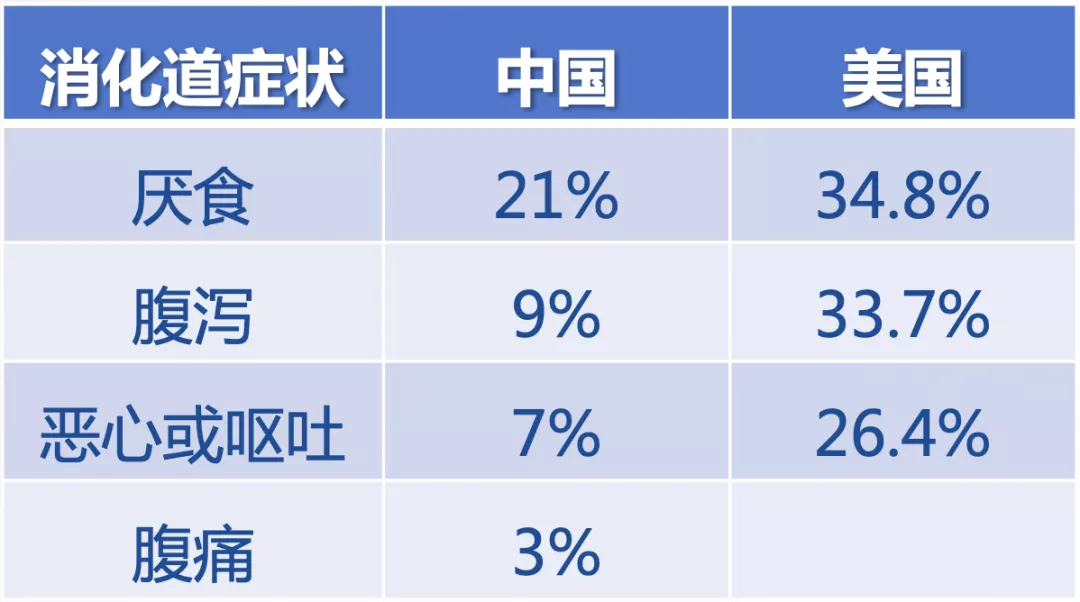
一项自美国的研究显示,胃肠道症状表现的发生率更高, 61.3%的新冠肺炎患者至少有1种胃肠道症状,有14.2%的患者的最初症状是胃肠道表现。
纽约市一家医院研究发现当检测者出现胃肠道症状时,新冠肺炎的检测风险增加70%。
因此,即使在没有呼吸道症状的情况下,胃肠道症状也应该被考虑作为新冠肺炎患者的鉴别诊断。在资源有限的情况下,除了呼吸道症状外,有腹泻或恶心或呕吐症状的患者应优先进行检测。如果检测资源匮乏,优先对同时出现呼吸道症状和胃肠道症状的患者进行新冠肺炎检测。
内分泌系统表现
患有糖尿病和/或肥胖症的患者感染新冠肺炎的风险更高。
在纽约市一家三甲医院中,对1150名新冠肺炎患者进行分析,发现在病情危重的257患者中,212名(82%)病人至少有一种慢性病,119名(46%)患者有肥胖症(定义为BMI≥30),92名(36%)的患者有糖尿病,表明肥胖症和糖尿病与新冠肺炎的严重程度和死亡率有关。
住院的新冠肺炎患者表现出一系列的糖代谢异常,包括恶化的高血糖、酮症和酮症酸中毒。
在一项来自中国的回顾性研究中,在658例新冠肺炎住院患者中,6.4%的患者在没有发热或腹泻的情况下出现酮症酸中毒。其中,64%的患者没有潜在的糖尿病(该组患者平均血红蛋白A1c水平为5.6%)。
神经系统表现
在一项研究中,对214例重症COVID-19患者进行分析,发现36%的患者出现神经系统症状。包括头痛(8-42%)、头晕(12%)、失眠(5%)和老年痴呆(5%)。
在发表在《脑》杂志上的一项研究中,该研究检查了43名在伦敦大学医院接受治疗的COVID-19患者,在这些患者中,研究人员发现有10例「暂时性脑功能障碍」、12例脑部炎症、8例中风和8例神经损伤。
大多数出现脑部炎症的患者会被诊断为一种特殊的、罕见的、有时是致命的疾病,即急性播散性脑脊髓炎(ADEM)。在大流行之前,伦敦的研究团队每月会看到大约一名ADEM患者。在研究期间,这个数字上升到每周至少一个。
新冠病毒大流行可能会引起脑损伤,因此对COVID-19患者后续研究将会很重要,以了解该流行病潜在的长期神经系统后果。
皮肤系统表现
新冠肺炎的皮肤病表现最早见于意大利的一项单中心观察性研究报道,在前2周无药物接触史的住院患者中发生频率为20%。皮肤病表现包括:皮肤尖锐湿疣病变(最常报告)、红斑性皮疹、荨麻疹、水痘样囊肿。约有44%的患者在发病时就有皮肤表现,而其余患者则是在病程中出现这些症状。最近有研究报道,在694名SARS-CoV-2阳性调查者中,有17%的患者皮疹表现为首发症状,而且在21%的患者中,皮疹是唯一的症状。
患者是一个整体,危重症患者的救治更需要整体观
新冠肺炎住院患者院内死亡风险的预测
为了将患者作为一个整体来观察,临床通常希望采用一些评价体系或评分系统来对疾病严重程度进行分层,以便及时采取相应的干预措施,避免错过时机。对社区获得性肺炎的严重性评估常用的有肺炎严重指数(PSI)、CURB-65、CRB-65、SMART-COP、PNEWS等,此外《日本成人社区获得性肺炎诊治指南》2017版中提出了A-DROP系统,可以看成是CURB-65的变异,但更适合老龄化社会。
A-DROP系统

武汉金银潭医院利用654名实验室确诊的新冠肺炎住院患者评估了多个严重程度评分预测院内死亡的准确性,研究发现A-DROP比其他评分预测准确性更高,更有效地评估患者的死亡风险。
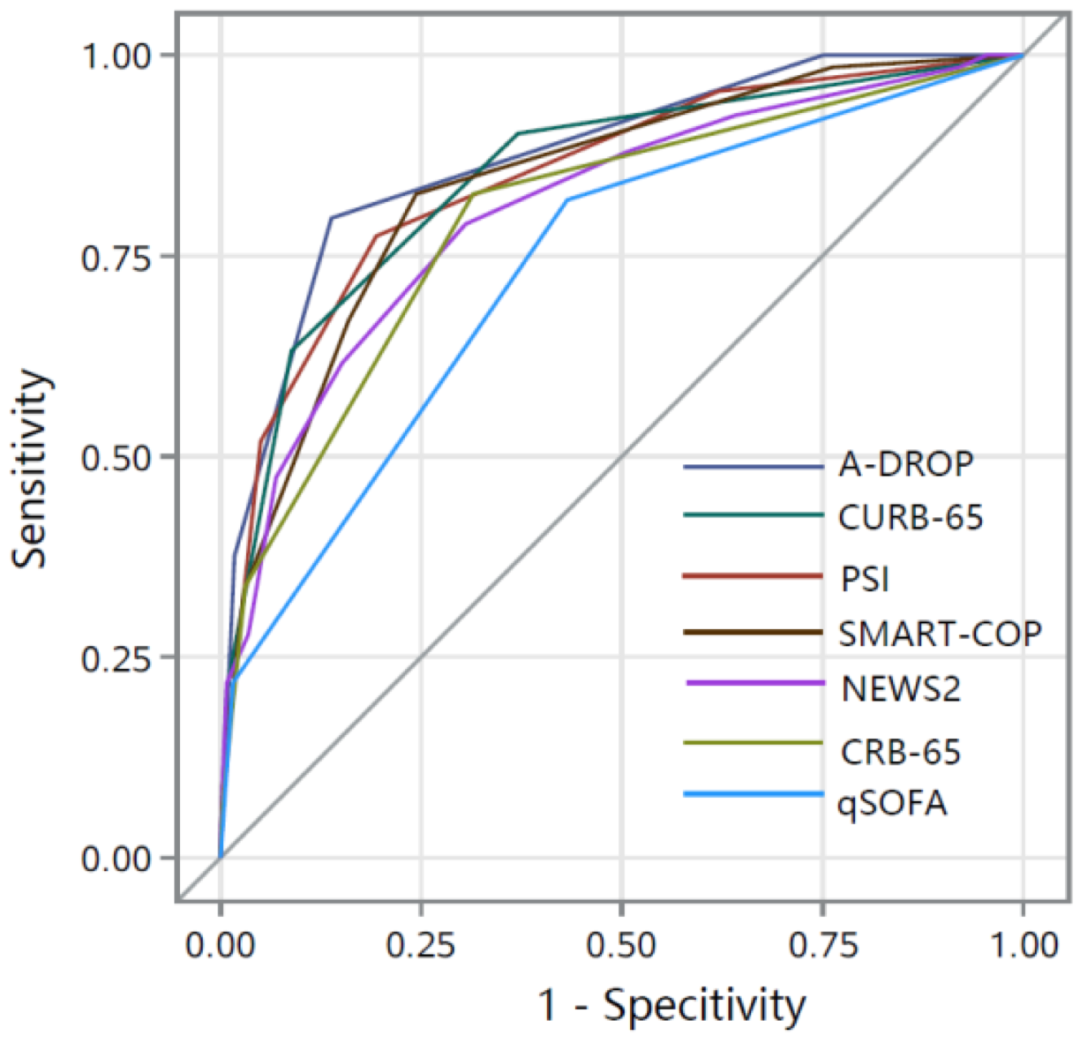
A-DROP与其他评分的优劣比较
CURB-65评分:更准确的呼吸功能评价(A-DROP :SpO2 < 90% / PaO2 < 60mmHg vs. CURB-65:respiratory rate ≥ 30/min);年龄分层更细致(A-DROP :male > 70/female > 75 vs. CURB-65:age > 65)
PSI评分:更侧重于基础病而减弱了呼吸功能的评价的权重,从而使其低估了新冠肺炎严重程度。
NEWS2评分:评估了呼吸频率、氧饱和度、收缩压、心率、体温和意识水平,在急诊室中也很容易评价,用于早期识别急性感染患者也行之有效。但NEWS2评分未考虑呼吸支持等级,因此其氧饱和度分级并不能准确反映低氧血症和肺损伤的严重程度。此外,还缺少其他器官功能障碍的评价指标。
科学评估早期发现COVID-19重症化趋势,及时采取侵入性诊治干预措施
1重症危重症COVID-19的治疗原则
在对症治疗的基础上,积极防治并发症,治疗基础疾病,预防继发感染,及时进行器官功能支持。
2呼吸支持
(1)鼻导管或面罩吸氧:重型患者应接受鼻导管或面罩吸氧,并及时评估呼吸窘迫和(或)低氧血症是否缓解,若效果不佳应及时采用更高强度的氧疗支持手段。
(2)高流量鼻导管氧疗或无创机械通气:当患者接受标准氧疗后呼吸窘迫和(或)低氧血症无法缓解时,可考虑使用高流量鼻导管氧疗或无创通气。若短时间(1-2 小时)内病情无改善甚至恶化,应当及时进行气管插管和有创机械通气。
(3)有创机械通气: 采用肺保护性通气策略,即小潮气量(6-8 ml/kg 理想体重)和低水平气道平台压力(平台压<30 cmH2O)进行机械通气,以减少呼吸机相关肺损伤。在保证气道平台压35cmH2O时,可适当釆用高PEEP,保持气道温化湿化,避免长时间镇静,早期唤醒患者并进行肺康复治疗。较多患者存在人机不同步,应当及时使用镇静以及肌松剂。
(4)挽救治疗: 对于严重 ARDS 患者,建议进行肺复张。在人力资源充足的情况下,每天应当进行 12 小时以上的俯卧位通气。
俯卧位通气效果不佳者,如条件允许,应尽快考虑体外膜肺氧合(ECMO)。其相关指征:① 在FiO2>90%时,氧合指数小于80mmHg,持续3-4小时以上;② 气道平台压≥35cmH2O。
单纯呼吸衰竭患者,首选VV-ECMO模式;若需要循环支持,则选用VA-ECMO模式。在基础疾病得以控制,心肺功能有恢复迹象时,可开始撤机试验。
3循环支持
充分液体复苏的基础上,改善微循环,使用血管活性药物,必要时进行血流动力学监测。密切监测患者血压、心率和尿量的变化,以及动脉血气分析中乳酸和碱剩余,必要时进行无创或有创血流动力学监测,如超声多普勒法、超声心动图、有创血压或持续心排血量(PiCCO)监测。在救治过程中,注意液体平衡策略,避免过量和不足。
如果发现患者心率突发增加大于基础值的20%或血压下降大约基础值20%以上时,若伴有皮肤灌注不良和尿量减少等表现时,应密切观察患者是否存在脓毒症休克、消化道出血或心功能衰竭等情况。
4肾功能衰竭和肾替代治疗
危重症患者的肾功能损伤应积极寻找导致肾功能损伤的原因,如低灌注和药物等因素。对于肾功能衰竭患者的治疗应注重体液平衡、酸碱平衡和电解质平衡,在营养支持治疗方面应注意氮平衡、热量和微量元素等补充。
重症患者可选择连续性肾替代治疗(continuous renal replacement therapy, CRRT)。其指征包括:①高钾血症;②酸中毒;③肺水肿或水负荷过重;④多器官功能不全时的液体管理。
5康复期血浆治疗
适用于病情进展较快、重型和危重型患者。用法用量参考《新冠肺炎康复者恢复期血浆临床治疗方案(试行第二版)》。
6血液净化治疗
血液净化系统包括血浆置换、吸附、灌流、血液/血浆滤过等,能清除炎症因子,阻断「细胞因子风暴」, 从而减轻炎症反应对机体的损伤,可用于重型、危重型患者细 胞因子风暴早中期的救治。
7免疫治疗
对于双肺广泛病变者及重型患者,且IL-6水平升高者,可试用托珠单抗治疗。首次剂量 4-8mg/kg,推荐剂量为400mg、0. 9%生理盐水稀释至100ml,输注时间大于1小时;首次用药疗效不佳者,可在12小时后追加应用一次(剂量同前),累计给药次数最多为2次,单次最大剂 量不超过800mg。注意过敏反应,有结核等活动性感染者禁用。
8其他治疗措施
对于氧合指标进行性恶化、影像学进展迅速、机体炎症反应过度激活状态的患者,酌情短期内(3~5 日)使用糖皮质激素,建议剂量不超过相当于甲泼尼龙 1~2 mg/kg/日,应当注意较大剂量糖皮质激素由于免疫抑制作用,会延缓对冠状病毒的清除;可静脉给予血必净 100 ml/次,每日 2 次治疗;可使用肠道微生态调节剂,维持肠道微生态平衡,预防继发细菌感染;儿童重型、危重型病例可酌情考虑给予静脉滴注丙种球蛋白。患有重型或危重型新型冠状病毒肺炎的孕妇应积极终止妊娠,剖腹产为首选。患者常存在焦虑恐惧情绪,应加强心理疏导。
再回到「时机」问题,《新型冠状病毒肺炎重症患者呼吸支持治疗和体外膜肺氧合临床应用指导方案(试行)》专门提到了临床预警指标:
重型和危重型患者,需要进行密切的生命体征、血氧饱和度(SpO2)、意识状态及临床常规器官功能评估。此外,以下指标变化应警惕病情恶化:
1. 低氧血症或呼吸窘迫进行性加重;
2. 组织氧合指标恶化或乳酸进行性升高;
3. 外周血淋巴细胞计数进行性降低或外周血炎症因子如IL-6、C反应蛋白进行性上升;
4. 胸部影像学显示肺部病变明显进展。
有创机械通气: 一般情况下,PaO2 /FiO2 小于150 mmHg,应考虑气管插管,实施有创机械通气。但鉴于重症新型冠状病毒肺炎患者低氧血症的临床表现不典型,不应单纯把PaO2 /FiO2 是否达标作为气管插管和有创机械通气的指征,而应结合患者的临床表现和器官功能情况实时进行评估。
值得注意的是,延误气管插管,带来的危害可能更大。气管插管的指征需要更加全面的评估和把握。
1、呼吸窘迫加重或吸气努力过强:实施HFNC或NIV治疗时,低氧血症无法改善(SPO2≤93%),或呼吸频数(RR≥35次/分)、潮气量过大(>9~10ml/kg 理想体重)或吸气努力过强等表现。
2、组织缺氧或乳酸进行性升高:实施HFNC或NIV治疗时,组织缺氧加重的表现,如乳酸进行性升高或中心静脉血氧饱和度(ScvO2)进行性下降等表现。
3、血流动力学不稳定或意识障碍:实施HFNC或NIV治疗时,仍然存在或合并意识障碍、休克时,立即开始有创机械通气治疗。
在实施无创通气时,气道的清理主要依靠鼓励患者通过自己的努力去咳嗽咳痰,一旦进行有创机械通气,必须重视和加强气道管理,应加强气道湿化,建议采用主动加热湿化器,有条件的使用环路加热导丝保证湿化效果;建议使用密闭式吸痰装置,必要时气管镜下冲洗吸痰;积极进行气道廓清治疗,如振动排痰、高频胸廓振荡、体位引流等。在氧合及血流动力学稳定的情况下,尽早开展被动及主动活动,促进痰液引流及肺康复。
ECMO启动时机也非常关键,延误治疗时机,导致患者预后不良。目前认为在最优的机械通气条件下(FiO2≥0.8,潮气量为6 ml/kg理想体重,PEEP≥5 cmH2O,且无禁忌症),保护性通气和俯卧位通气效果不佳,并符合以下之一,应尽早考虑评估实施 ECMO:
1. PaO2/FiO2<50 mmHg超过3小时;
2. PaO2/FiO2<80 mmHg超过6小时;
3. 动脉血pH<7.25 且PaCO2>60 mmHg超过6小时,且呼吸频率>35次/分;
4. 呼吸频率>35次/分时,动脉血pH<7.2且平台压>30 cmH2O或驱动压 > 15cmH2O;
5. 合并心源性休克或者心脏骤停。
符合ECMO指征,且无禁忌证的危重型患者,应尽早启动ECMO治疗。
总体来讲,为了正确把控重型及危重型COVID-19侵入性诊治的最佳时机,我认为首先要对发病机制有深刻了解,为何在疫情爆发早期治疗失败率高,一方面可能与医疗资源发生挤兑有关,更重要的是可能与初期对SARS-CoV-2的致病机制不了解有关;第二,要在了解发病机制的基础上进行科学量化评估,通过各类评估系统及相关生物标记物的监测,争取提前介入恰当的干预手段,尽量避免重症趋势。在侵入性诊治策略,一般通常是从无创到微创,再到有创,要循序渐进、把握时机,但同时也警惕过犹不及。
专家介绍

黄怡
海军军医大学第一附属医院(上海长海医院),呼吸与危重症医学科教授、主任医师、博导。中华医学会呼吸病学分会感染学组委员兼秘书,上海市医学会呼吸病学分会委员感染学组组长。主要研究方向为下呼吸道感染诊治、抗菌药物合理应用等问题。曾获教育部科技进步一等奖1项,军队医疗成果一等奖1项、二、三等奖各2项,军队科技进步奖三等奖1项,上海市医疗成果三等奖1项。获军队院校育才银奖和第二军医大学特级优秀教师。获「十一五」、「十二五」国家科技重大专项和「十三五」重大研发项目等各类科研基金资助,总协调完成多部我国有关肺炎诊治相关指南的更新,发起并牵头完成我国首部实体器官移植供者相关感染防控专家共识,发表SCI收录论文十余篇,核心期刊二十余篇,主编专著两部,参编二十余部。
本文由《呼吸界》编辑 Jerry 整理、排版,感谢黄怡教授的审阅修改!



