肺泡蛋白沉积症(pulmonary alveolar proteinosis, PAP)[1] 是一种罕见的疾病,其特征为酯蛋白类的物质会沉积在肺泡中,以及肺泡巨噬细胞的表面活性剂生成受损。尽管PAP的发病机制并不完全清楚,越来越多的研究者认为,嵌合抗B细胞单克隆抗体或单核粒细胞集落刺激因子用于自身免疫性PAP患者时,可以治愈PAP。
然而,对于PAP来说,全肺灌洗(whole lung lavage, WLL)疗法在手术室是最有效和常用的方法。案例报告和研究表明支气管肺泡灌洗(bronchoalveolar lavage, BAL)是一种有效的替代治疗方式。但在PAP合并严重低氧血症时,单纯的WLL或BAL可能难以达到满意的治疗效果。
我们提出一个在重症监护室(intensive care unit, ICU)中应用的WLL-BAL联合治疗策略,对一位氧合指数为93mmHg的中年女性进行治疗,取得了成功。这一策略包括几种技术:BAL,WLL,机械通气,俯卧位通气,双腔气管插管,脉波指示剂连续心排血量监测 (pulse index continuous cardiac output, PICCO)指导下的液体管理。这一治疗策略可能适合呼吸储备极其有限,不允许进行全肺灌洗灌洗的患者,并能提高治疗过程的安全性。
临床资料
患者,女,32岁。主因「干咳,气短9个月,加重1个月」入院。9个月前无明显诱因出现干咳、气短症状,未予重视。1个月前症状加重,无发热、胸痛,无恶心、呕吐,无咳痰,无腹痛,无晨僵等。先后就诊于多家医院,诊断为「肺间质纤维化」,给予激素及抗生素治疗1月,效果不佳。既往甲状腺功能减退症病史10余年,闭经10余年,无生育史,无月经,无过敏史,家族无类似病患。
入院查体
体温 35.5℃,脉搏 84次/分,呼吸 34次/分,血压 127/75mmHg,营养中等,发育差(身高 130cm,体重 40kg),神志清楚,黏液性水肿面容,喘息貌,双肺管状呼吸音,左下肺可闻及湿性啰音。心脏、腹部查体无异常。乳房未发育,无腋毛、阴毛,双下肢轻度指凹性水肿。
入院时辅助检查
肺CT(2015年6月8日,图1)示两肺弥漫性病变,两侧胸膜增厚,甲状腺密度减低。血气分析(2015年6月16日):pH 7.444,PO2 55.8mmHg,PCO2 45.2mmHg(面罩 8L/min),氧合指数 93mmHg。血常规(2015年6月17日):白细胞10.79×10^9/L,血红蛋白149g/L,血小板122×10^9/L;甲功检测(2015年6月17日):FT4 44.9pmol/L。垂体激素六项(2015年6月17日):FSH 87.17mIU/ml;皮质醇及促肾上腺皮质激素未见明显异常。自身抗体(2015年6月17日):阴性。
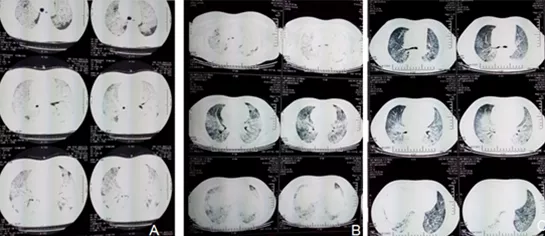
【图1】2015年6月8日肺CT表现
入院后给予抗生素升级并高流量吸氧,低氧血症及气短进一步加重,给予有创通气,并行诊断性纤维支气管镜下灌洗。回收灌洗液PAS染色阳性。在不间断机械通气状态下(PEEP 4cmH2O,FiO2 100%)进行支气管肺泡灌洗3分钟,即出现氧合下降,SpO2由92%降至80%,给予呋塞米、加强镇静,增加PEEP后SpO2逐渐上升至92%(FiO2 100%)。鉴于患者氧储备能力极差,无法耐受WLL,治疗方案修订为联合治疗策略,即小量多次BAL+单肺通气下WLL+PiCCO监测下的液体管理。
1 持续有创通气下的BAL
BAL时通气参数 P A/C模式 (IP 20cmH2O,PEEP 4cmH2O,FiO2 100%,SpO2 92%)。患者深度镇静,直径4.9mm纤维支气管镜经7#气管插管进入,逐个嵌顿在肺亚段开口,以37℃生理盐水每次50ml实施灌洗,反复经气管镜注入亚段并吸出,直至该肺段灌洗液转为清亮。BAL的灌洗次数与持续时间取决于患者的耐受性。BAL后呋塞米注射、肺复张和俯卧位通气会有助于低氧血症和肺水肿的恢复。对本例患者实施过包括俯卧位通气状态下BAL共6次(图2,图3),每次总灌洗量为100-1000ml,回收量60-620ml之间,时间跨度8天。在完成6次BAL后,肺部顺应性由14 mL/cmH2O升至19 mL/cmH2O,肺CT表现较前有所好转,通气参数较前降低(IP 16cmH2O,PEEP 10cmH2O,FiO2 40%,SpO2 97%)。

【图2】持续俯卧位通气下BAL
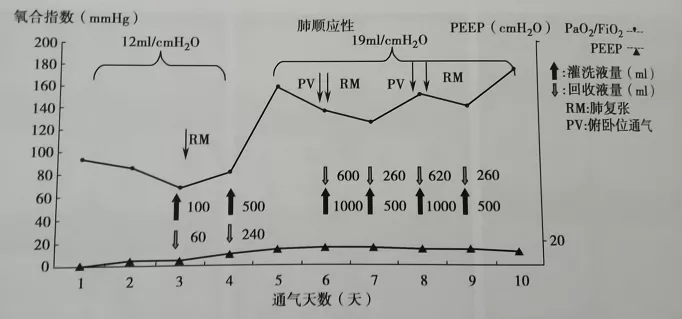
【图3】通气前后动脉血气分析、肺顺应性及PEEP变化
2、双腔气管插管和单肺通气
7#单腔气管插管更换为7#双腔气管插管,并经单肺通气5分钟,患者生命体征稳定。
3、WLL和液体管理
选择病变较重侧左肺为首次WLL灌洗肺,实施单肺通气,全麻状态下,以37℃生理盐水进行灌洗,以吸痰管辅以胸部震荡回收灌洗液,灌洗入3500ml,回收1500ml。WLL后,再次出现FiO2上升至100%,指氧下降至82%,PiCCO监测示血管外肺水指数(extravascular lung water index ,EVLWI) 34,心指数(cardiac index ,CI) 3.9, 全心舒张末期容积指数(global end diastolic volume index ,GEDVI) 676,在保证基础心排血量的情况下大量利尿,配合呼吸机参数调节,氧合情况逐渐恢复,EVLWI降至26。
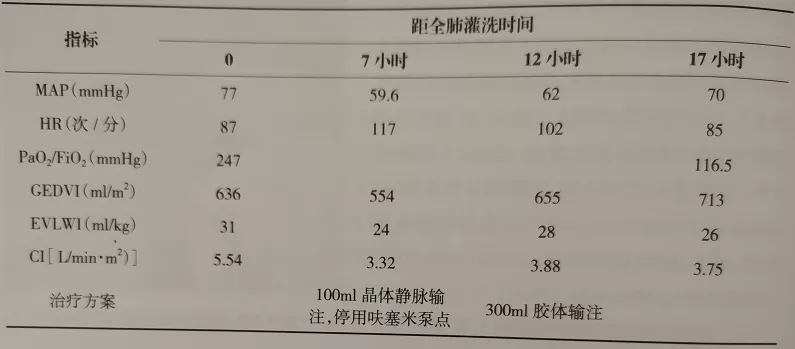
在第2次左肺灌洗前即开始呋塞米泵点10mg/h,总灌洗量5500ml,回收3800ml,低氧血症程度较前次弱,SpO2仅降至88% (FiO2 80%)。但仍出现休克,并根据PiCCO指导液体复苏(表1)。第3次对右肺进行灌洗,总灌洗量11150ml,回收9500ml。3次灌洗结束后,肺顺应性升至28mL/ cmH2O,呼吸机支持IP 14 cmH2O,PEEP 8cmH2O, FiO2 40%, SPO2 95%。拔出双腔管更换为单腔管,8天后拔除气管插管序贯无创通气,复查肺CT较前好转。6天后出院。
【表1】第2次灌洗根据PICCO指导液体复苏
讨论
文献报道应用体外膜肺氧合技术联合治疗极严重PAP合并严重低氧血症患者,效果显著[2]。但在发展中国家的绝大部分医院,由于各种条件的限制,上述方案难以实行。在此种情况下,BAL-WLL联合策略可能是治疗此类疾病的又一选择。
该患者在灌洗过程中存在由于灌洗液回收量偏低,出现外源性肺水肿的情况,应用PiCCO监测可以观察到血管外肺水指数明显上升,氧合指数下降,在应用相应治疗措施后患者临床情况明显改善。这提示该项指标能够反映此类因素(如淹溺)造成肺水肿的严重程度,并能通过改善血管内胶体渗透压、利尿剂、肺复张及高PEEP改善患者氧合状态。
参考文献
[1] Trapnell,BC,Whitsett JA,Nakata K. Pulmonary alveolar proteinosis. N Eng J Med,2003,349 (26):2527-2539 .
[2] Noirez L, Koutsokera A, Pantet O, et al. A 3-step therapeutic strategy for severe alveolar proteinosis. Ann Tho Surg,2015,99 (4),:1456-1458 .
作者: 徐海博、阎锡新 - 河北医科大学第二医院呼吸一科
本文转载自订阅号「重症与康复」(ID:CriticalAndRehabCare)
原链接戳:病例集锦47 | 肺泡蛋白沉积症合并重度低氧血症——联合治疗策略


