小细胞肺癌在肺癌中约占15%左右,呼吸与危重症医学科为其首诊科室,我们常在临床中碰到这样的患者。小细胞肺癌分两种类型,一种是局限期小细胞肺癌,一种是广泛期小细胞肺癌。小细胞肺癌的特点是化疗敏感性高,化疗有效率可达50%-80%,但患者大多在化疗有效后约3-5个月发生进展,复发是小细胞肺癌最 令人头疼的问题,其总生存时间小于1年,约为10个月左右。
整个治疗过程中他都一直迫切希望能有靶向药物,我们想尽办法也就延长了他 4 个月寿命……「近期疗效好、总体疗效差」是小细胞肺癌目前的现状和局面
我曾经碰到一个患者,他是一家工厂的一把手,42岁,经济条件优越,生存意愿非常强,整个治疗过程中他都一直希望有一种靶向药物能够治疗他的疾病。他首次就诊是源于左下肺块影,支气管镜病理示小细胞肺癌,全身评价为局限期。我们先给予化疗4疗程,随后进行放疗,结束后再加入化疗2疗程。患者治疗结束后进入随访。非常遗憾的是,当随访到第3个月后,患者出现咳嗽症状,同时全身再次评估发现脑转移。患者本属于局限期,治疗6个月后发展成广泛期。之后,尽管我们加化疗、脑部放疗,想尽办法,也就只多延长了患者4个月生存期。化疗到最后,患者血小板非常低,最终去世。临床中我们碰到过很多这样遗憾的例子。小细胞肺癌在最近20年一直没有太多进展,多以放化疗为主的综合治疗,患者长期生存很难,化疗后副作用很大,缓解时间、维持时间特别短。
诊治方面,我们以往探讨主要为三个方面,第一是增加化疗的剂量强度,希望化疗更「狠」一点,患者缓解时间会长一点;第二是尽早结合放疗。比如化疗完后立即放疗,或者同步放化疗;第三是再次进展后进行多线治疗。但很多患者二三线治疗时效果很差,即使多线治疗,仍总生存改善有限。因此,「近期疗效好、总体疗效差」就是小细胞肺癌目前的现状和局面。
这个患者确诊时间是2018年9月,到现在已整整两年……肺癌的诊治,需要多学科的合作、个体化治疗,动态评估,有可能会延长部分患者生存期
面对肺癌的诊治,我们一定需要多学科合作。先举一个非常典型的例子:今天上午门诊复诊的一个病人。该病人是一个58岁的局限期小细胞肺癌,女性。初诊时表现为右肺结节,经皮穿刺活检确诊,没有胸水,只有肺部病灶。一个疗程化疗后就序贯放化疗,结束后转入我科维持化疗,总共6疗程化疗。患者确诊时间是2018年9月,到现在已整整两年。现在患者出现咳嗽比以前多,有胸闷,肺部CT复查有转移,我们准备开始为下一步治疗创造条件。虽然我们不知道到底哪一类局限期患者将获益更多,但从整个过程看,多学科合作、放化疗的结合,有可能会延长部分患者的生存期。因此我们能否从病理表现细微区别小细胞肺癌疗效好与疗效差的原因。这样的结果也说明,并非所有小细胞肺癌获益都很差,经过规范化治疗,确实有一部分患者生存期可延长到两年以上或者更长。
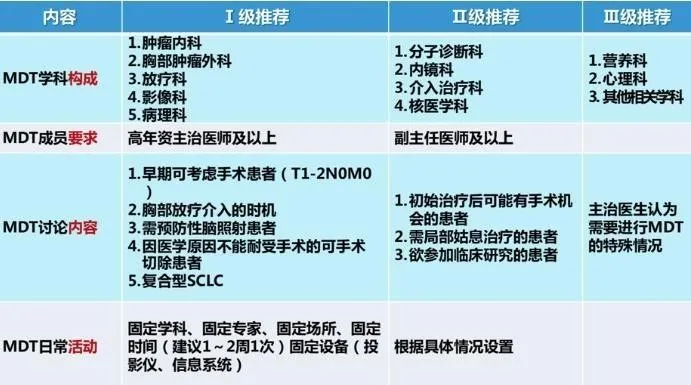
小细胞肺癌的特点决定了实施多学科MDT的重要性:
1、小细胞肺癌异质性、侵袭性强,与其他肿瘤相比,小细胞肺癌诊治过程中更应重视多学科团队的作用;
2、小细胞肺癌MDT 实施的目的:由多个学科的专家共同分析患者的病史、临床表现、影像学、病理学和分子生物学资料等,对患者的一般情况、疾病诊断、分 期、发展趋势和预后做出全面的评估,结合患者治疗意愿等制定个体化的整体治疗策略;根据治疗过程中患者体能状态的变化、治疗疗效、适时调整治疗方案,最大化延长患者生存、提高治愈率和改善生活质量。
多学科合作的意义体现在三个方面:
第一、肺癌的诊断一般都在呼吸与危重症医学科,呼吸学科的优势是可以利用多种诊断技术对肺癌进行分型。比如小细胞肺癌,我们可以了解它与肿瘤里浸润淋巴细胞之间到底占比多少?有没有PD-L1上的表达?病理组织里面微血管密度怎样?在诊断方面,我们迫切需要更细化,尤其对类型进行更详细化的分型,不能笼统为一型,针对不同分类会有不同的治疗,而这些都需要病理科进行细化分类为多学科合作创造条件;
第二、及时发现早期阶段的小细胞肺癌,需要胸外科先进行手术以后再辅助化疗,以使得患者生存得到改善;
第三,局限期小细胞肺癌通过化疗缩小后,需要对原发灶进行根治性放疗,这需要放疗科参与。除此之外,围绕患者的其他方面问题,也需要其他学科的参与,比如患者可能有其他合并症,如血液学毒性处理等还需要血液科的参与。多学科合作得越好,病人的预后越好,这是非常重要的。
目前我们医院正在做一些探索,以往的小细胞肺癌我们常与放疗科、胸外科合作,早期时请他们先做手术,我们再负责化疗。局限晚期先化疗一个疗程,再加同步放化疗,最后再化疗维持。这样的确让小细胞肺癌在中位生存率有所改观,与国际国内局面一致,中位生存期为10个月左右。随着免疫治疗进入临床,我们应该还能做得更好,尤其对广泛期小细胞肺癌,可以进行更多探索。
IMpower133研究取得的革命性、创新性的突破……较好的安全性,让阿替利珠单抗在临床中可以有更好的应用,希望可以惠及更多患者
对于局限期小细胞肺癌的治疗,目前治疗方案变化并不大,但对于广泛期小细胞肺癌的一线治疗,伴随着IMpower133研究结果发布,带来一线治疗方案的重大更新。
IMpower133研究是首次在ES-SCLC一线治疗中显示出较当前标准治疗有显著OS改善的研究。根据此研究结果,2019.V1 NCCN SCLC指南列入一线治疗推荐;2020年2月获我国国家药监局(NMPA)适应症审批;今年6月我国CSCO指南推荐「Atezolizumab + 依托泊苷/卡铂」作为广泛期SCLC一线治疗的Ⅰ级推荐(优选,1A类证据)。
这项研究的设计是随机双盲和双终点,一组是安慰剂组(依托泊苷和卡铂),一组是阿替利珠单抗加上依托泊苷和卡铂,四个周期治疗之后,两组分别用安慰剂或者是阿替利珠单抗进行维持治疗直到病情进展。两组试验组和对照组的基线水平,包括脑转移、肝转移以及病人的一般情况相似。

IMpower133研究是免疫治疗在小细胞肺癌方面取得的重大突破。它具有多方面的意义:
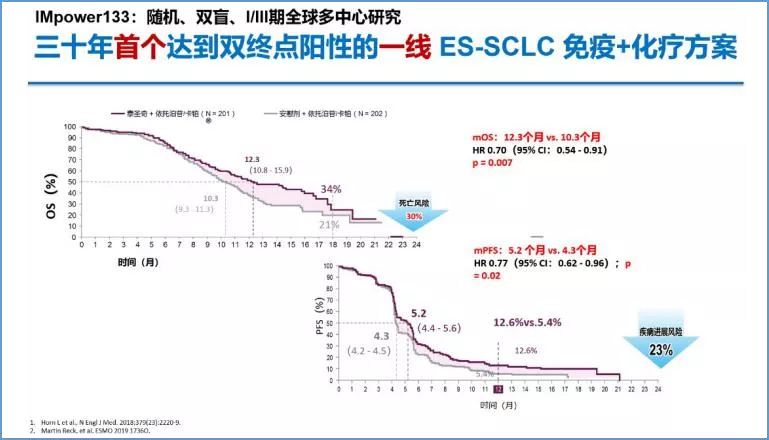
第一,从研究公布的结果,我们发现化疗与免疫结合带来了生存期的延长,拖尾效应在研究中很明显。研究组中位OS是12.3个月,对照组10.3个月,从表面上看,他们之间的中位OS只相差两个月,但从图像上看,这两组到了一年及一年以后两条曲线分得更开,有51.7%的患者,即超过一半的患者中位OS时间超过1年,从这一点讲,它具有里程碑式的意义,总死亡风险可降低30%;
第二,获益更好。因为PFS率得到了改善。除OS以外,还有一个研究者评估的PFS作为另外一个主要终点,分别是5.2个月对比4.3个月,虽然我们看到的是绝对值差别并不大,但如果能够体会到免疫治疗对于小细胞肺癌的长期获益,会看到12个月的PFS率,是12.6%对比5.4%,两组之间的差异很明显。
因此,小细胞肺癌有免疫治疗的加入,最大优点在于小细胞肺癌患者整体人群中位生存超过1年及1年以上生存率比例广泛提高。因此说小细胞肺癌进入了免疫时代。从它的亚组分析还发现,如果是没有脑转移及肝转移的患者,获益会更好,这对临床有很多启示意义。
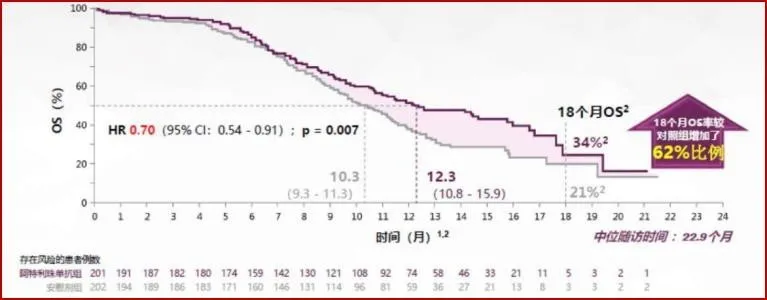
第三,通过长期随访会发现有1/3的患者生存时间超过18个月,即34%患者超过18个月OS。从这个数字讲,对于临床医生是个很好的信心,毕竟广泛期小细胞肺癌化疗时代非常难以达到18个月以上的生存;
第四、从安全性看,治疗手段增加,不良反应的几率增高有限。首先可以看到在试验组当中,免疫治疗加入后并没有产生新的不良事件。EP方案联合免疫和不联合免疫,5级副反应的增加几乎没有。在3-4级不良反应当中,与单纯化疗相比相差不多,没有显著性差异,致死性副作用几乎没有。
现在我们临床使用阿替利珠单抗联合化疗真实情况疗效看效果非常好,副作用非常小,这也给我们带来信心,创新性的研究和突破在临床中得到应用。小细胞肺癌人群少,治疗难度大,阿替利珠成为唯一一个NMPA获批的治疗小细胞肺癌的PD-L1,填补了小细胞肺癌免疫治疗的空白,也希望未来能尽快进入国家医保,让更多的患者能够有条件使用上。
PS 评分与肿瘤侵犯位置有关,肿瘤转移引起的、状况并未达到,则不能评估 3 分,因为 3 分是化疗的禁界
说到小细胞肺癌的内科治疗,根据患者分期、分层从而采取不同的治疗方案,在分层中,PS 评分决定患者治疗方案起着非常重要的作用。在临床实践中,评估PS 评分时,临床医师该注意哪些?如何才能比较准确地评估 PS 评分,从而确保能给患者制定最适合的治疗方案?
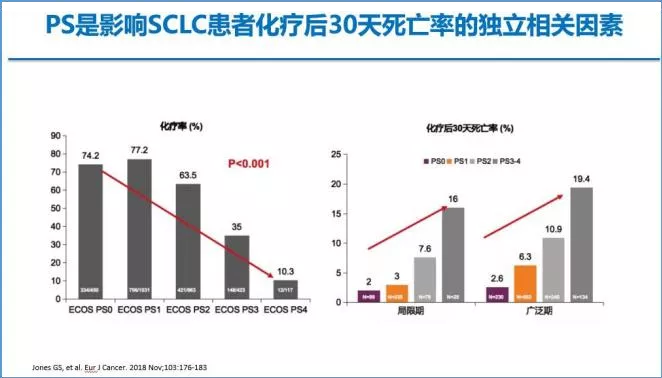
首先,PS评分对决定患者治疗方案是非常重要参考因素,不管是局限期小细胞肺癌还是广泛期小细胞肺癌,PS评分是影响小细胞肺癌患者化疗后30天死亡率的独立相关因素。
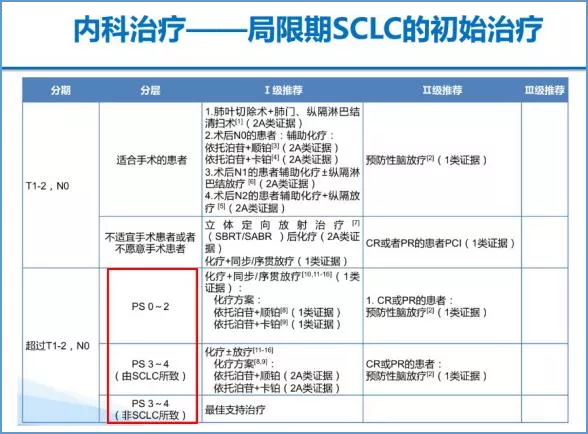
局限期小细胞肺癌的初始治疗,除了能手术的患者外,对于超过T1-2、N0者:如果患者的PS评分较好(0-2),优先推荐EP/EC方案化疗同步或序贯放疗;
如果患者PS评分3-4(小细胞肺癌所致),推荐EP/EC方案化疗,并酌情考虑联合或不联合放疗;如果患者PS评分3-4分(不是小细胞肺癌所致),不建议化放疗,仅建议最佳支持治疗。
对于广泛期小细胞肺癌的初始治疗,对于无局部症状且无脑转移患者,对于PS 0-2分,或者由于小细胞肺癌所致的PS评分3-4分患者,可以一线使用化疗联合免疫治疗;而对于不是小细胞肺癌所致的PS评分3-4分患者,则建议最佳支持治疗。
实际上,PS评分是根据患者的活动状况,比如能否起床、能够从事集体劳动或日常活动等来做评分的,它与肿瘤侵犯的位置有关系,比如侵犯活动的位置是腰椎,患者起身就不容易,所以他总是睡在床上,因此按照卧床时间超过50%,评分就是3分。关键点是评分要与病人是否为肿瘤引起的要区别对待,如果是肿瘤转移引起的,状况并没有达到这个状况,不能认为它为3分。因为3分是化疗的禁界。
对PS评分,我建议最好泛化一些,结合患者其他情况,比如营养、饮食,以及内脏功能如何?不能光靠评分。如果患者心脏有明显的化疗或者免疫禁忌症,都是非常重要的问题。一个广泛期小细胞肺癌患者,一般至少可以把PS评分分成两种,第一种是肿瘤引起的PS评分下降,是肿瘤累及部位相关,把肿瘤控制好了它就能改善;第二种是癌症患者的全身状况衰竭,如果是以往长期经历导致身体状况差,上化疗免疫就特别困难。如果是肿瘤侵犯某个位置造成患者的体位或者是活动受限,我认为通过治疗完全可以改变。因此要告诉大家,要根据不同的情况做适当的处理,需要丰富的经验,最好是多学科讨论,再结合治疗,努力改善患者状况。
肺部放疗必须排除有肺气肿、肺大泡、肺功能严重损害,上免疫治疗后建议3周期后再上放疗……积极推动基层慢阻肺和肺癌「双筛查」
在免疫一线治疗的背景下,又应该如何看待免疫治疗联合放疗的疗效和安全性呢?
首先,对于免疫联合放疗的合理合法性依据:我们看到IMpower133研究中,允许了预防性脑照射(PCI)的应用,安全性AE无增加,但基于研究中样本量并不大(44 例),入组患者PS评分也比较好,所以在临床实践中还是要密切关注患者的不良事件。IMpower133研究给我们提供了这方面的循证证据,同时我国CSCO指南也做了推荐,这就为我们临床拓宽治疗手段,提供了合理合法的依据。
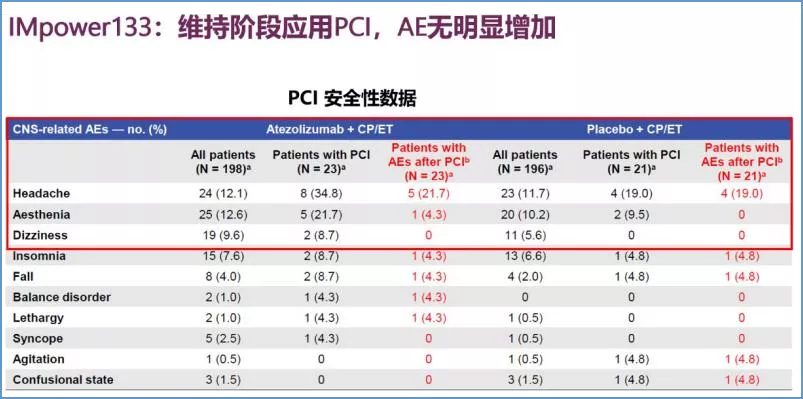
这部分的内容更新较多,主要体现在以PD-L1单抗(阿替利珠单抗/度伐利尤单抗等)为代表的免疫治疗与化疗、放疗等传统治疗手段的联合正在成为一线治疗的新选择。
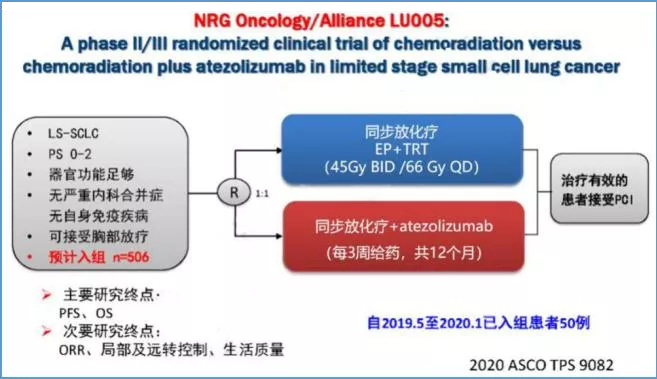
目前关于小细胞肺癌的免疫联合放疗的临床研究,研究结果也值得期待:由国家癌症研究所与NRG肿瘤学合作赞助的NRG-LU005试验是一项II/III期试验,旨在探讨阿替利珠单抗联合同步放化疗治疗局限期小细胞肺癌的疗效和安全性。试验组是阿替利珠单抗联合同步放化疗(阿替利珠单抗与同步放化疗同时开始),对照组是同步放化疗。主要研究终点是PFS和OS。小细胞肺癌免疫联合放疗,目前还处于临床经验的积累阶段。但毋庸置疑的是放射治疗能增进免疫治疗疗效。但是结合到肺部病灶,是否需要加放疗,我们还需要全面考虑。
最近我们碰到一个患者,他是肺鳞癌,我们用的是化疗加免疫。患者本身有慢阻肺,放疗24天以后出现肺癌缩小,但出现放射性肺炎造成患者呼吸衰竭。由于患者是重度的肺气肿加呼衰,目前脱离不了呼吸机,病人吸氧浓度要达到70%才能维持。这个病人从确诊到现在一共才7个月左右时间,我们一直在思考合并慢阻肺的肺癌患者是否应该加肺部放疗?因为慢阻肺本身有肺气肿,加放疗肯定会发生放射性肺炎,同时在上免疫治疗时,特别是联合PD-1的时候是联合放疗放射性肺炎会更多、更重。从PD-L1研究来看,同步放化疗后免疫维持,它的放射性肺炎增加不多。
如果是给肺部放疗,有3点非常重要。第1点,一定要排除患者有肺气肿、肺大泡、肺功能严重损害,因为这会带来严重后果;第2点,对肿瘤患者的放疗尽量采用立体定向精准放疗,减少肺损伤;第3点,最好在免疫治疗后的一个月内不要上放疗,意思就是上免疫治疗以后,建议40-50天约3个周期后再上放疗,既不影响疗效也可把放射性肺损害降到最低。因此,我们认为,放疗要尽量与免疫治疗间隔一个月时间,这会把放射造成的肺损伤降到最小。
除了治疗方面,我更想强调的是必须积极推动双肺检查。什么叫双肺检查呢?第一,是查慢阻肺,叫基层慢阻肺的筛查。因为很多医院不关注这个问题,他们只关注肺癌,但慢阻肺筛查非常重要;第二,是查肺癌,筛查肺结节。因为抽烟造成肺癌的发生率升高。尤其是既有肺癌又有慢阻肺的,要高度重视。为什么?因为病人有慢阻肺,他的肺功能下降,好的药物很敏感,一用以后增加感染机会,增加肺纤维化的机会。
所以,当病人出现咳嗽、喘的时候,到底是什么原因?很多医生都判断不清楚。因此,第一,我认为需要呼吸医生的积极参与,我们如何把慢阻肺合并肺癌的这些人群早发现出来,作为特别化的处理,这是需要关注的;第二,出现合并慢阻肺的肺癌,气道的抗炎平喘处理非常关键。如果不把气道扩开,气道炎症控制住,病人照样咳嗽、喘,不易分辨清楚到底是慢阻肺引起的还是肿瘤引起的,所以一定要区分开;第三,在是否联合放疗处理的时候特别关键,要采取损伤小的放疗或者精准度高的放疗。同时还要考虑患者肺功能如何,肺功能太差的根本不能放疗。这就需要综合性处理,需要多学科的团队协作。
免疫治疗应尽量延长一线治疗时间,减少复发的几率和次数……特殊、复合型、转化性小细胞肺癌的治疗是临床医师的关注点和难点,应积极探索放化疗加免疫
对于复发小细胞肺癌的内科治疗方案,免疫治疗的地位、多靶点药物安罗替尼的应用等方面,应该如何看待呢?首先,我们还是要肯定免疫治疗的地位,尽管二线治疗的免疫状态和疗效没有一线那么好,但二线治疗同样有所获益,但二线治疗药物目前在二线的治疗缓解率都较低,患者维持时间更短,大概两三个月后就不行,缓解很有限。二线治疗是以拓扑替康为主要的治疗选择,对于使用Atezolizumab或 durvalumab维持治疗>6个月后复发的患者,建议再次使用卡铂+依托泊苷或顺铂+依托泊苷。


三线及以上治疗:安罗替尼作为小细胞肺癌三线及以上治疗的I级推荐(2A 类证据)。我国自主研发的多靶点新药安罗替尼以及pembrolizumab、nivolumab打破后线治疗壁垒,创历史进展。但对于临床医生来讲,我们应该尽量延长一线治疗的时间,减少二线或三线治疗的机会,减少复发的几率。
关于特殊小细胞肺癌的治疗,复合型小细胞肺癌的治疗、腺癌转化性小细胞肺癌的治疗都是临床医师的关注点和难点,支气管肺/胸腺神经内分泌肿瘤的治疗其实是比较陌生的。特殊小细胞肺癌存在的问题是,它既有小细胞肺癌,又有鳞癌,我在临床中碰到过这样的案例,小细胞肺癌合并腺癌的案例也碰到过,还有小细胞肺癌合并神经内分泌的,像这些恶性程度比较高的案例。因此我们面对小细胞肺癌,以前往往认为它应该是单一的一种,而现在知道它是分很多种,混搭存在的多,这样的肿瘤治疗难度也很大。
我们曾经碰到一例小细胞肺癌合并类癌的患者,这个患者比较幸运,他首先就诊的原因是咳嗽,做肺部CT发现左上肺有约4厘米的肿块,最后通过做气管镜确诊为类癌合并小细胞肺癌。我们用紫杉+卡铂对患者上了6个疗程化疗后放疗序贯后观察,患者的两种癌症对药物都很敏感。患者可以说是十分幸运,发现时处于局限期,一直到现在还生存。当然,临床碰到更多的属于广泛期的患者,也有合并类癌的,生存时间都特别短。
以前我们没有尝试过免疫,只是从化疗这个层次来看待,我想,未来对这些有合并肿瘤的,如果联合化疗的同时把免疫加上,如果还能把放疗加上,可能多种治疗会带来一定效果,这方面我们在探索。
专家介绍

操乐杰
中国科大附一院、安徽省立医院 呼吸与危重症科 主任医师、教授、硕导;中华医学会结核病分会全国委员,安徽省医学会结核病分会主任委员;中国抗癌协会肿瘤靶向专委会全国委员;CSCO血管靶向专委会全国委员;中国医药教育协会肿瘤免疫与呼吸康复专委会常委;中国防痨协会临床专委会常委;安徽省抗癌协会肿瘤免疫与靶向治疗专委会主委;中国医师协会安徽省呼吸分会常委;安徽省抗癌协会肺癌专委会副主任委员。


