
基本信息、主诉
陈**,男。61岁,汉族,农民,2018-12-10入院,主诉:肺癌术后5天,呼吸困难2天。
现病史
患者于北京市某解放军医院拟行鼻部手术,住院期间查胸部CT示左上肺小结节影12.3x17.7mm,内见小泡状透亮影,边缘毛糙、胸膜牵拉,右下肺见小结节影,直径约4.3mm,双上肺小条索影。
于2018年12月5日行右下肺楔形切除及左肺上叶切除术,术中胸腔镜转开胸术。术后患者咳嗽、咳少量淡咖啡色粘痰,自觉胸闷,无发热、寒战。
2018年12月8日晚(术后第三天)出现胸闷加重,心率达100次/分以上,无胸痛咯血、无剧烈咳嗽,无恶寒发热,予对症治疗,症状无明显缓解(具体用药不详)。
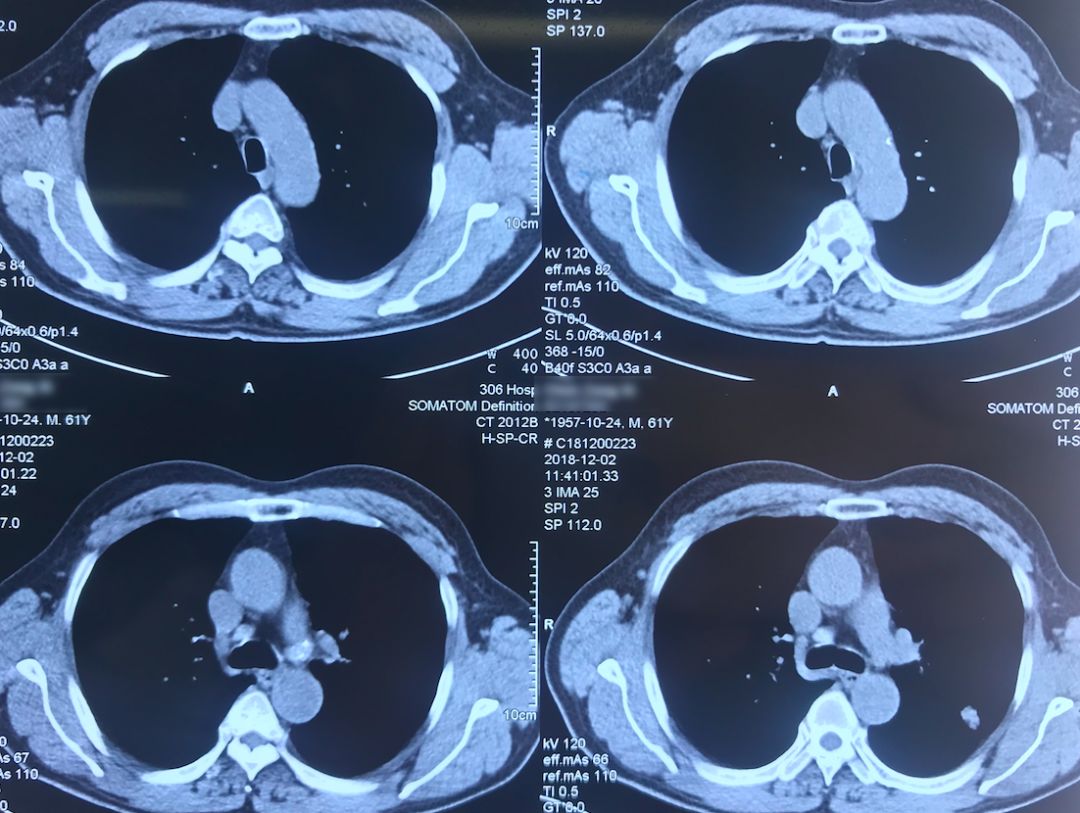
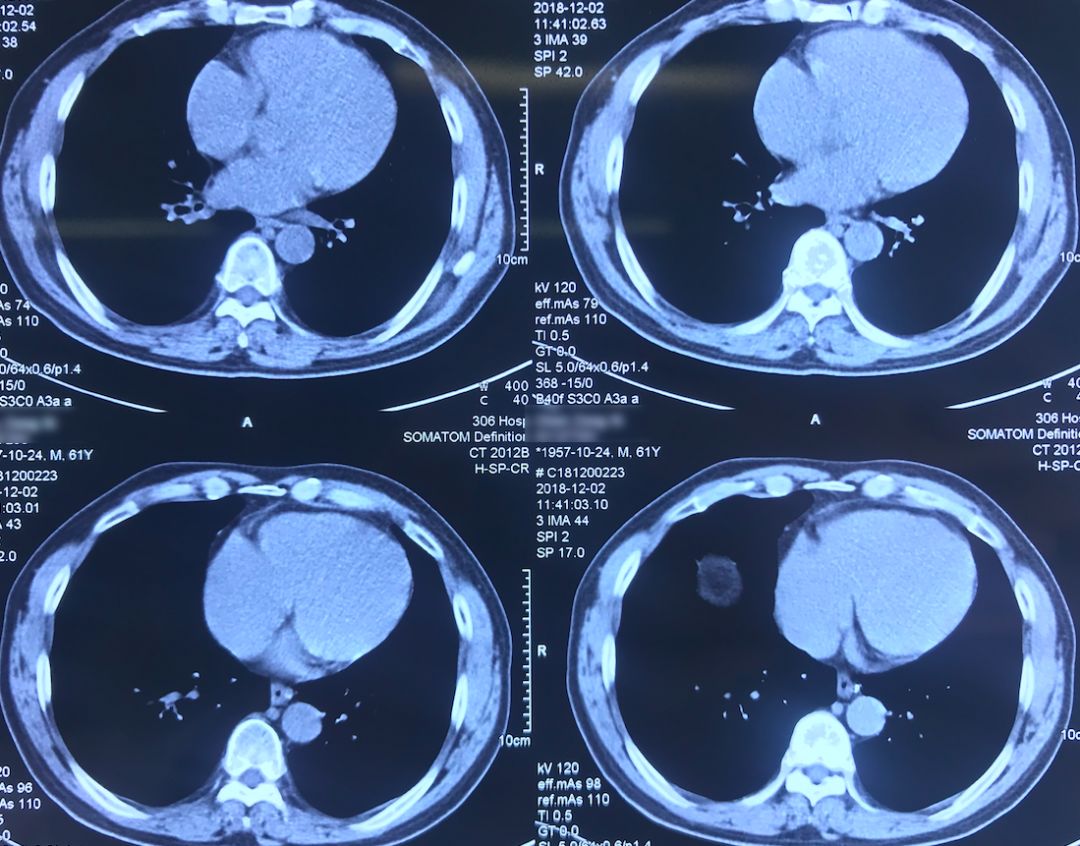
外院术前胸部CT(2018-12-2)
术前双肺比较「干净」,主要是左肺上叶结节,有一些毛刺、胸膜牵拉征,考虑恶性的可能性大,因此直接做了手术治疗。
CT:

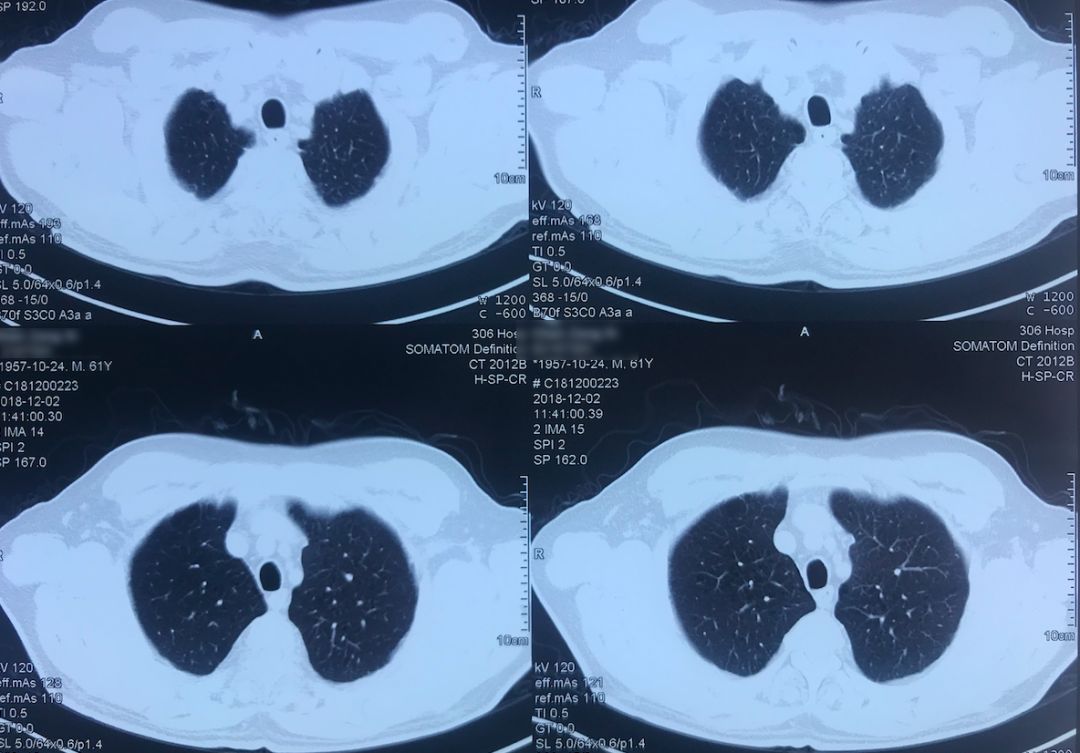
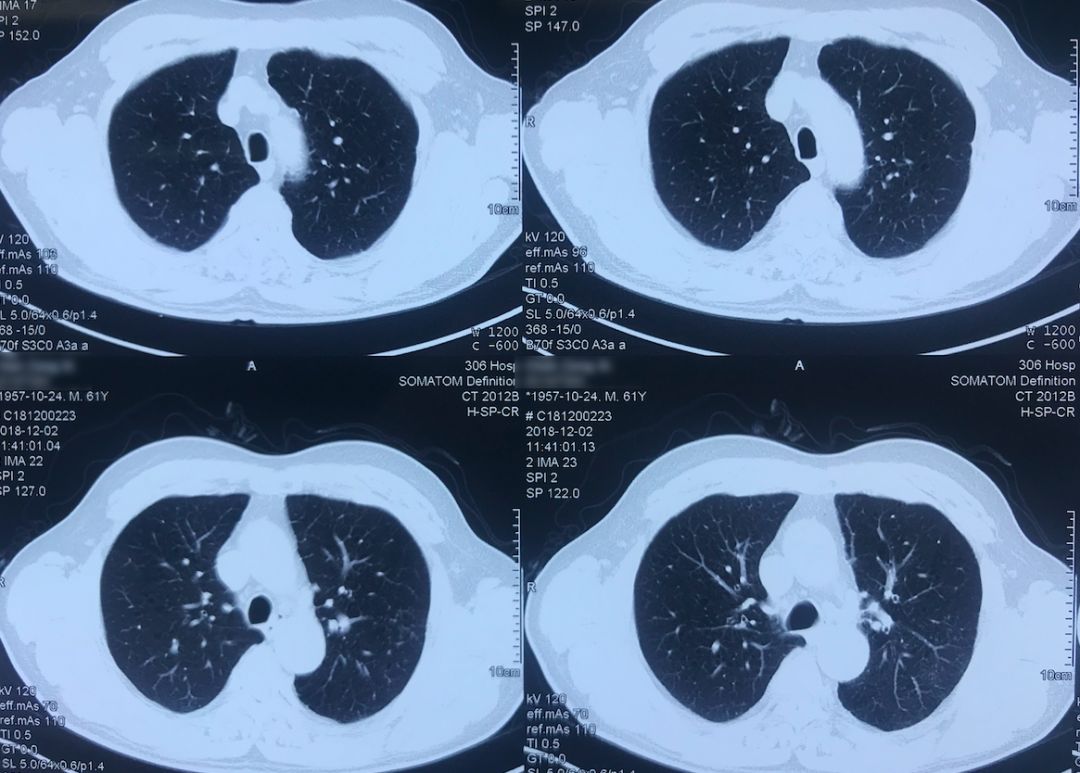
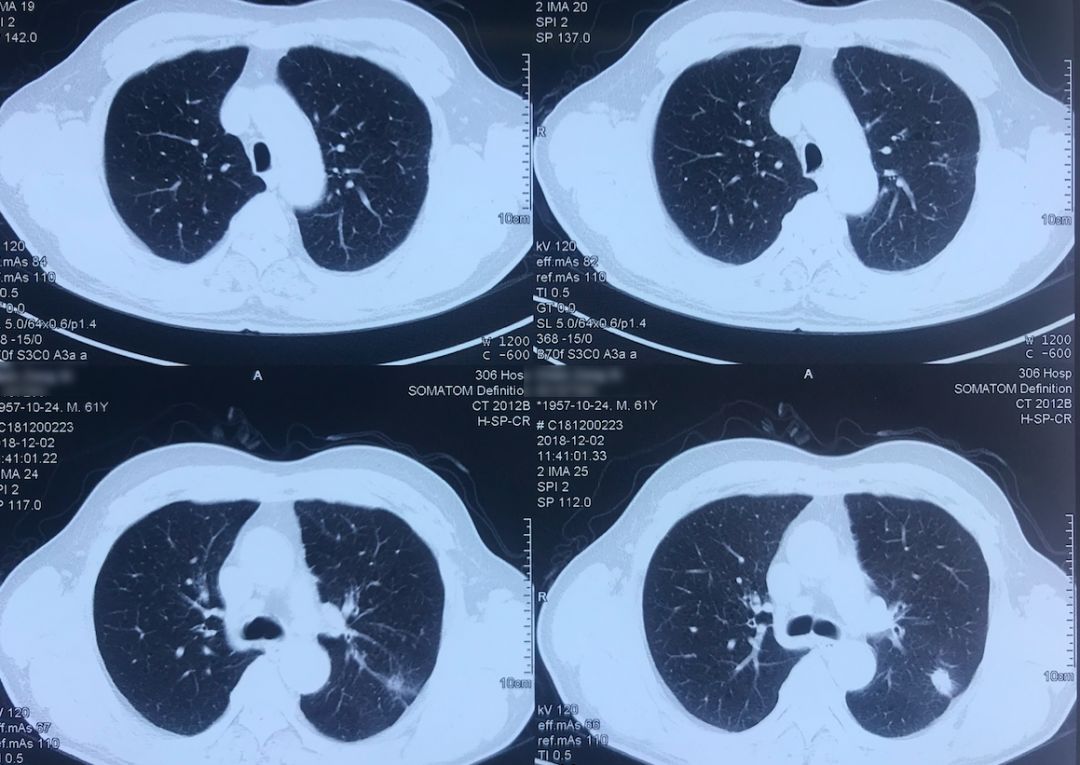
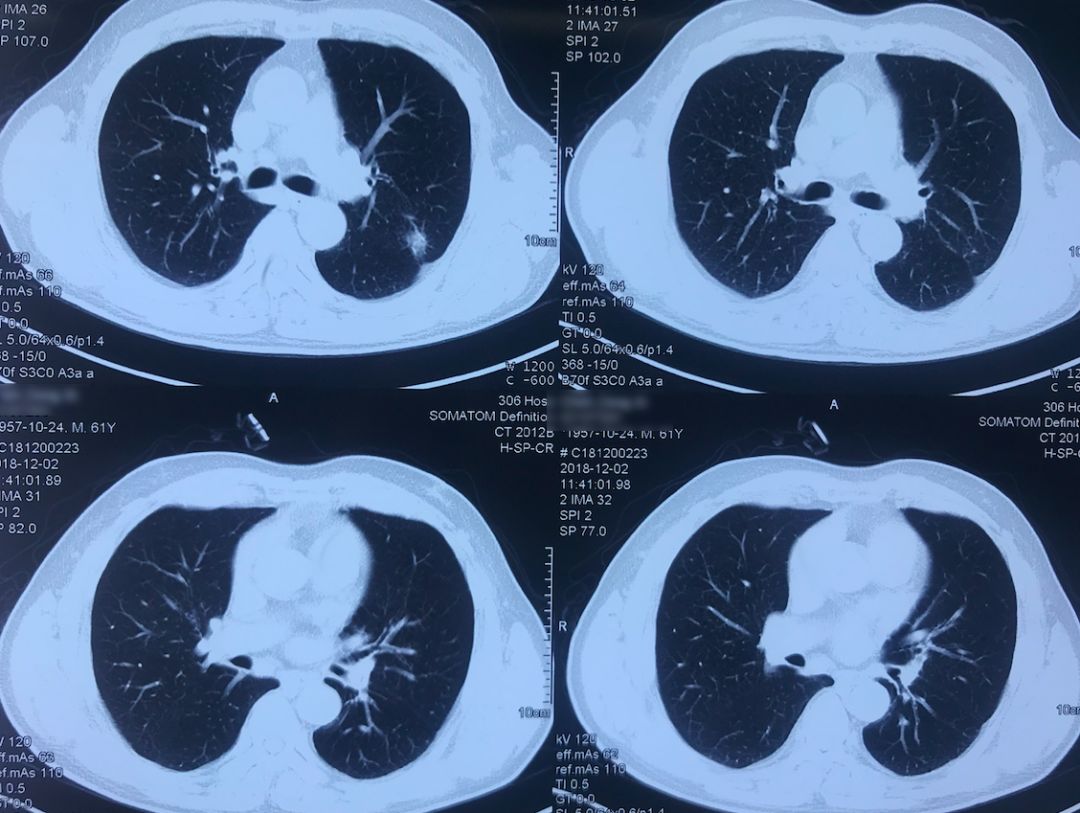

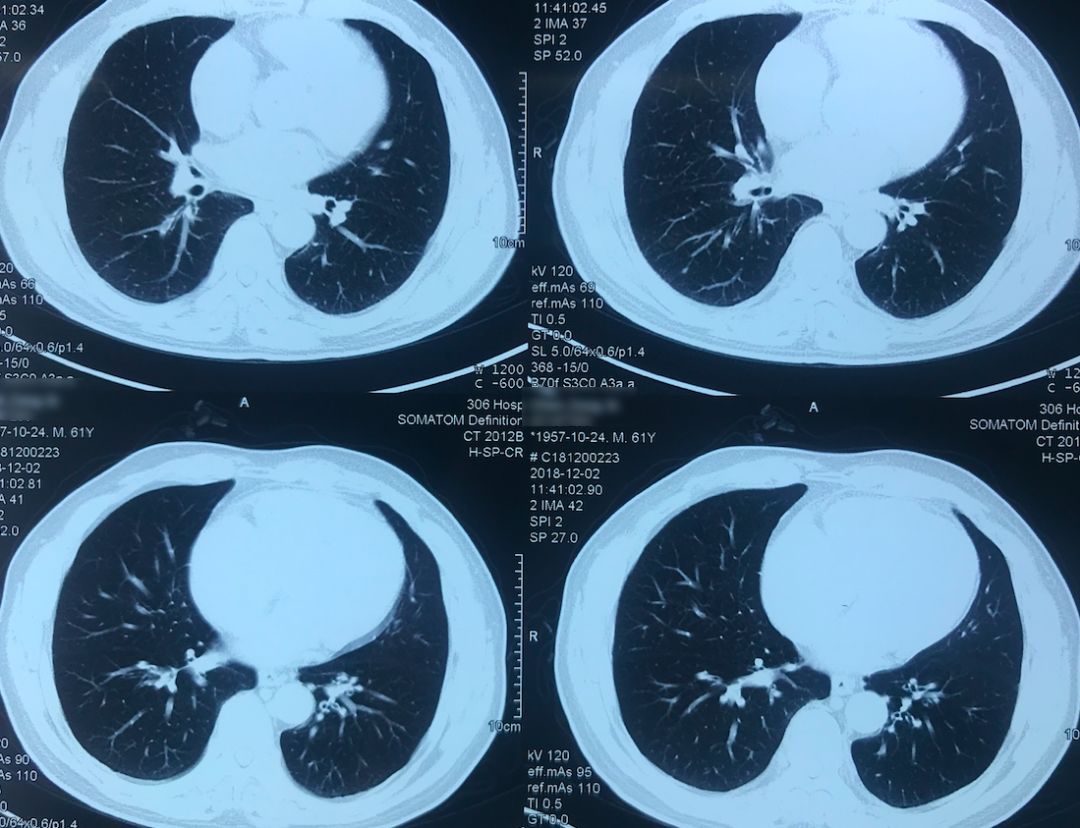
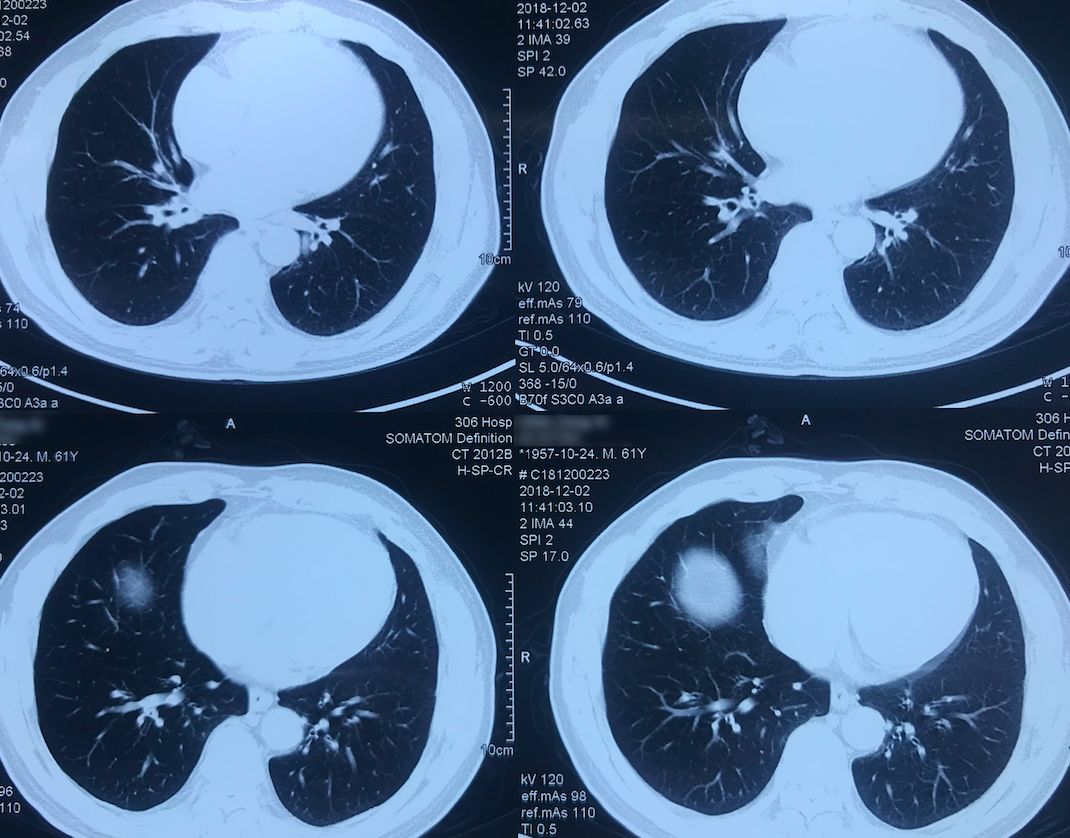
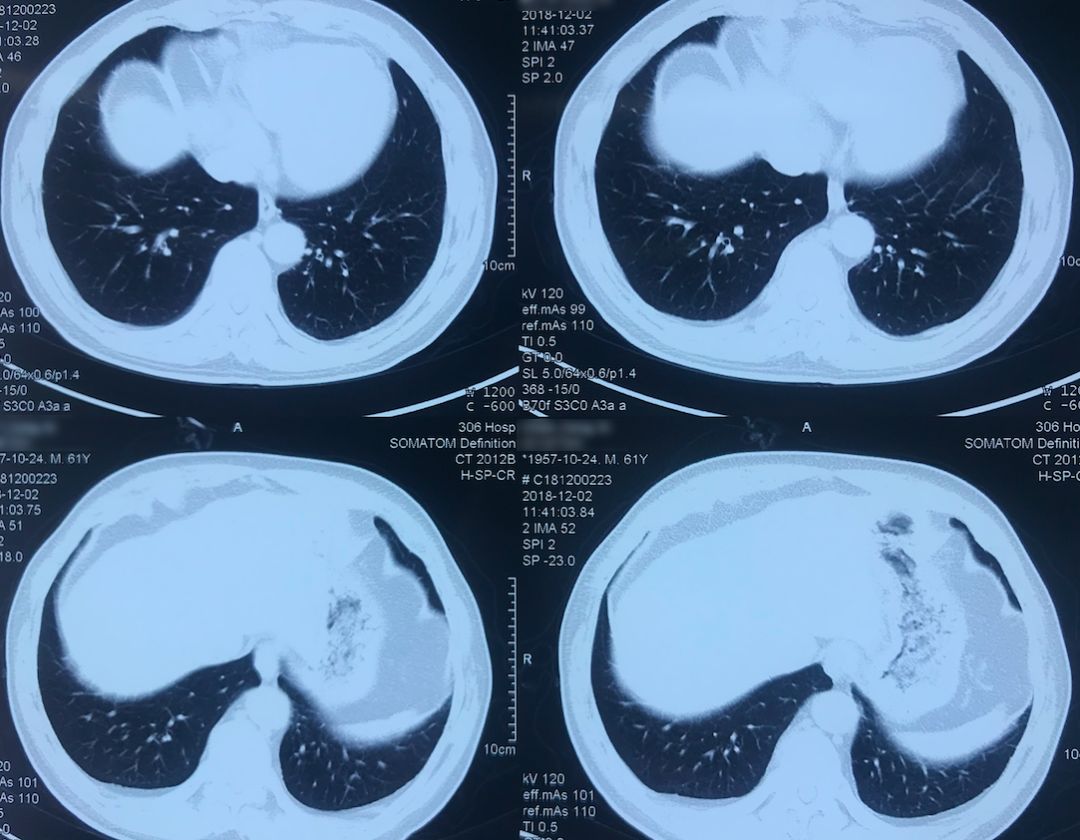
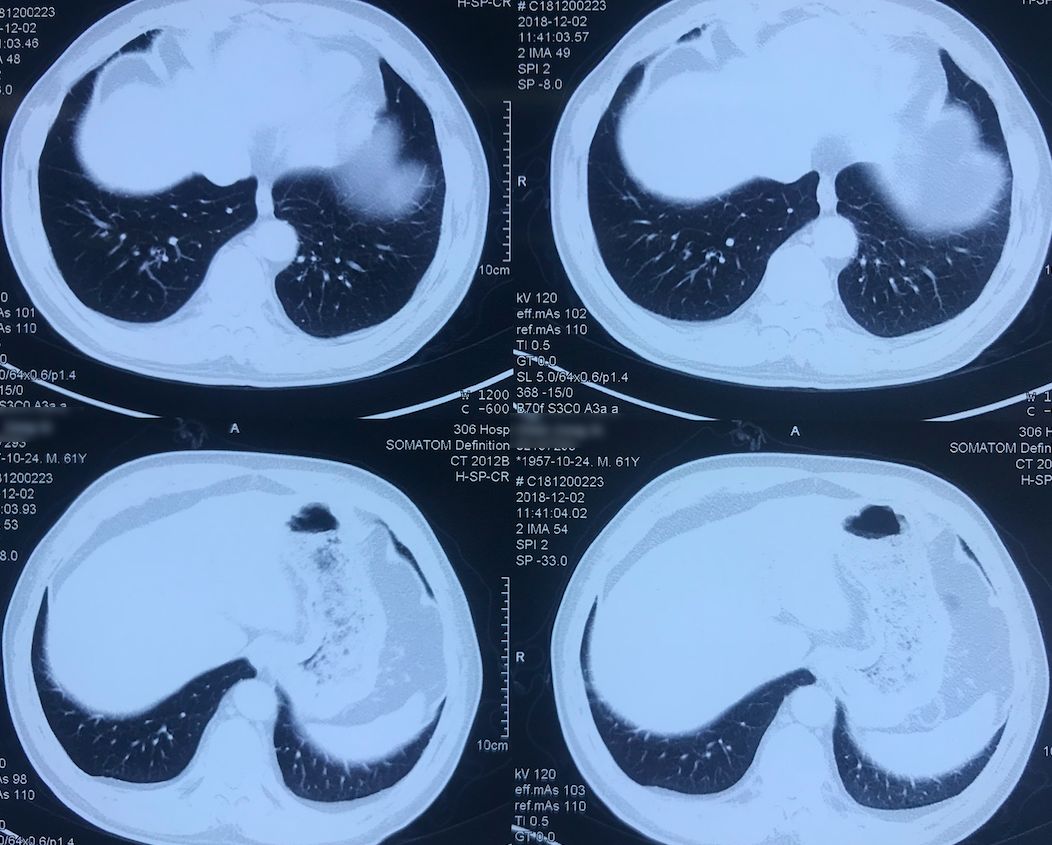
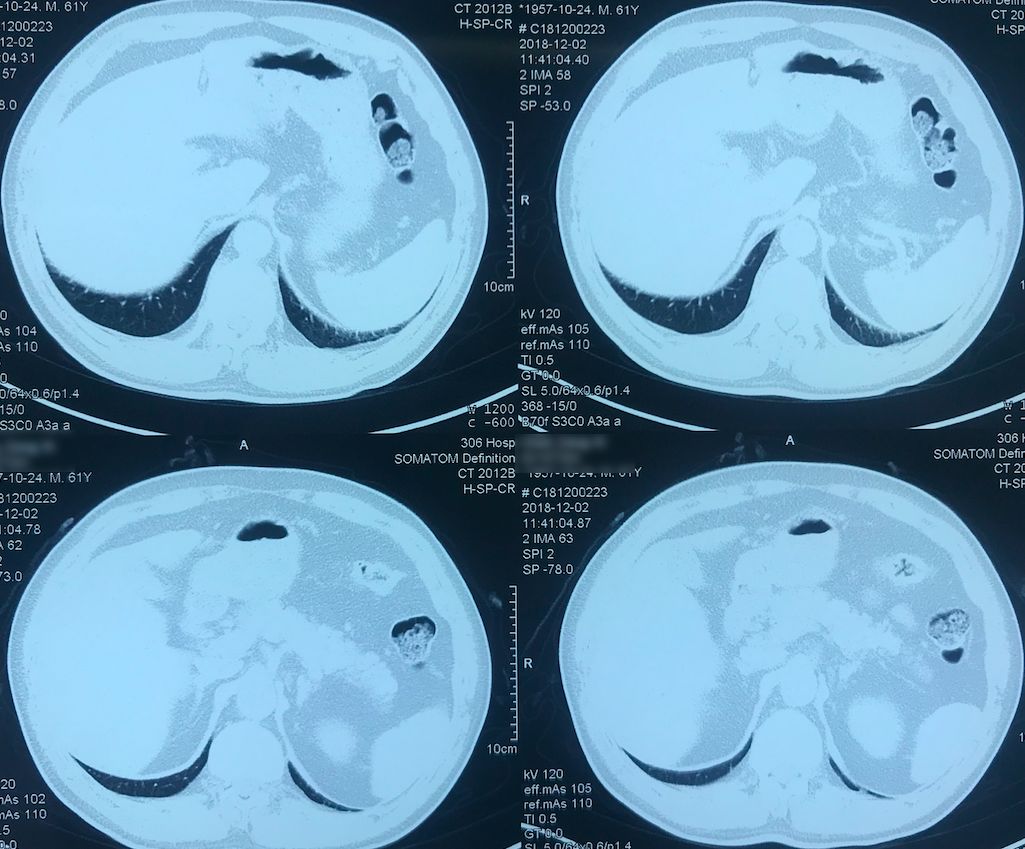
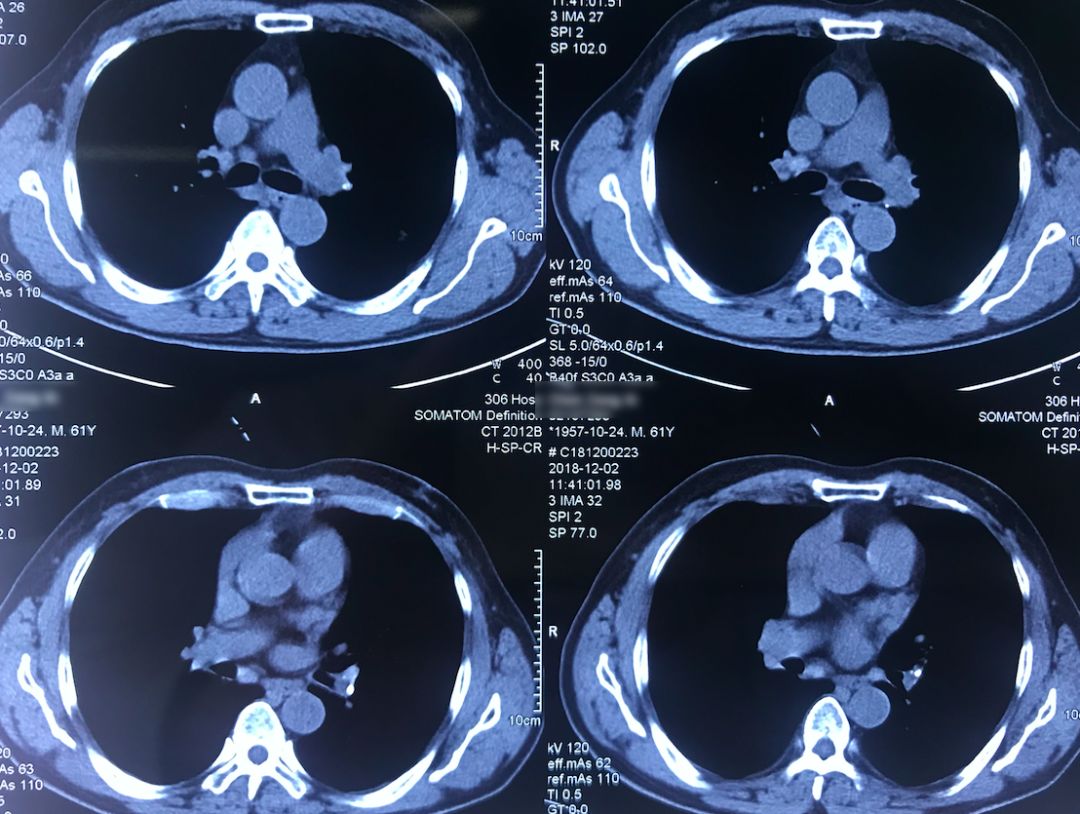
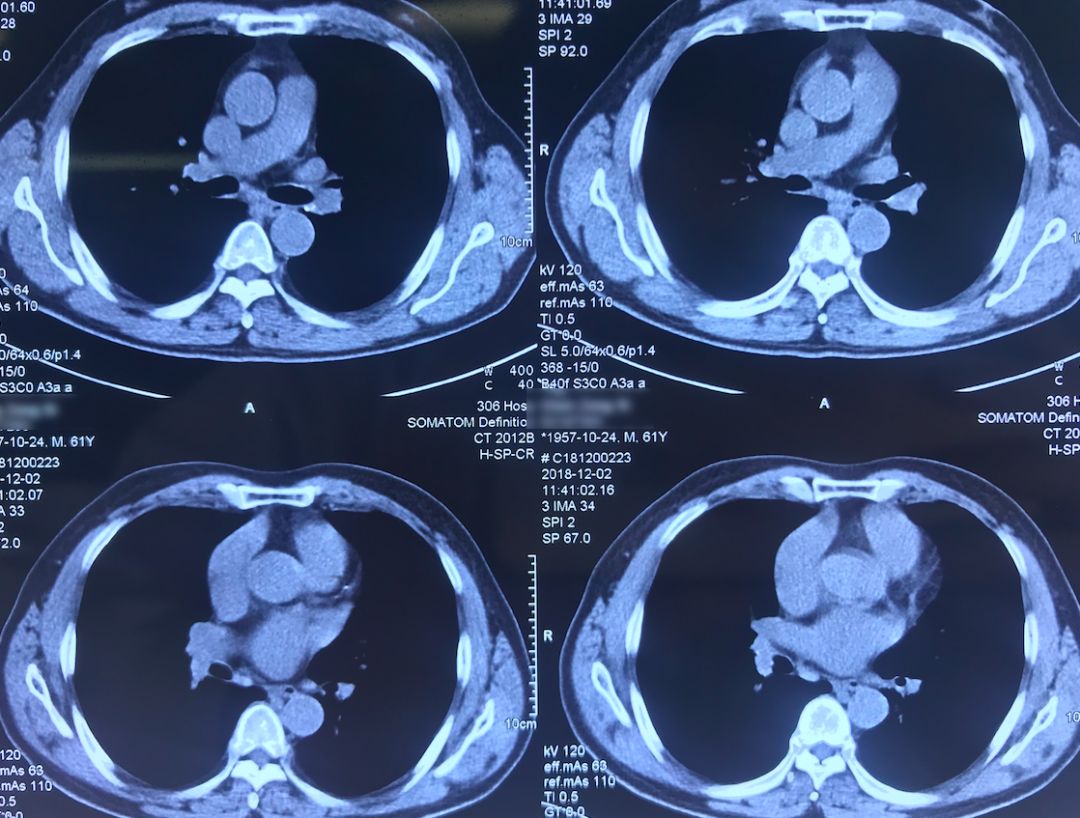
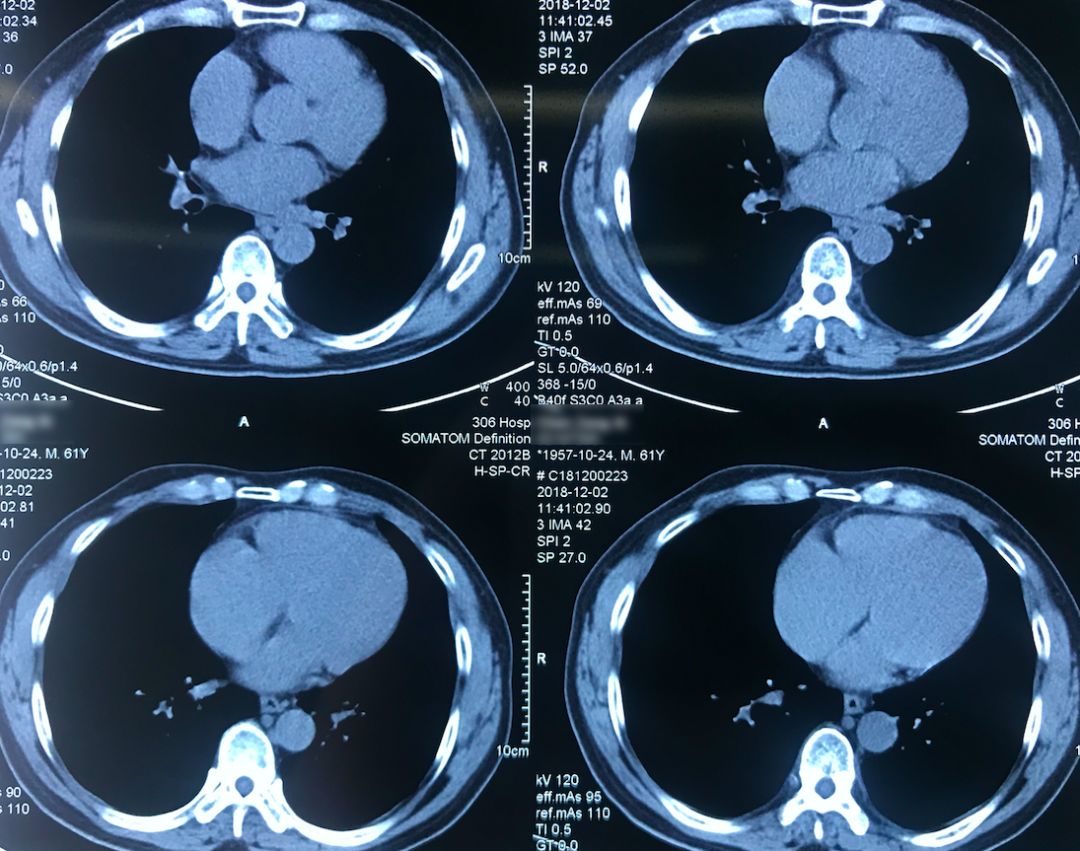
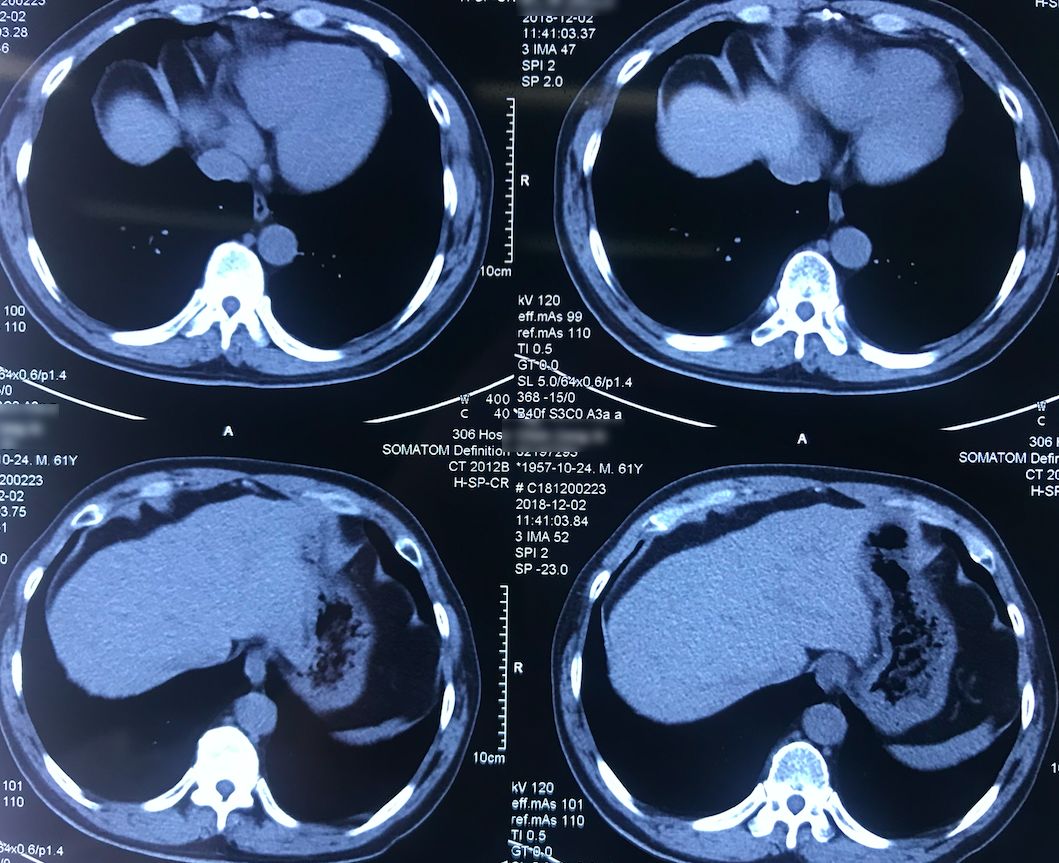
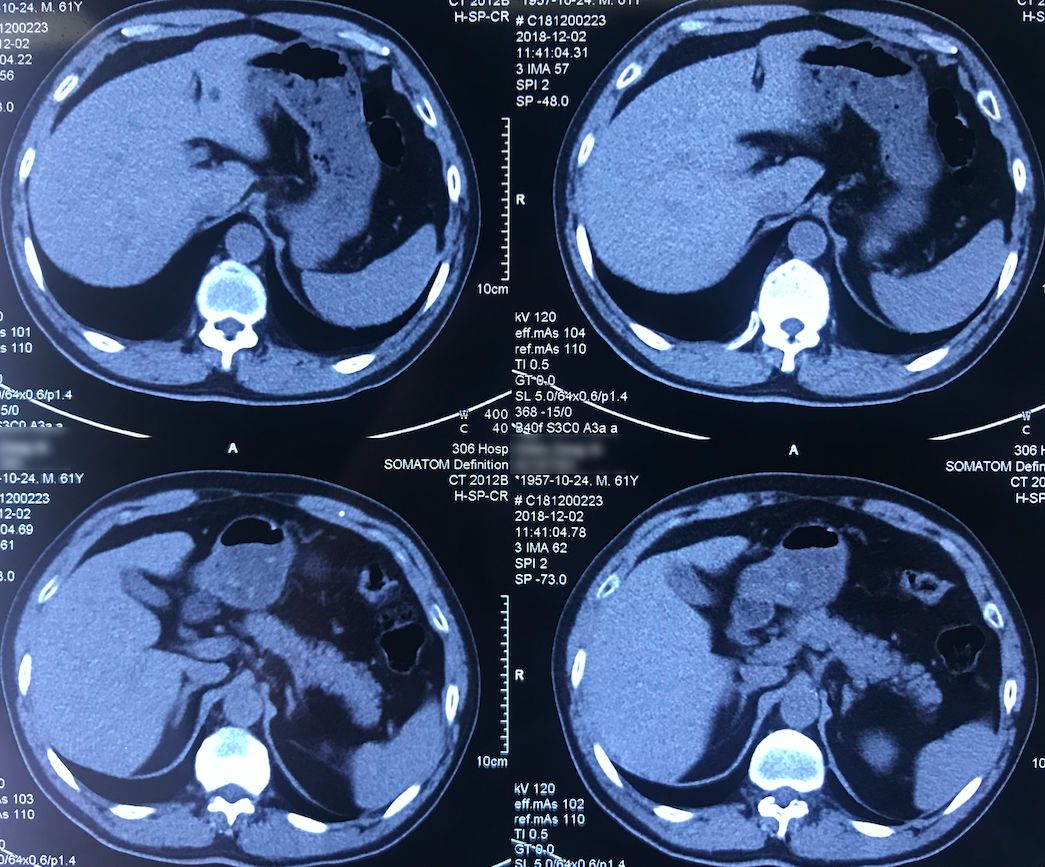
院外胸部CT 纵隔窗(2018-12-2)
淋巴结无明显增大。
CT:
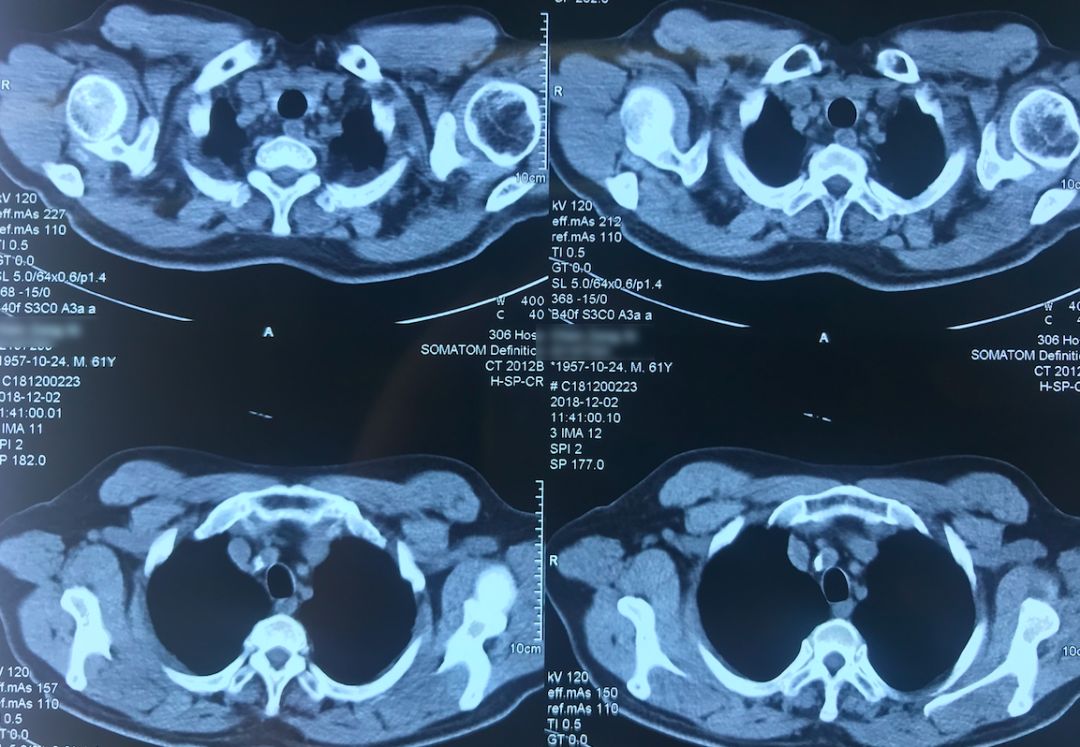
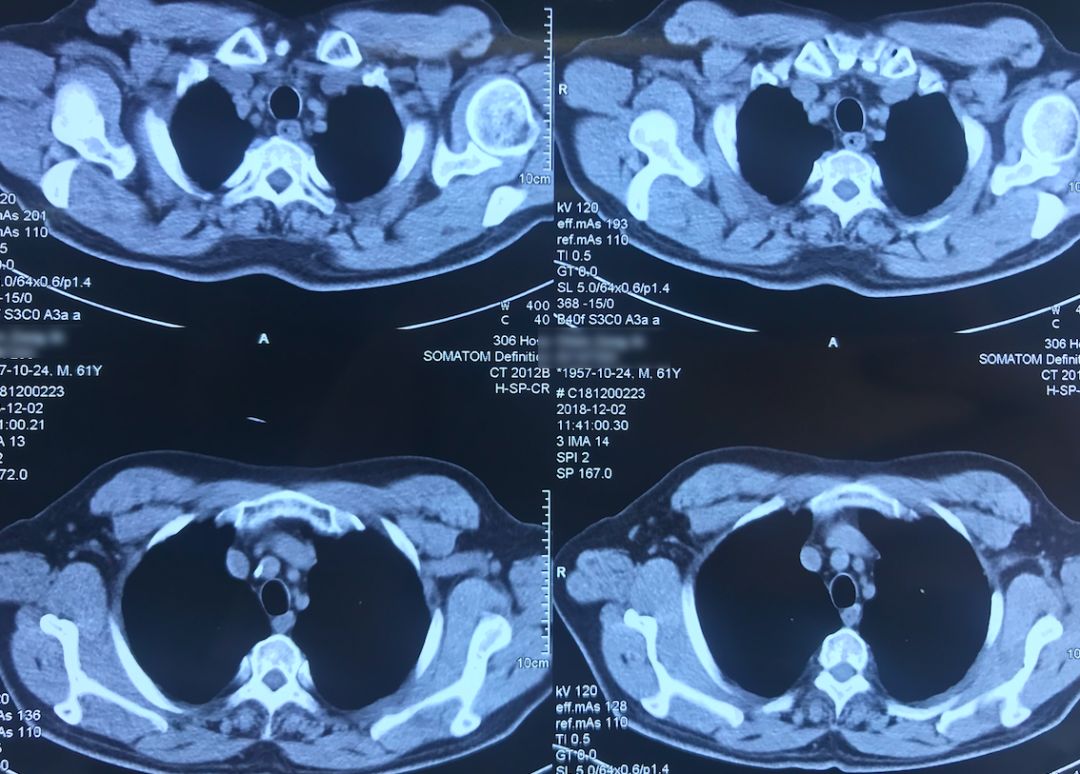
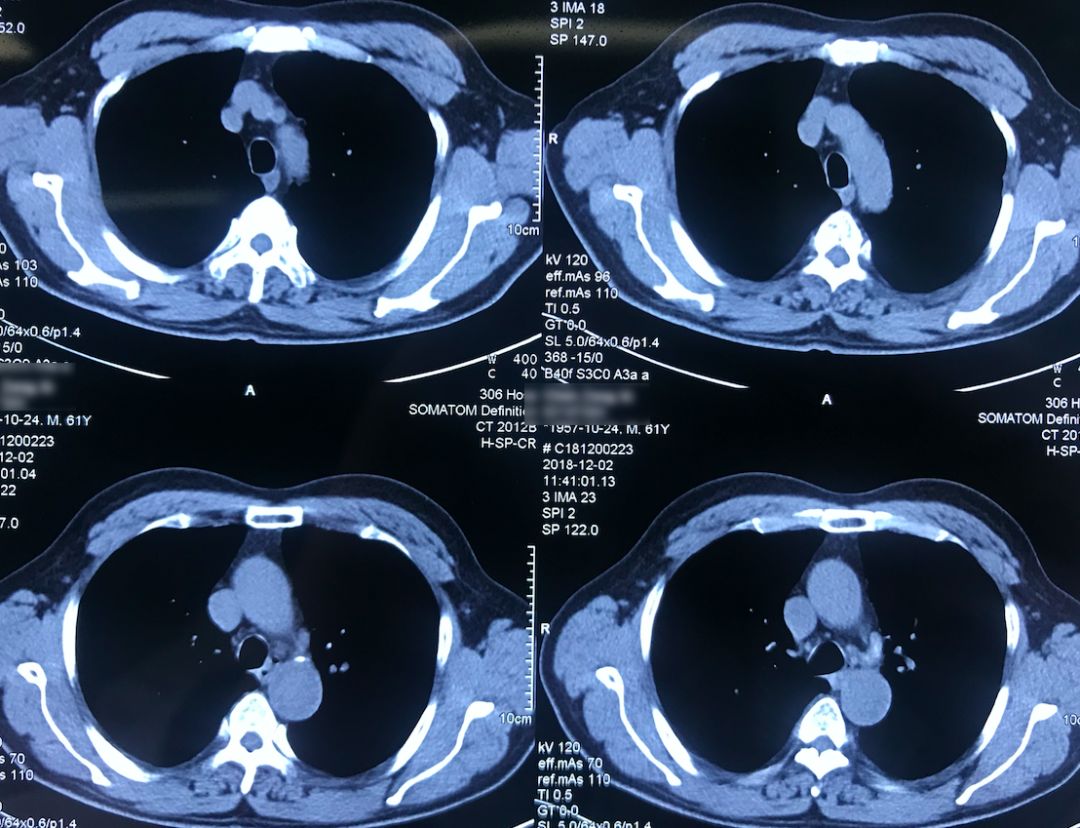

现病史
患者12月9日(术后第四天)上午呼吸困难突然加重,意识清楚,颜面口唇紫绀,伴大汗,无胸痛咯血,无发热,循环较稳定。外科手术后突然出现呼吸困难,一般来说首先会怀疑肺栓塞(PE),所以当时也立即完善了相关检查。双下肢静脉彩超示「左小腿部分肌间静脉血栓形成,双下肢深静脉及部分大隐静脉回流通畅」,肺动脉CTA示「肺术后,左上肺动脉缺如,余肺动脉内造影充盈欠佳,右侧肺动脉多发分支似见低密度影,左下肺动脉主干见条形低密度影,皮下广泛气肿、纵隔气肿,左侧液气胸,双肺渗出性改变」,(当时正逢流感季节)甲型流感病毒蛋白抗原:阳性。
患者于当天转入该院ICU,予静点泰能、莫西沙星、氟康唑,口服达菲,皮下注射低分子肝素钙4000IU Q12h及静点甲强龙80mg Qd。经1天治疗,呼吸困难症状略有好转,偶有咳嗽、咳少量淡血性粘痰。请我科会诊,为进一步诊治收入我院。
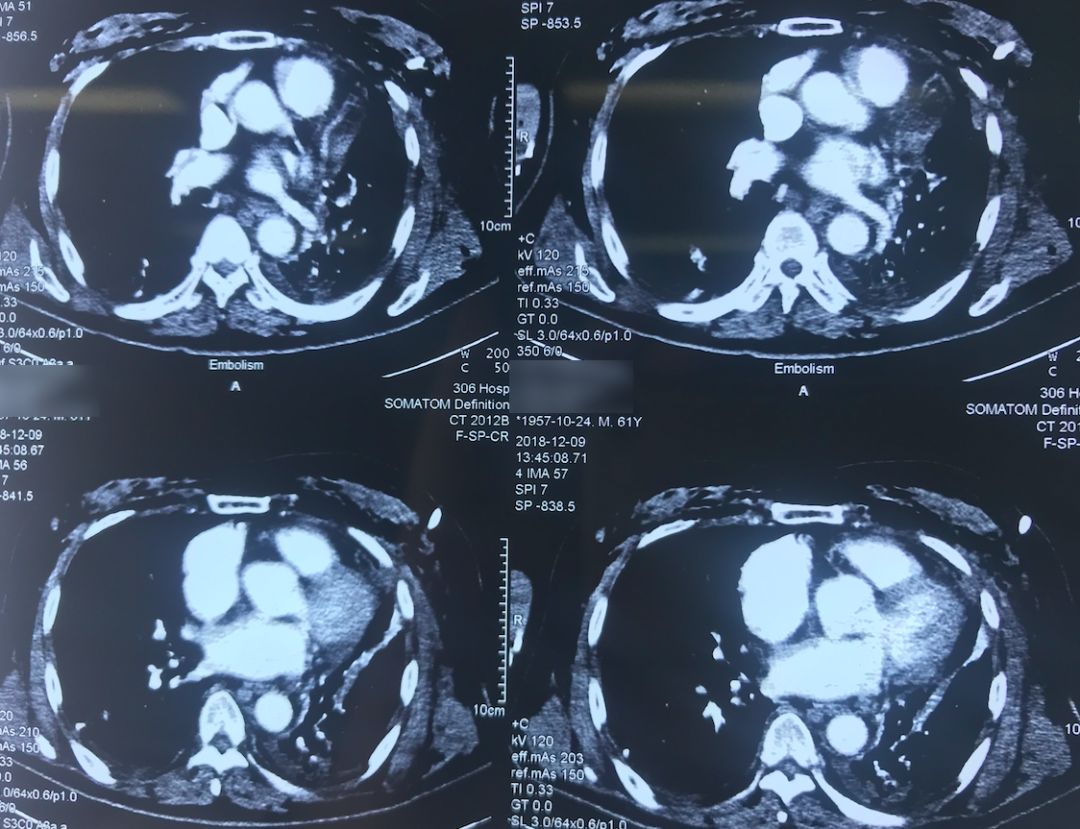
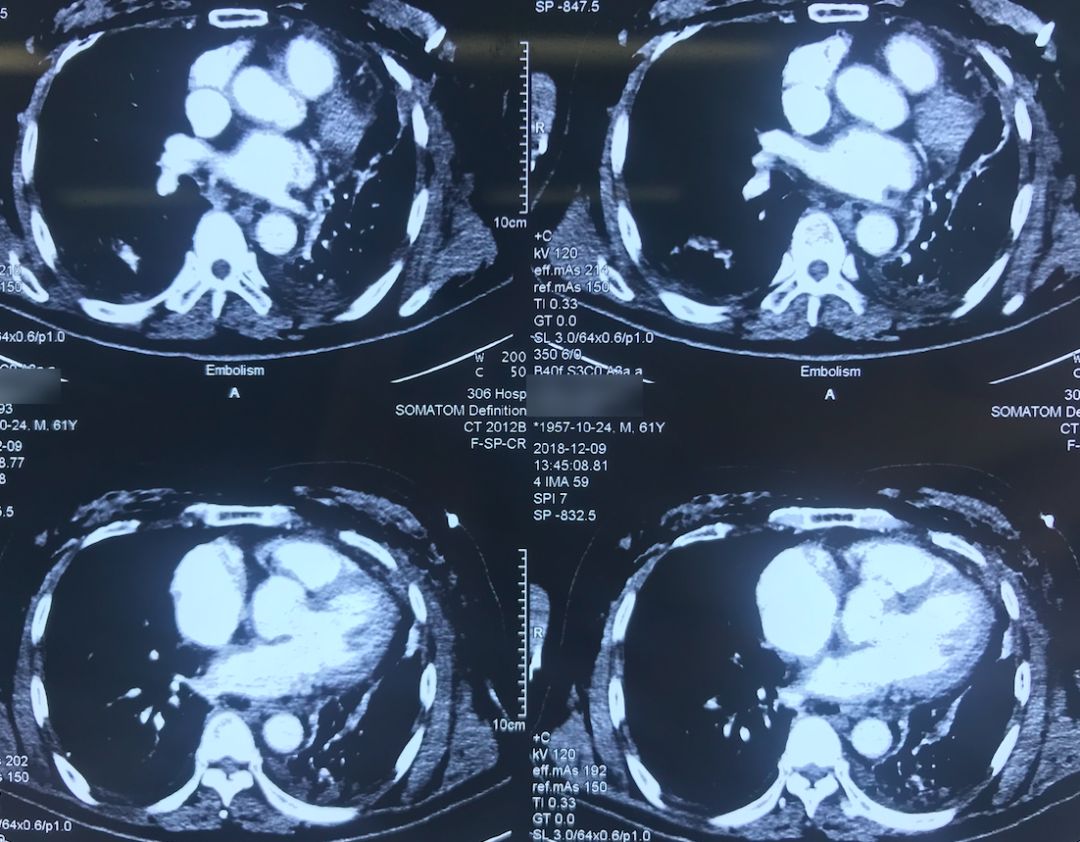
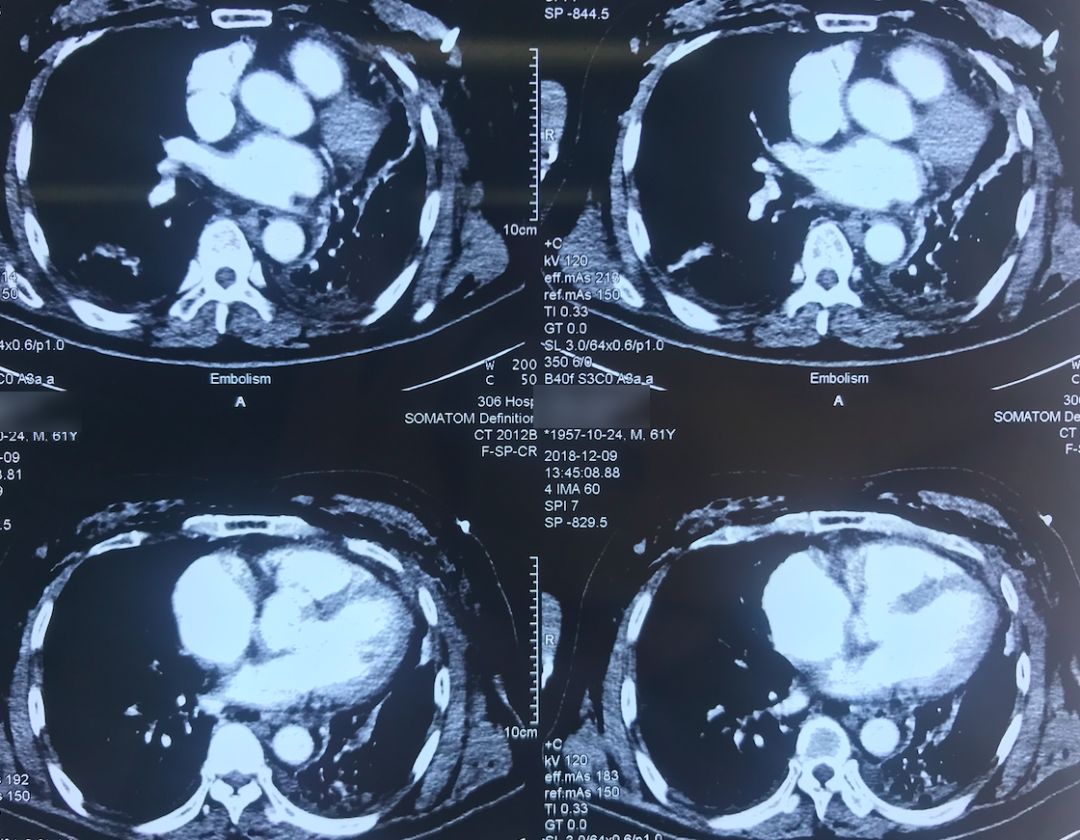
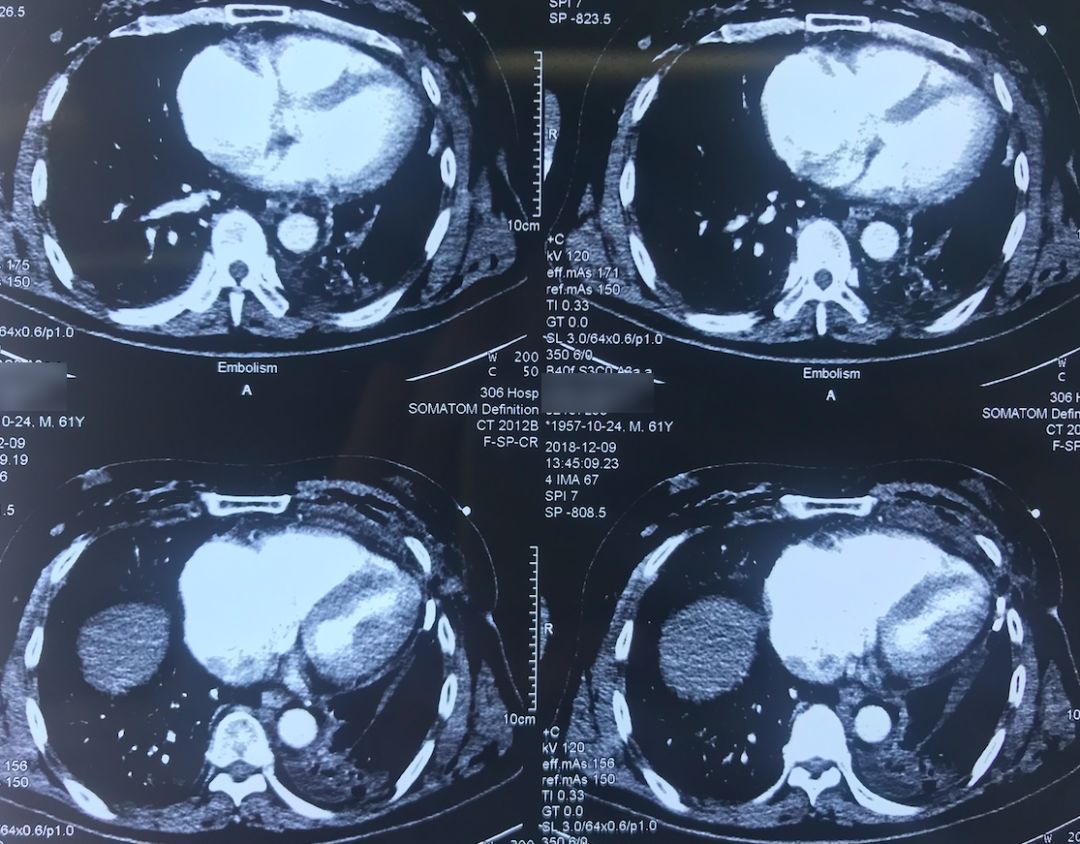
肺动脉CTA(2018-12-9)
术前,患者的双肺除了结节以外都是比较「干净」的,但是现在可以看到,右肺上叶和右肺下叶都有比较多的小叶间隔增宽以及磨玻璃影、网格影,左肺下叶有些实变影(左肺上叶已经切除)。
CT:
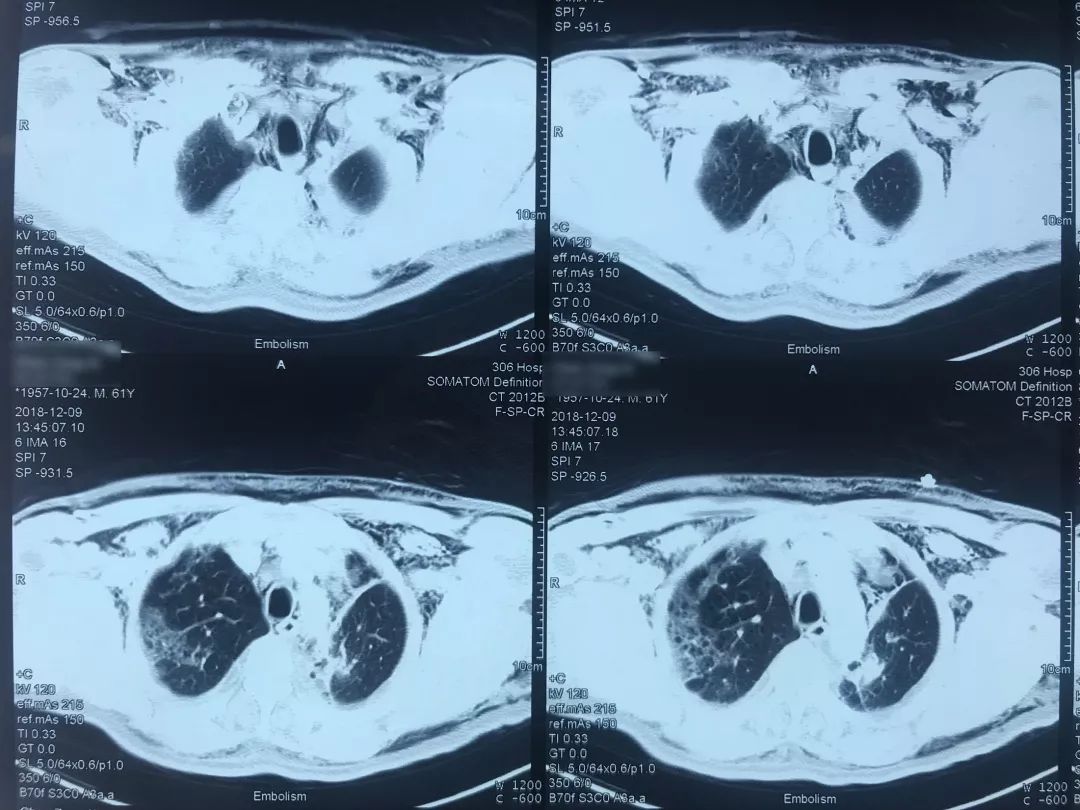
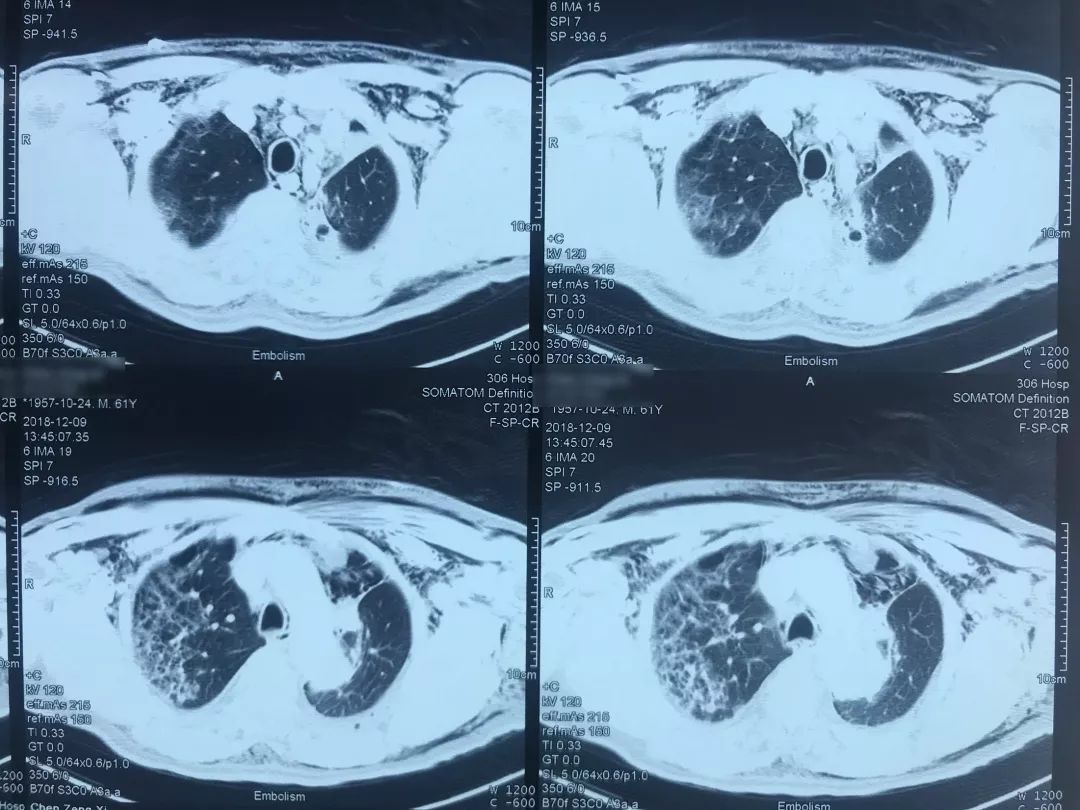
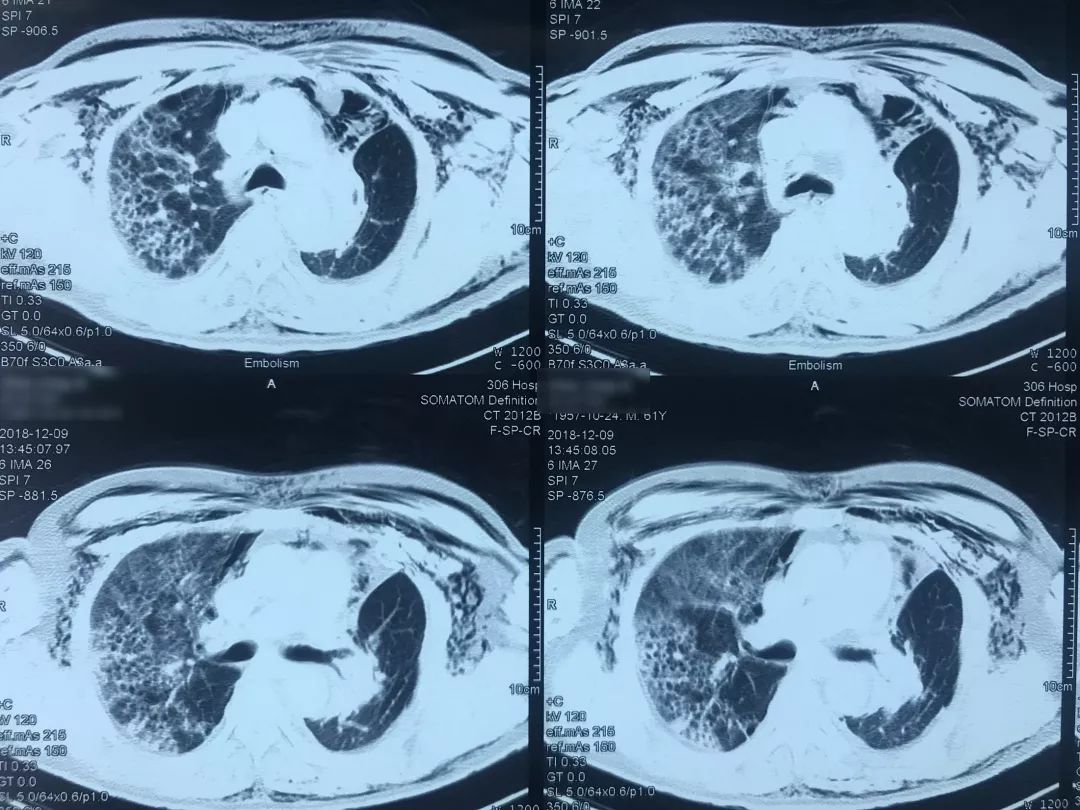
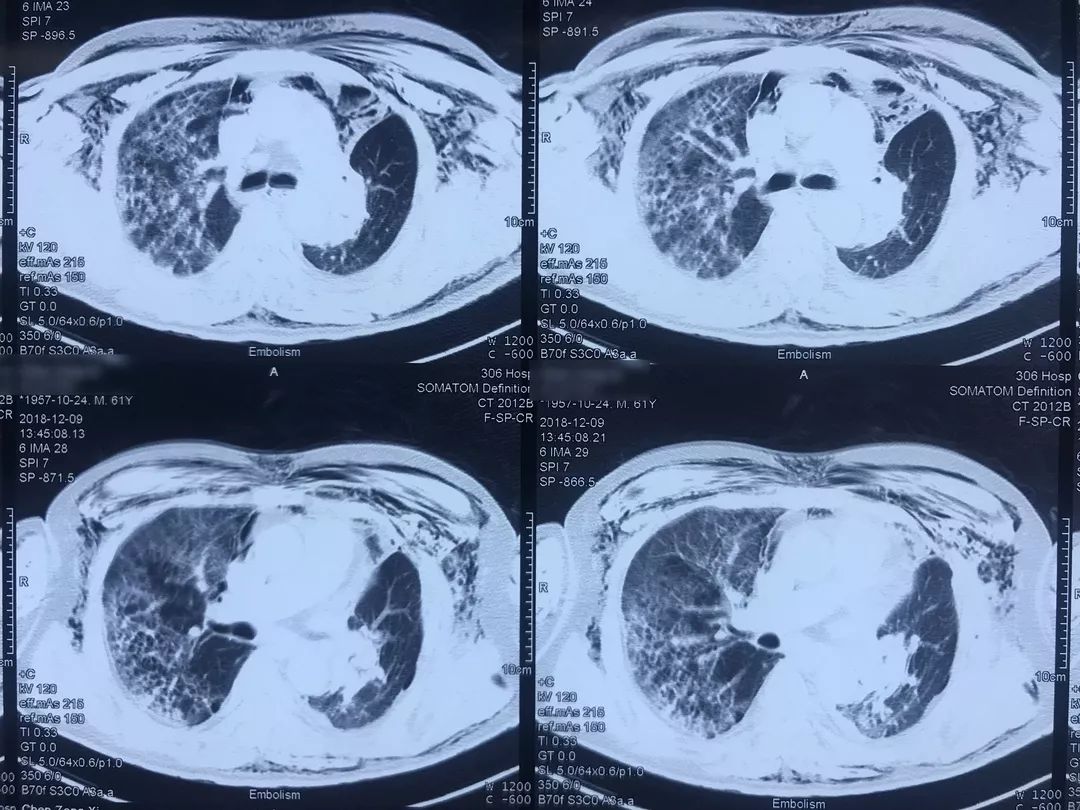
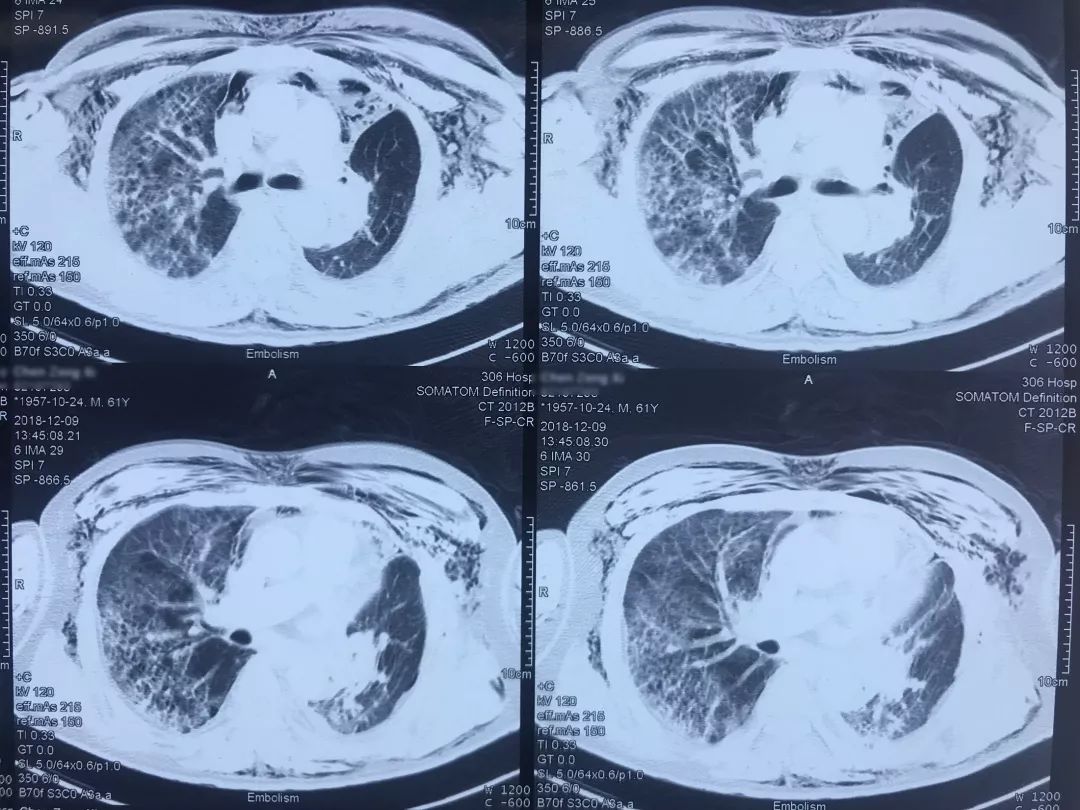
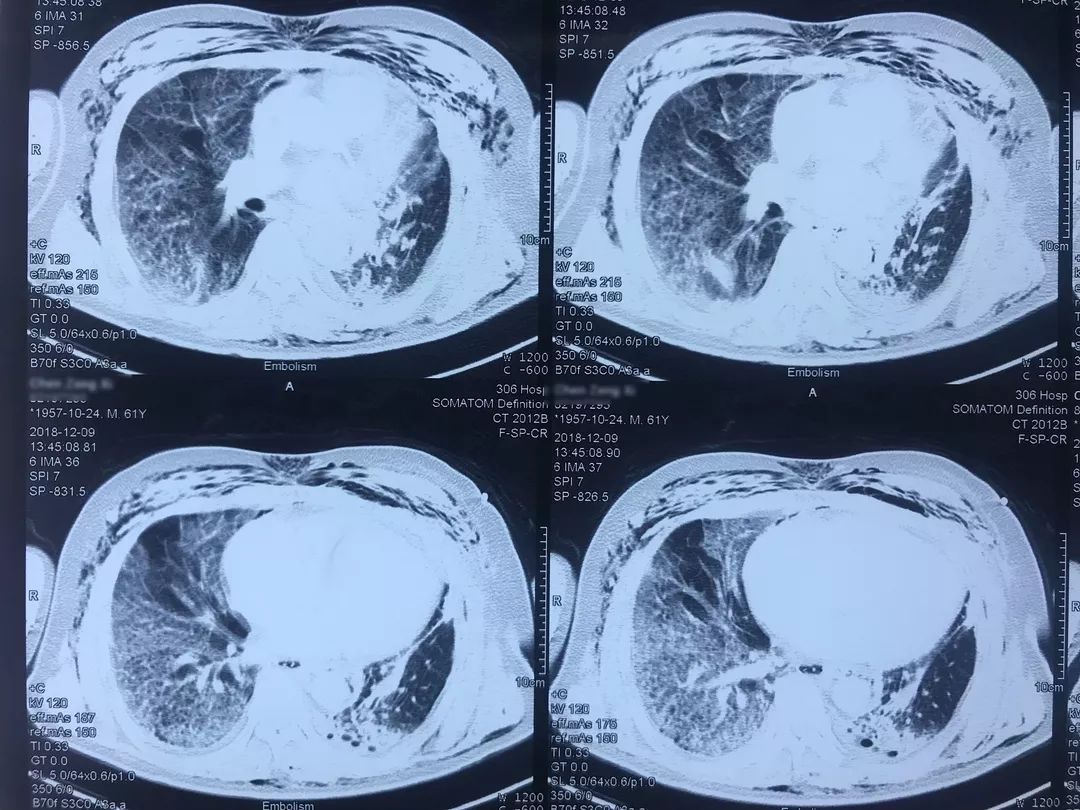
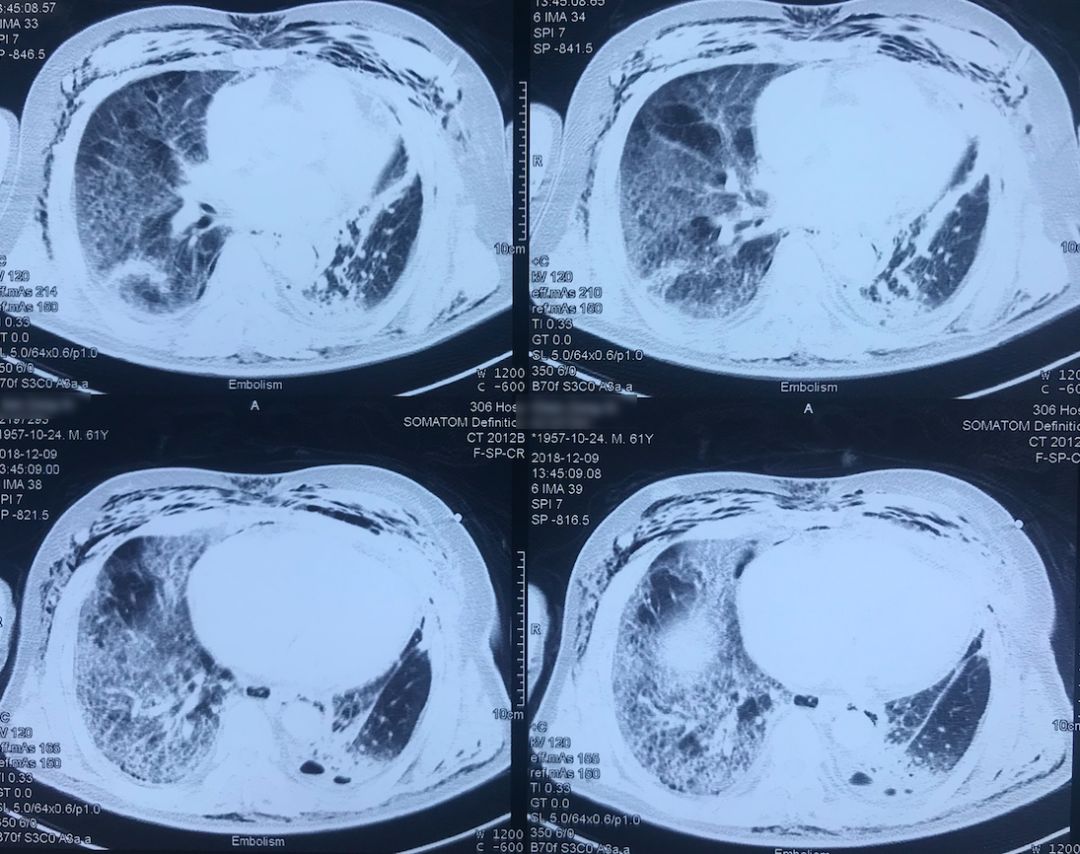
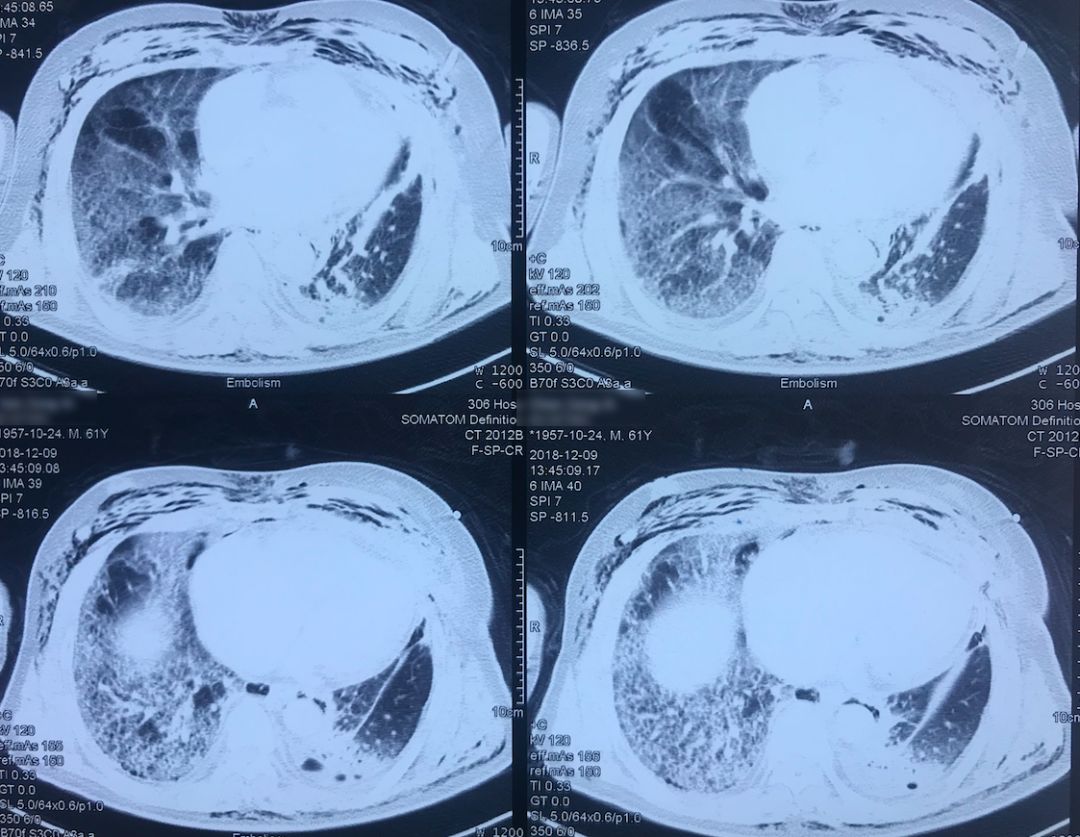
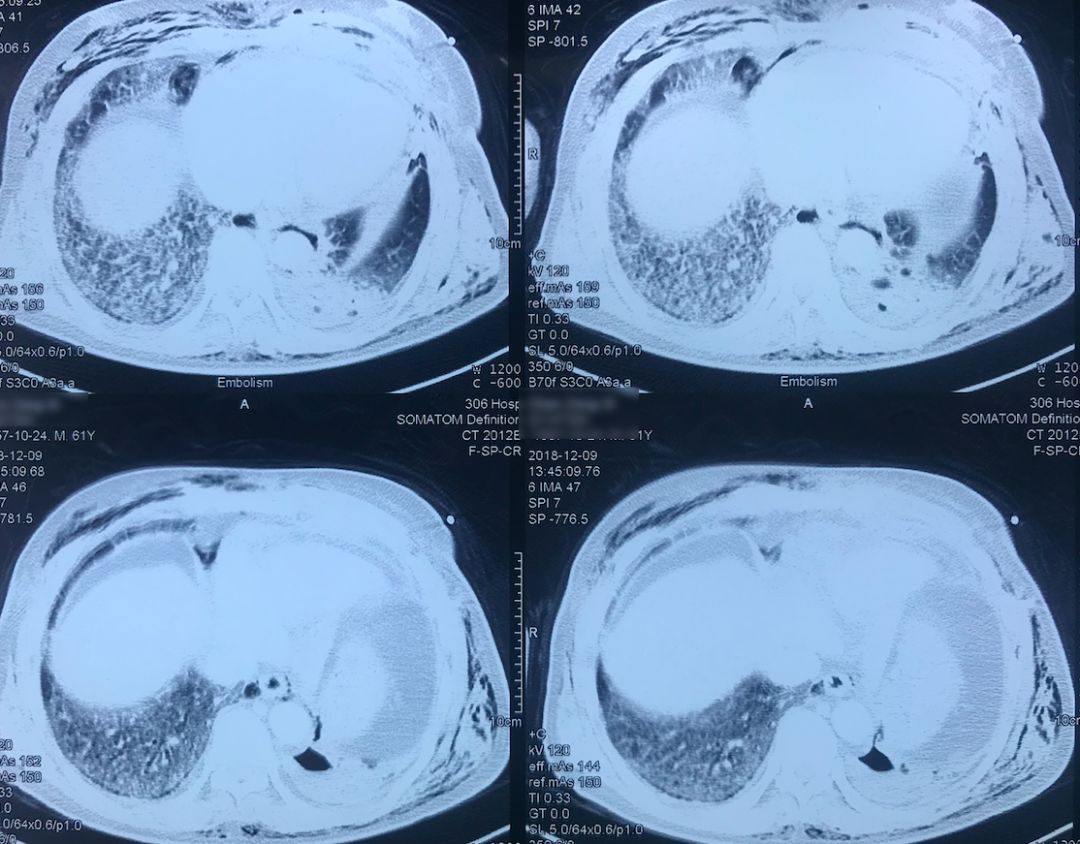
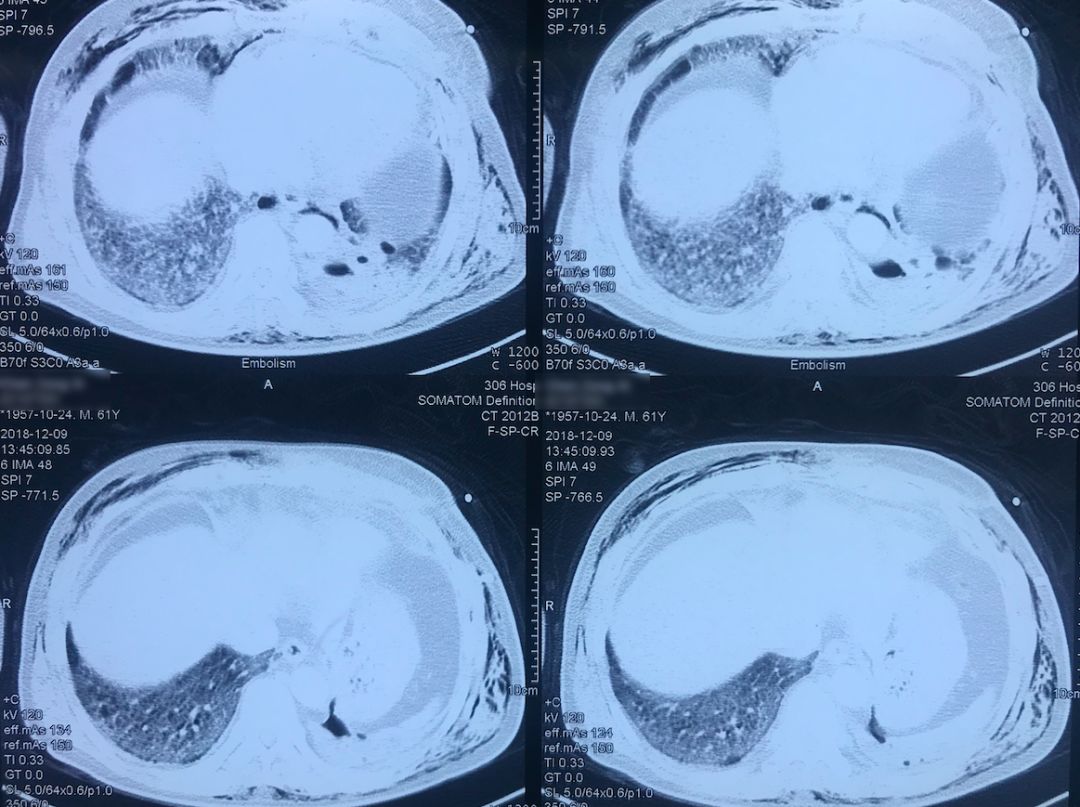
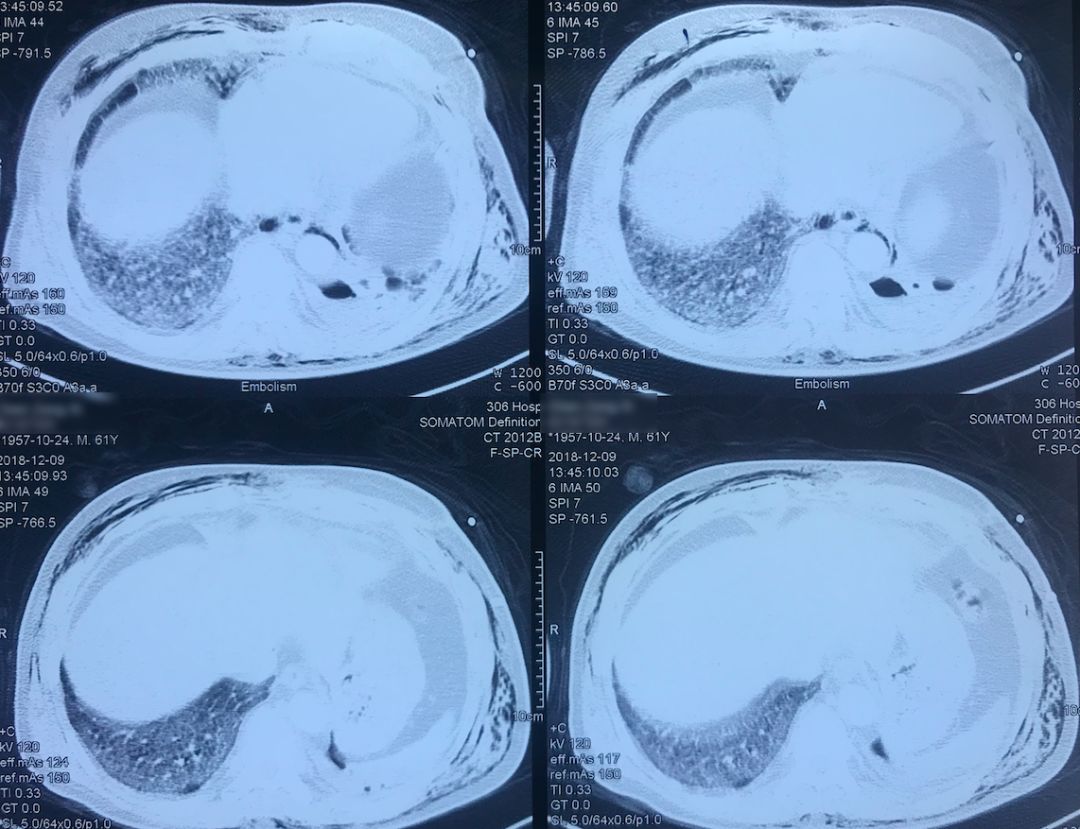
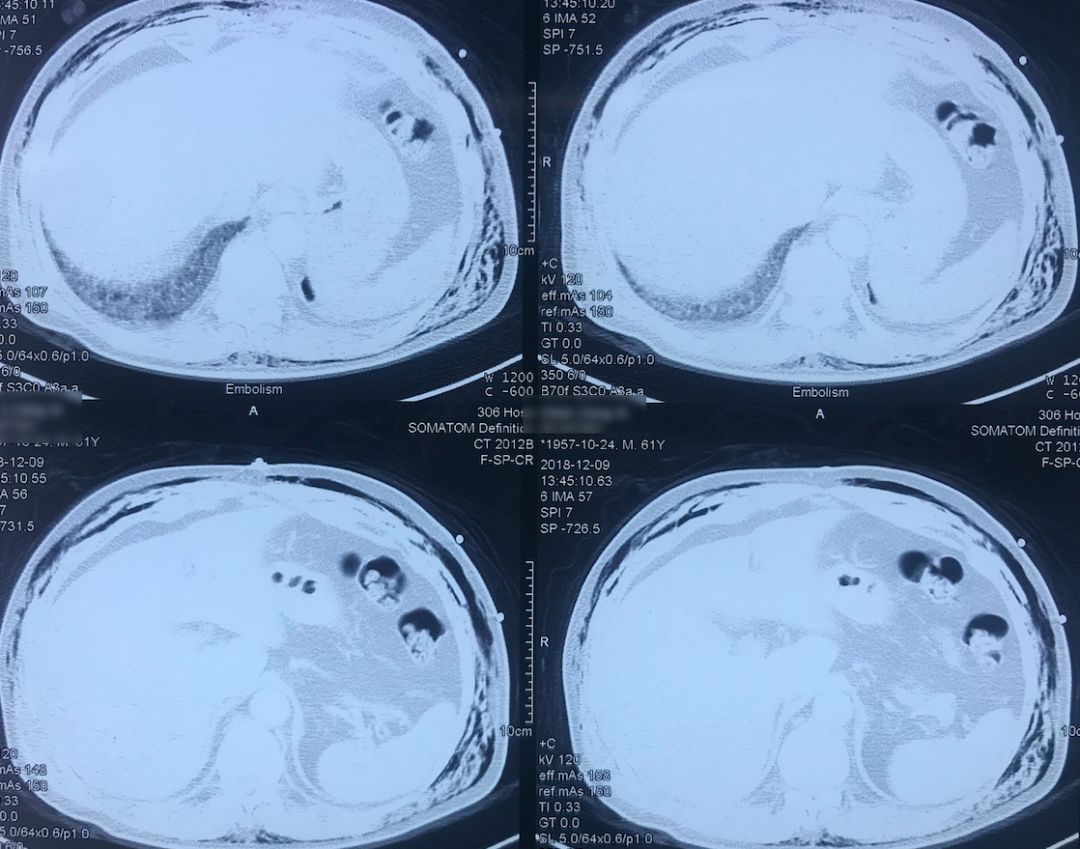
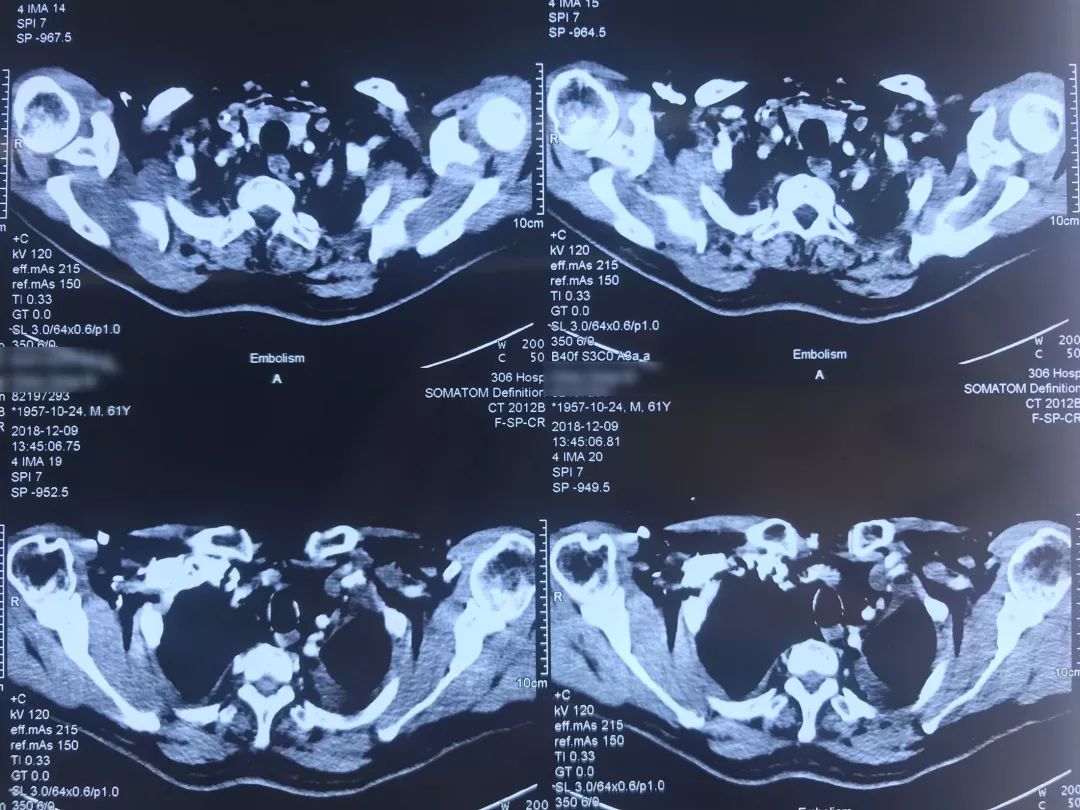
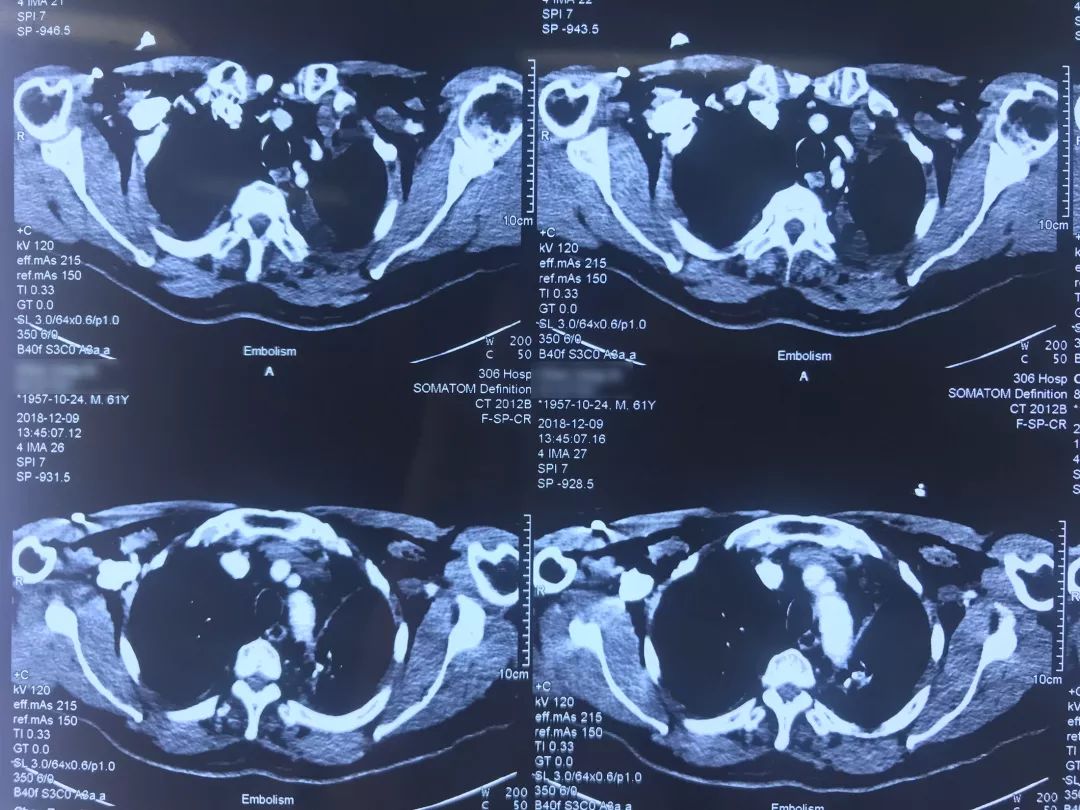
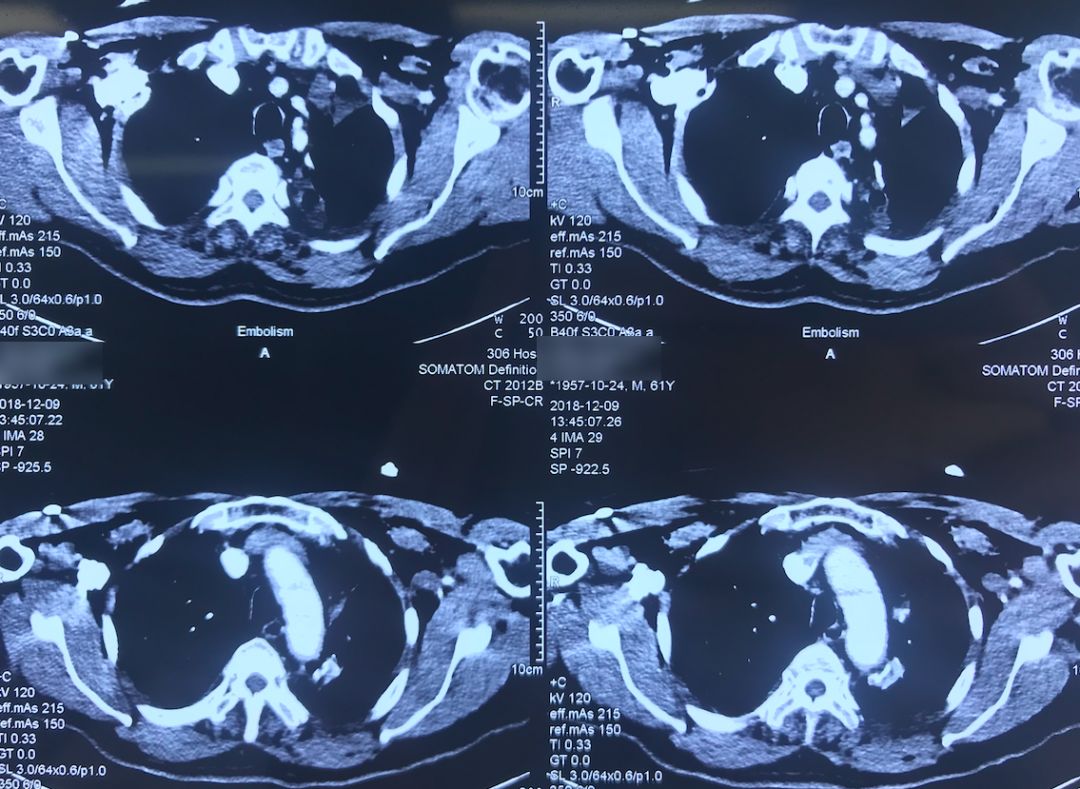
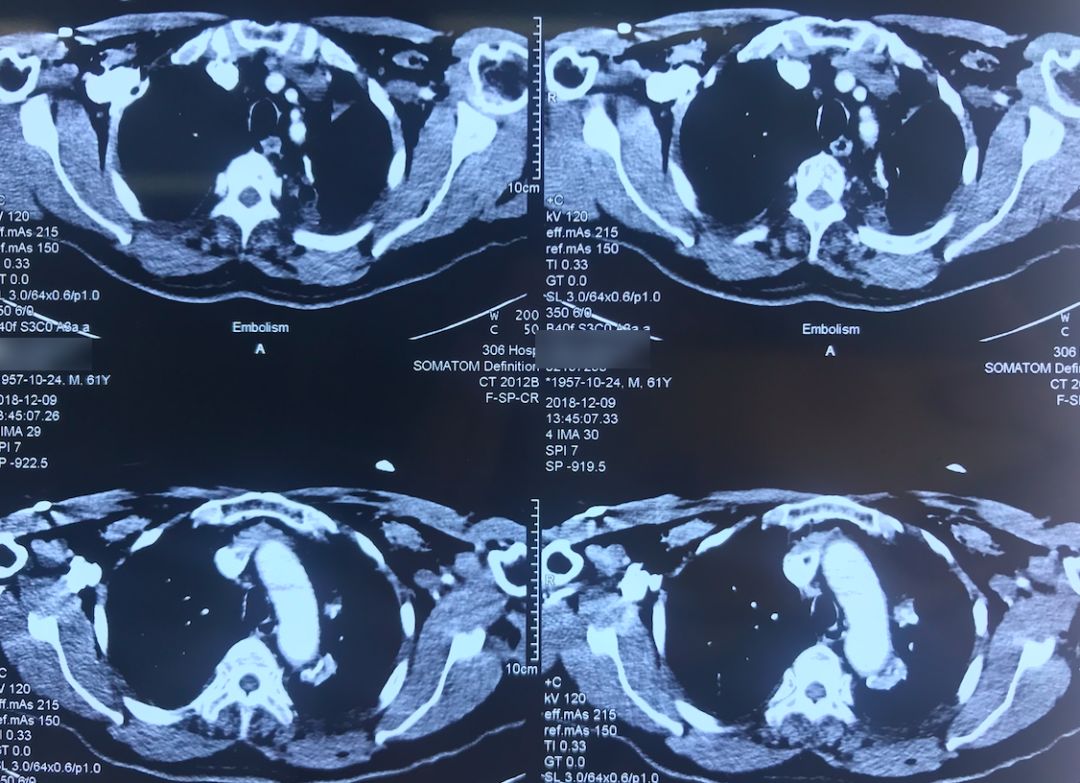
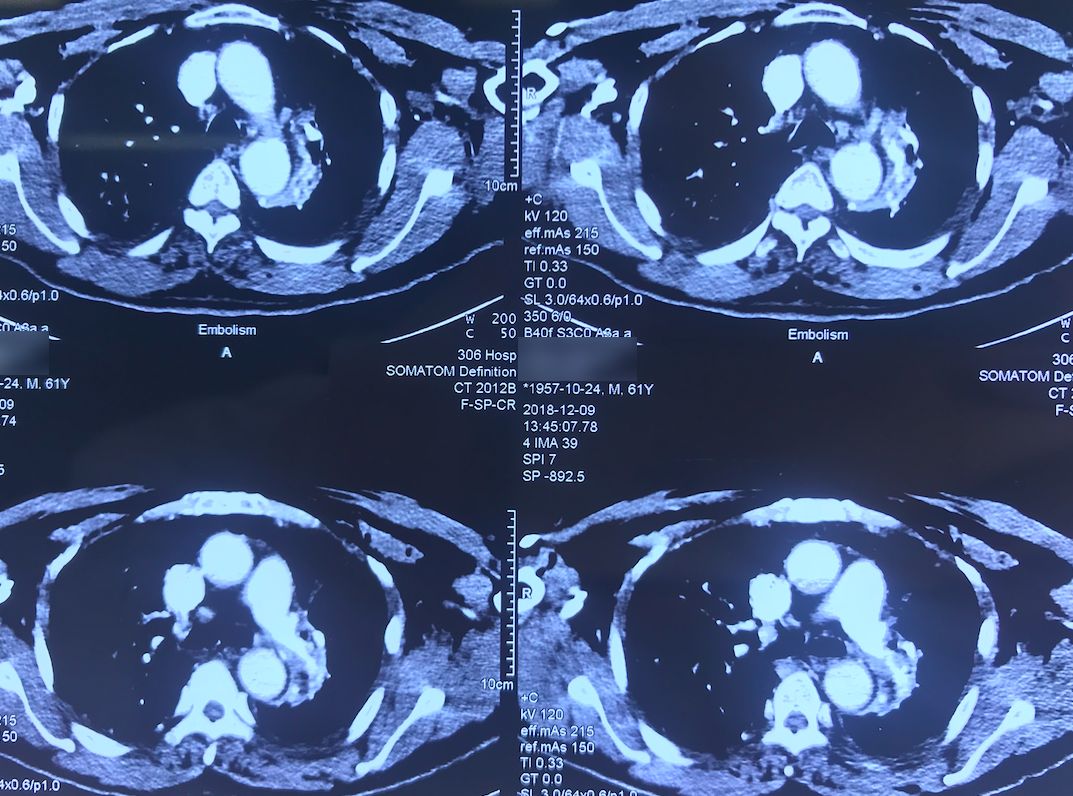
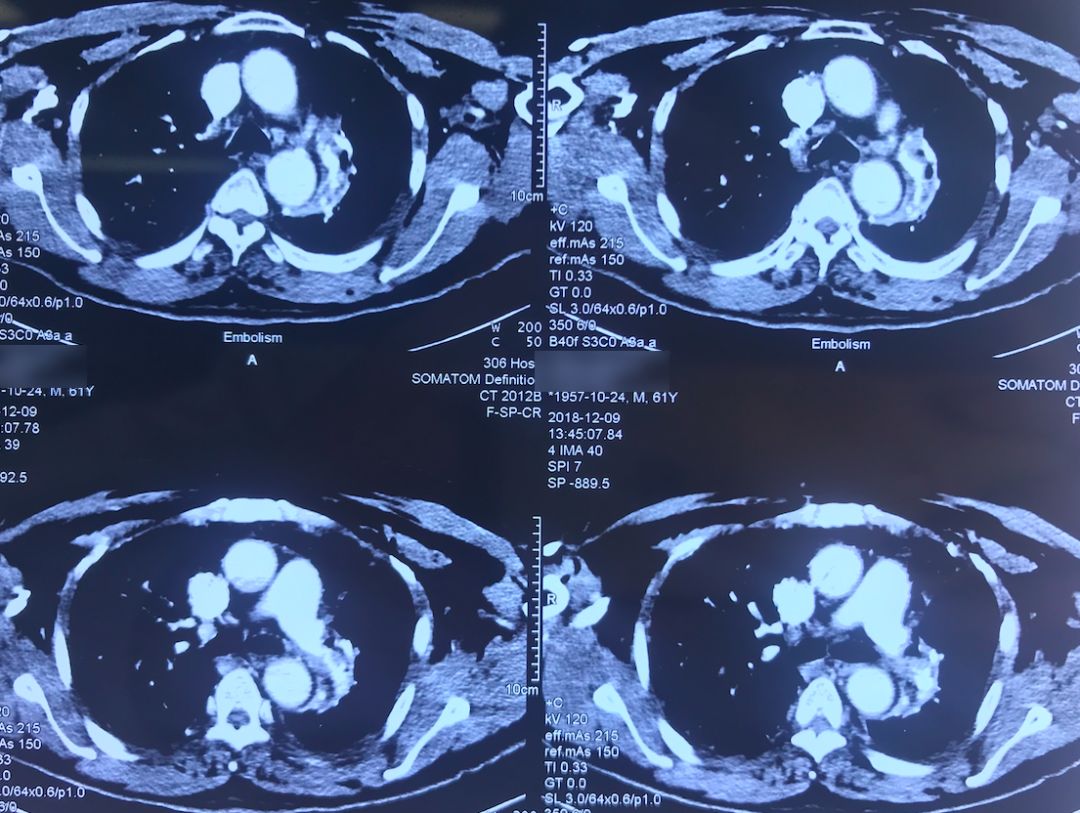
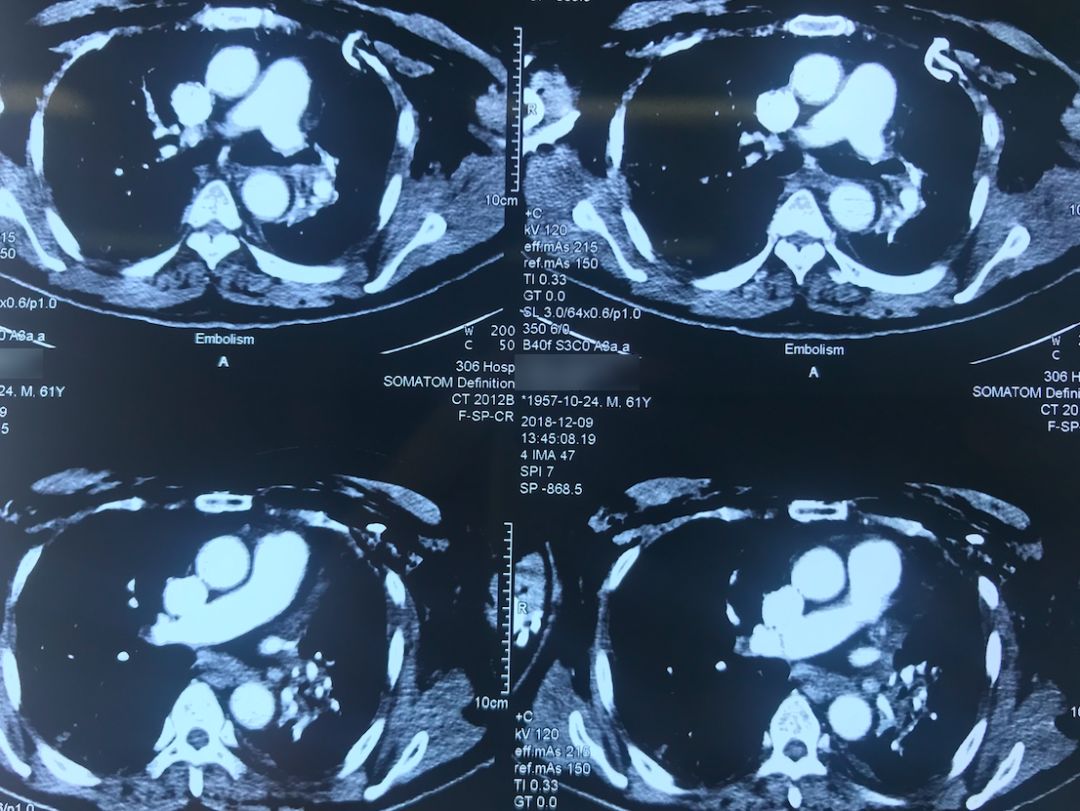
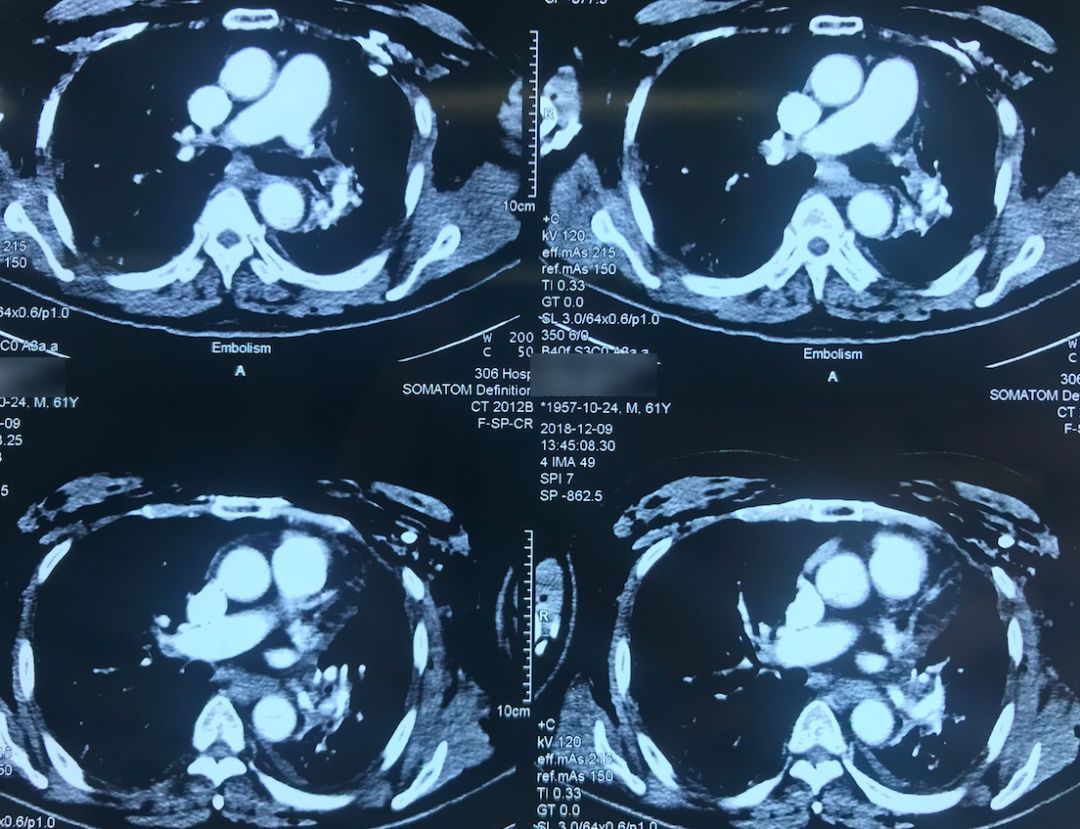
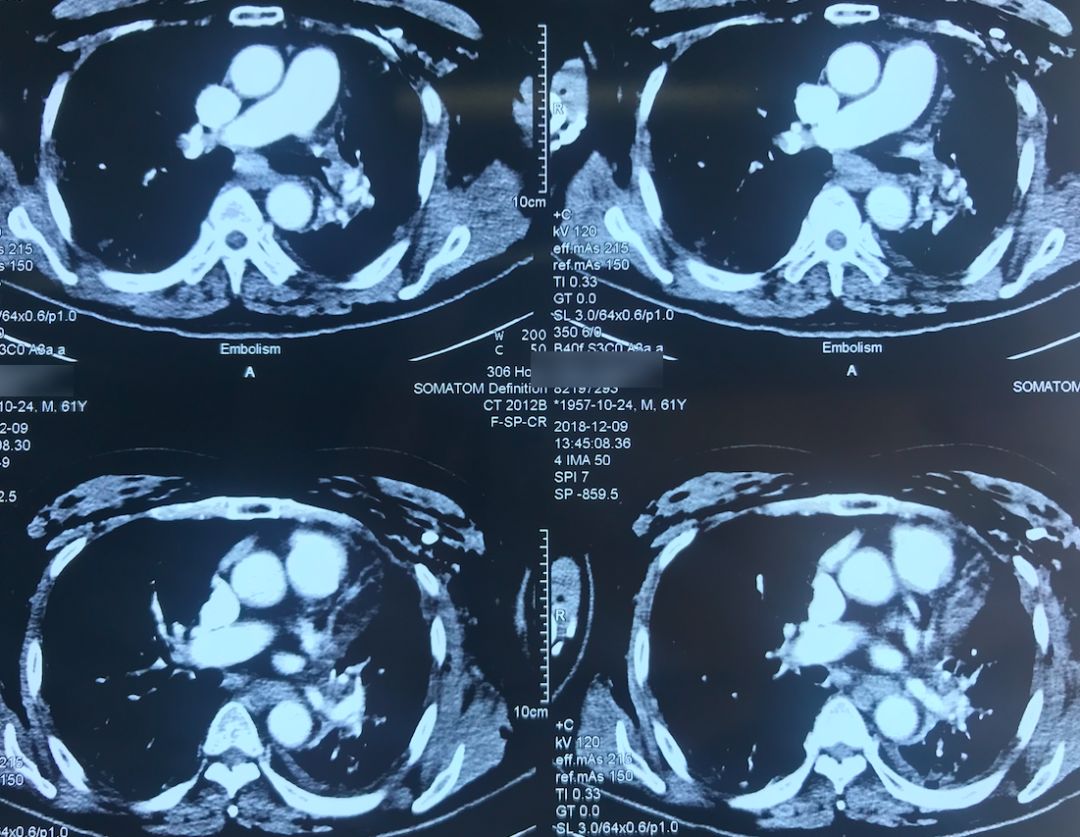
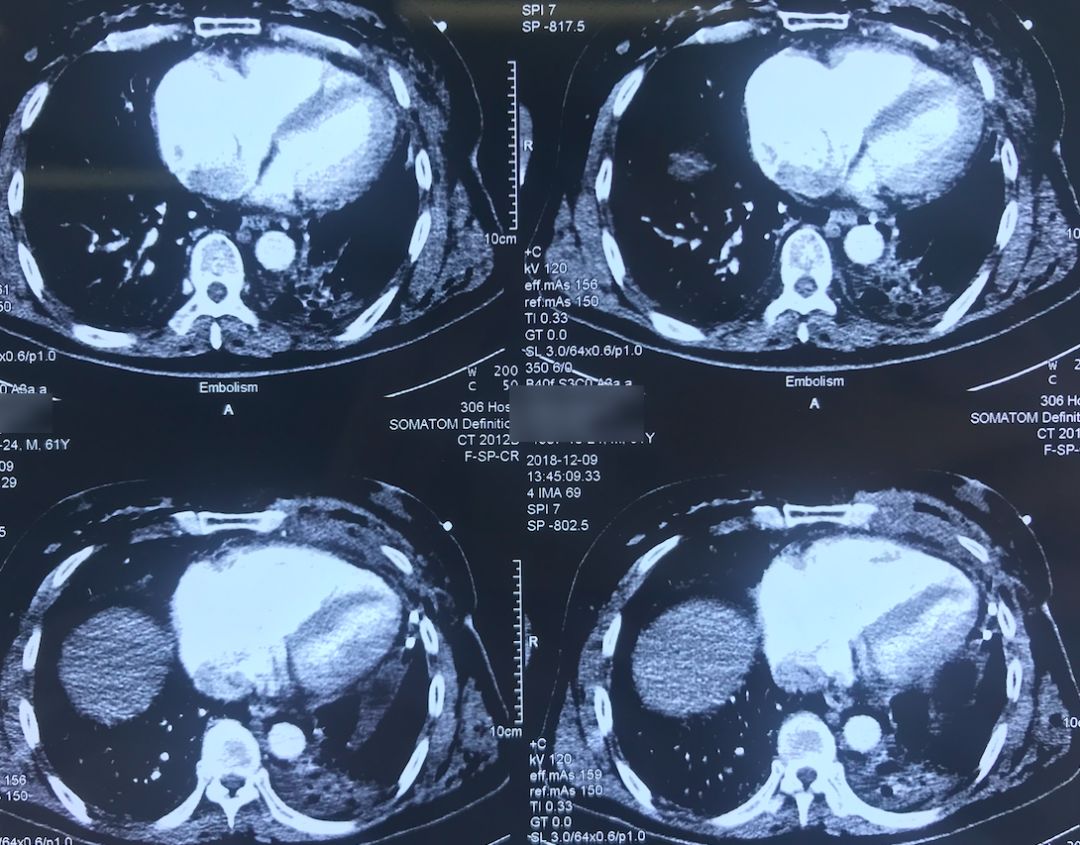
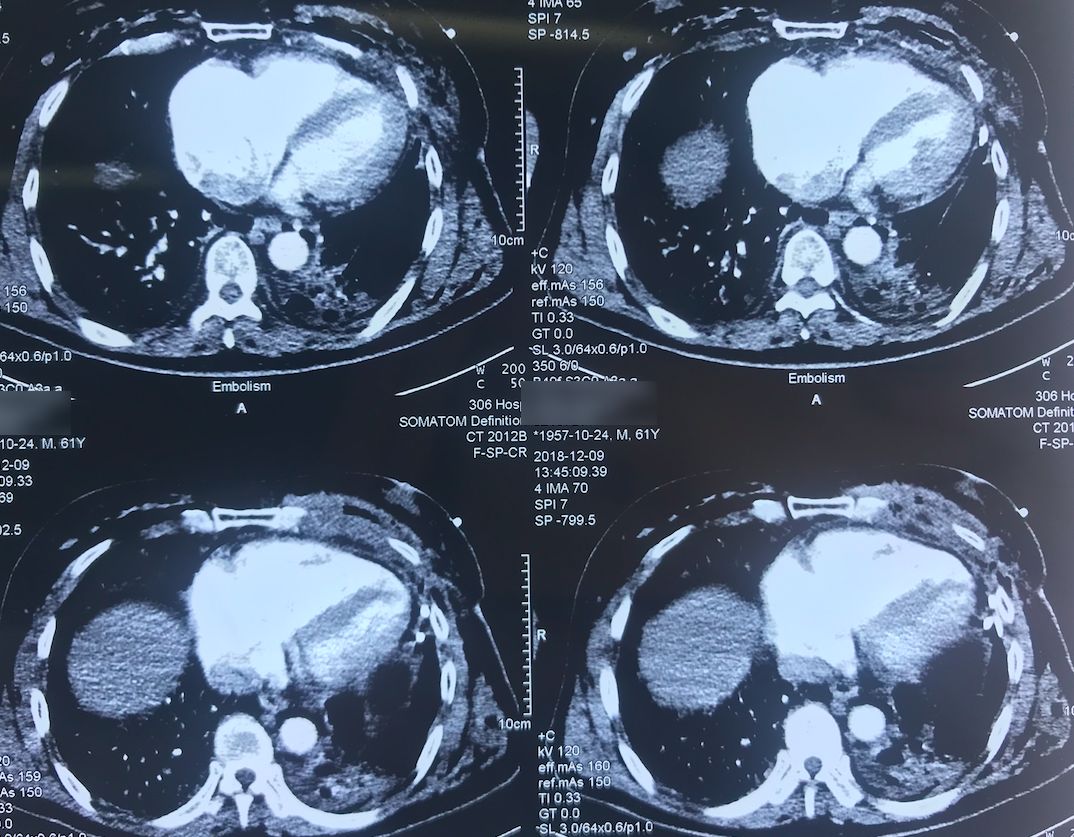
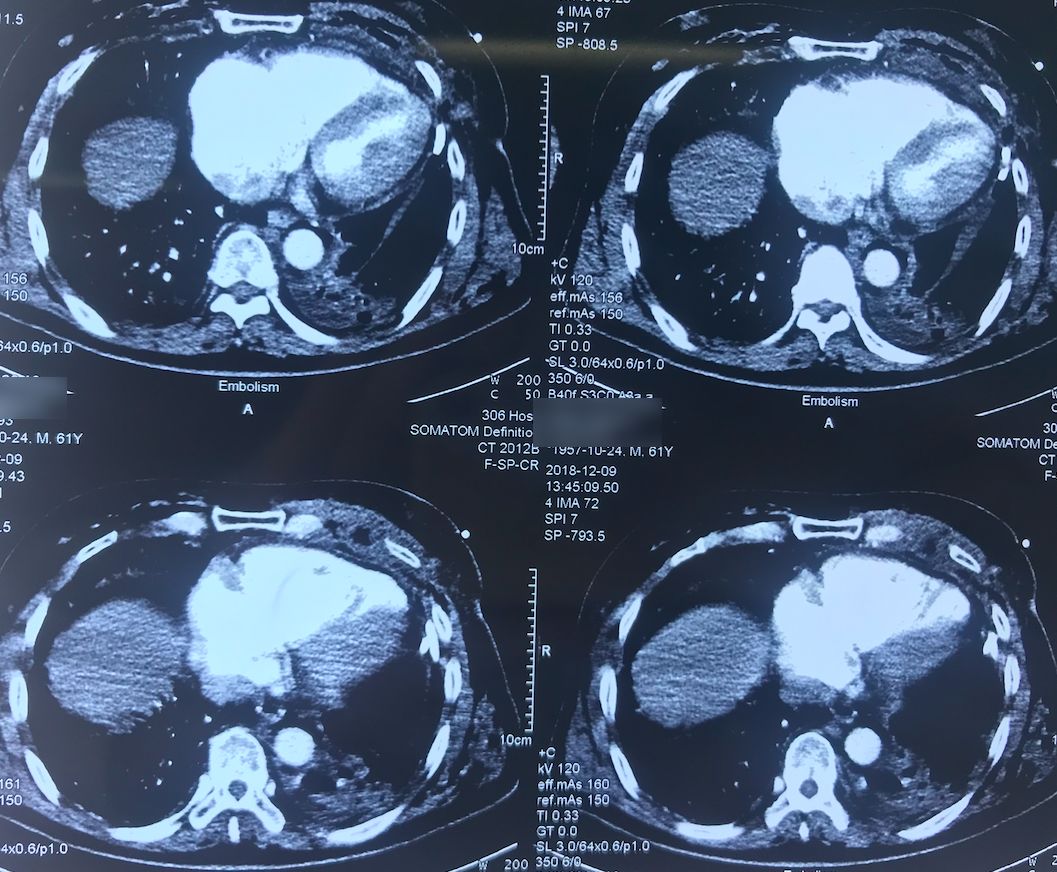
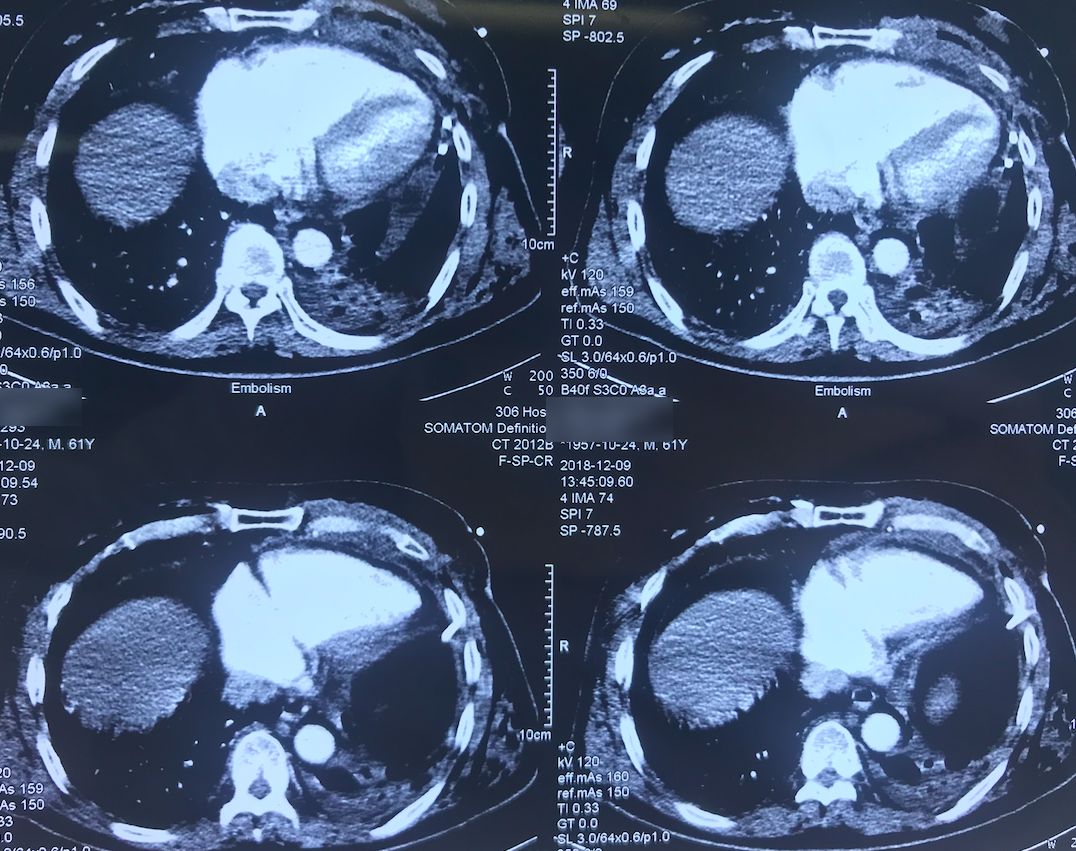
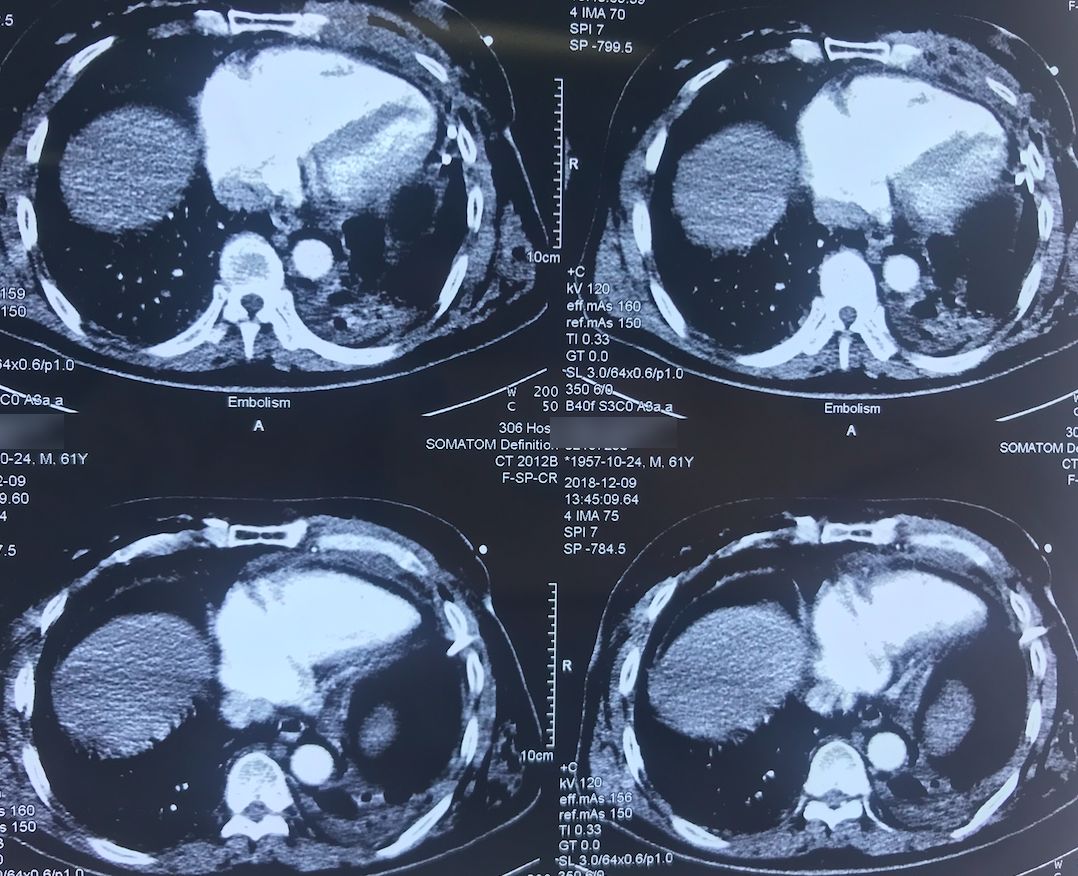
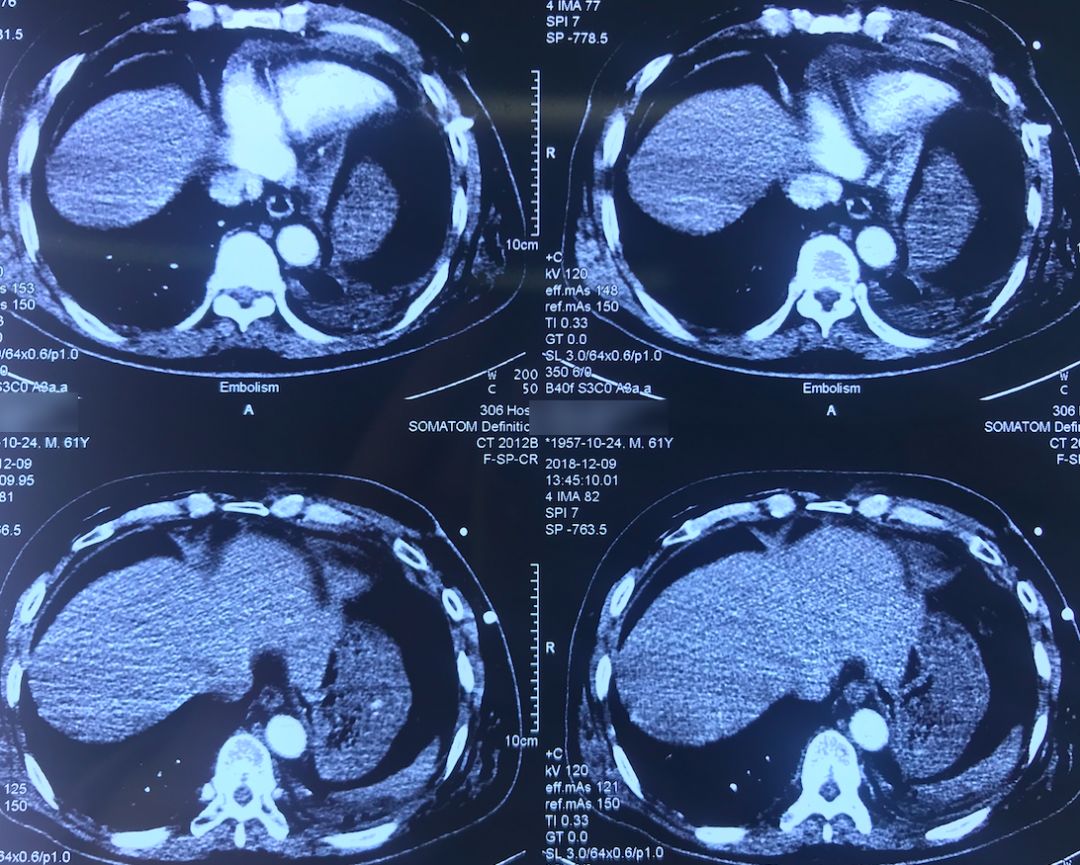
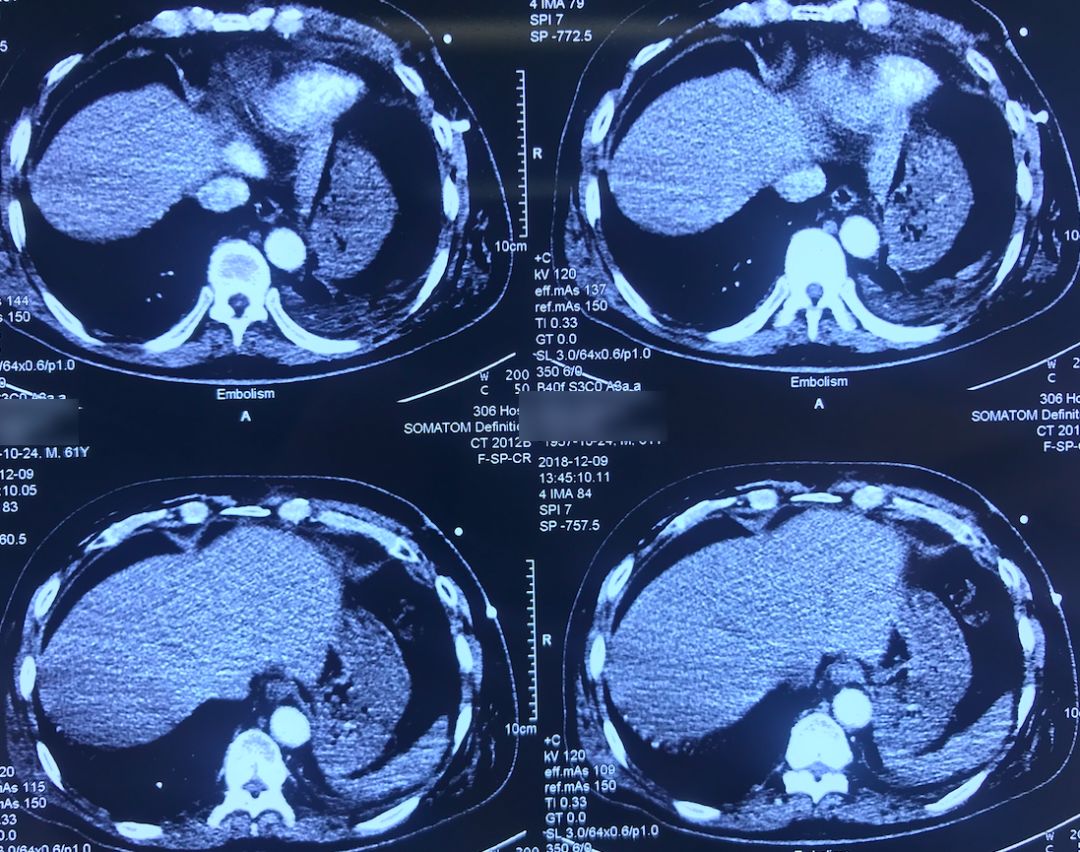
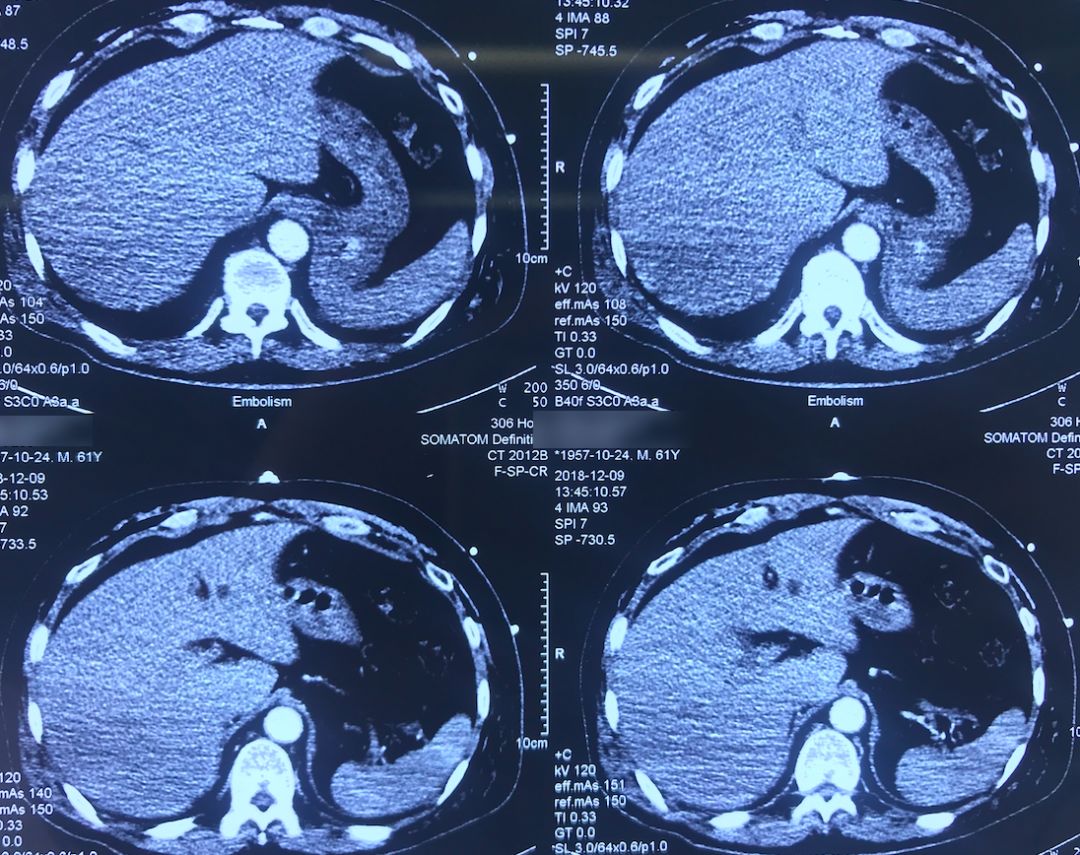
肺动脉CTA(2018-12-9)
左下肺动脉干有较明显的低密度影,考虑是左下肺动脉肺栓塞。
CT:

肺组织病理(外院)
(右下肺结节)楔形切除肺组织:肺不典型腺瘤样增生,伴中央局部间质纤维组织增生及慢性炎,直径0.3cm,周围肺组织多灶状慢性炎、纤维组织增生及炭末沉着。
(左上叶)肺叶切除标本:肺浸润性腺癌,腺泡型约40%,乳头型约30%,实性型约20%,微乳头型约10%,肿物直径1.7cm,镜下距肿物约1cm处见癌组织(镜下最大径约1mm),局部可见淋巴管内癌栓及局灶肺泡腔内癌细胞团,癌组织临近胸膜(镜下<1mm)但未累及,周围肺组织多灶性纤维组织增生伴炭末沉积及慢性炎至胸膜增厚,支气管切缘未见癌组织,支气管旁未查见淋巴结;送检第(7、9组)淋巴结未见癌转移(0/1、0/2);免疫组化显示肿瘤细胞:TTF-1(+),NapsinA(+),CD34(-),P53(-),Ki-67(10~40%),EGFR(-),PD-1(-),PD-L1(TC+,约60%),ROS1(-),ALK(-),P63(-),D2-40(-),PGP9.5(-),弹力纤维染色阳性。
既往史+个人史+家族史
既往史:慢性鼻炎病史2年。
个人史:吸烟30年,平均4支/日,未戒烟。否认饮酒史。
否认家族遗传病史。
入院查体
生命体征:T 37.0℃,P 116bpm,RR 20/min,BP 220/100mmHg。
发育正常,营养良好,急性病容,自主体位,神志清楚。
桶状胸,左侧胸壁于第3肋间隙左锁骨中线外2cm处留置胸引管;左侧胸壁第5肋间隙腋前线处留置胸引管;左侧胸壁可见长约20cm手术瘢痕,右侧胸壁可见长约10cm手术瘢痕。双侧前侧胸壁可及握雪感。
双肺呼吸音粗,双肺可闻及湿性啰音,未及胸膜摩擦音。
心率116次/分,律齐,各瓣膜听诊区未及杂音及额外心音。
腹软,无压痛及反跳痛,肝脾肋下未及,肠鸣音4次/分。
双下肢轻度对称可凹性水肿。无杵状指(趾)。
入院诊断
> 急性间质性肺炎?
I型呼吸衰竭
> 静脉血栓栓塞症
急性肺动脉血栓栓塞症(中危组)
左下肢肌间静脉血栓
> 原发性支气管肺癌(腺癌 左上肺 T1bN0M0 I 期)
左肺上叶切除术后
右肺下叶楔形切除术后
皮下气肿 纵隔气肿
左侧液气胸
> 甲型流感病毒感染
> 慢性鼻炎
入院后首先进行常规检查
血气分析(无创呼吸机的情况下,FiO2 0.65):pH 7.45,pCO2 50mmHg,pO2 79.4mmHg,HCO3- 32.3mmol/L,BE 6.6mmol/L,Lac 1.2mmol/L。
血常规:WBC 17.43x10^9/L,N% 91.5%,L 0.44x10^9/L,HGB 117g/L,PLT 186x10^9/L。
尿常规:血 330/ul,红细胞 1611.4uL,红细胞 290.1HPF。
血生化:ALT 127IU/L,AST 68IU/L,TBIL 10.2μmol/L,ALB 32.8mmol/L,LDH 636IU/L,CK 74IU/L,BUN 8.77mmol/L,SCr 55.3μmol/L,K 4.8mmol/L,Na 141mmol/L。
凝血功能:PT、APTT正常,D-Dimer 2mg/L,FDP 11.14ug/ml,Fib 8.91g/L。
心梗四项:NTproBNP 2018pg/ml。
首先患者的PE诊断明确,但是PE不会引起肺间质病变,那么间质病变是什么原因引起的?因此,我们进行了一些筛查,先要除外感染,所以先完善了感染指标。
感染指标
血GM试验 0.59(<0.5)。血G试验、T-spot 阴性。多次血培养阴性。
BALF(2018-12-11)细菌涂片、真菌涂片、抗酸涂片、Gene-Xpert、细菌培养、真菌培养、病毒核酸(甲流、乙流、腺病毒、呼吸道合胞病毒)、GM试验、CMV、PCP均为阴性。
导管头细菌培养 阴性。
尿液细菌培养 阴性。
免疫相关指标
抗核抗体谱+血管炎抗体谱+类风湿关节炎抗体谱:阴性。
免疫球蛋白+补体:正常范围。
蛋白电泳:白蛋白 48.4%(55.8-66.1%),α1球蛋白 11.7%(2.9-4.9%),α2球蛋白 15.8%(7.1-11.8%)。
T细胞亚群(2018-12-17):N 510cell/ul,CD3+ 425cell/ul,CD3+CD4+ 360 cell/ul(380-1208),CD3+CD8+ 73 cell/ul。
淋巴细胞亚群(2018-12-24):N 430cell/ul,CD3+ 302cell/ul,CD3+CD4+ 214 cell/ul,CD3+CD8+ 83 cell/ul;NK 71cell/ul;B细胞亚群B2 14.6%(1.45-9.49%)。
KL-6 498U/ml(<500)。
全都是阴性。
肿瘤相关指标
CEA 14.26 ng/ml(<5);CA125 95.83U/ml(<35);NSE 23ng/ml(<16.3);CYFRA21-1 9.61ng/ml(0-3.3);
余均正常。
支气管镜(2018-12-11)
各叶段开口通畅,支气管黏膜光滑,未见充血水肿,气管镜下多叶段内可见少量白色粘稠痰液。
由于患者还有液气胸,所以对胸水进行检查。
胸水化验
胸水常规(2018-12-12):外观 血性;黎氏试验 阳性;细胞总数 满视野;有核细胞 120mm³,单核51.0%,多核49.0%。
胸水生化(2018-12-12):总蛋白定量 15.2g/L,ADA 8U/L,LDH 459IU/L,GLU 8.69mmol/L,CL 109mmol/L 。
胸水真菌涂片、抗酸涂片、Gene-Xpert均为阴性。
那么,入院后如何开始治疗?
首先完善病原学检查,除外感染。由于入院时血象明显升高,所以考虑有感染的情况,于是亚胺培南+奥司他韦抗感染治疗。
但是针对肺间质病的情况,首先明确的是PE不会引起间质性病变,其次是甲流有阳性,但是影像学又不是典型的甲流影像,何况在我院复查时,不仅甲流为阴性,所有病原学检查均为阴性,这种情况下,我们考虑间质病是肺癌术后出现的急性间质性肺炎。
所以进行激素冲击治疗:2018-12-12(入院第3天)开始甲强龙500mg*3d,同时给予呼吸支持:无创呼吸机辅助通气,S/T 模式:IPAP 8cmH2O,EPAP 4cmH2O,FiO2 0.65。
入院后感染指标情况:
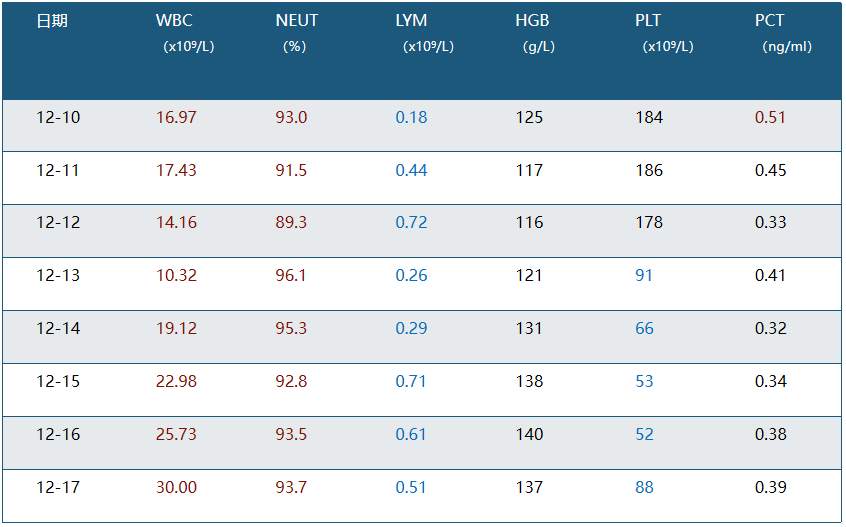
入院前3天,血象较高,经过抗感染治疗后血象逐渐下降,刚入院时的PCT轻度升高,后来也逐渐下降。12月12日开始使用激素冲击治疗,所以后来血象再次升高,但是PCT一直都是比较正常的情况。
入院一周后复查胸部CT:
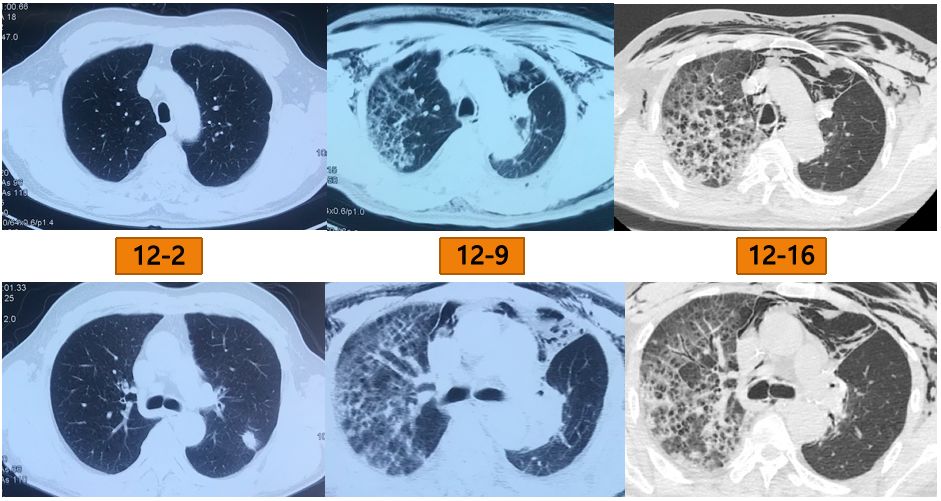
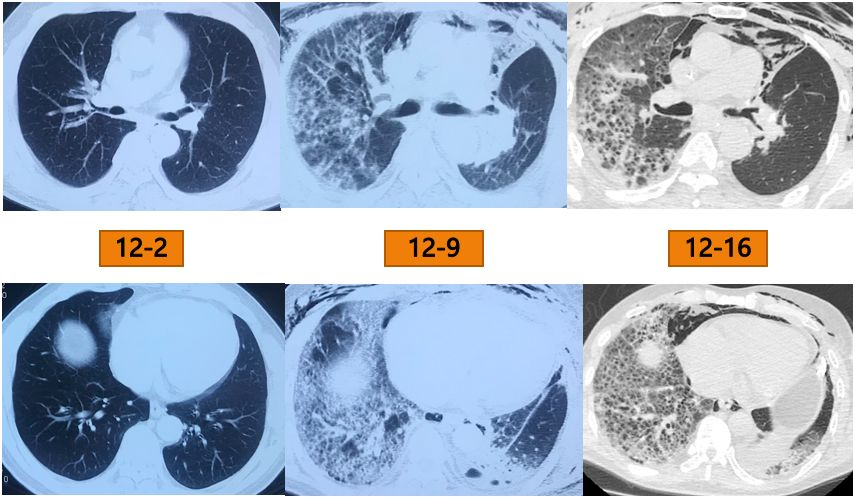
HRCT(2018-12-16):左下肺开始出现一些网格影;颈部、纵隔/双侧前侧胸壁气肿,左侧少量气胸,左侧少量胸腔积液;左肺下叶炎性病变;右肺间质性改变较前进一步加重,并出现蜂窝样的改变。
影像学的变化:
术前CT(12-2)可以看到双肺比较干净,没有任何间质性改变;但是在术后第4天(12-9),右肺出现明显的网格影、小叶间隔增宽;一周后(12-16),间质性病变出现进一步加重。
再来看看血气分析:

患者刚入院时氧合指数122.2mmHg,但是随着入院后病变的进展,氧合指数进行性下降。12月17日(入院一周后),我们已经给予患者无创呼吸机吸纯氧,但是PaO2也只有66.4mmHg,勉强维持,而且患者还有明显的气肿、气胸的情况。
在这种情况下,我们继续使用无创呼吸机可能难以维持氧合了。那么考虑气管插管?但这位患者已经使用500mg的激素冲击治疗,很明显是免疫抑制的情况,如果插管后,如何预防VAP?

于是我们决定给予患者使用清醒ECMO,2018-12-17开始 VV-ECMO +HFNC/NPPV 支持治疗。
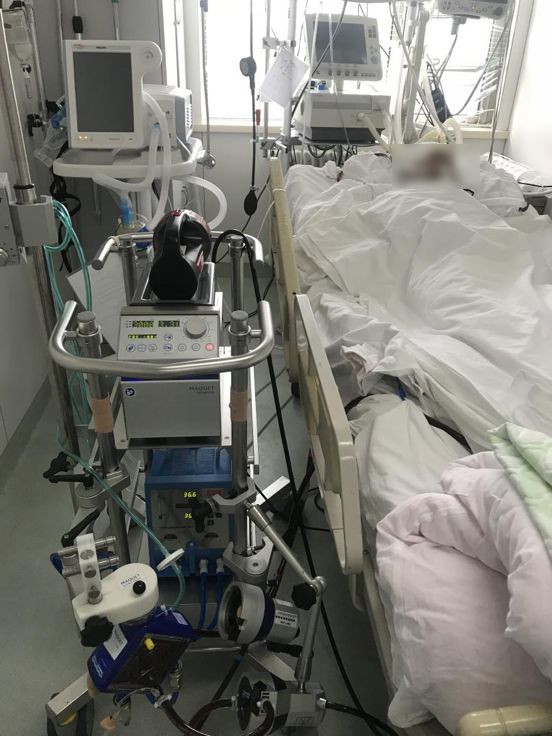
患者入院初期治疗情况
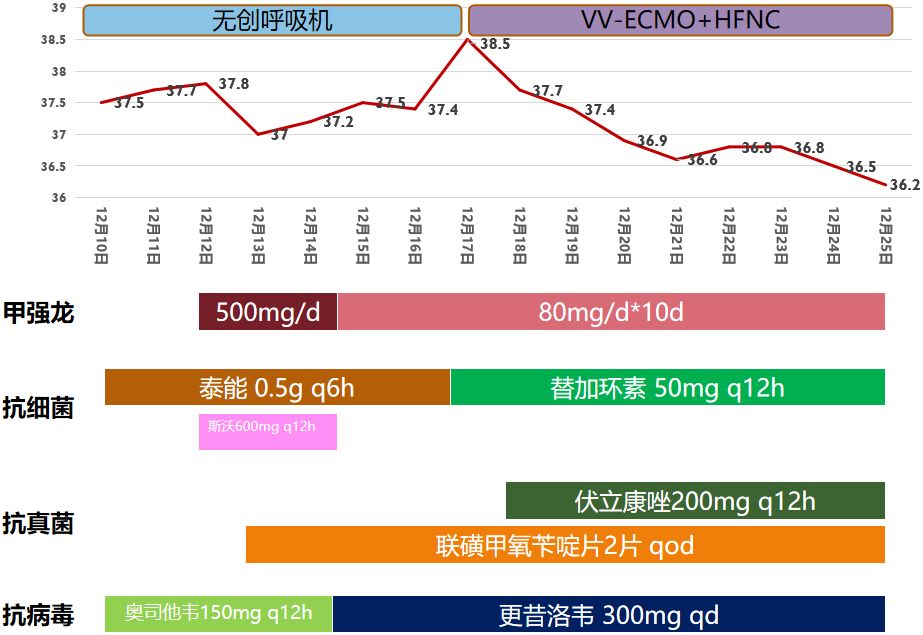
从入院第3天开始给予3天500mg/d的甲强龙,然后降到80mg/d,维持10天,之后减到40mg/d。同时给予抗感染治疗,尤其是在使用激素后,我们给予预防性的抗细菌、抗真菌、抗病毒治疗。
入院一周后影像学又发生了怎样的改变?
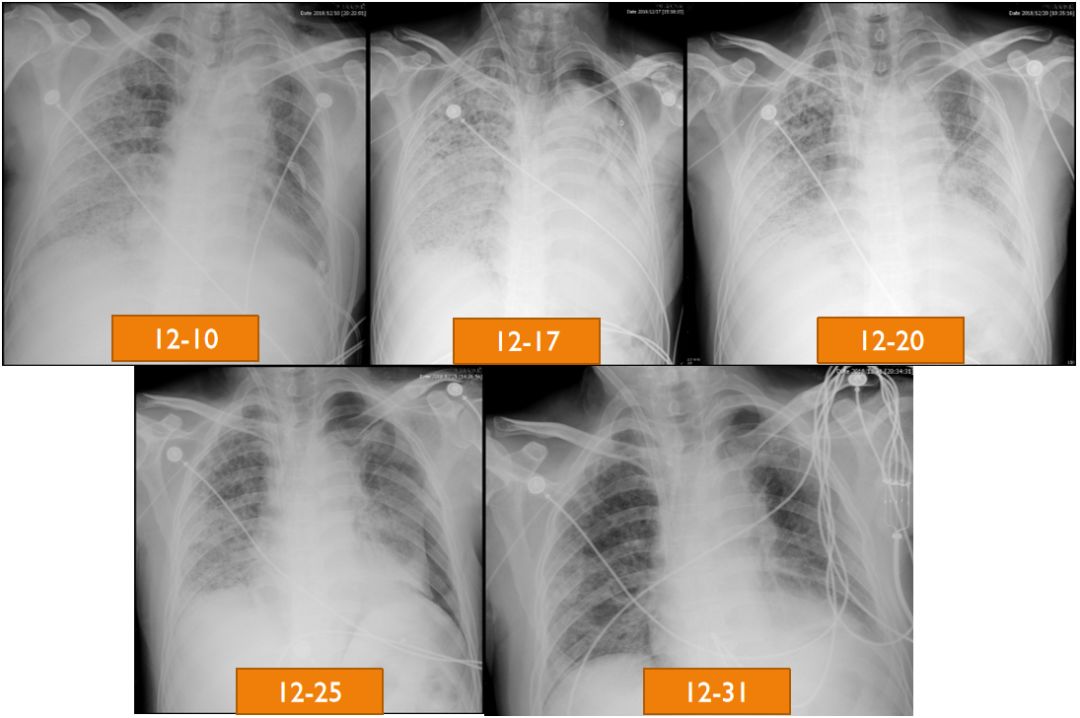
入院一周后病情进行性加重,但是在第二周病情有所改善,12月31日的胸片已经很「清楚」了。
复查胸部 CT(2019-1-2):
左肺术后改变,左侧液气胸较前吸收好转,双肺间质性肺炎较前好转,右侧少量胸腔积液。
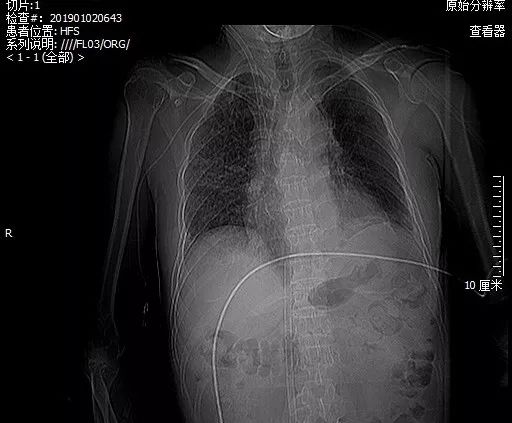
转归
2019-1-2夹闭ECMO 气源,HFNC 吸氧40%,2小时后复查血气分析:pH 7.44,pCO2 42mmHg,pO2 103mmHg,Lac 1.6mmol/L;
2019-1-3撤离 ECMO;
2019-1-10转出 ICU;
2019-1-20好转出院。
出院一个多月后随访(2019-3-1):
影像学较前进一步吸收。左肺及右肺下叶术后改变,大致同前。左侧胸腔积气现已消失,胸腔积液略减少,双肺间质性炎症,较前减少。
讨论要点
1、我们治疗时,考虑患者是肺癌术后的急性间质性肺炎——术前肺部很干净,仅为单纯的小结节,但是术后出现急性间质性病变。这种情况不是我们遇到的第一例,文献上也查到了相关资料,所以我想听听各位老师的经验。
2、关于激素治疗的剂量。我们给予了500mg的激素冲击。对于这类患者,500mg的剂量是否过大?还是240mg或者160mg就足以?
3、另外,清醒ECMO在免疫抑制患者中的应用。因为免疫抑制患者很容易继发院感,尤其是VAP,那么对于这种患者,如果能够避免插管,对于院感的预防应该会有比较好的改善。
专家介绍

吴小静
主治医师,医学博士,毕业于北京大学医学部,现就职于中日医院呼吸与危重症医学科。2014年9月进入 PCCM 培训体系,2018年6月通过全国PCCM 结业考试。熟练掌握呼吸与危重症基础理论及各项支持技术,包括严重呼吸衰竭的诊治、呼吸支持、呼吸机管理、血流动力学管理、CRRT、ECMO 等。主要研究方向为重症肺炎的诊治及发病机制。


