
一、无创通气概述
无创正压通气(noninvasive positive pressure ventilation,NPPV)指通过口鼻面罩、全脸面罩、鼻罩、鼻枕、头盔等无创性的连接方式,将患者与呼吸机相连接,进行正压辅助通气。近年来,无创通气的使用日益增多。美国一项回顾性研究纳入了2000—2009年1200万呼吸衰竭患者,结果发现,无论是慢阻肺患者还是非慢阻肺患者,无创通气的使用都有明显上升趋势[1]。2002—2017年国家住院患者数据库及ICD编码查询结果显示,无创通气的使用从2002年的41/100000增长至2017年的220/100000,而有创通气的应用同期并没有明显上升趋势[2]。
随着治疗理念的更新以及治疗技术的进步,无创通气和有创通气患者的住院死亡率都有明显下降趋势。总体而言,无创通气的使用日益增多,成为高达42%的呼吸衰竭患者的首选支持方式[3]。但无创通气失败概率高居不下,根据病种不同,无创通气失败率为5%~60%。与无创通气成功组相比,无创通气失败组的死亡率明显上升。既往研究表明11.4%~15%的患者无法耐受无创通气,5%~40%的患者会因无创通气失败行气管插管。即刻(<1 h)和早期(<48 h)失败分别占无创通气失败患者的15%和68%[4]。导致无创通气失败的高危因素是我们临床工作中需要关注的问题(表1)。
表1 无创通气失败高危因素
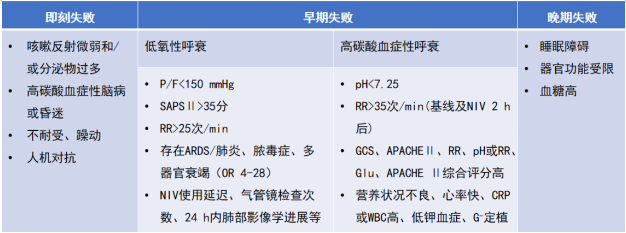
早在2009年,中华医学会呼吸病学分会就制定了《无创正压通气临床应用专家共识》[5],其中提到了非常经典的无创通气操作程序,包括患者评估、治疗场所选择、患者的教育、患者体位、连接方式选择、呼吸机的选择、参数设置、后续监测等。
二、无创通气患者的选择与教育
1. 患者的选择
1.1 适应证
无创通气的总体应用指征包括:①基础疾病或急性加重疾病有可逆性;②需要辅助通气:a. 症状:中至重度呼吸困难和呼吸增快【RR>24次/min(慢阻肺患者);RR>30次/min(心衰患者),伴辅助呼吸肌肉动用或胸腹矛盾运动】;b. 血气分析:pH<7.35,PaCO2>45 mmHg,或PaO2/FiO2<200 mmHg。③排除有无创通气禁忌证的患者。
疾病的可逆性对无创通气的成功至关重要,疾病进程处于不断恶化的状态,无创通气不足以改变疾病恶化的趋势(ARDS);对于可逆性疾病,无创通气可以改变疾病进程。这也是患者上机过程中需要密切监测的原因,要及早识别无创通气失败的患者,减少因无创通气导致的气管插管延迟。
无创通气作为一种呼吸支持方法,具有最佳适应证。指南和共识中提及的对无创通气治疗反应最好的疾病,例如2009年中国专家共识[5]提出,慢阻肺急性加重、慢阻肺急性加重脱机、心源性肺水肿以及免疫功能受损的呼吸衰竭,这几类患者可以从无创通气中明确获益。但2017年ATS/ERS指南[6]仅对慢阻肺急性加重以及心源性肺水肿提出了强推荐,这两类患者可以从无创通气中获益,慢阻肺急性加重脱机、免疫功能受损的呼吸衰竭以及术后呼吸衰竭,仅为条件性推荐。后续研究发现,并非所有患者都可以从无创通气中获益,临床中需要评估无创通气的效果,然后决定是否继续使用。
1.2 禁忌证
(1)绝对禁忌证(有1个或以上谨慎尝试无创通气):①呼吸或心跳骤停;②意识严重受损;③严重威胁生命的非呼吸系统器官衰竭(上消化道大出血、血流动力学不稳定等);④上气道梗阻;⑤气胸(未引流);⑥无法配合、无气道保护能力;⑦面部手术、创伤或畸形;⑧近期食管吻合术等。
(2)相对禁忌证:①轻度昏迷;②躁动;③严重低氧血症(PaO2/FiO2<100 mmHg);④自主呼吸微弱等。
1.3 应用时机
临床上使用NPPV时,需要有明确的目标:①预防拔管后呼吸衰竭发生;②当存在呼吸衰竭时,防止临床生理情况进一步恶化,预防插管;③辅助有创通气撤机;④作为DNI/DNR患者的保守治疗手段。临床上多数采用“试验治疗-观察反应”的策略。如果没有无创通气禁忌证的呼吸衰竭患者,则先试用无创通气治疗观察1~2 h,根据治疗后的反应决定是否继续应用无创通气或改为有创通气。不同的目标,无创通气成功的可能性不同,指南中推荐的比较适合进行无创通气的患者成功率最高,而拔管后呼吸衰竭、ARDS、重症肺炎、哮喘急性发作以及插管的患者成功的可能性比较低[7]。
(1)慢阻肺急性加重患者:对于慢阻肺急性加重患者,目前多采用动脉血pH对呼吸衰竭进行分层(表2)。
表2 利用动脉血pH对呼吸衰竭进行分层

当患者pH≤7.35,PaCO2>45 mmHg,且呼吸频率超过20~24次/min时,应使用无创通气。无创通气是慢阻肺急性加重患者首选的呼吸支持手段,无论pH多低,都可以试用无创通气,但需要注意pH越低,越需要对患者进行密切监护,无创通气失败后及时转为有创通气。
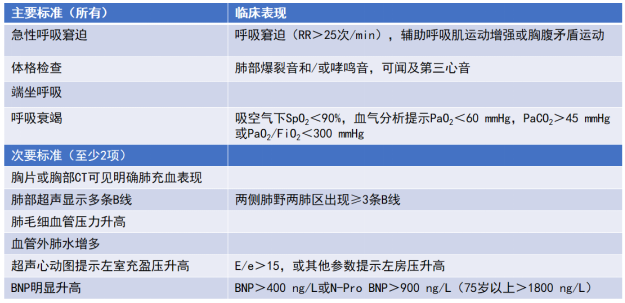
(2)心源性肺水肿:满足下表中4项主要标准和2项以上次要标准即可诊断为心源性肺水肿(表3)[8],就可以开始无创通气治疗。
表3 心源性肺水肿诊断标准
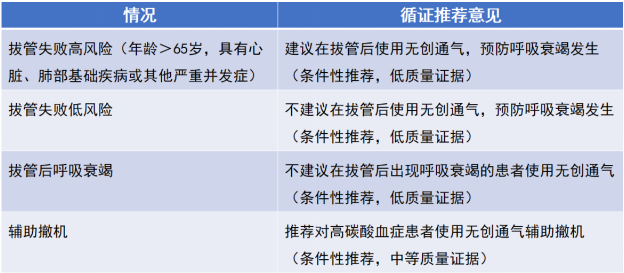
(3)气管插管拔管后:表4列举了拔除气管插管后适合采取无创通气的情况。
表4 气管插管拔管后适合无创通气的情况
2. 患者的教育
与有创通气不同,无创通气需要争取患者合作,对患者的教育可以消除恐惧,争取配合,提高患者的依从性与舒适感,也有利于提高患者的应急能力,如在咳嗽、咳痰或呕吐等紧急情况下能够迅速拆除连接,提高安全性。
患者教育的目标是:消除恐惧,争取配合,提高依从性。
患者需要知道:①治疗作用和目的(缓解症状、避免插管);②治疗时间长短及无创撤离计划;③治疗过程中可能出现的各种感觉,如佩戴面罩会有压迫感和束缚感、正压通气可能会导致憋气、不适感等,帮助患者正确区分和客观评价自身感受;④无创过程中可能出现的问题和处理措施,如面罩导致的面部不适、眼部刺激、胃肠胀气,需要咳痰、饮水或感觉不适时可呼叫医务人员;⑤需要指导患者佩戴时尽量闭口呼吸,规律放松呼吸;⑥连接和摘除面罩的方法,或呼叫医务人员的方法。
三、无创呼吸机选择
对于呼吸机的选择,有很多方面的考量,例如:漏气补偿能力、人机同步性(随患者呼吸触发和切换)、氧源类型、监测功能、报警功能、防干扰能力、体积、花费等[9]。因为不同的呼吸机,其无创通气效果大相迳庭。例如,PB840有创呼吸机进行无创通气,其漏气补偿能力会较差,如果漏气量很多,可能会导致人机不同步。V60无创呼吸机,最大漏气补偿可达到240 L/min,SV70最大漏气补偿为120 L/min。
临床上可用来进行无创通气的呼吸机主要有三大类。第一类是配备无创模块的重症呼吸机,即有创呼吸机,其特点是双回路,内置呼气阀门,漏气补偿仅在PCV模式或无创模式打开时才能使用;氧源为高压氧,通过空氧混合器控制,氧浓度在21%~100%之间连续可调,因此低氧患者可用;连接时注意选择本身不带漏气的面罩。第二类是专业重症无创呼吸机,第三类为家用无创呼吸机。后两类均为单回路无创呼吸机,通过面罩自带或管路中的呼气阀呼气,可使用自带呼气阀的面罩或额外使用单独呼气阀。家用无创呼吸机用外接的低流量氧气,能达到的实际氧浓度非常低,不适合严重低氧患者[10]。
四、无创通气连接方式选择
呼吸机连接方式直接决定了患者对无创通气的依从性。2015年一项针对五大洲57个国家157家医院普通病房使用无创通气的调查发现,32%的医院中对无创通气很有经验的医务人员不能24小时在医院,病房使用无创通气时,医生和护士的参与度也比较低,分别有19.9%的医生和24.8%的护士完全不参与无创通气治疗;46.3%的医院完全没有呼吸治疗师。这会导致与面罩或连接方式相关的并发症发生率非常高,72%的患者发生了面罩相关的皮肤压伤,65.6%的患者发生了面罩相关的漏气量过大,67.5%的患者拒绝使用无创通气;由于依从性不好,最终导致42%的患者单纯由于对面罩或连接方式不耐受而治疗失败,行气管插管[11]。
无创通气理想的连接方式主要包括:漏气量小,死腔小、阻力低,重量轻、质地软,不致敏(硅胶),与患者面部相吻合,经济实惠,有多种型号大小。理想的固定方式主要是:稳定(防止面罩位移),穿戴简单、快捷,重量轻,质地软,型号大小多样,适配多种面罩,可清洗(家用),可抛弃(医用)。
无创通气的连接方式主要有六种,包括口鼻面罩、鼻罩、鼻枕、全脸面罩、口含嘴、头盔。重症患者常用口鼻面罩、全脸面罩及头盔。不同连接方式各具优缺点。①口鼻面罩:优势为漏气较少、无需额外配合、可调整舒适度;劣势为可引起呕吐、幽闭恐惧、交流、咳痰障碍、患者不舒适;②鼻罩:优势为可讲话/进食、可咳嗽、减少呕吐风险;劣势为张口呼吸时漏气、鼻梁皮肤压伤风险、使用时鼻腔必须通畅;③全脸面罩:优势为漏气较少、无需额外配合、减少鼻梁压迫;劣势为可引起呕吐、交流、咳痰障碍;④头盔:优势为漏气量少、无需额外配合、无面部压伤风险;劣势为CO2重复呼吸、呕吐、噪音、人机不同步、腋窝不适(固定带)、上肢静脉血栓风险。
不同连接方式之间也存在一定的区别。例如,口鼻面罩分为两种,一种是面罩自身带漏气孔,另一种是面罩没有漏气孔,没有漏气孔的口鼻面罩可用于有创呼吸机进行无创通气时以及经口呼吸的患者。如何区分?如果转接头为蓝色,通常是无漏气孔的面罩,其他颜色一般都自带漏气孔。全脸面罩更适合幽闭恐惧、面部异常、没有牙齿、眼部刺激的患者。鼻罩一般在慢性病患者中使用更多。
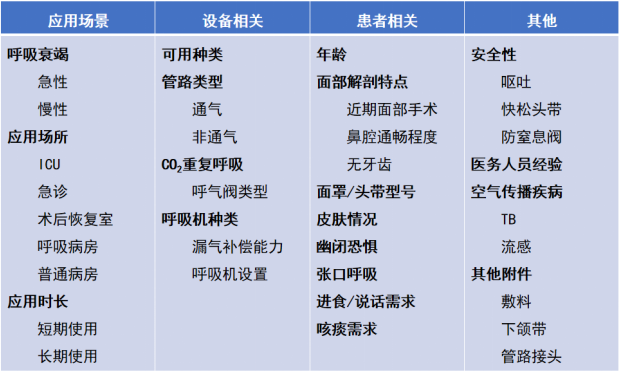
还有一些因素会影响无创通气连接方式的选择(表5)。
表5 影响无创通气连接方式选择的因素
2010年一项研究对25个欧洲国家272名医生(呼吸科136名,ICU/麻醉104名,其他32名)进行了调查。在德国、西班牙、法国、英国和意大利使用最多的呼吸机主要包括两种,一种是有创呼吸机进行无创通气(30%),另一种是专业重症无创呼吸机;连接方式选择最多的还是口鼻面罩[12]。
合适的口鼻面罩的解剖标记为:下唇之下(注意口微张状态),嘴角之外,鼻梁末端。可以选择好口鼻面罩后,要检查漏气量、人机同步性、呼吸机设置,判断患者是否适应。如果患者适应无创通气,再观察有无副作用,如果没有,患者有改善,则无创通气成功。如果患者不适应无创通气,要评估其是否适合继续使用无创通气,如果适合,再选择其他的连接方式。合适的鼻罩的解剖标记为:鼻翼两侧,鼻梁末端,上唇之上。面部异常、缺少牙齿、幽闭恐惧症的患者,还可以选择全脸面罩。
对于单回路管路,呼气装置是必须的。呼气阀有两类:面罩自带,管路连接(包括侧孔阀,平台阀,静音阀)(图1)。
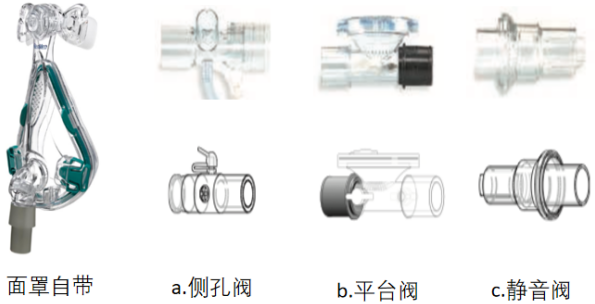
图1 呼气阀的种类
一项研究对比了在不同压力下不同呼气阀的漏气情况,可以发现,随着压力的升高,侧孔阀和静音阀的漏气量线性上升,但平台阀在压力很低的情况下,漏气量很大,随着压力升高,平台阀的漏气量处于恒定状态。这可以带来一定的益处:首先,在低压力情况下,漏气量大,可以减少二氧化碳重复呼吸。其次,在不同压力下,平台阀的二氧化碳重复呼吸量都很低。另外,使用平台阀时,随着压力升高,其漏气量并未进一步上升。可以减少因单纯压力升高导致的漏气阀额外漏气,无法达到治疗压力。所以对于二氧化碳重复呼吸或二氧化碳潴留的患者,可能使用平台阀更好。
五、患者连接
将患者与呼吸机进行连接时,首先协助患者取坐位或半卧位;选择合适的鼻/面罩,正确置于患者面部,用头带将面罩固定;调整面罩的位置和松紧度(1或2指原则);对自理能力较强患者,鼓励自己掌握佩戴和摘除方法。通常先佩戴好面罩,后接通呼吸机。这是由于呼吸机有漏气补偿机制,如果先断开呼吸机再佩戴面罩,可能会有大量气体吹向患者面部,导致患者拒绝使用无创通气。连接好呼吸机后,再次检查面罩,防止出现上紧下松或上松下紧的情况。
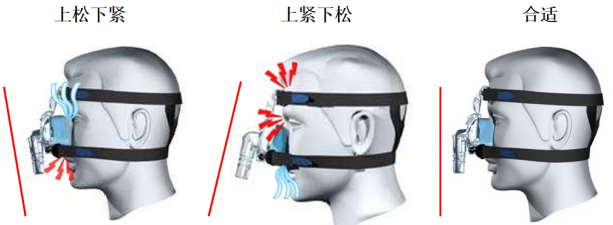
图2 检查面罩佩戴是否合适
如果患者对无创通气不耐受,再次检查面罩和头带大小是否合适,然后进行调整,降低漏气量。如果观察到患者胸廓起伏和呼吸机送气不匹配,可以降低漏气量,提高触发灵敏度,使患者触发更顺畅;增加EPAP直至8 cmH2O,改善人机同步性;同时可以考虑降低IPAP,增加后备的呼吸频率。
六、无创通气监测、评估与失败判断
无创通气上机后的监测和评估有助于尽早识别对无创通气治疗无反应的患者,减少插管延迟。在床旁要观察如下指标[13]:①患者的治疗反应,包括:a. 生理学指标,如饱和度、潮气量、血气分析;b. 客观指标,如呼吸频率、血压、心率;c. 主观指标,如呼吸困难程度、舒适性及神志情况;②患者的呼吸形式,有无出现胸腹矛盾运动及人机不同步;③面罩情况:佩戴是否合适,询问患者是否舒适,漏气量如何,分泌物及皮肤压伤情况;④辅助呼吸肌或胸腹矛盾运动是否缓解;⑤腹部情况,如有无胃肠胀气。此外,还应时刻准备插管。如果患者对无创通气没有反应性,且插管延迟,则患者预后会非常差。
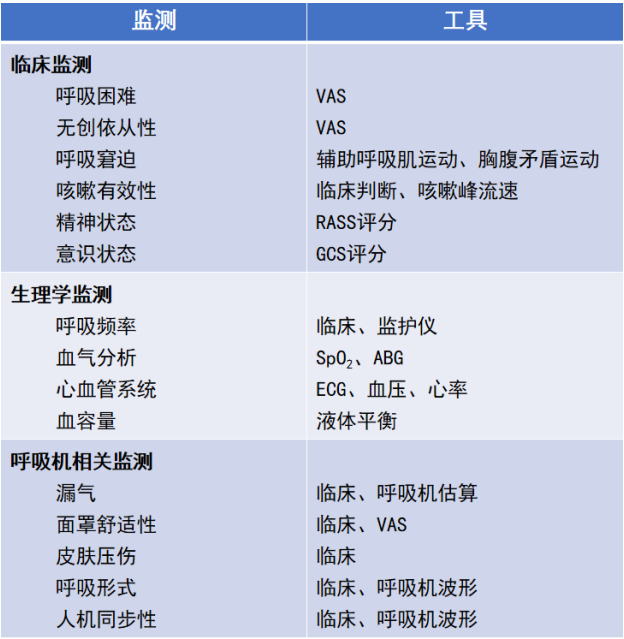
无创通气监测内容及评估工具如表6所示。
表6 无创通气监测内容及评估工具
1. 呼吸机监测
1.1 人机同步性
在RICU会遇到如下情况,慢阻肺患者漏气量很好,但参数设置不合适,监护仪显示呼吸频率30次/min,而呼吸机显示只有18次/min,观察患者的胸廓起伏,发现患者吸气与呼吸机送气不匹配,这可能是内源性PEEP(PEEPi)导致的无效触发。传统的PEEPi测定方法在无创通气中不容易实现,可以采用滴定法逐渐增加EPAP,当EPAP能够克服或对抗PEEPi时,可以明显改善人机同步性。
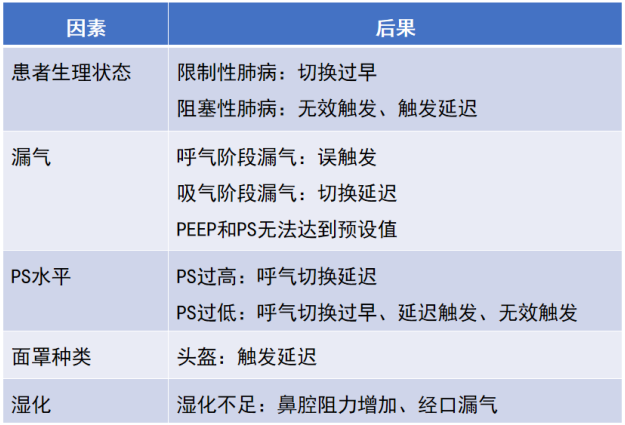
此外,还有很多因素影响人机同步性并导致相应的后果[14](表7)。
表7 影响人机同步性的因素及后果
针对无创通气人机不同步,也有文献提出了一些处理方法。①误触发:去除诱因,倾倒冷凝水或引流分泌物;如未发现诱因,可以调高触发阈值(如果可调)。②双触发:调整呼气触发灵敏度(如果可调)。③面罩周围大量漏气:调整面罩、头带以减少漏气。建议先将面罩摘下,然后再次佩戴,之后再调整头带,这样可使面罩的硅胶垫重新与面部吻合,效果更好。降低PS水平;缩短吸气时间。④无效触发:增加EPAP以对抗PEEPi;调低触发阈值(如果可调)[14]。
1.2 漏气量监测
漏气是无创通气与有创通气之间非常大的区别,漏气的监测也至关重要。漏气一般包括两种,一种是允许漏气,即从呼气阀中漏出的气体,它是患者呼出气体排出的地方,另一种非允许漏气,是由于使用鼻罩时张口呼吸或面罩没有戴好,从面罩周围或经口漏出气体。在使用无创通气时,一般要限制非允许漏气量<25 L/min,才能达到较好的人机同步性。
监测漏气量需要进行适当的设置,包括面罩种类的选择以及呼气阀的选择,选择好之后,呼吸机就会显示总漏气量以及患者漏气量。如果漏气量过大又没有及时处理,会导致不良后果。一项研究分析了不同漏气量(28 L/min和52 L/min)对实际的PEEP和PS的影响,当漏气量>28 L/min或>52 L/min,实际的PEEP和PS均无法达到设定值,治疗效果不理想。随着漏气量的增多,患者会出现触发延迟和切换延迟,都会导致人机同步性或患者耐受性下降,最终可能引起无创通气失败[15]。
另外,漏气量也会影响潮气量的监测。随着漏气量的增加,监测潮气量和实际潮气量之间的差值会不断的增大,漏气量越多,监测潮气量会比实际潮气量低得越多[16]。
1.3 潮气量监测
我们用模拟肺做过实验,漏气量从30 L/min增加到60 L/min,监测潮气量比实际潮气量最大可低25%。另外,当实际潮气量开始下降,监测潮气量并没有明显下降,而是缓慢下降,当实际潮气量恢复正常后,监测潮气量还没有恢复。无创通气并非实时监测,为估计潮气量,是对过去6次呼吸求平均。潮气量监测具有延迟性,需在多次稳定后记录。
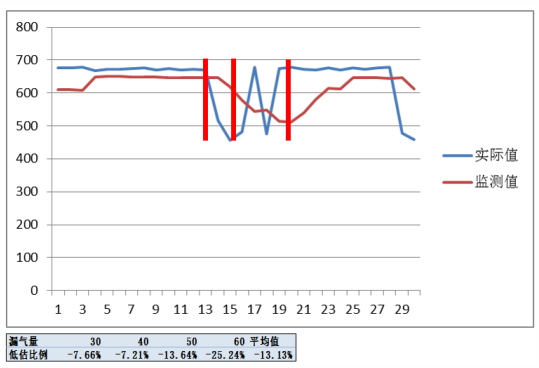
图3 模拟肺监测潮气量和实际潮气量与漏气量之间的关系
2. 患者监测
在不同时间点,无创通气患者的监测指标不同[17]。例如,上机5 min后,需观察漏气量是否合适?患者是否适应?患者主观感受如何?呼吸困难是否有所缓解?人机协调性如何?15 min后,观察胸廓起伏、呼吸音清晰是否改善?辅助呼吸肌动用消失/减少?呼吸频率及心率减慢?SpO2是否改善?30 min后,血气分析结果如何?是否需要调整参数?60和120 min后,动脉血气分析结果如何?
3. 无创通气成功患者特征
预测无创通气成功的因素有很多,包括:年龄小,疾病严重程度低(APACHEⅡ评分),漏气量少、牙齿完整,中度高碳酸血症(45 mmHg<PaCO2<92 mmHg),中度酸中毒(7.10<pH<7.35),无创通气2 h内气体交换、心率、呼吸频率改善,等。
七、无创通气失败的判断
1. 无创通气失败预测——慢阻肺急性加重
一项单中心前瞻性队列研究分析了超声评估膈肌功能不全对慢阻肺急性加重无创通气治疗失败具有预测价值,连续纳入75例慢阻肺急性加重呼吸性酸中毒患者,测量自主呼吸过程中膈肌厚度的变异度(ΔTdi),将ΔTdi<20%定义为膈肌功能不全(DD+)。膈肌超声采用7~12 MHz线阵探头,患者取45°半卧位,厚度测量取腋中线和腋后线之间膈肌与胸壁接合处图像最好的位置。膈肌功能不全组和膈肌功能正常组的年龄、基础疾病、pH和PaCO2均无统计学差异。结果显示,与膈肌功能正常组相比,膈肌功能不全组的无创通气失败率、RICU死亡率和90 d病死率均显著增加,机械通气时间更长,气管切开率更高,住ICU时间更长。ROC曲线分析发现,与基线pH<7.25、无创通气开始2 h后pH和PaCO2变化相比,ΔTdi<20%能更好地预测无创通气治疗的失败。该研究得出结论:早期超声评估膈肌功能不全,有助于识别无创通气高失败风险和不良预后的慢阻肺急性加重患者[18]。
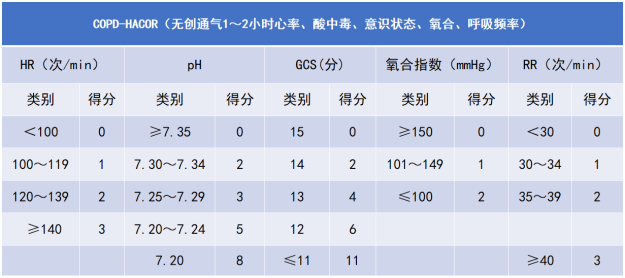
国内段均等开展的一项多中心研究选取500例慢阻肺无创通气患者作为推导队列,另取323例和395例患者作为内部和外部验证队列,通过单/多变量分析筛选无创失败相关变量,随后通过多元回归明确独立危险因素,构建回顾模型、评估权重、赋分,最终得到总分为27分的慢阻肺HACOR风险评分。研究发现,慢阻肺急性加重患者无创通气1~2 h,HACOR评分≤5分,无创失败概率为5.8%;而HACOR评分>5分,无创通气总体失败概率为50.2%,此时早期插管可以降低患者住院死亡率[19]。HACOR评分赋分见表8。
表8 慢阻肺患者HACOR评分赋分情况
2. 无创通气失败预测——心源性肺水肿
心源性肺水肿患者插管标准为:呼吸心跳骤停,意识状态持续恶化;无创通气下,pH、PaCO2或PaO2持续恶化;无创通气下,呼吸肌肉疲劳无法缓解;需要气道保护;持续血流动力学不稳定;躁动不安、无法耐受无创通气且呼吸衰竭持续进展。
心源性肺水肿患者无创通气失败的危险因素分为,①无创通气开始前的危险因素:肺部感染;意识状态改变;低血压;疾病严重度评分高;痰液量大;呼吸频率极快;高FiO2下,严重低氧血症。②无创通气开始后:参数设置不合理;连接方式不合适;漏气量过大;人机不同步;患者对无创通气耐受性差。③无创通气60~90 min后:呼吸频率、PaCO2无下降;pH、氧合无改善;呼吸肌肉疲劳。
3. 无创通气失败预测——低氧性呼吸衰竭
一项研究采用post hoc分析纳入既往RCT研究中23个ICU中RR>25次/min且氧合指数<300 mmHg的低氧性呼吸衰竭患者,探讨预测普通氧疗、经鼻高流量氧疗(HFNC)、无创通气治疗成败的预测指标。无创通气组共纳入110例患者。该研究发现,无创通气治疗1 h后氧合指数≤200 mmHg和潮气量>9 ml/kg为无创通气治疗失败的重要预测指标,无创通气1 h后潮气量>9 ml/kg与患者90 d死亡率独立相关[20]。
另一项前瞻性多中心RCT研究纳入21个中心200例轻度ARDS患者(氧合指数200~300 mmHg),对比文丘里氧疗和无创通气对插管率的影响,无创通气组共纳入102例患者。与文丘里氧疗相比,无创通气并不能降低插管率;无创通气第48小时,分钟通气量超过11 L/min是无创失败的独立危险因素[21]。
有研究通过二次分析的方法对既往一项前瞻性观察性队列研究中的426例接受无创通气患者的呼吸困难数据进行分析。呼吸困难情况通过改良Borg评分(1~10分,≥4分提示中至重度呼吸困难)进行评估。该研究发现,中至重度呼吸困难是无创失败的独立预测因素,同时也是住院期间死亡的独立预测因素[22]。
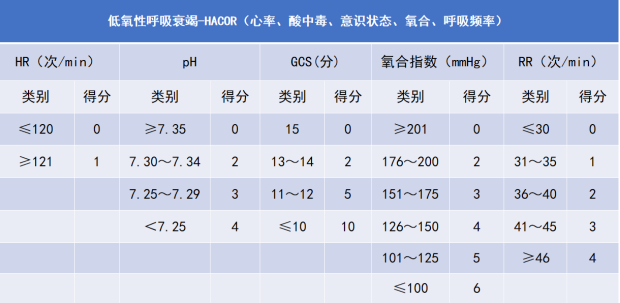
段均等开展的另一项HACOR评分预测低氧血症患者无创通气失败的研究,纳入449例低氧性呼吸衰竭无创通气患者,验证队列纳入358例患者。此研究中HACOR评分的赋分与上述慢阻肺患者不同(表9)。研究发现,HACOR评分越高,患者无创通气失败概率越高。无创1 h,HACOR评分≤5分,无创通气失败率为18.4%,住院死亡率为21.6%;HACOR评分>5分,无创通气失败率为87.1%,住院死亡率为65.2%。HACOR评分诊断低氧性呼吸衰竭患者无创通气失败的敏感性为72.6%、特异性为90.2%、阳性预测值为87.2%,阴性预测值为78.1%,无创通气失败诊断准确度达到81.8%。对HACOR评分>5分的低氧性呼吸衰竭患者早期插管,可以显著减少患者的死亡率[23]。
表9 低氧性呼吸衰竭患者HACOR评分赋分情况
4. 无创通气失败预测——评分系统
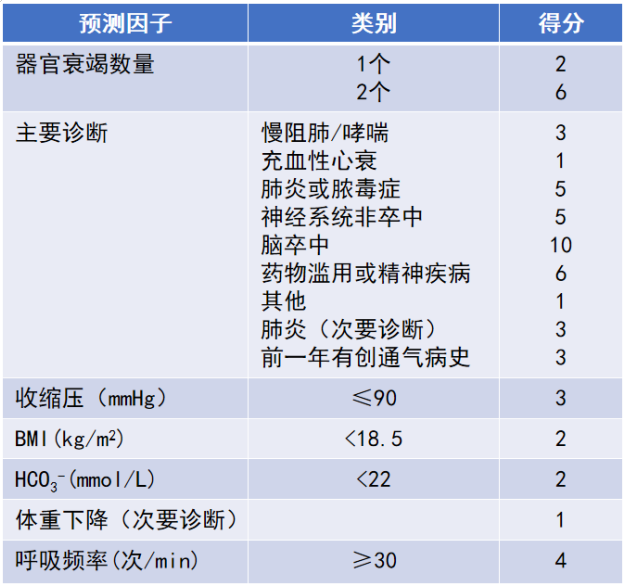
一项基于电子病历数据库的回顾性队列研究纳入2010—2014年数据进行风险模型建立,并利用2015—2016年数据进行模型验证,共纳入非手术无创通气患者47749例。该研究通过多元Logistic回归分析筛选出10个预测因子,并根据插管风险对预测因素进行赋分,根据得分多少识别无创失败风险。不同诊断的赋分不同(表10),这也代表了无创通气失败的风险。研究发现,低风险(评分≤5分)患者的插管率仅为2.3%,中风险(评分6~14分)患者的插管率为9.3%,高风险(评分≥15分)患者的插管率为35.7%。此评分量表也可以帮助我们评估患者无创通气失败的风险[24]。
表10 识别无创通气失败的综合评分系统
八、总结
近年来,无创通气的应用逐年增多,高达40%的呼吸衰竭患者接受无创通气作为一线治疗。合适的患者和连接方式选择,规范的无创通气上机及监测是无创通气成功的关键。然而,临床实践中,无创通气失败率仍居高不下,尤其是与患者耐受性差相关的即刻和早期失败,无创通气失败与患者不良预后密切相关,及早识别无创通气失败高危因素至关重要。除常见的无创通气失败高危因素之外,慢阻肺急性加重患者自主呼吸过程时膈肌功能不全(ΔTdi<20%)、无创通气1~2 h后HACOR评分>5分;低氧性呼吸衰竭患者,Borg评分≥4分、无通气1 h后潮气量>9 ml/kg、HACOR评分>5分、无创48 h后分钟通气量>11 L/min,预测无创失败的价值较高,对此类患者早期插管或可降低住院死亡率。此外,还可采用综合评分系统对无创通气失败概率进行预估,以及早识别无创失败高危患者。
参考文献
[1] Walkey A J, Wiener R S. Use of noninvasive ventilation in patients with acute respiratory failure, 2000-2009: a population-based study[J]. Ann Am Thorac Soc, 2013, 10(1):10-17.
[2] Kempker JA, Abril MK, Chen Y, et al. The Epidemiology of Respiratory Failure in the United States 2002-2017: A Serial Cross-Sectional Study[J]. Crit Care Explor, 2020, 2s(6):e0128.
[3] Schnell D, Timsit J F, Darmon M, et al. Noninvasive mechanical ventilation in acute respiratory failure: trends in use and outcomes[J]. Intensive Care Med, 2014, 40(4):582-591.
[4] Chandra D, Stamm J A, Taylor B, et al. Outcomes of noninvasive ventilation for acute exacerbations of chronic obstructive pulmonary disease in the United States, 1998-2008[J]. Am J Respir Crit Care Med, 2012, 185(2):152-159.
[5] 中华医学会呼吸病学分会呼吸生理与重症监护学组,《中华结核和呼吸杂志》编辑委员会. 无创正压通气临床应用专家共识[J]. 中华结核和呼吸杂志, 2009, 32(2):86-98.
[6] Rochwerg B, Brochard L, Elliott M W, et al. Official ERS/ATS clinical practice guidelines: noninvasive ventilation for acute respiratory failure[J]. Eur Respir J, 2017, 50(2):1602426.
[7] Scala R, Pisani L. Noninvasive ventilation in acute respiratory failure: which recipe for success?[J]. Eur Respir Rev, 2018, 27(149):180029.
[8] Masip J, Peacock W F, Price S, et al. Indications and practical approach to non-invasive ventilation in acute heart failure[J]. Eur Heart J, 2018, 39(1):17-25.
[9] Hess D R. Noninvasive ventilation for acute respiratory failure[J]. Respir Care, 2013, 58(6):950-972.
[10] Scott J B. Ventilators for Noninvasive Ventilation in Adult Acute Care[J]. Respir Care, 2019, 64(6):712-722.
[11] Cabrini L, Esquinas A, Pasin L, et al. An international survey on noninvasive ventilation use for acute respiratory failure in general non-monitored wards[J]. Respir Care, 2015, 60(4):586-592.
[12] Crimi C, Noto A, Princi P, et al. A European survey of noninvasive ventilation practices[J]. Eur Respir J, 2010, 36(2):362-369.
[13] Meduri G U. Noninvasive positive-pressure ventilation in patients with acute respiratory failure[J]. Clin Chest Med, 1996, 17(3):513-553.
[14] Al Otair H A, BaHammam A S. Ventilator- and interface-related factors influencing patient-ventilator asynchrony during noninvasive ventilation[J]. Ann Thorac Med, 2020, 15(1):1-8.
[15] Ueno Y, Nakanishi N, Oto J, et al. A bench study of the effects of leak on ventilator performance during noninvasive ventilation[J]. Respir Care, 2011, 56(11):1758-1764.
[16] Luján M, Sogo A, Pomares X, et al. Effect of leak and breathing pattern on the accuracy of tidal volume estimation by commercial home ventilators: a bench study[J]. Respir Care, 2013, 58(5):770-777.
[17] Bello G, De Pascale G, Antonelli M. Noninvasive Ventilation[J]. Clin Chest Med, 2016, 37(4):711-721.
[18] Marchioni A, Castaniere I, Tonelli R, et al. Ultrasound-assessed diaphragmatic impairment is a predictor of outcomes in patients with acute exacerbation of chronic obstructive pulmonary disease undergoing noninvasive ventilation[J]. Crit Care, 2018, 22(1):109.
[19] Duan J, Wang S, Liu P, et al. Early prediction of noninvasive ventilation failure in COPD patients: derivation, internal validation, and external validation of a simple risk score[J]. Ann Intensive Care, 2019, 9(1):108.
[20] Frat J P, Ragot S, Coudroy R, et al. Predictors of Intubation in Patients With Acute Hypoxemic Respiratory Failure Treated With a Noninvasive Oxygenation Strategy[J]. Crit Care Med, 2018, 46(2):208-215.
[21] He H, Sun B, Liang L, et al. A multicenter RCT of noninvasive ventilation in pneumonia-induced early mild acute respiratory distress syndrome[J]. Crit Care, 2019, 23(1):300.
[22] Dangers L, Montlahuc C, Kouatchet A, et al. Dyspnoea in patients receiving noninvasive ventilation for acute respiratory failure: prevalence, risk factors and prognostic impact: A prospective observational study[J]. Eur Respir J, 2018, 52(2):1702637.
[23] Duan J, Han X, Bai L, et al. Assessment of heart rate, acidosis, consciousness, oxygenation, and respiratory rate to predict noninvasive ventilation failure in hypoxemic patients[J]. Intensive Care Med, 2017, 43(2):192-199.
[24] Stefan M S, Priya A, Pekow P S, et al. A scoring system derived from electronic health records to identify patients at high risk for noninvasive ventilation failure[J]. BMC Pulm Med, 2021, 21(1):52.
作者介绍

王蒙
北京大学第三医院呼吸与危重症医学科呼吸治疗师;主要从事呼吸支持、气道管理、血流动力学监测及重症超声等;北京大学重症医学系呼吸治疗学组委员;北京医学会呼吸分会呼吸治疗学组委员;中国康复医学会呼吸康复委员会呼吸治疗学组委员;中国残疾人康复协会肺康复专业委员会ICU肺康复专业学组委员。
本文转载自订阅号「重症肺言」(ID:RCCRC_0067)
原链接戳:无创呼吸机上机流程
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


