近年有关进展性纤维化间质性肺疾病的话题引起了大家的关注,今天将从以下几个方面来和大家进行探讨。
一、间质性肺疾病的概念与分型演变
间质性肺疾病 (ILD)/ 弥漫性实质性肺疾病(DPLD)是指由许多已知或未知原因引起的一组弥漫性肺疾病的总称。它们具有共同的病理特征,如累及部位为肺泡壁和肺泡腔,病变特征主要是「炎症和纤维化」,但是这些病变形式、程度和分布不同(下图),形成不同类型的间质性肺炎和不同的临床表型;共同的临床、病理生理特征是呼吸困难,肺功能呈换气功能障碍和限制通气功能障碍,影像显示为胸部广泛浸润影。
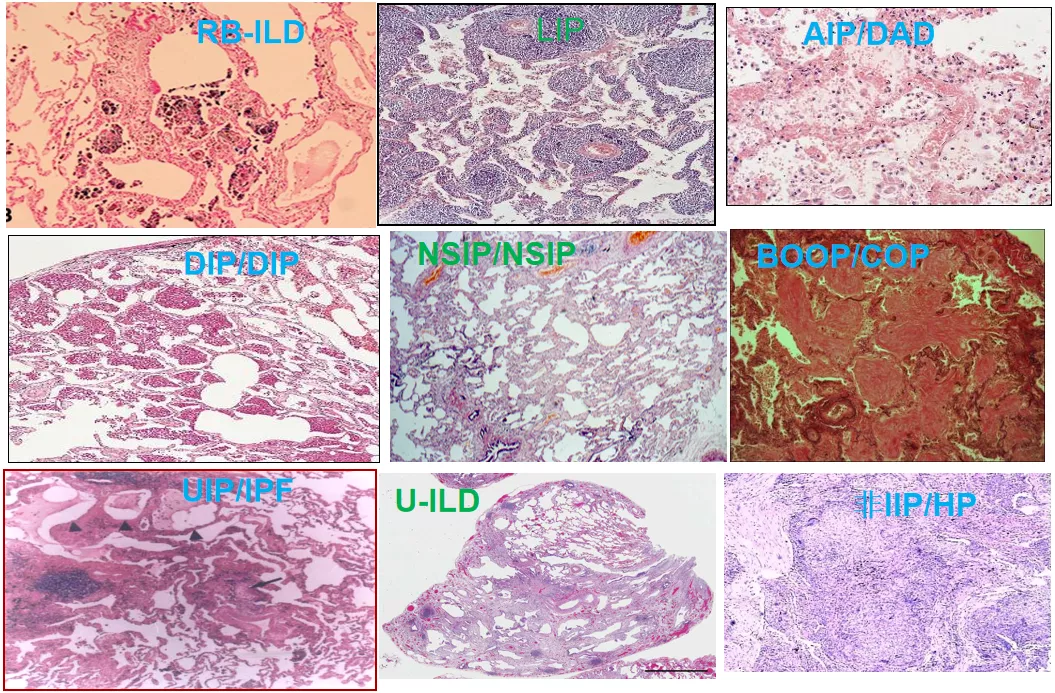
图:不同类型间质性肺炎的病理表现
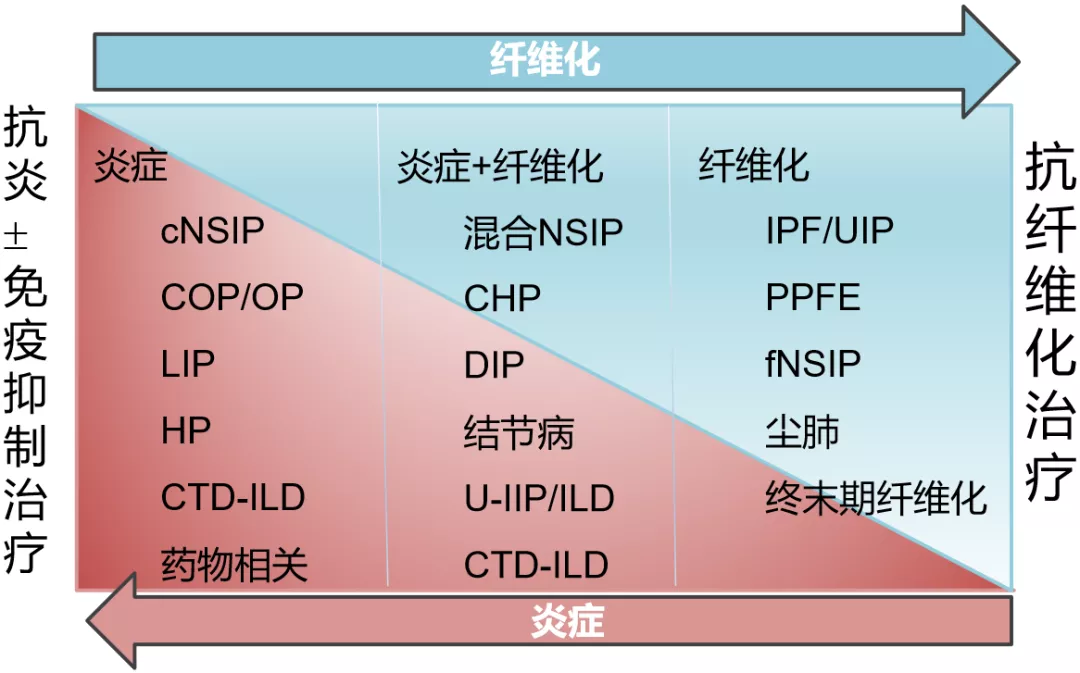
ILDs的特征通常是炎症和纤维化并存 [1-8]
炎症和纤维化在ILDs早期发病时可以共存,但是在疾病发展过程中,炎症和纤维的程度会有些不同,比如,特发性肺纤维化早期时就是纤维化较明显,但过敏性肺炎早期是炎症比较突出(到后期也变成纤维化比较明显),相应的,「纤维化性间质性肺疾病」的治疗也可根据其炎症和纤维化的具体程度进行调整,纤维化是影响疾病治疗反应和预后的重要方面,抗纤维化药物可以延缓疾病进展。

图:纤维化性间质性肺疾病的发生发展与治疗策略
何为「纤维化性间质性肺疾病」?
从病理来看,有肺泡、小叶间隔间隔增厚,还有成纤维细胞增生,胶原沉积,最后导致蜂窝肺,肺结构破坏。
从影像学看,高分辨CT显示有磨玻璃样改变、网格,蜂窝,还有牵拉性的支气管扩张,最后导致肺结构破坏。
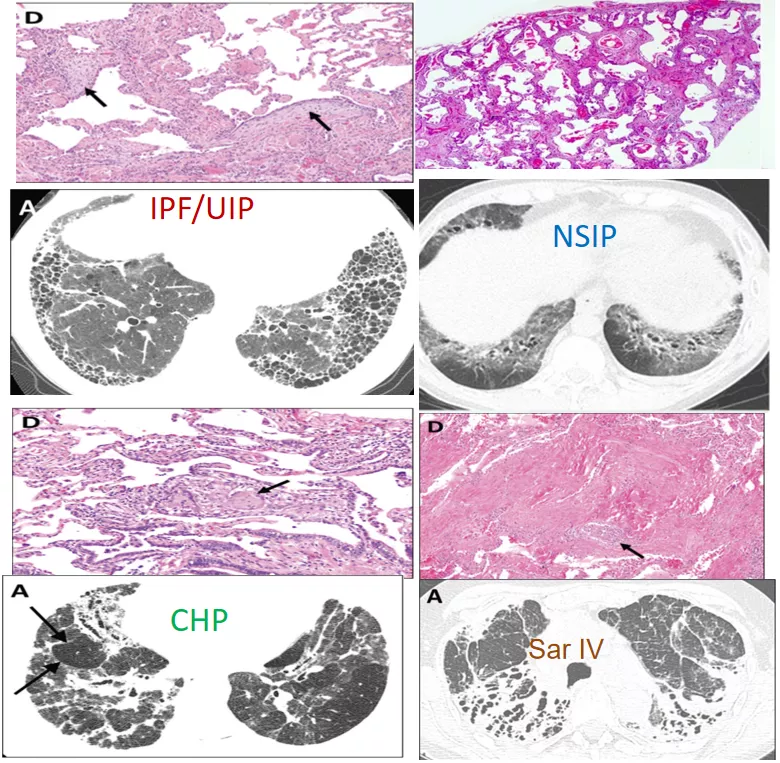
图:纤维化性间质性肺疾病的影像与病理改变 [9-12]
间质性肺炎的预后与临床行为或表型相关 [13,14]
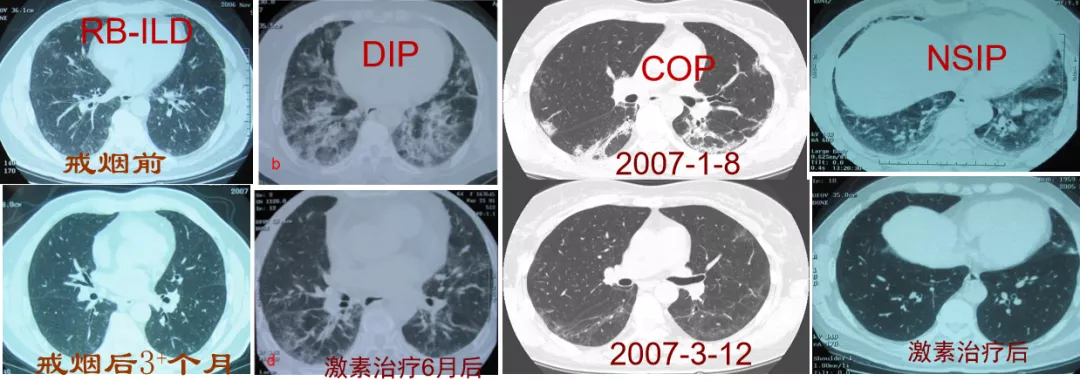
在临床中,我们可以看到,这些不同的高分辨率CT表现所对应的间质性肺炎类型是不一样的, 比如这 些分别是RB-ILD、DIP、COP、NSIP……我们可以发现,患者经过戒烟或激素治疗,大部分能够基本甚至完全吸收。
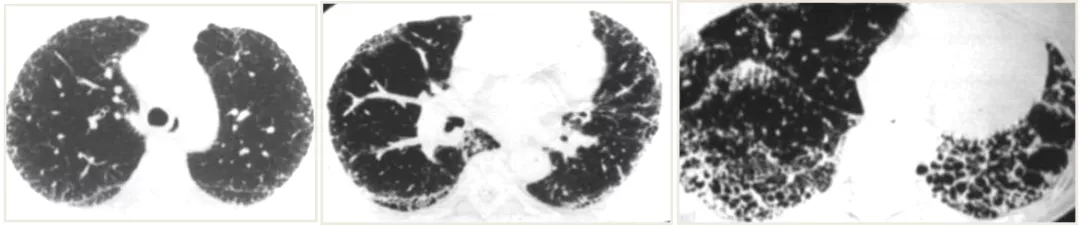
但是,下图是特发性肺纤维化(IPF)早、中、晚期,疾病在不断进展,最后出现弥漫的网格、蜂窝样改变。
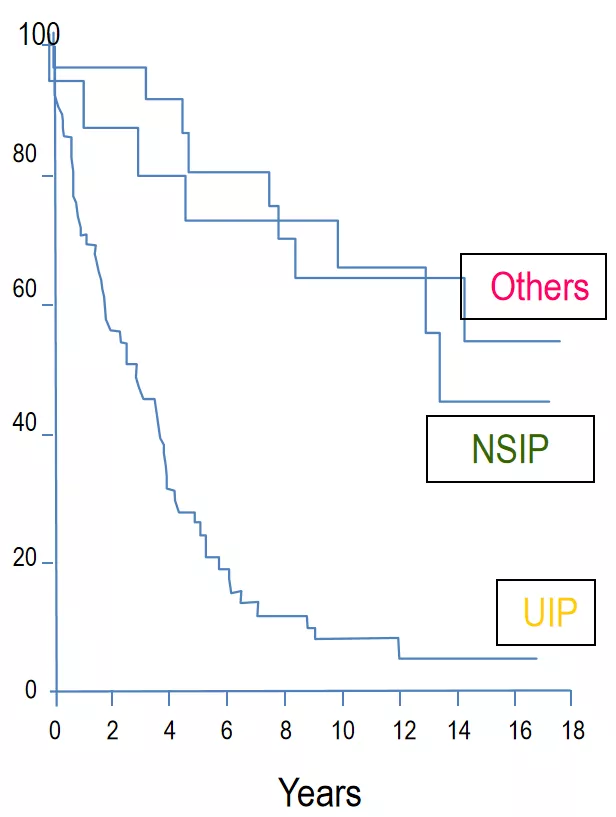
由此可见,患者的预后是和病理类型,或临床表型或者疾病行为是相关的。下图为不同类型IIP存活率,与NSIP等类型相比,IPF/UIP患者生存预后最差。
过敏性肺炎的预后与病理类型或纤维化相关,我们发现,有些过敏性肺炎的预后好,有些不好,这是根据它不同的组织病理类型决定的。[15,16]
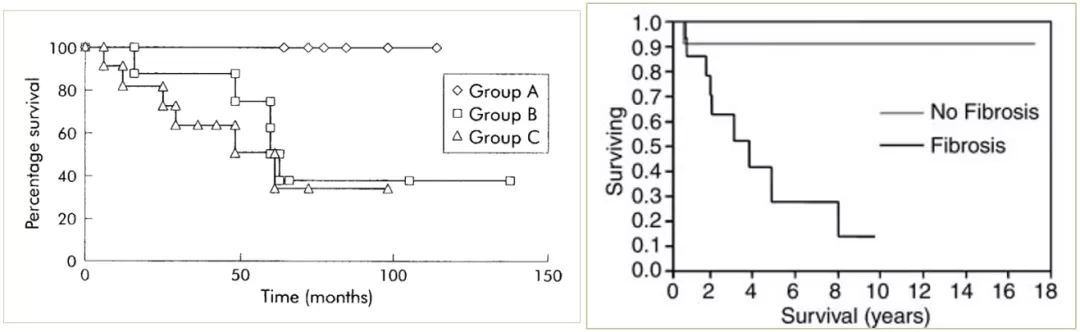
(Group A:BOOP/cNSIP;Group B:fNSIP;Group C:UIP-like)
观察发现BOOP、cNSIP相对来说预后较好,但是fNSIP和UIP-like的预后不好(上图左),再进一步把它们分成「是否有纤维化」,同样也是有纤维化的患者预后不好(上图右),就再次证实患者预后和他的病理类型、是否有纤维化是有关系的。
因此,2020年,ATS发布了一个过敏性肺炎相关的临床指南,指南对HP进行了临床分型。

我们过去知道,过敏性肺炎是分为急性、亚急性和慢性的,因为研究发现患者的预后实际上与是否有纤维化有关,所以这版指南就把患者分为「非纤维化型和纤维化型」。
我结合过去的内容给大家总结一下,「非纤维化型」就是过去所谓的急性和亚急性,在数天、数周发病的,影像学主要表现磨玻璃影、马赛克征,还有小气道病变(小叶中心结节,air-trapping),对应的间质性肺炎的类型就是NSIP、OP、肉芽肿、细支气管炎。
「纤维化型」相对于过去所谓的慢性,所以它要么就是一个隐匿疾病,要么就是数月或者数年才发生的,在影像学上表现为不规则细、粗网格,小叶间隔增厚,蜂窝,牵拉支扩,马赛克;对应的病理类型是fNSIP,可能UIP,UIP,小气道病变。[17]

这是纤维化性间质性肺疾病谱,它是非常庞大的疾病谱。「特发性肺纤维化」是一种表现不断进展的纤维化疾病,所以在间质性肺疾病中是一个恶性的疾病,其他一些非IPF的间质性肺疾病(n-IPF-ILD),如刚才所讲的慢性过敏性肺炎等,无论从疾病行为还是病理生理都与IPF非常相似,都具有纤维化性间质性肺疾病的表现。[18]
ILD的疾病行为进行分类:
ATS/ERS对IIPs的分类为炎症主导、纤维化主导 [19-21]:

1、炎症主导:
这些患者要么通过戒烟、要么通过激素治疗就能够缓解。
1)可逆性和自限性:RB-ILD;
2)可逆性,但可能进展:炎症主导伴纤维化——NSIP、COP、DIP。
2、纤维化主导:
这里又可分为相对稳定的、不断进展的,IIP共识工作组也建议将纤维化ILDs分类:
1)稳定型肺纤维化:NSIP,它不可逆,稳定,是非进行性的;
2)进行性肺纤维化:fNSIP,不可逆、进展,但可能稳定——是进行性的,但至少在短期内,对免疫调节有反应(如果纤维化ILDs在免疫抑制治疗后发生进展,这种疾病行为也可能发展为进展性纤维化表型)
3)恶化加重的进行性肺纤维化:IPF, fNSIP,不可逆,治疗仍进展,无论何种个体化ILDs治疗仍为进行性。
这是近些年的间质性肺疾病分类与概念演变:
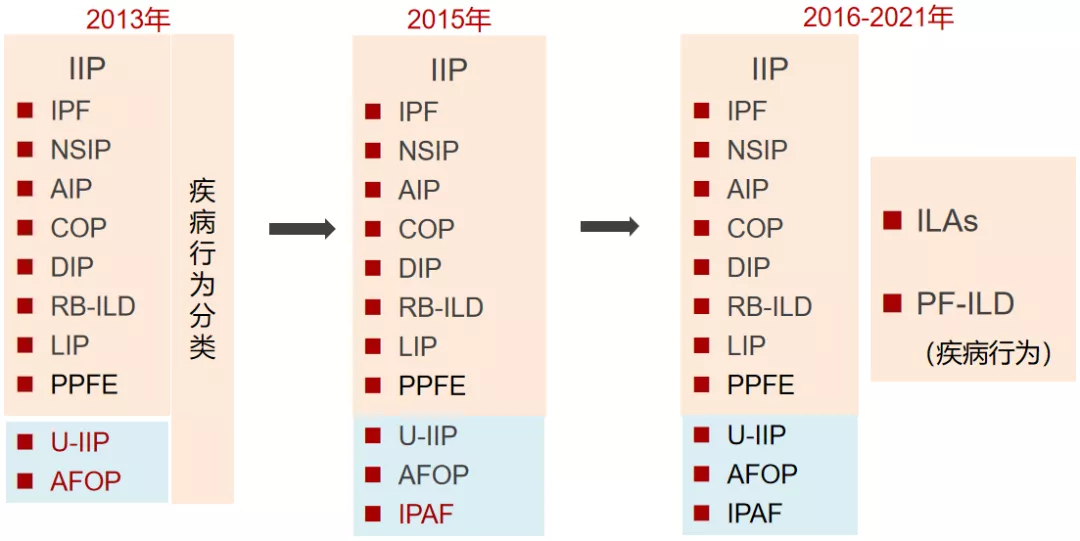
2013年的分类比较完整,但也提出了还有一部分不能进行很好的分类,如不能分类的IIP(U-IIP)、AFOP,实际上这时已经提出了疾病行为分类,就是刚才我所讲的,是炎症主导还是纤维化主导?这两者的预后是不一样的。后来,又有一些新类型,例如IPAF这种具有自身免疫色彩的类型逐渐被认识,但还没有作为「能达到一致意见」的分类。近些年,相继有进展性纤维化间质性肺疾病(PF-ILD)和肺间质异常。在我们对间质性肺疾病的不断认识中(尤其是做肺癌的早期筛查中),更多地注意到有些患者虽然尚无症状,但已经发现一些纤维化的改变,即有肺间质异常,这些就有可能会进展为纤维化间质性肺疾病,所以他们也有预后不好的可能。这些目前还没有达到特别统一的认识,还在不断完善中。
二、进展性纤维化间质性肺疾病的表型
下面重点来说一下,进展性纤维化间质性肺疾病。
病例1 [22]
这可能是大家在临床中经常见到的一些影像学表现,这是一位49岁的男性PF-ILD,影像最初表现为弥漫的细网格磨玻璃样改变伴牵拉支气管扩张(左),三年后,病变不断扩展,牵拉支气管扩张更加的明显(中)。6年后更加的严重了,肯定是进展的表现了(右)。
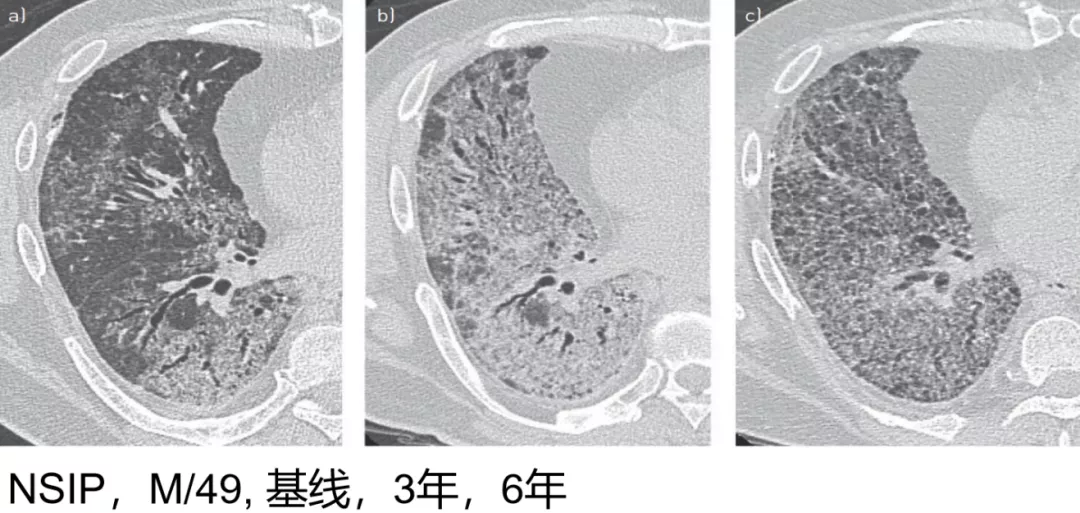
(来源:Eur Respir Rev 2018; 27: 180076 [https://doi.org/10.1183/16000617.0076-2018].)
病例2 [23]
这个病例早期还是一个比较轻的、不能分类的间质性肺疾病。三年后更加严重,已经有蜂窝样改变伴牵拉支气管扩张,随着病程延长更加明显了,这也是一个具有进展表型的纤维化型间质性肺疾病。
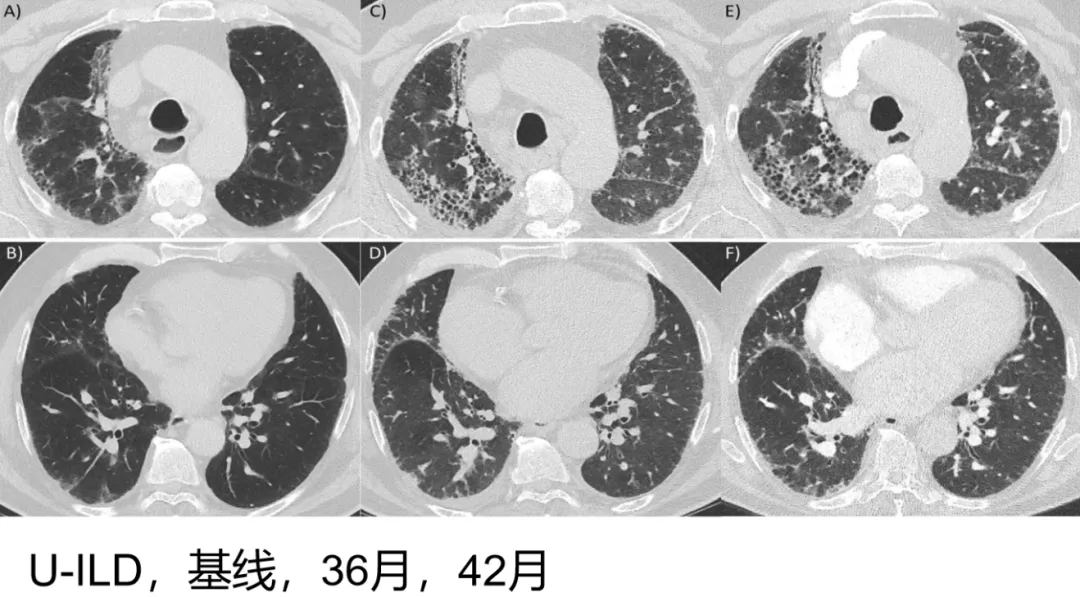
(来源:Wong et al. Respiratory Research (2020) 21:32)
病例3 [24]
过敏性肺炎的预后常常是很好的,但如果持续暴露、不去处理也一样可以进展,例如这位CHP患者的影像学表现相对较轻,逐渐有比较明显的改变。所以非IPF的这些间质性肺疾病,也可能会表现为不断进展的、呈现纤维化的表现。
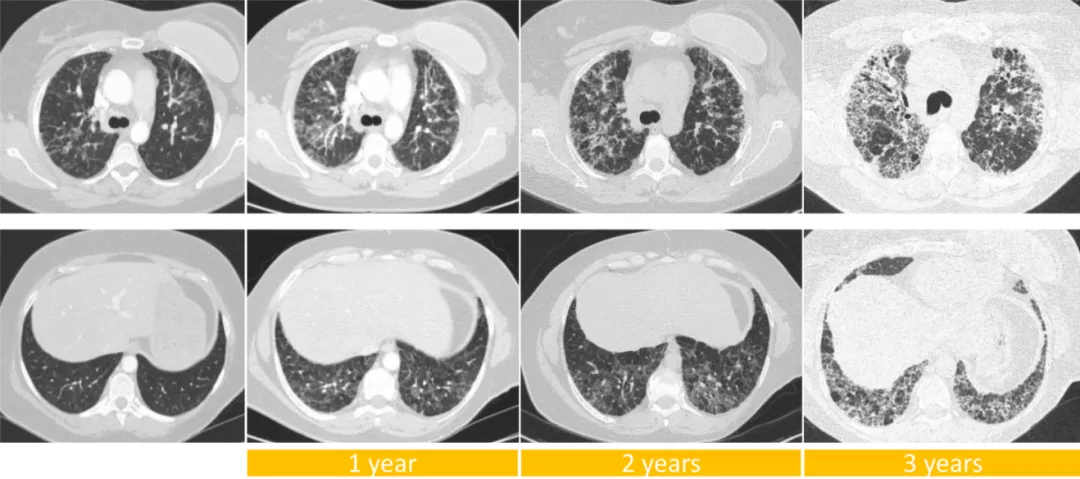
(来源:Wijsenbeek M, Cottin V. Spectrum of fibrotic lung diseases. N Engl J Med 2020;383:958-68.)
进展性纤维化性ILD(PF-ILD)[21,25]:
定义:胸部高分辨率CT(HRCT):纤维化性病变呈弥漫性分布,范围>10%(蜂窝肺、网状影、牵拉性支气管扩张等),在经过积极的药物治疗病情仍持续恶化(症状无改善/加重、肺功能进行性下降、胸部影像学提示病情进展)。
PF-ILD与IPF有许多相似的临床表现: 进行性肺纤维化、呼吸道症状持续恶化、肺功能下降、抵抗经验性的免疫治疗、预后差。
PF-ILD流行病学 [25-29]:
除IPF,多达1/3非IPF-ILD呈进行性纤维化性表型。IPF的患病率为8-60/10万,是常见PF-ILD,(13-40)%的非IPF-ILD也呈PF-ILD表型;在欧洲,ILD患病率为76/10万,PF-ILD患病率为20/10万;在美国,ILD患病率为74.3/10万,PF-ILD患病率为28/10万。
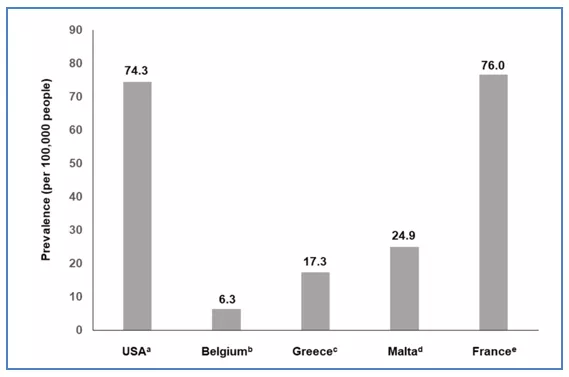
图:ILD在美国和欧洲的患病率
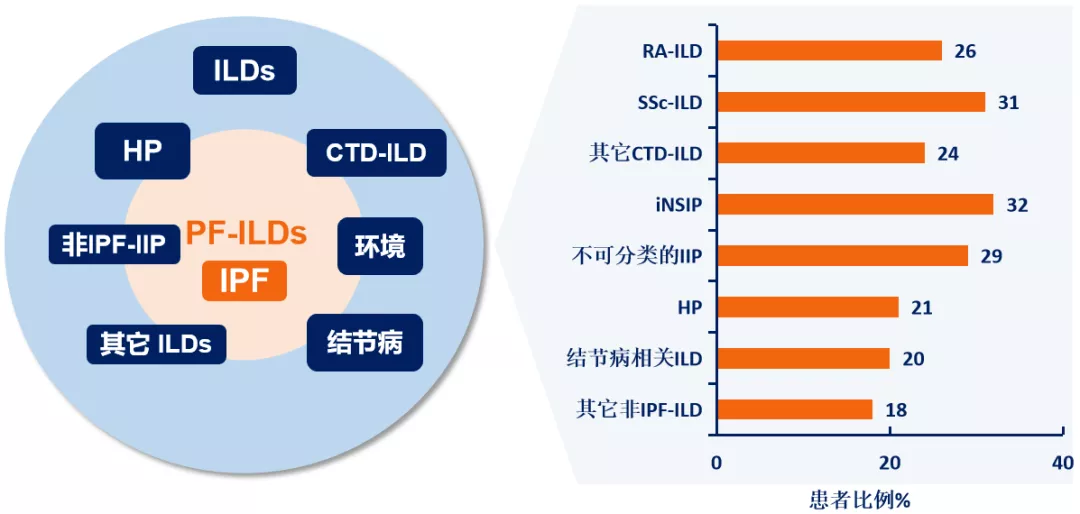
进行性纤维化性ILDs的特征 [30-32]:
非IPF的慢性纤维化性ILDs患者具有发展进行性表型的风险,进行性纤维化性ILDs自然病程特点与IPF相似——从症状来看,呼吸困难不断加重、肺功能不断恶化、纤维化程度增加、最后导致早期死亡。
纤维化性ILD的HRCT表现 [24]:
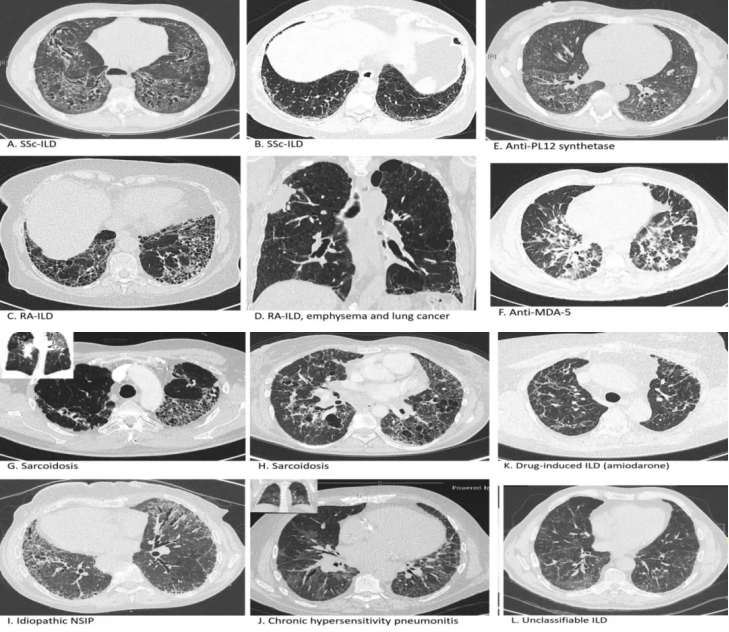
(来源:Wijsenbeek M, Cottin V. Spectrum of fibrotic lung diseases. N Engl J Med 2020;383:958-68.)
这些影像是系统性硬化症、抗合成酶综合征、类风湿关节炎引起等不同类型疾病导致纤维化的HRCT表现。
我们怎么能够判断疾病是不是进展了呢?在HRCT显示有纤维化的基础上,24个月内符合以下任意一项标准即可判断为「进行性(progressive)」。如果没有肺功能,只有症状和HRCT,这也能够判断存在加重、有进展表现。
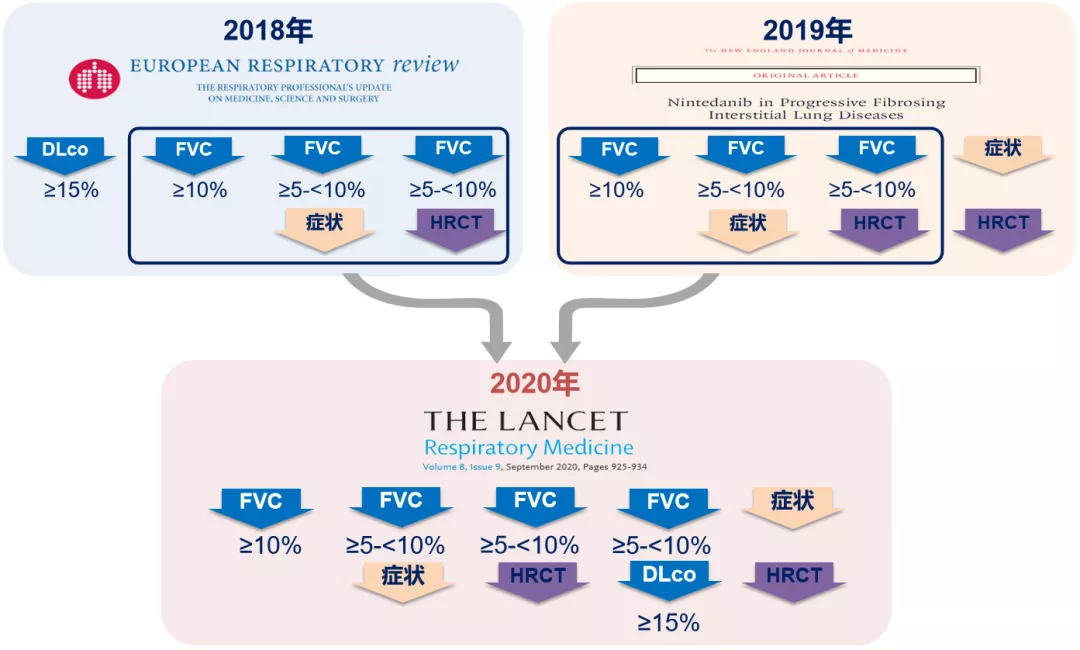
再次强调,胸HRCT中,纤维化性病变(蜂窝肺、网状影、牵拉性支气管扩张等)呈弥漫性分布的范围>10%即为PF-ILD。
三、进展性纤维化间质性肺疾病的综合处理
看看肺纤维化的形成机制,在早期纤维化启动,具有疾病特异性:遗传易感、老化、环境危险因素(trigger)、初始炎症反应等等;在晚期纤维化,呈现纤维化机制共享,profibrotic milieu TGF-β/CTGF/PDGF/WNT,持续纤维化形成 [24]。
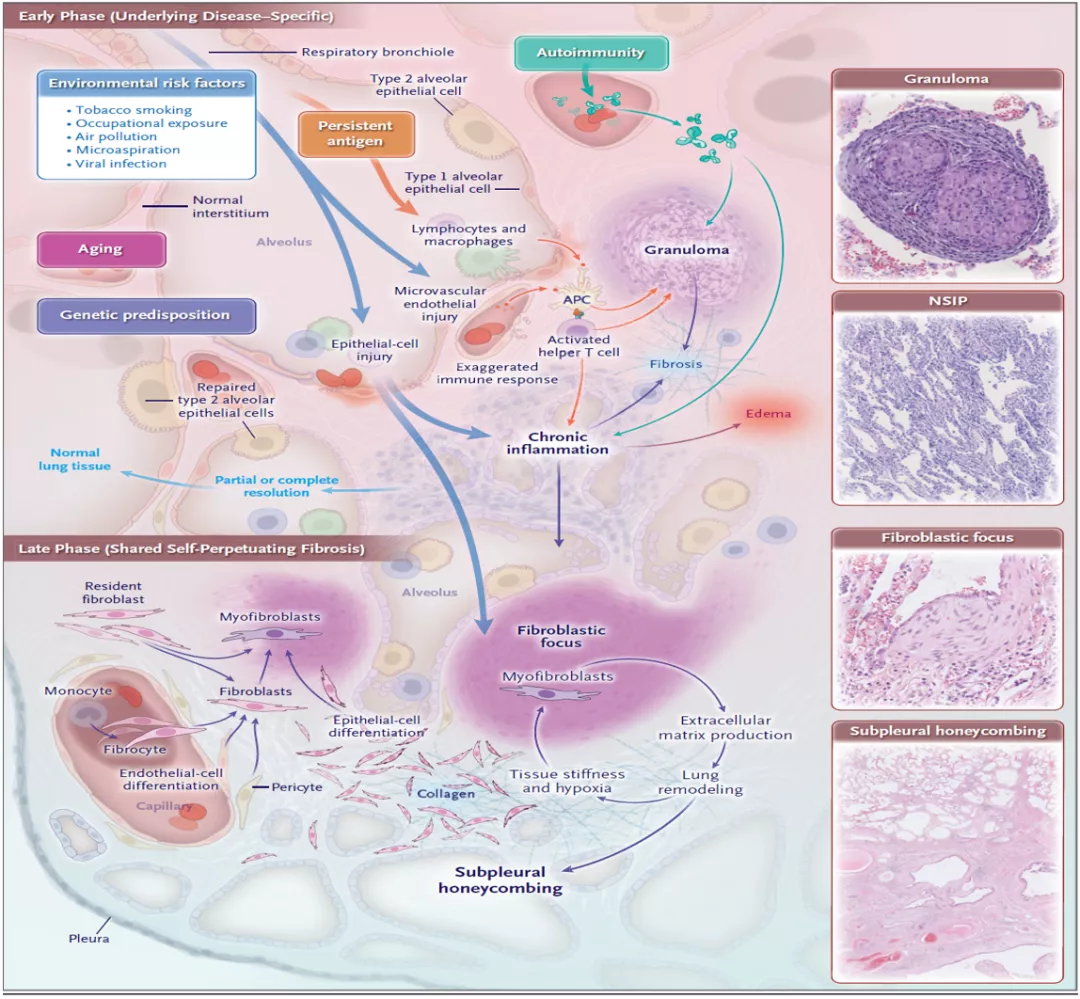
来源:Wijsenbeek and Cottin.N Engl J Med 2020: 383: 956-68
IPF/UIP始于肺泡上皮损伤后异常修复,在这个过程中,炎症可能不那么明显。而过敏性肺炎、结缔组织疾病这些都是和免疫反应相关的,早期炎症反应比较明显。 但无论是何原因所致肺损伤,都可能会涉及到肺泡上皮-成纤维细胞异常通讯,最终都 导致了成纤维细胞不断被激活, 产生纤维化,甚至产生恶性循环导致纤维化不断加重。
在抗纤维药物方面,尼达尼布和吡非尼酮是目前临床可用的。
1、尼达尼布(Nintedanib)
它是血小板衍化生长因子受体(PDGFR)/血管内皮生长因子受体(VEGFR)/成纤维细胞生长因子受体(FGFR),可以用来治疗特发性肺纤维化,既然和其他一些间质性肺疾病的纤维化形成机制是共通的,所以,尼达尼布是否可以运用到其他疾病的治疗中?能否延缓病情进展呢?
这是一项SENSCIS试验,目的在于探究尼达尼布治疗SSc-ILD患者52周的疗效及安全性。研究证实:和安慰剂组相比,尼达尼布显著减缓SSc-ILD患者FVC年下降率,延缓下降44%;两组之间的差值为40.95 mL/年,P=0.0350。[33]

在整体人群第52周FVC自基线处绝对变化均值(mL)来看,第52周的FVC自基线期的绝对改变结果和在52周内FVC的年下降率的减缓保持一致,尼达尼布组第52周的FVC自基线期的绝对改变均值约为安慰剂组的一半,两组间的差值为46.41 mL。
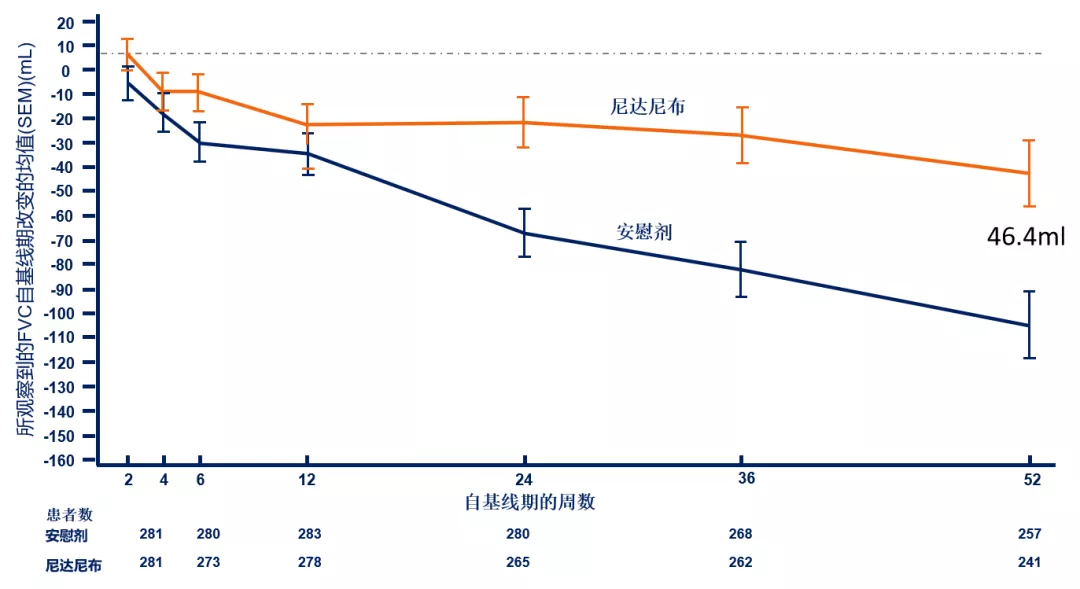
图:在52周内所观察到的FVC自基线期改变均值显示,两条曲线从一开始即缓慢分离,第12周以后分离更加清晰,而此趋势一直保持到第52周。
这项研究中整体人群的ILD分类如下 [35]:
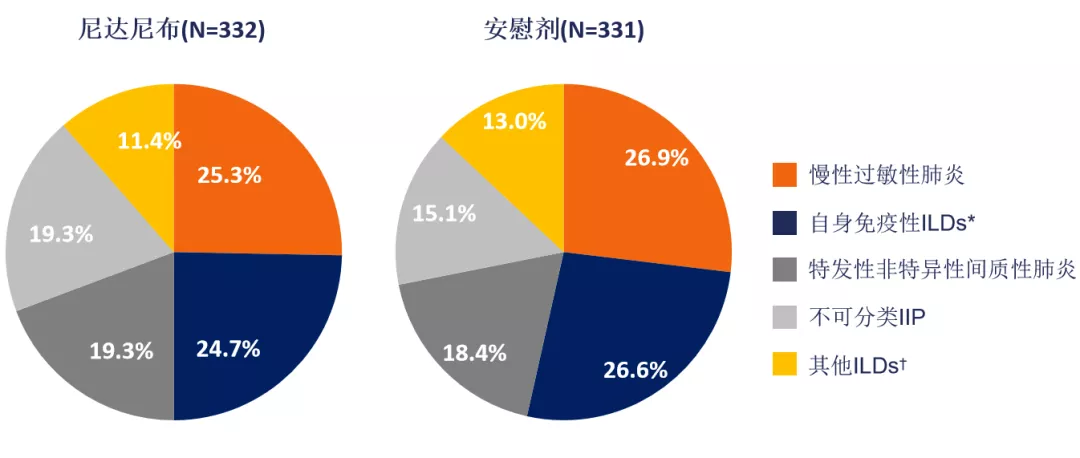
注:自身免疫性ILDs包括类风湿关节炎相关ILD(尼达尼布12.7%;安慰剂14.2%),SSc-ILD(尼达尼布6.9%;安慰剂4.8%),混合性结缔组织病-ILD(尼达尼布2.1%;安慰剂3.6%)以及「其他纤维化ILD」中选择的其他术语;其他ILDs包括结节病、暴露相关ILD和「其他纤维化ILD」中选择的其他术语。
无论ILD诊断如何,尼达尼布均能有效减缓CTD-ILD患者的FVC下降率。[36]
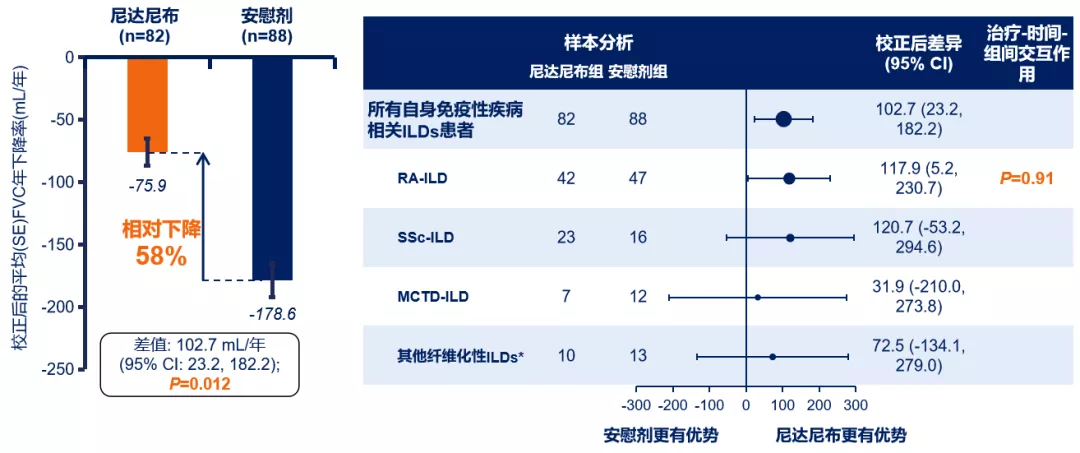
图:(左)自身免疫性疾病相关ILD患者在52周内的FVC下降率;(右)根据ILD诊断结果分组,各亚组患者52周内的FVC下降率。
2、吡非尼酮
它是一个多靶向的抗纤维化药物——拮抗炎症因子、拮抗氧化应激、拮抗纤维化因子、促进抗纤维化因子,进而产生抗纤维化作用……那么,它可不可以用来治疗除特发性肺纤维化以外的进行性纤维化间质性肺疾病患者?[34]
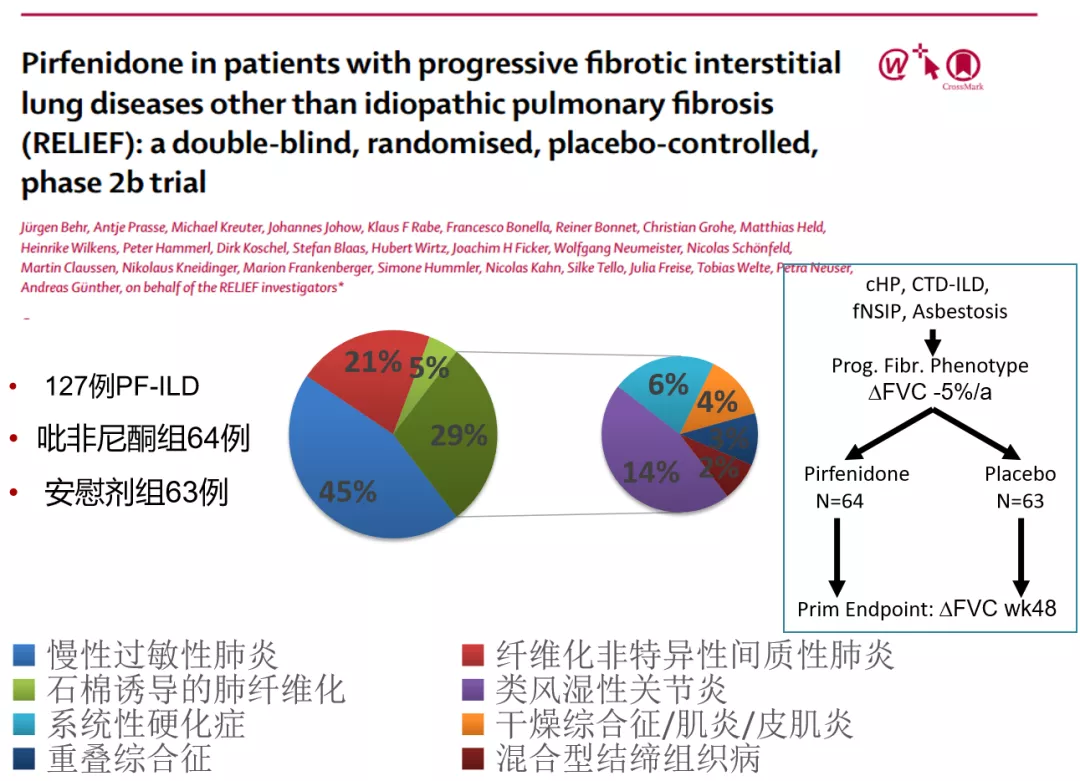
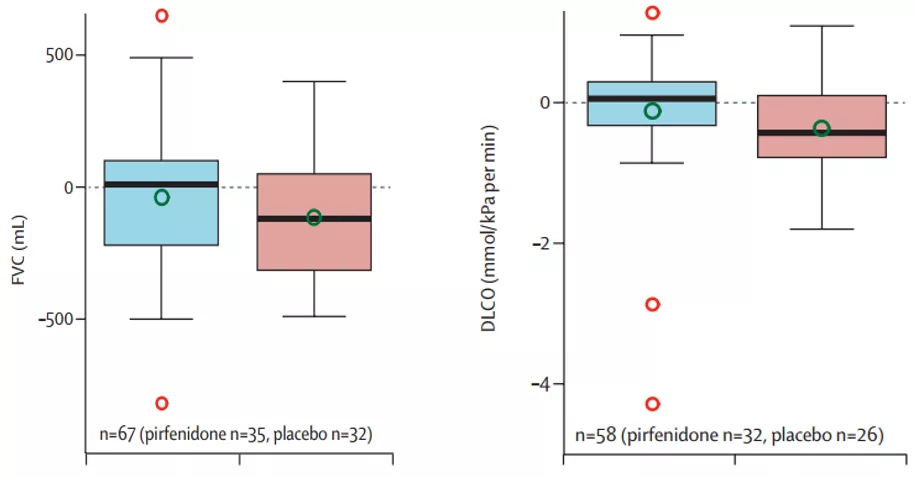
图:(左)吡非尼酮治疗组FVC%预测值从基线至第48周的下降显著低于安慰剂组(p = 0.043),(右)吡非尼酮治疗组DLco预测值从基线至第48周的下降显著低于安慰剂组(-0.1 vs -0.4mmol/kPa/min,p = 0.023)。
RELIEF试验表明,吡非尼酮治疗除IPF以外的PF-ILD,可减缓患者FVC下降趋势,副作用特征与IPF试验中报告的相似,可能是PF-ILD患者的合理选择。
同时,研究也显示,吡非尼酮较安慰剂,显著改善不可分类的进行性纤维化ILD患者的肺功能。[37,38]
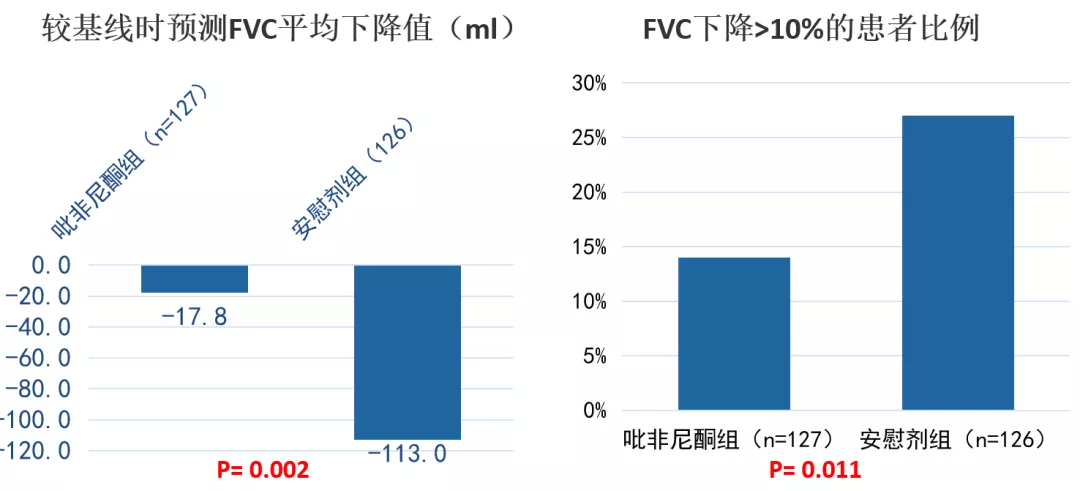
图:(左)较基线时预测FVC平均下降值(ml);(右)FVC下降>10%的患者比例
进展性纤维化间质性肺疾病实际包括很多类型,需要分类处理 [24]:
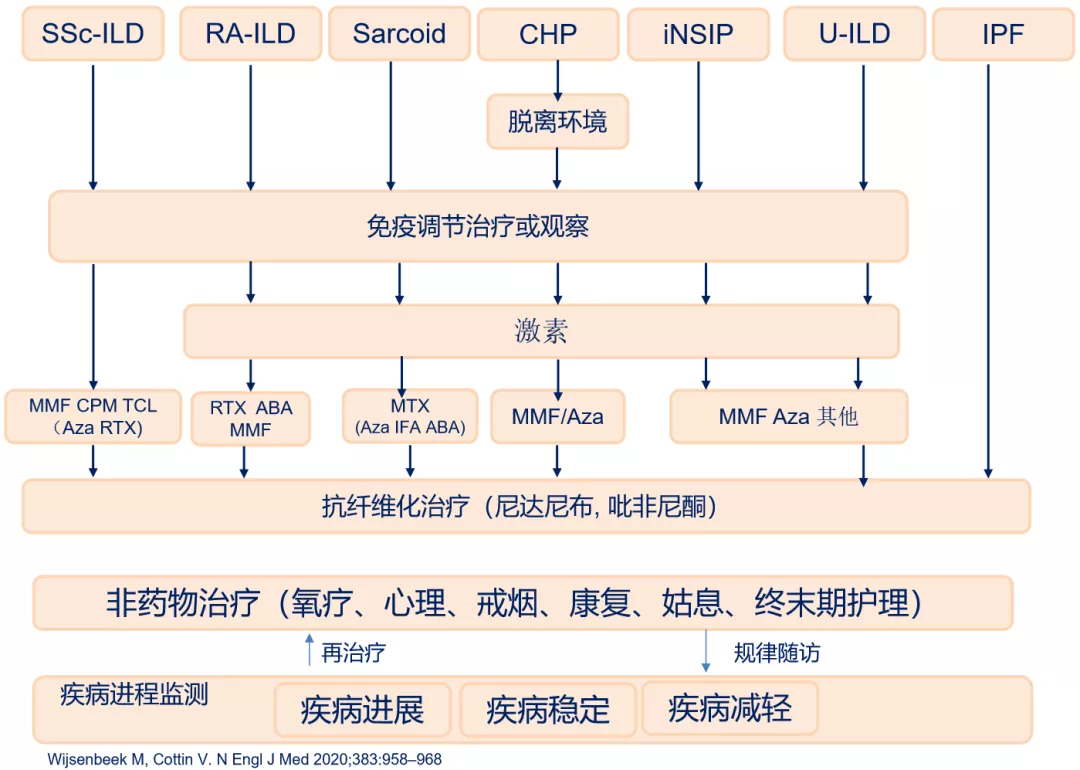
间质性肺炎表型及处理:
纤维化ILD的综合管理 [41]:
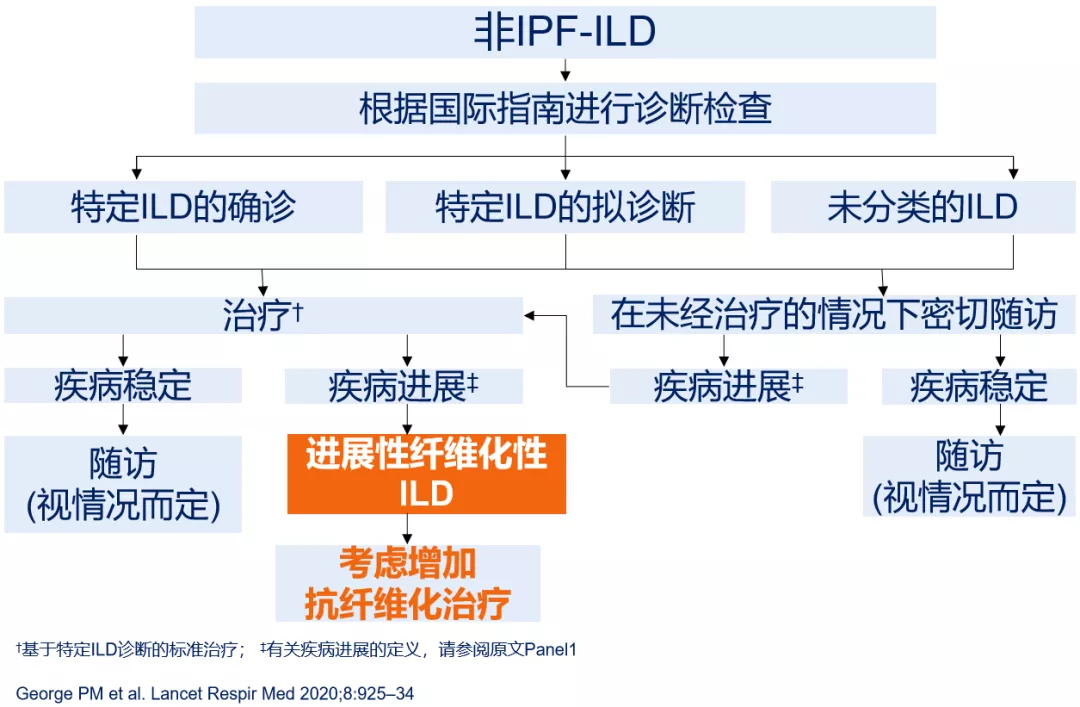
注:†基于特定ILD诊断的标准治疗;‡有关疾病进展的定义,请参阅George PM et al. Lancet Respir Med 2020;8:925–34原文Panel1
总结一下:间质性肺疾病或者纤维化性间质性肺疾病的诊断是一个动态的过程,治疗也应该是动态的过程。
参考文献
[1] Cottin V et al. Eur Respir Rev 2018;27:180076
[2] Wells AU et al. Nat Rev Rheumatol 2014;10:728–39
[3] Spagnolo P et al. Ann Rheum Dis . 2021 Feb;80(2):143-150
[4] Wongkarnjana A et al. Curr Opin Pulm Med 2020;26:436–42
[5] Wollin L et al. Eur Respir J 2019;54:1900161
[6] Duarte AC et al. Acta Reumatol Port 2019;44:161–2
[7] Cottin V et al. Eur Respir Rev 2019;28:190109
[8] Kolb M, Vašáková M. Respir Res 2019;20:57
[9] Lancet Respir Med 2020; 8: 726–37
[10] CHEST 2020; 157:612-635
[11] Arch Pathol Lab Med. 2017;141:901–915
[12] AJ RCCM 2008;177:1338–47
[13] Bjoraker JA et al. Am J Respir Crit Care Med. 1998;157:199
[14] Daniil ZD et al. Am J Respir Crit Care Med. 1999;160:899.
[15] Ohtani Y, et al. Thorax 2005; 60: 665-71
[16] Sahin H, et al. Radiology 2007; 244: 591-598
[17] Am J Respir Crit Care Med 2020;202(3) :e36–e69
[18] Wells AU, et al. Eur Respir J. 2018 May 17;51(5). pii: 1800692.
[19] Travis WD et al. Am J Respir Crit Care Med 2013;188:733–48;
[20] Wells AU et al. Eur Respir J 2018;51.pii: 1800692;
[21] Flaherty KR et al. BMJ Open Respir Res 2017;4:e000212
[22] Eur Respir Rev 2018; 27: 180076 [https://doi.org/10.1183/16000617.0076-2018].
[23] Wong et al. Respiratory Research (2020) 21:32
[24] Wijsenbeek M, Cottin V. Spectrum of fibrotic lung diseases. N Engl J Med 2020;383:958-68.
[25] Kolb M, et al. Respir Res 2019;20:57
[26] Wijsenbeek M, et al. Curr Med Res Opin. 2019 Jul 22:1
[27] Adv Ther 2021;38:854–867
[28] Raghu G et al . Eur Respir J 2016; 48:179-86;
[29] Duchemann B, et al. Eur Respir J 2017;50:1602419.
[30] Brown KK et al. Eur Respir J 2020;55:2000085
[31] Wells AU et al. Lancet Respir Med 2020;8:453–60
[32] Wijsenbeek M. Lancet Respir Med 2020;8:424–5
[33] Oliver Distler, et al. N Engl J Med. published on May 20, 2019,at NEJM.org.
[34] Behr J. et,al. Lancet Respir Med. 2021 Mar 30:S2213-2600(20)30554-3.
[35] Flaherty KR, et al. N Engl J Med 2019.
[36]Matteson EL et al. Oral presentation at EULAR European Congress of Rheumatology 2020. E-congress, June 3–6, 2020; abstract OP0115
[37] Lancet Respir Med 2019. Published Online, September 29, 2019.
[38] https://doi.org/10.1016/S2213-2600(19)30341-8
[39] Patel AS, et al. Thorax 2012;67:804–10.
[40] Flaherty KR et al. BMJ Open Respir Res 2017;4:e000212;https://clinicaltrials
[41] George PM et al. Lancet Respir Med 2020;8:925–34
专家介绍

代华平
主任医师,教授,博士生导师;中日医院呼吸与危重症医学科三部主任;中华医学会呼吸病学分会间质性肺疾病学组组长,中国医师协会呼吸医师分会秘书长。
本文由《呼吸界》编辑 Jerry 整理、排版,感谢代华平教授的审阅修改!
本文完
未经许可,请勿转载


