
肺癌的死亡原因很多,比如我们有时候看到肺癌患者化疗后肿瘤在明显缩小,认为效果不错,但病人预后很差、OS短,其中一个特别重要的原因与肿瘤相关静脉血栓栓塞症有关。近几年,新冠病毒导致的肺炎合并血栓问题备受关注,许多重症新冠患者死于血栓,因此,今天与大家分享的内容先从回顾肿瘤相关静脉血栓栓塞症开始,再讲讲肿瘤相关静脉血栓栓塞症的预防和治疗。
肿瘤患者在确诊时VTE风险约是正常人群的5倍,直至姑息性治疗,VTE风险持续处于极高水平……VTE高风险贯穿整个肿瘤病程
为什么肿瘤会与血栓有关?常见的静脉血栓大家比较熟悉,它一方面是下肢深静脉血栓的形成,另一方面是尤其危险的肺栓塞。
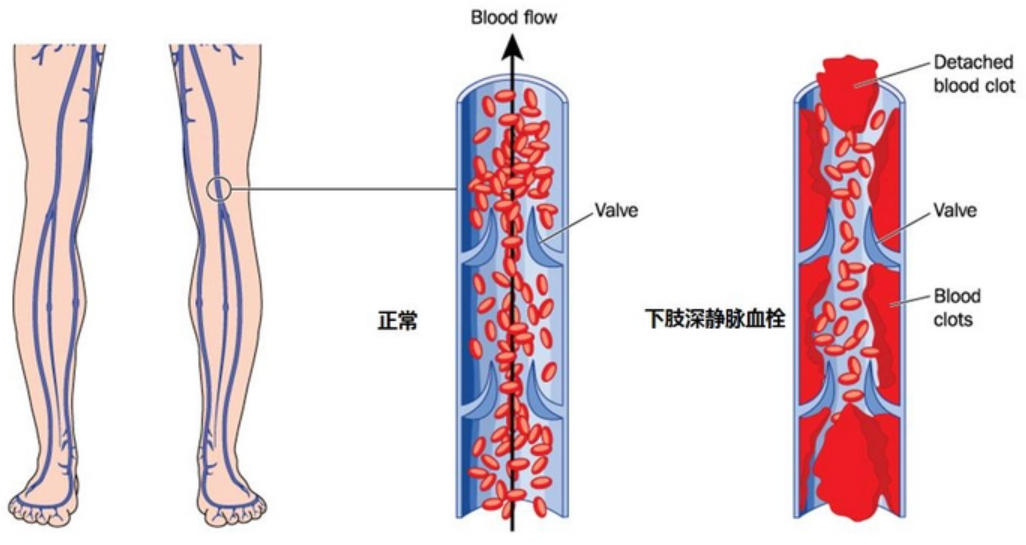
DVT,我们叫深静脉血栓,是指血液非正常地在深静脉内凝结,导致静脉回流障碍,血栓脱落进入肺动脉形成肺动脉栓塞。血栓形成大都发生于制动状态(尤其是骨科大手术)。
血栓形成后,除少数能自行消融或局限于发生部位外,大部分会扩散至整个肢体的深静脉主干,若不能及时诊断和处理,多数会演变为血栓形成后遗症,长时间影响患者的生活质量;还有一些病人可能并发肺栓塞,造成极为严重的后果。比如说有的骨科病人手术做得很成功,但是术后几天一下床就突然死亡,一查原因就是患者在骨科术后发生了深静脉血栓,因血栓脱落导致肺栓塞,一旦发生,严重者会危机患者生命。
PE,我们叫肺栓塞症,肺栓塞在欧美西方国家病死率很高,病因常见的原因正是深静脉血栓,尤以下肢深静脉血栓最多。患者的股静脉中可形成较大的血凝块,并直接通向肺部,危险性最大,其次为生殖腺静脉、子宫静脉、盆腔静脉内的血栓,再次就是右心房或右心室附壁血栓或心内膜炎、下肢静脉炎等感染病灶,也可引起肺栓塞,为肺血栓栓塞(即PTE)。
因PE中最为常见者为PTE,所以一般PE也指PTE。恶性肿瘤的瘤栓、动脉粥样硬化的粥样斑块、羊水、脂肪、赘生物等均可成为堵塞血管的栓子,而近年来放置静脉内的导管或起搏器等装置也成为引起血栓性栓子的因素。
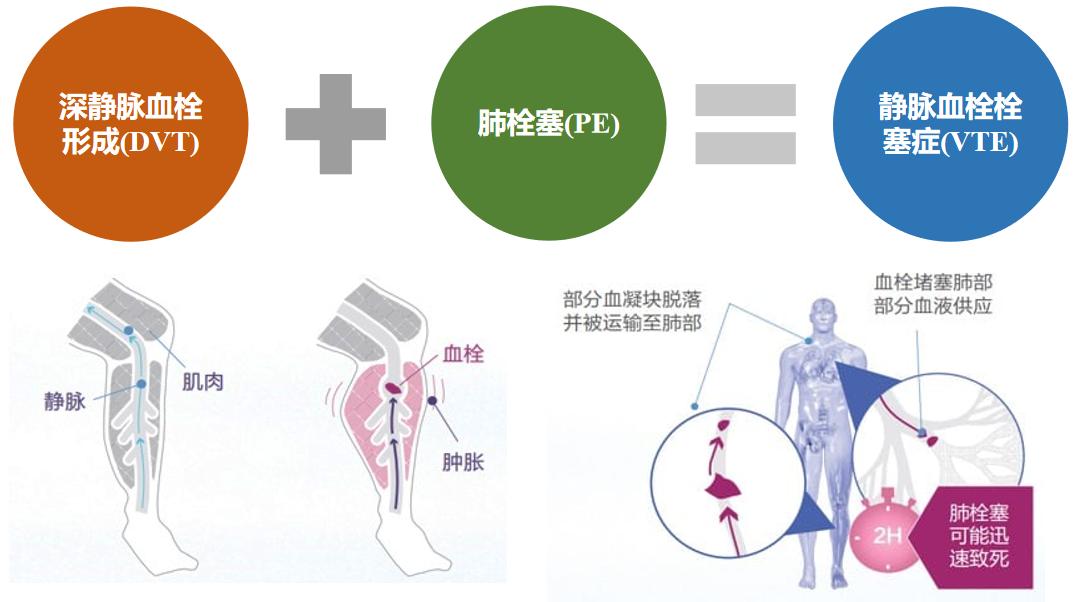
什么是静脉血栓血栓症(VTE)?VTE包括DVT和PE。
DVT和PE是VTE在不同部位和不同阶段的两种临床表现形式,90% PE栓子来源于DVT[1]。VTE是继缺血性心脏病和卒中之后,第3常见的心血管疾病[2]。
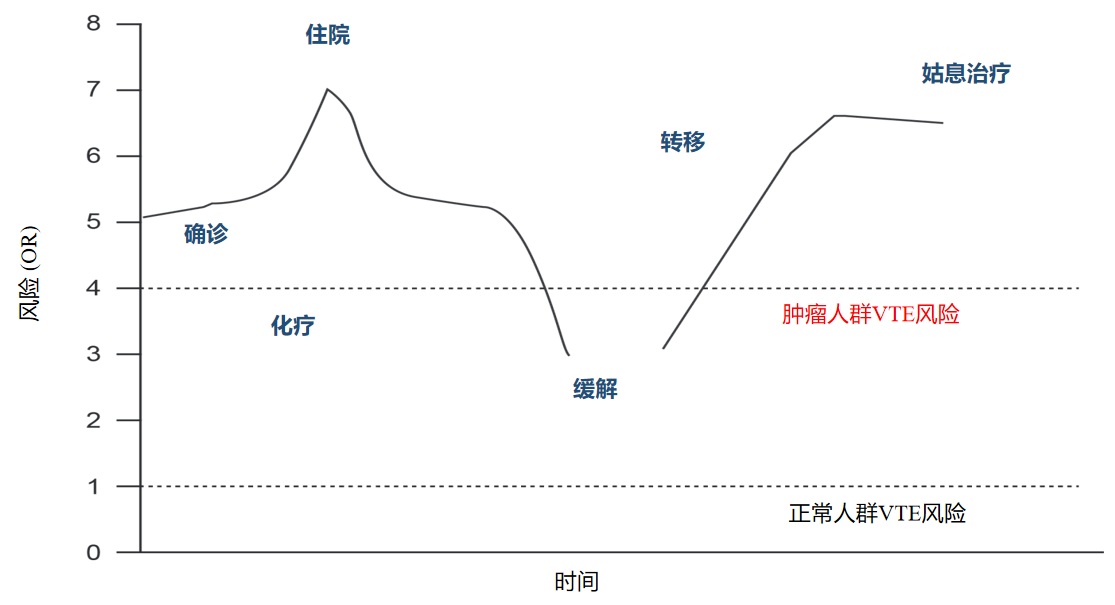
VTE高风险贯穿整个肿瘤病程。从风险(OR)表分析,肿瘤患者在疾病的不同时期,始终伴有较高的VTE风险:肿瘤患者在刚确诊时,VTE风险约是正常人群的5倍;患者在住院期间,VTE风险最高时约为正常人群的7倍;即便肿瘤缓解后,VTE风险随之下降,但仍比正常人群高;而当肿瘤出现转移后,VTE风险又会快速增加;直至姑息性治疗,VTE风险持续都处于极高水平。
肿瘤相关VTE的流行病学显示:VTE是肿瘤患者最常见的并发症之一;首次发生VTE的病例中20%-30%与肿瘤相关,其中接受化疗的患者约占13%;肿瘤相关VTE发病率为4%-20%,高发肿瘤为胰腺癌、肺癌、胃肠道肿瘤、卵巢癌。
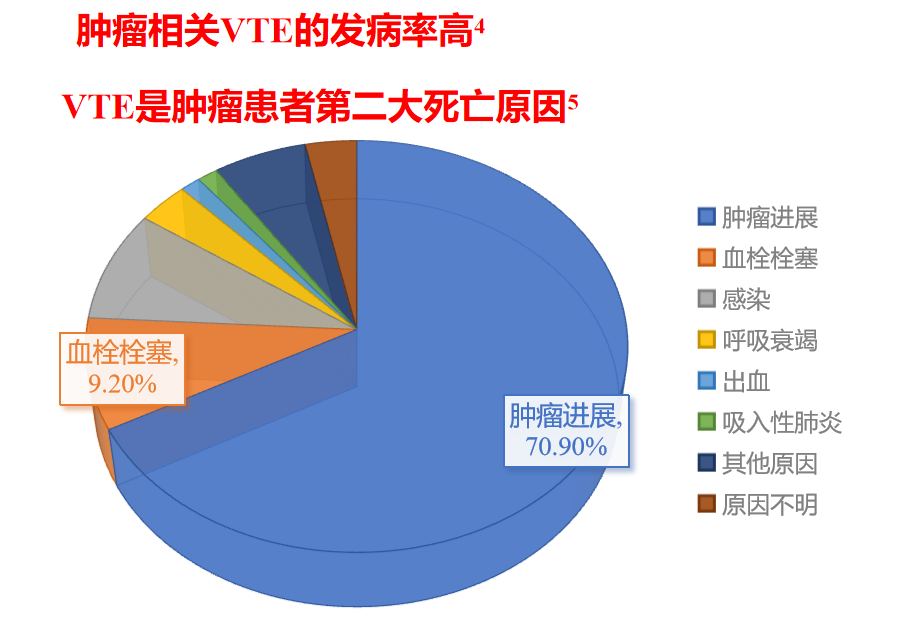
肿瘤患者的死亡原因中,肿瘤进展占比为70.9%,血栓栓塞为9.2%,VTE成为肿瘤患者的第二大死亡原因。其余分别是感染、呼吸衰竭、出血、吸入性肺炎,以及其他原因(包括原因不明)。
很多肿瘤患者即便外科手术做得好,同样会有血栓形成的风险。比如我们曾经有一例罹患早期原位癌的患者,手术非常成功,大家都以为手术以后就相当于彻底治愈,但就在这位患者出院的时候突然发生晕厥,查其原因正是因为深静脉血栓引发的肺栓塞所致。这样的例子还有很多,每一个都是深刻的教训。
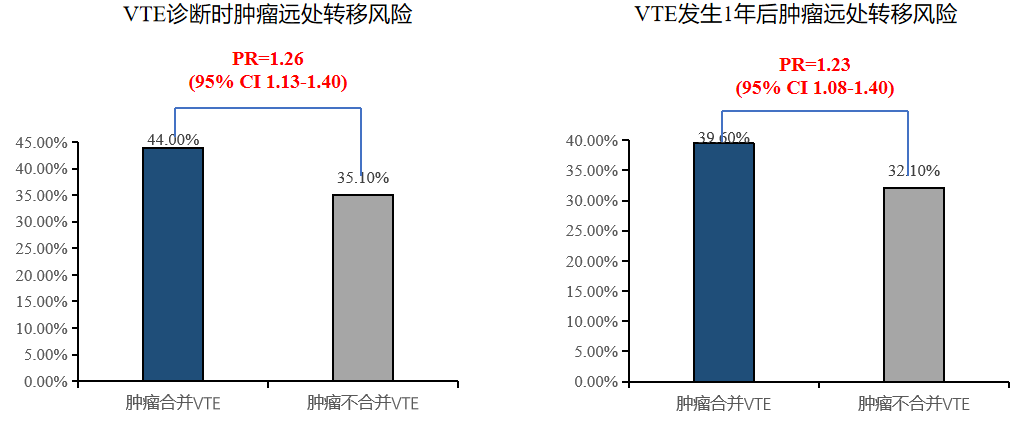
VTE显著增加肿瘤远处转移的风险。即便现在肿瘤的治疗手段很多,效果也很好,假如一旦形成血栓,它转移的风险也会明显增加。从柱状图中也可以清晰地看到VTE诊断时肿瘤远处转移风险比例,以及VTE发生1年后肿瘤远处转移风险比例。这是一份来自丹麦病例的对照研究,该研究纳入了1977-1992年间丹麦国家病人注册目录中登记的至少一次住院期间发生原发性VTE的患者共27321例,以非VTE的肿瘤患者作为对照组,通过肿瘤类型、性别、肿瘤诊断时的年龄以及肿瘤诊断年份进行匹配,了解VTE时或发生后肿瘤的预后。
了解这些对我们今后的探索或许有所帮助,至少我们清楚了肿瘤转移后除了治疗效果差,还有一个重要机制就是形成了血栓。
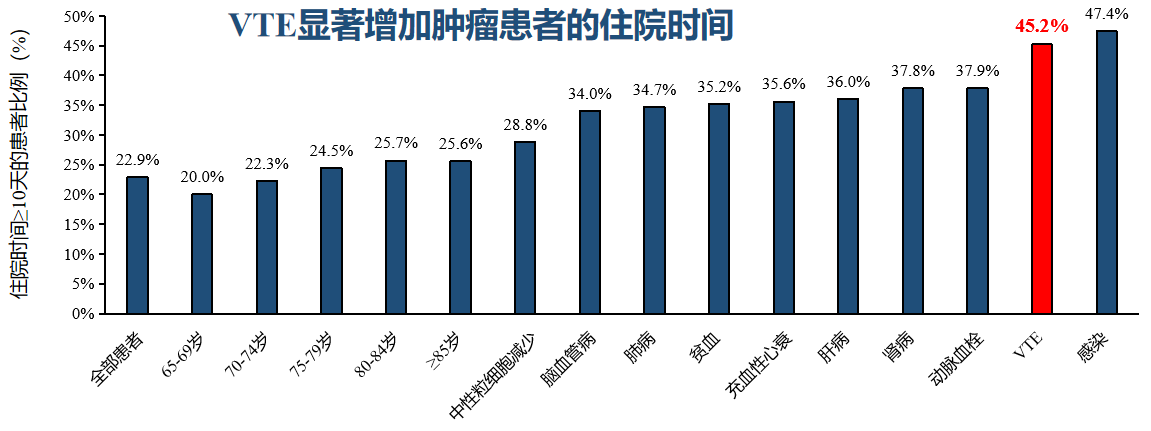
VTE高风险贯穿整个肿瘤病程还体现在它明显延长了患者的住院时间。这项回顾性队列研究,纳入了共386377例年龄≥65岁的实体肿瘤患者,旨在评估与老年肿瘤患者住院死亡率和住院时间延长相关的风险因素。住院时间延长的危险因素包括胃癌、感染、VTE和红细胞输注。多因素分析显示,VTE与患者住院时间延长显著相关:OR=2.25(95%CI 2.17-2.33,P<0.001)。
同时,从这张柱状图中我们可以非常直观地看到肿瘤患者为什么会住院。是不得已的情况下住院,因为肿瘤患者如果是单纯化疗,并不需要住院,口服靶向药也可以在家服用,也不需要住院。哪些情况会导致住院呢?高龄是原因之一,感染是占比最大的原因,但其中非常重要的一个原因就是发生了静脉血栓,占比达45.2%。
与无VTE的患者相比,合并VTE的肿瘤患者死亡率成倍增加……肿瘤相关VTE常见的危险因素有哪些?肿瘤患者易患VTE的机制?
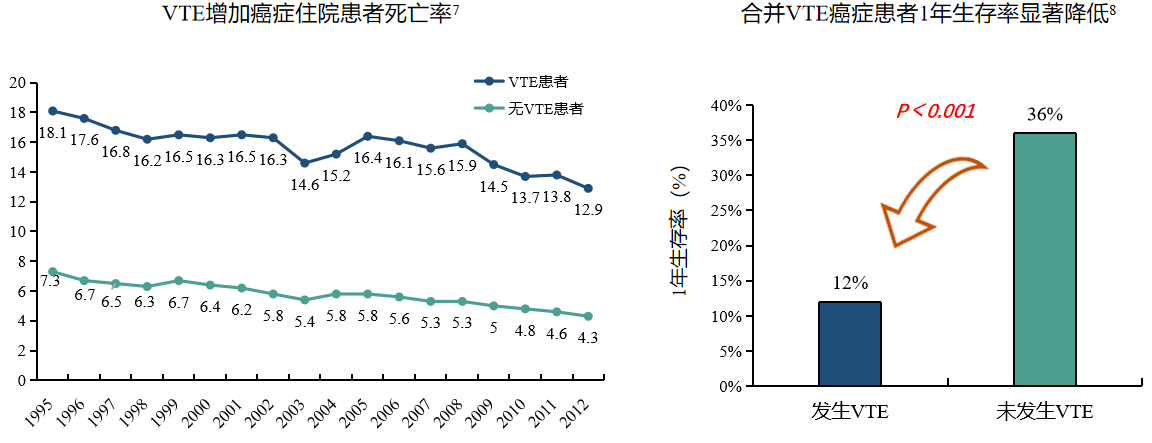
因此,VTE显著增加肿瘤患者的死亡风险是毋庸置疑的,肿瘤患者只要新增加疾病,死亡风险就一定会增加。左边的曲线图是美国1995-2012年肿瘤住院患者的数据显示,我们可以看到,与无VTE的患者相比,合并VTE的肿瘤患者死亡率成倍增加。右边的柱状图来自一篇纳入了多项肿瘤和VTE相关研究的综述,发现合并VTE的肿瘤患者生存率更低。
既然流行病学已证实VTE显著增加肿瘤患者的死亡风险,我们要分析为什么,肿瘤相关VTE常见的危险因素有哪些?主要分为以下四个方面:
一、一般性危险因素:
① 活动性癌症;
② 晚期癌症;
③ 风险更高的肿瘤类型:脑瘤、胰腺癌、胃癌、肺癌、转移性肿瘤等;
④ 局部大淋巴结病变伴外部血管压迫;
⑤ 家族性和/或获得性高凝状态(包括妊娠);
⑥ 内科合并症:感染、肾病、肺病、充血性心力衰竭、动脉血栓栓塞症;
⑦ 体力状态差;
⑧ 高龄。
二、治疗相关危险因素:
① 大型手术;
② 中心静脉插管/外周静脉插管;
③ 化疗:例如沙利度胺/来那度胺/泊马度胺加高剂量地塞米松;
④ 外源性激素治疗:例如激素替代治疗(HRT);避孕药;他莫昔芬/雷洛昔芬;己烯雌酚。
三、门诊化疗高风险患者包含因素:
① 活动性癌症:胃癌、胰腺癌、肺癌、淋巴瘤、妇科癌症、膀胱癌和睾丸癌;
② 化疗前血小板计数>350x10^9/L;
③ 化疗前白细胞计数>11x10^9/L;
④ 血红蛋白<100g/L;
⑤ 使用促红细胞生成素;
⑥ 体重指数≥35kg/㎡;
⑦ 既往VTE。
四、可干预危险因素:
① 吸烟;
② 肥胖;
③ 活动水平/运动量。
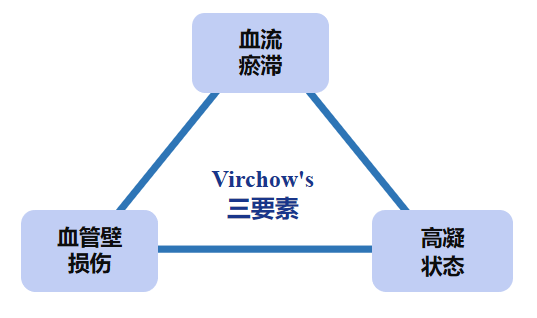
究其根本,肿瘤患者为什么易患VTE?我们从机制、从本源上解释,血栓形成的三要素我们称之为「Virchow's三要素」,即血流瘀滞、血管壁损伤和高凝状态。
肿瘤患者会不会导致血流瘀滞呢?比如进行化疗时,包括「打囊泡」(这是一项基于细胞外囊泡来源的、具有天然特性的肿瘤治疗技术,将来源于肿瘤细胞的囊泡,与微量的化疗药物结合后,将化疗药物富集于囊泡内,并激活免疫反应,用于恶性肿瘤的治疗)治疗的时候,患者都必须卧位,躺着不动,因此这是一个卧床与制动的过程。从制动过程来看,就可能导致血流瘀滞;又比如肿瘤压迫淋巴血管,也会导致血流瘀滞。
可导致肿瘤患者血管壁损伤的行为有哪些呢?比如手术,比如中心静脉置管、肿瘤放疗化疗损伤内皮、肿瘤直接侵蚀,这些在病程以及治疗过程中都无法避免。
而恶性肿瘤细胞及其产物与宿主细胞相互作用就可以产生高凝状态,引起机体防御血栓形成的功能减弱。
正因肿瘤患者同时具备了血流瘀滞、血管壁损伤和高凝状态这三大要素,因此他们更易患VTE。
评估内、外科肿瘤患者VTE风险,分别运用Khorana和Caprini评分量表……预防肿瘤相关静脉血栓栓塞症CSCO、ISTH指南有何推荐?
如何预防肿瘤相关静脉血栓栓塞症?实际上最重要的是提高意识,我目前正在负责河南省卫健委静脉血栓质控中心的工作,因此深有体会。院内VTE防治工作是国家卫健委医疗质量提升十大改进目标之一。在这项工作推进过程中,需要明确高危科室及高危化患者,肿瘤科以及各个相关科室收治的肿瘤患者都是高危科室以及高危化患者。这是什么意思呢?并非肿瘤患者是肿瘤相关静脉血栓栓塞症的高危因素,就只归肿瘤科管,但凡收治这个病种患者的科室,都是我们质控的重点,都是「高危科室」。
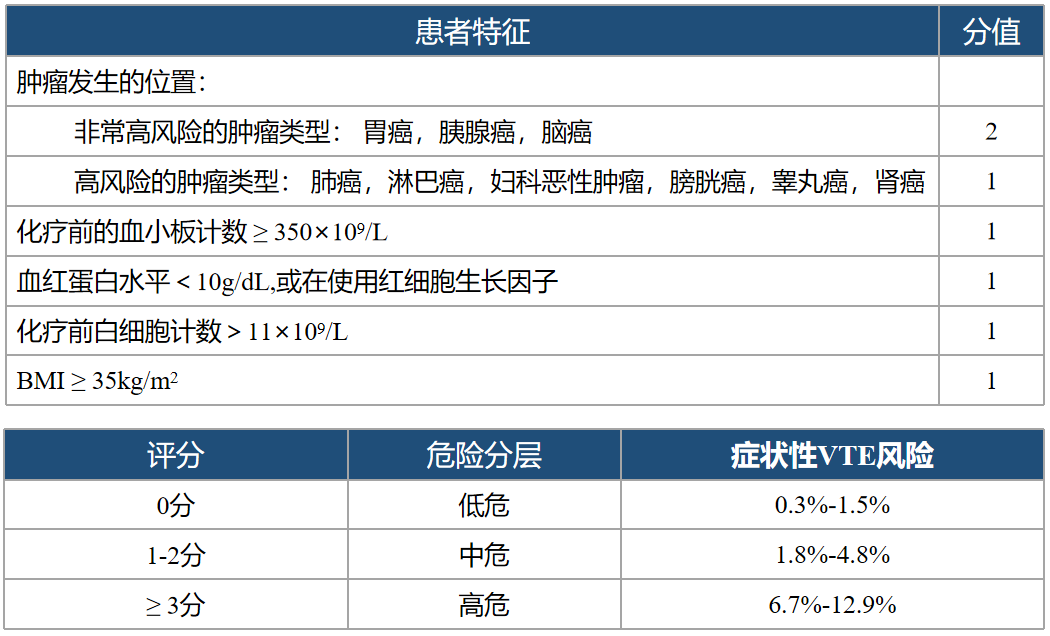
Khorana评分量表
对于在门诊的肿瘤患者,也就是普通的打化疗、用靶向药的患者,我们称内科患者,他们的预防相对而言就比较简单,可以运用Khorana评分量表评估内科肿瘤患者的VTE风险。
这张评分量表直接看肿瘤发生的位置即可,比如胃癌、胰腺癌、脑癌的患者,分值2分,危险分层属于中危,症状性VTE风险为1.8%-4.8%;比如肺癌、淋巴癌、妇科恶性肿瘤、膀胱癌、睾丸癌、肾癌患者,以及按照化疗前血小板计数和白细胞计数,血红蛋白水平、BMI指数,这几项分值都只有1分。
但如果肿瘤患者按照发生的位置得2分或1分,又有重叠后面几项指数的分值得分,则可能大于或等于3分,危险分层就属于高危,症状性VTE风险为6.7%-12.9%。分层为高危的症状性VTE风险平均可达到10%左右,这个比例已经非常值得大家的重视。
举例1:评估患者VTE发生风险,患者为45岁,身高158cm,体重62kg,肺腺癌肺内转移合并肺部感染的女性,白细胞计数13×10^9/L。
第一步,分析患者风险因素:高风险恶性肿瘤肺癌——1分;化疗前白细胞计数13×10^9/L——1分;BMI≈24.83——1分
第二步,计算患者风险评分:1+1+1=3分
第三步,风险评估分级:≥3分,危险分层为高危,6.7%-12.9%可能性发生症状性VTE。
举例2:评估患者VTE发生风险,患者为69岁,身高159cm,体重51kg,胃癌转移致肺合并肺部感染的女性,白细胞计数12×10^9/L。
第一步,分析患者风险因素:非常高风险恶性肿瘤胃癌——2分;高风险恶性肿瘤肺癌——1分;化疗前白细胞计数12×10^9/L——1分
第二步,计算患者风险评分:2+1+1=4分
第三步,风险评估分级:≥3分,危险分层为高危,6.7%-12.9%可能性发生症状性VTE。
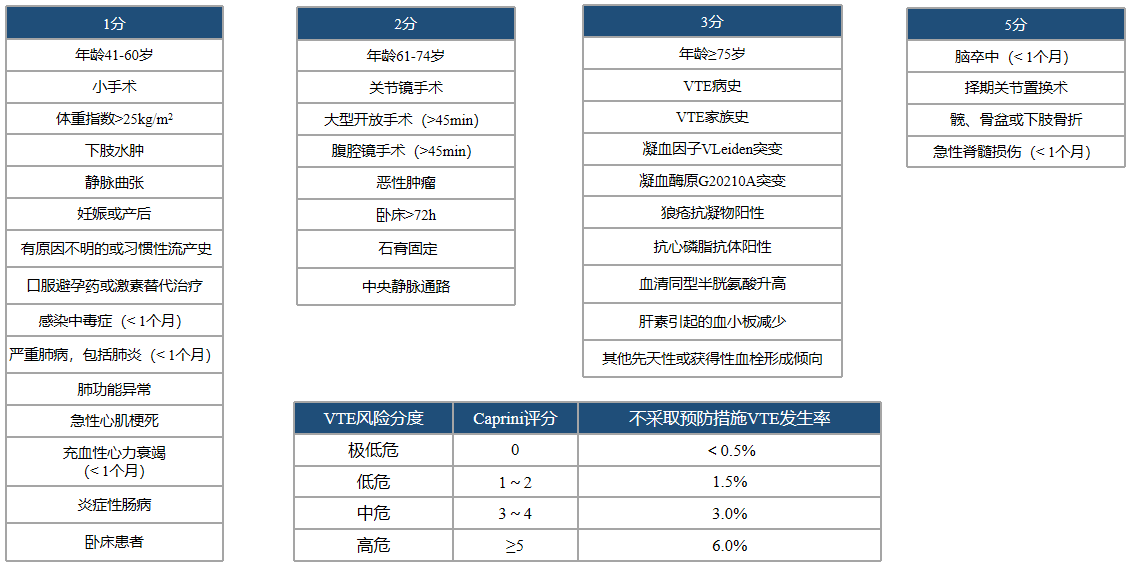
Caprini评分量表
对于外科患者,我们可以运用Caprini评分量表评估外科肿瘤患者的VTE风险。这张评分量表在临床上运用得也比较多,它是一种有效、简单方便、经济实用的VTE风险预测评估工具,能有效帮助临床医生鉴别VTE高危患者,辅助预防方案的选择,从而减少VTE发生率,改善患者预后及生活质量,减少医疗费用。
可以直观地看到,Caprini评分量表分为1分项、2分项、3分项和5分项,如果得分为0分,形成血栓的风险比较小,但如果超过或等于5分,则有6%的可能性会形成血栓。我们再详细解读一下这张评分量表:
首先从适用范围来看,它应用于所有住院患者,包含一般情况、体质指数、VTE病史等40个危险因素,按不同因素对VTE风险的影响不同,危险因素分别赋值,每个危险因素的评分1-5分。
低危风险:1分,DVT发生率<10%,尽早活动,基础预防;
中危风险:2分,DVT发生率10%-20%,药物预防(LMWH)+物理预防;
高危风险:3-4分,DVT发生率20%-40%,药物预防(LMWH)+物理预防;
极高危风险:≥5分,DVT发生风险40%-80%,死亡率1%-5%,药物预防(LMWH)+物理预防。
如存在5分项危险因素,直接定为极高危。
举个例子:评估患者VTE发生风险,患者为55岁接受肺腺癌根治术的正常体重男性。
第一步,分析患者风险因素:年龄41-59岁——1分;大手术(>45分钟)——2分;卧床(>72h)——2分;恶性肿瘤——2分;中央静脉通路——2分
第二步,计算患者风险评分:1+2+2+2+2=9分
第三步,风险评估分级:≥5分,极高危风险,药物预防(LMWH,例如;依诺肝素钠)+物理预防。
Caprini评估表是一种有效、简单方便、经济实用的VTE风险预测评估工具;能有效帮助临床医生鉴别VTE高危患者,辅助预防方案的选择,从而减少VTE发生率,改善患者预后及生活质量,减少医疗费用。

鉴于前面的这些数据,很多指南推荐了对肿瘤患者一定要进行静脉血栓的抗凝预防,尤其是中国的CSCO指南也推荐肿瘤患者进行VTE的抗凝预防,包括外科、内科患者,可先运用各自的评分量表来进行风险评估,再采用抗凝药物治疗,指南对治疗疗程和治疗相关的药物都给予了推荐。
外科住院患者:
VTE风险中、高度(Caprini评分≥3)患者,推荐使用抗凝药物预防。具有VTE风险,但同时存在较高出血风险或抗凝禁忌,推荐应用机械预防。
内科住院患者:
对所有诊断为活动性肿瘤患者,可考虑预防性抗凝治疗;对中、高危( Khorana评分≥2)患者,建议贯穿住院期间抗凝治疗±机械预防。
门诊患者:
门诊经过Khorana评估为中、高危风险(Khorana评分≥2)的肿瘤患者,可以考虑使用利伐沙班或低分子肝素进行血栓预防。

包括2019年的血栓指南(ISTH指南),也强调了对包括门诊在内的肿瘤患者要高度关注抗凝问题,该指南推荐利伐沙班用于门诊肿瘤患者的VTE预防。
ISTH指南:
对于起始化疗、 Khorana评分≥2、无药物间相互作用且无出血高风险(例如胃肠道肿瘤)的门诊肿瘤患,建议采用NOAC作为血栓一级预防。目前只有阿哌沙班和利伐沙班拥有RCT证据。
如采用NOAC作为门诊肿瘤患者的血栓一级预防,建议给药至起始化疗后6个月。推荐在抗凝过程中监测血小板计数和出血并发症风险。
对于计划进行血栓一级预防的高危门诊肿瘤患者,如担心NOAC的安全性(例如担心药物相互作用或胃肠道高出血风险的患者),建议采用低分子肝素。
比如一个65岁的男性胃癌患者,血常规中血红蛋白含量为90g/L,经Khorana评分为3分,VTE风险为高危,需要进行抗凝预防,担心出血风险,建议选择低分子肝素抗凝,尽量不要选择口服抗凝药。
如果是一个50岁的肺癌患者,血常规中血红蛋白含量为90g/L,经Khorana评分为3分,VTE风险为高危,该患者可以低分子肝素抗凝,也可以选择口服抗凝药利伐沙班,严密监测。
肿瘤相关DVT的诊治流程、肿瘤相关PE的诊治流程、肿瘤相关VTE抗凝治疗的疗程……肿瘤相关静脉血栓栓塞症的诊断和治疗
假如,采取了一系列措施,依然「防不胜防」出现了肿瘤相关DVT、肿瘤相关PE、肿瘤相关VTE,该怎么办呢?这就需要了解下一个阶段:诊断和治疗。
诊断分成两部分:一是下肢深静脉血栓形成,二是肺栓塞。
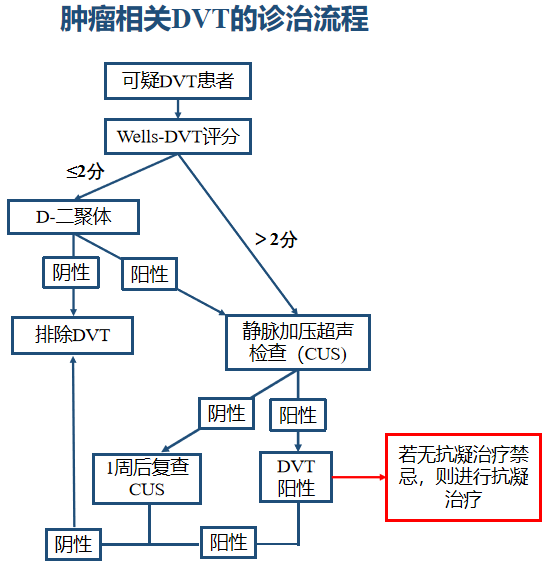
肿瘤相关DVT的诊治流程
对于下肢深静脉血栓形成的患者,从开始怀疑发生起,就要用上Wells-DVT评分。过去这种评分是不收费的,但现在国家医保也批准了收费,有些省份已经实施了。这种评分比较简单,是通过累积记分来进行,内容都是平时在临床中比较关注的特点。
如果得分小于或等于2分,再测D-二聚体,如果D-二聚体为阴性,患者基本上就可以排除下肢深静脉血栓;如果D-二聚体为阳性,或者是得分超过2分,则要做超声来排除有没有下肢深静脉血栓;超声若为阳性,没有抗凝治疗禁忌,要按照DVT进行抗凝治疗。
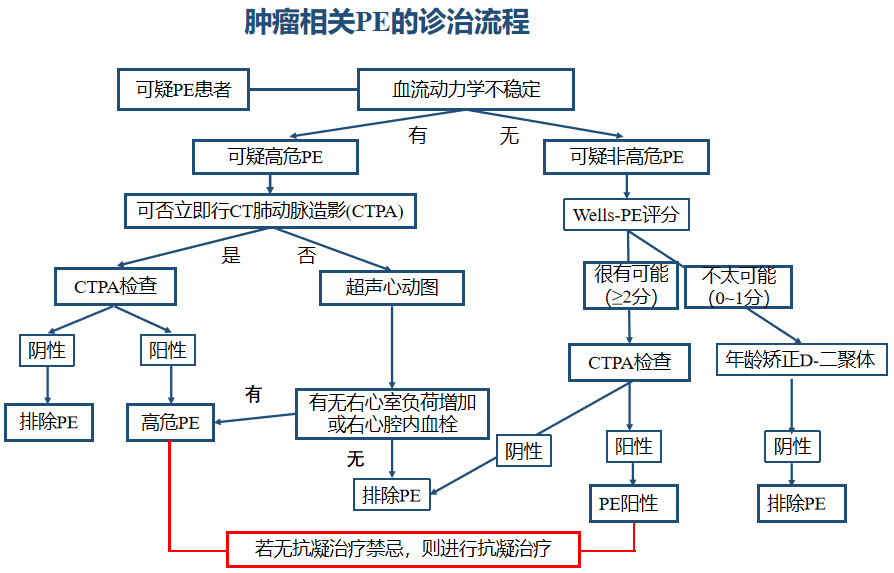
肿瘤相关PE的诊治流程
最危险、也是最重要的问题仍然是肺栓塞。肿瘤相关肺栓塞的诊治也是同样的流程,如果临床上怀疑这个患者是肺栓塞,如果血流动力学不稳定,那就是可疑高危。经层层筛查下来,最终结果为高危肺栓塞的患者,若无抗凝治疗禁忌就直接进行抗凝治疗;如果血流动力学是稳定的,有可能是中低危,这时还是可以采用Wells-PE评分。
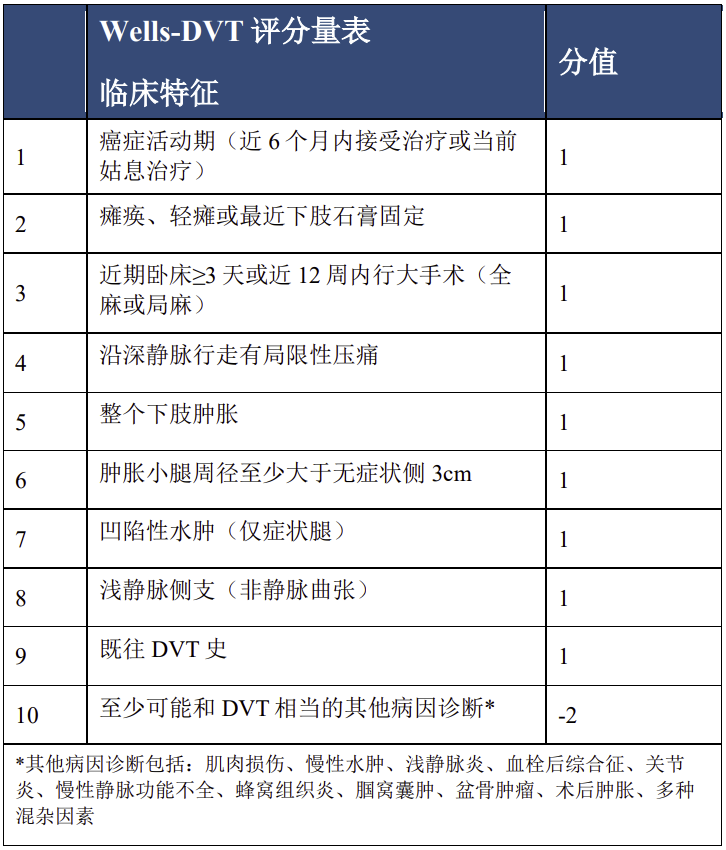
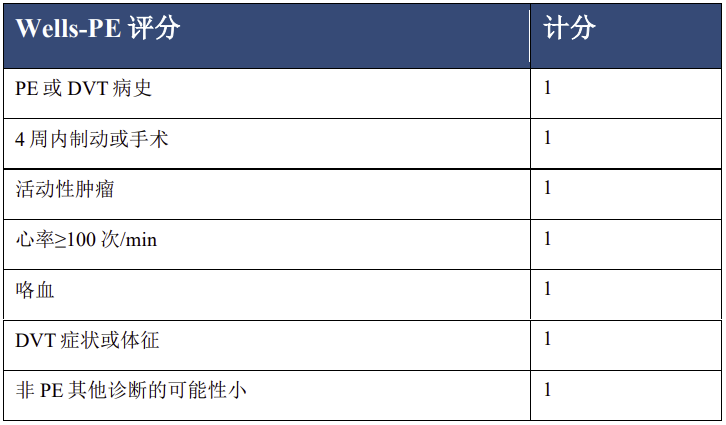
我们可以看到,Wells有两个评分系统,一个是-DVT的评分,一个是PE的评分。两张评分量表都可以依次按项进行加分,但要注意Wells-DVT评分量表中有一项减分2分的,至少可能和DVT相当的其他病因诊断,对其他病因也都有备注说明,很好理解,像诊断为肌肉损伤、慢性水肿、浅静脉炎、血栓后综合征、关节炎、慢性静脉功能不全、蜂窝组织炎、腘窝囊肿、盆骨肿瘤、术后肿胀、多种混杂因素这些疾病,它与肿瘤相关性不大。如果患者已出现的临床特征得分刚好为4分,而恰好又诊断为关节炎,那么4分-2分=2分,这时就需要先查D-二聚体,而不是先做超声。
因此,肿瘤相关DVT的诊治流程和肿瘤相关PE的诊治流程这两张流程图是比较细致的,指南中都有比较明确的推荐,且多家指南都进行了推荐,包括中国的CSCO指南、2018年呼吸学会制定的静脉血栓栓塞症的预防和治疗,都给了相对比较清晰的流程。
确诊后就是进行治疗,关于肿瘤相关VTE抗凝治疗的疗程:
1.如果肿瘤患者的特征是仅仅合并DVT,应接受3-6个月或根据病情给予6个月以上的抗凝治疗。
强调一下,肿瘤患者合并DVT的抗凝疗程至少是3-6个月。举个身边的例子:前段时间我院一位教授的亲戚在北京进行了脑部肿瘤手术,术后合并典型的肺栓塞,治疗后症状得到改善,于是患者这时就开始纠结,认为有没有必要再继续服用抗凝药?说症状已经好了,不闷气了,是否可以停药观察?我明确地告诉他,必须坚持服药,这是一个疗程的问题。我们知道像社区获得性肺炎这样的疾病一般治疗时间比较短,大约10天左右,有的患者需要治疗1-2周,但抗凝不是这样,这需要严格对患者进行管理,因为患者很容易犯这种错误,腿不肿了就自行停药,但这时的复发概率非常高。
2.如果肿瘤患者的特征是合并PE,应接受6-12个月或根据病情给予12个月以上的治疗。
3.如果肿瘤患者的特征是活动性肿瘤或存在持续危险因素,应考虑无限期抗凝。
如果肿瘤是持续存在的,甚至有的患者会采用无限期抗凝,这也是必须坚持的关于抗凝疗程的问题。还有其他的一些治疗,包括溶栓、取栓,还有对于高危的患者采用呼吸支持等等治疗,但最基本的治疗依然是以抗凝为主,而且抗凝的药物基本上与预防的药物都是这几大类:维生素K拮抗剂、新型口服抗凝药。当然还有一些物理的预防。
因此,关于VTE的治疗我们牢记一点,所有VTE患者均需以抗凝治疗作为基础治疗。记住这个流程:
早期治疗【抗凝治疗:包括普通肝素、低分子肝素、维生素K拮抗剂、新型口服抗凝药等;溶栓治疗;手术取栓;呼吸循环支持】—→长期治疗(防止血栓蔓延和/或复发)【抗凝治疗:维生素K拮抗剂、新型口服抗凝药等;物理治疗:包括加压弹力袜和间歇气压治疗】

如何评估抗凝治疗的终点在哪里?根据危险因素是否去除而决定是否继续抗凝,合理地延长VTE患者的抗凝疗程
关于预防很多指南也明确指出最根本的是抗凝,所以我们也再次强调。比如2016年ACCP 10 VTE抗栓指南推荐:所有急性VTE患者应进行至少3个月的抗凝治疗,高危患者应延长抗凝。在下述人群,延长抗凝治疗优于3个月长期抗凝治疗:
无诱因:
·首次发生无诱因下肢近端DVT/PE,伴中低出血风险(2B级推荐)
·再发无诱因VTE,伴中低出血风险(2B/1B推荐)
肿瘤患者:
·有下肢DVT/PE的活动期肿瘤患者,且无高出血风险(2B级推荐)
起始治疗,也就是起始抗凝的一般方案相对比较强,无论用低分子肝素还是普通肝素,或者是利伐沙班,可能在前21天里都属于起始抗凝,剂量要偏大,比如利伐沙班,一般是15mg/bid,到后面长期抗凝的时候,也就是疗程3个月时,可以采用20mg/qd,所以它用法和用量都是不一样的。
但是,如果到最后高危因素始终解除不了,这部分患者要采用无限期抗凝。这时诊断也是清楚的,用药的选择也很清楚,出现一个最大的问题就是抗凝的终点到底在哪?这是需要特别关注的,因为无论是患者还是家属,甚至一些其他专业的老师特别容易停药,可能认为化疗的药物都可以停一停再继续用,抗凝药是不是也可以停一停再用?经常可能会忽略这个问题。
一定千万记住对于持续的危险因素不能解除,包括肿瘤持续活动的患者,抗凝绝对是不能停的。但如果危险因素已经明显解除,举个例子:患者是一个原位腺癌,做了手术以后当时出现了栓子,但实际上他的肿瘤因素已经解除了,这种情况后续是可以停止抗凝的,因为高危因素已经解除了,就可以终止治疗。但如果是肺腺癌Ⅳ期的患者,如果没有抗凝禁忌,危险因素一直解除不了就需要一直抗凝。
因此我们专门做了下面这张表,可以参考,如何合理地延长VTE患者的抗凝疗程:
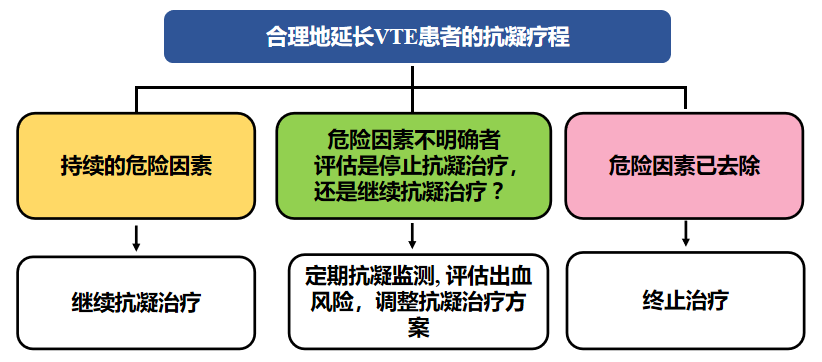
目前,临床上的抗凝药物非常多,静脉血栓的患者到底该怎么选择?VTE长期抗凝该选择哪种?这个问题往往也非常棘手,就如同我们选择靶向还是选择免疫治疗?选择单免治疗还是双免治疗?同样,对于抗凝的选择也有诸多考量因素,比如要选用低分子肝素还是普通肝素?是用华法林还是用口服抗凝药(包括利伐沙班)等等。
还有一个问题就是抗血小板的治疗,其实抗血小板治疗一般更多是用于动脉血栓,比如脑梗、心梗,大多数采用抗血小板治疗。抗血小板治疗对于静脉血栓原来是不推荐的,但后来也认为毕竟抗血小板治疗还是具有一定的抗静脉血栓作用。
这里我想提出一个问题供同道们讨论:今年美国做的一个样本量特别大的研究,我当时看到后感到很震撼,但我不知道将来指南是否会有修改。那篇文章里纳入了几千例的患者用阿司匹林来对静脉血栓进行预防,而在过去这是并不推荐的,因为过去我们一般认为抗凝药物对静脉血栓和动脉血栓都是同时起作用的,但是抗血小板的治疗它对动脉血栓是经典的治疗方案,对于静脉血栓其实作用相当微弱,一般我们不太推荐。
VTE给肿瘤患者带来了严重的危害,临床上应该重视肿瘤相关VTE的预防和治疗,我们可以通过运用前述所讲的Khorana和Caprini评分量表,评估内、外科肿瘤患者VTE风险,包括治疗流程中运用到的Wells-DV、Wells-TPE评分,正确选择肿瘤患者抗凝治疗方案,优选肿瘤患者的抗凝药物。
参考文献
1. Cheuk B, et al. British Journal of Surgery, 2010, 91(4):424-428.
2. Cushman M, et al. Seminars in Hematology, 2007, 44(2):62-69.
3. Farge-Bancel D, et al. Rambam Maimonides Med J. 2014;5(4):e0041.
4. CSCO《肿瘤患者静脉血栓防治指南(2020版)》
5. Khorana AA. Thromb Res. 2010;125(6):490-3.
6. Sørensen HT, et al. N Engl J Med. 2000;343(25):1846-50.
7. Lyman GH et al. Thromb Res. 2018 Apr;164 Suppl 1:S112-S118.
8. Liebman HA. Thromb Res. 2018 Apr;164 Suppl 1:S19-S22.
9. 2020 NCCN临床实践指南:肿瘤相关VTE
10. Wang TF, et al. J Thromb Haemost. 2019 Oct;17(10):1772-1778.
11. 李晓强, 等. 中华普通外科杂志,2017,32(09):807-812.
12. Kearon C, et al. Chest. 2016;149(2):315-52.
13. Prins MH, et al. Blood Adv. 2018;2(7):788-796.
14. Nat Med. 2013 Nov;19(11):1423-37.
专家介绍

程哲
主任医师、医学博士、博士生导师、博士后合作导师;郑大一附院呼吸内五科科主任、大内科党总支副书记;河南省优秀青年科技专家、河南省卫生科技创新型人才、美国Johns Hopkins University和VCU访问学者、中国医师协会首届“全国优秀中青年呼吸医师”、2020年获国家三部委表彰“全国抗击新冠肺炎先进个人” ;河南省医学会内科学分会 候任主任委员;河南省静脉血栓质控中心主任委员;中华医学会呼吸分会基层学组委员;中国医师协会肺栓塞与肺血管病工作委员会委员;河南省医学会呼吸分会副主任委员;中国基层呼吸疾病防治联盟河南省执行主席;河南省呼吸与危重症学会肺栓塞与肺血管病分会主任委员;河南省慢阻肺联盟执行主席;中国残疾人康复协会呼吸康复专委会常委;中国康复医学会呼吸分会呼吸慢病学组副组长;主持国家自然科学基金2项、参与科技部重大专项3项、主持省部级课题10余项。
本文由《呼吸界》编辑 冬雪凝 整理,感谢程哲教授的审阅修改!
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


