引言
双肺肺炎,多次抗感染治疗病灶依然不见吸收,反反复复……这样的案例我们在临床多次遇到,该患者的呼吸道症状及影像学表现不具备特异性,很难单纯根据影像学进行鉴别感染与非感染;而外周血白细胞、CRP、以及PCT等炎性指标在非感染时也可能升高,假如在基础疾病上合并影像学肺部病灶增加以及感染及非感染因素合并往往导致诊治更为复杂。面对鉴别诊断中多方面的困扰,诊治思路应围绕哪些方面展开?
患者两次受凉发病,心脏基础疾病给本就疑点重重的感染「雪上加霜」……抗感染药物牵一发而动全「心」?
患者是一名59岁男性,2019年4月5日主诉「咳嗽咳痰伴咯血2月余,再次发作4天多」入住我院呼吸与危重症医学科。两个多月前,该患者受凉后出现咳嗽,咳白色泡沫痰,伴痰中带血丝,量不多,伴活动时气短,无畏寒、发热,无胸闷、心悸、胸痛等不适,于当地医院就诊,查血常规示「白细胞计数 9.14*109/L,中性粒细胞百分比 70.1%」;胸部CT提示「双肺各叶多发状密度影,边界模糊,其内见支气管通气征」(图1)。
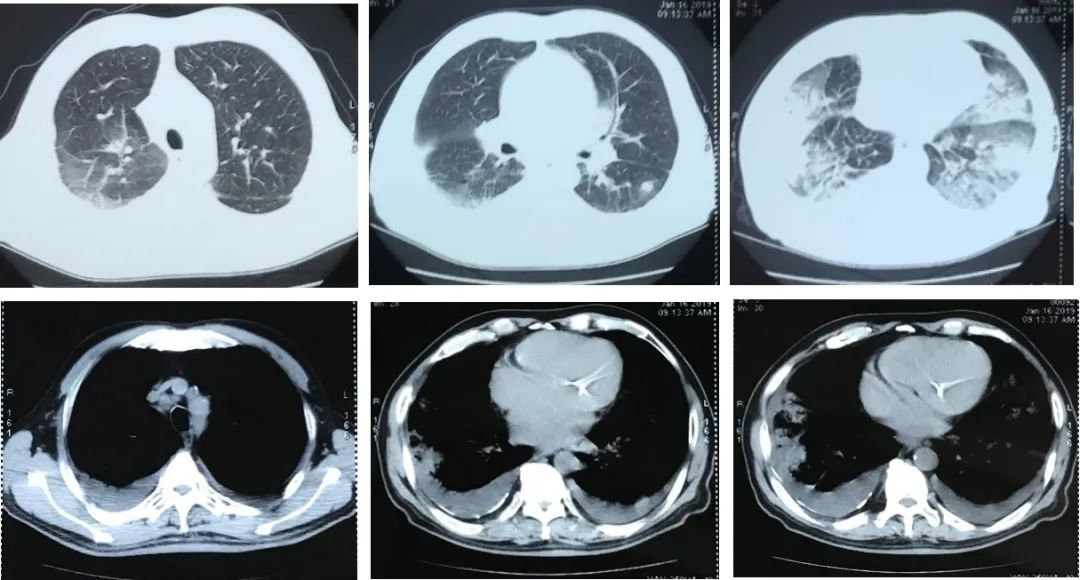
图1:院外胸部CT(2019-1-16)
随即患者被诊断为「大叶性肺炎」,先后予以「头孢他啶」、「左氧氟沙星」、「头孢曲松」抗感染治疗,以及「溴己新」化痰等,治疗10天后,症状好转出院。院外仍有轻微咳嗽,咳少量白色泡沫痰。
此后,距第二次入院1个多月前,患者又一次受凉后出现咳嗽症状加重,咳橙红色痰,每日量总约15ml,伴发热,自测体温38.0℃,气紧明显,无胸痛,于兰州某医院就诊,查血常规示「白细胞计数10.89* 109/L,中性粒细胞百分比69.0%」;心电图提示「心房颤动伴快速心室率」;行胸部CT提示「双肺散在絮状密度增高影,双肺下叶为著;双侧胸腔积液」(图2)。
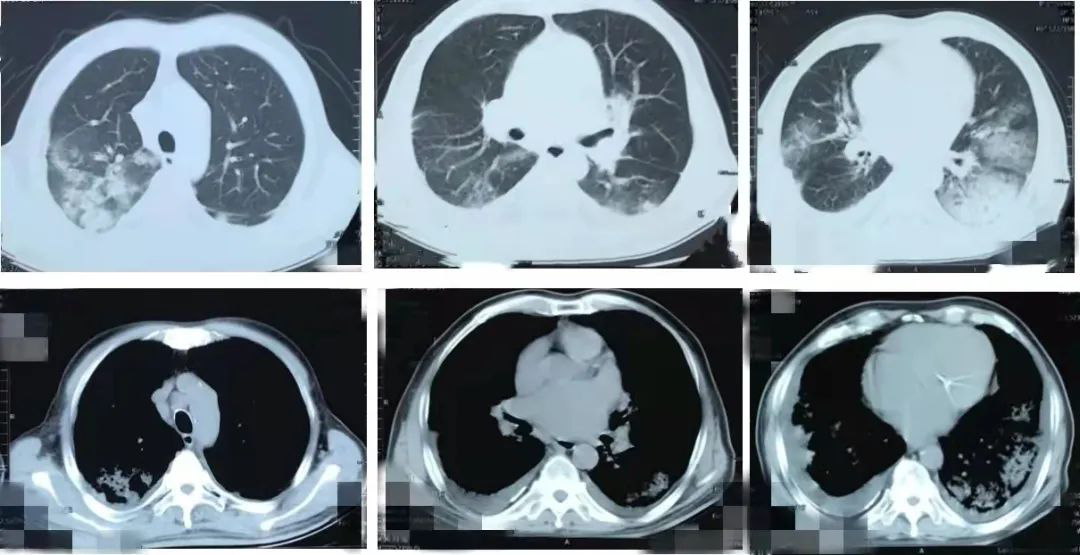
图2:院外胸部CT(2019-2-11)
心脏彩超提示「风湿性心脏病,二尖瓣重度狭窄伴关闭不全;左房增大;肺动脉压增高(中度)」。先后予以「泰能」、「头孢哌酮他唑巴坦」抗感染,其间予以「异烟肼+利福平」诊断性抗结核治疗,以及强心、利尿、抗凝、控制心室率等治疗,患者咳血量明显减少,体温正常后出院。
入院4天之前,患者咳嗽症状再次加重,咳白色粘痰,痰中带血,量少,伴低热,体温最高37.7度,无胸痛,呼吸困难,为进一步诊治来我院急诊,行血常规提示白细胞计数8.16 *109/l,中性粒细胞百分率70.6%;胸部CT提示「双肺散在斑片影,条索影,实变影;纵隔淋巴结增多增大;心脏增大,主动脉及双侧冠状动脉壁,二尖瓣钙化;右侧胸膜增厚,钙化,双侧胸腔少量积液。」(图3)。急诊住院期间停用抗结核药,予以「莫西沙星」抗感染,「利伐沙班10mg qd」抗凝,纠正心功能等治疗后收住我科。
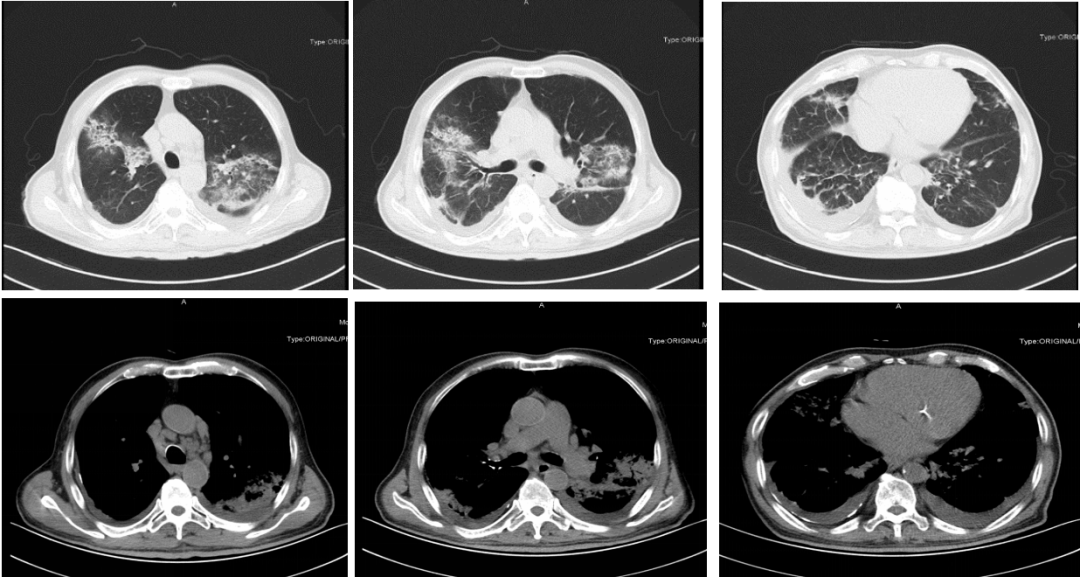
图3:急诊胸部CT(2019-4-3)
自患病以来,患者精神、睡眠、食欲尚可,大小便正常,体重减轻约2kg。
详细追查既往史发现「漏洞」,患者曾长期进行抗凝治疗但未监测凝血功能……结合病史及辅助检查可查明患者反复双肺渗出病因?
经了解,患者10余年前发现血糖升高,空腹血糖最高8+mmol/L,间断服用口服降糖药,此后并未长期监测血糖;6年多前,患者又发现风湿性心脏病,伴二尖瓣重度狭窄,关闭不全,房颤,冠脉粥样硬化心脏病。既往长期口服华法林抗凝及阿托伐他汀调脂,未监测INR,1月余前于兰州某医院查INR 7.68,换用利伐沙班10mg qd抗凝。此外,该患者自幼发现为乙型肝炎病毒携带者,未进行抗病毒治疗;否认结核、慢性支气管炎、高血压等病史。其长期生活在甘肃省兰州市,无食物药物过敏史,无手术、外伤史。吸烟20余年,已戒烟10余年。偶尔少量饮酒。家族史无特殊。
入院查体的情况如下:
T:36.7℃ ,P:132次/分,R:22次/分,BP :129/80 mmHg。神志清楚,精神尚可,慢性病容,皮肤巩膜无黄染,全身浅表淋巴结未扪及肿大,颈静脉正常。心界向左侧扩大,心律不齐,二尖瓣听诊区可闻及舒张期隆隆样杂音,胸廓未见异常,双肺叩诊呈清音,双肺可闻及散在湿啰音,未闻及胸膜摩擦音。腹部平坦,全腹软,全腹无压痛及反跳痛,腹部未触及包块。肝脾肋下未触及。双下肢无水肿。
辅助检查情况如下:
2019年2月11日于当地医院:白细胞计数10.89*109/L,中性粒细胞百分比69.0%,血糖 15.15mmol/l,PT 81.1秒,INR 7.68,PCT 0.046 ng/ml,CRP 145.99 mg/l,九项呼吸道病原体检测阴性。胸部CT:双肺肺炎,双侧胸腔积液,主,冠状动脉硬化,心影增大,心包少量积液,纵隔淋巴结钙化。心脏彩超:风湿性心脏病,二尖瓣狭窄(重度)伴关闭不全(轻中度),主动脉瓣轻度反流,二尖瓣轻度反流。
辅助检查(华西急诊):血常规示白细胞计数 8.16 * 10 9/l,中性粒细胞百分率70.6%。尿常规、大便常规、肝肾功能、电解质正常。
动脉血气分析:PH 7.484,PO2 74.6mmHg,PCO2 31.8mmHg,Lac 1.1mmol/L,HCO3- 23.4mmol/L。
凝血功能示:凝血酶原时间12.9 秒,国际标准化比值1.18,活化部分凝血活酶时间34.9秒,D-二聚体0.93 mg/l FEU。糖化血红蛋白A1c 8.0%。尿钠素 460pg/ml,心肌标志物正常。PCT小于0.02ng/ml,血沉47.0mm/h。
床旁心电图示:心房扑动(2:1下传)。
心脏彩超示:二尖瓣狭窄(重度)反流(轻度),三尖瓣反流(轻度)肺高压(中度),左室收缩功能测值轻度降低(LV 48,LA 60,RV 21,EF 49%)。
胸部CT(2019-4-3,图3)示:1,双肺散在斑片影,条索影,实变影。2,纵隔淋巴结增多增大。3,心脏增大,左心房增大为主,主动脉及双侧冠状动脉壁,二尖瓣钙化 。4,右侧胸膜增厚,钙化,双侧胸腔少量积液。
患者入院后,团队立即对其做进一步检查:
1、感染指标:血沉48.0-81.0mm/h(2次);C-反应蛋白74.80-94.90mg/L(2次),PCT<0.02ng/ml(3次)
2、痰涂片、痰培养阴性(3次);呼吸道13项病毒阴性;TB-IGRA阴性;TORCH 阴性;G试验、GM试验 阴性,CMV-DNA 1.31E+01 copies/mL ;EBV-DNA (-)
3、免疫:抗链「O」阴性;免疫球蛋白A 5710.00 mg/L,免疫球蛋白M 543.00 mg/L,C3、C4正常。ANCA、GBM阴性。T细胞亚群:CD4 31.20 %
4、肿标:CA-125 117.80 U/ml,余阴性。
5、心肌标志物及BNP检测正常。
结合现有的病史及辅助检查,分析患者反复双肺渗出的病因可能为:(单选)
肺部影像学加重但血常规及炎性指标不高,基础风湿性疾病合并房颤及心功能不全需高度警惕什么?……继续抗感染效果如何?
根据该患者的病史特点我们进行了回顾:
1、患者为中老年男性,起病急,病程稍长;
2、主要表现为反复于受凉后出现咳嗽、咯痰、发热及呼吸困难,反复咯血,经抗感染治疗后症状可好转;
3、既往有风湿性心脏病,伴二尖瓣重度狭窄,关闭不全,房颤,冠脉粥样硬化心脏病病史,长期进行抗凝治疗,未监测凝血功能。有糖尿病病史,血糖控制不详。
4、辅助检查提示血象不高,感染指标不高,血沉稍快,胸部CT提示双肺散在斑片影,条索影,实变影,伴有胸腔积液。
据此,应如何诊断分析及鉴别诊断?我们首先以反复的肺部阴影为切入点来进行分析,以下为诊断思路线图(图4)。
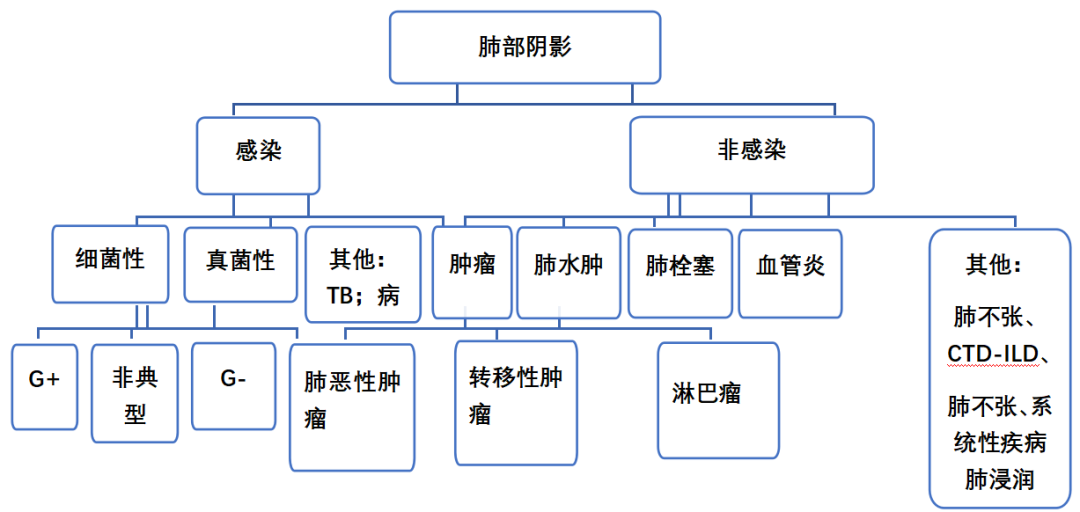
图4:肺部阴影诊断思路线图
思考:患者为感染性疾病吗?
分析:典型的细菌性肺炎多为急性起病,伴发热,多为高热,可能出现寒战甚至休克,痰多为黄色或者脓痰,外周血白细胞总数及中性粒比例明显升高,以及炎症指标比如PCT、C反应蛋白(CRP)升高。肺部查体可有实变体征或湿性啰音,影像学多表现为肺泡浸润或实变呈叶段分布。经验性抗感染治疗常常有效。
该患者感染中毒的症状不重,肺部影像学加重的同时,血常规及炎性指标不高,这些均提示可能为非细菌感染。更重要的是,患者使用的抗感染药物基本可以覆盖除MRSA、部分非典型病原体、以及特殊病原体感染等常见社区获得性病原体。
MRSA在社区获得性肺炎中较为少见,常见于合并流感、以及外周脓肿等合并因素,且影像学多表现为坏死性肺炎或合并空洞;支原体或者衣原体多见于基础情况良好的患者,起病缓,多为干咳,影像学多见上肺野为主,细支气管炎基础上可出现实变;军团菌影像学可能出现大片实变影及支气管气相,但往往病情进展迅速,是重症CAP常见的病原体之一;病毒多具有季节性及流行病学史,影像学早期多为间质性肺炎改变;真菌感染往往具有临床因素、影像学特征、以及病原学检查特征,尤其是免疫抑制患者,或者影像学出现晕征及空洞,肺泡灌洗液GM试验阳性,否则可能性偏小;而结核的影像学具有起病缓,病灶多位于上叶尖后段、下叶背段,以及多形性改变。
该患者虽然在外院诊断性抗结核治疗过,但目前并无结核相关证据。因此,感染方面可进一步完善抗原抗体检测、以及支气管镜肺泡灌洗搜寻特殊或非典型病原体,以及排除细菌耐药、并发症、以及肺外感染可能。
思考:患者为非感染性疾病吗?
分析:与非感染性疾病的鉴别,往往贯穿于肺炎诊治的全过程,尤其是常规抗感染治疗无效的患者,包括疾病反复的患者,需考虑非感染性疾病可能。
该患者基础风湿性疾病,合并房颤及心功能不全,需高度警惕肺水肿可能,但心衰合并肺水肿的患者往往合并夜间阵发性呼吸困难及不能平卧,BNP升高,且影像学常常有典型「蝶翼征」表现。加之该患者有反复咯血,且合并肺动脉肺动脉高压,以及长期抗凝治疗,不排除肺泡出血可能。
如果患者合并血栓高危因素,这种反复的肺部阴影也需要与肺栓塞相鉴别,患者常常表现为不能解释的呼吸困难或者氧饱和度下降,或者合并胸痛及咯血症状,而影像学表现为胸膜下间断朝肺门的楔形影或斑片实变影,多与肺梗死相关, D-二聚体检测小于0.5mg/l FEU,往往在中低危患者中具有排除性意义。
肺部病灶进展或者未吸收,还需与肺部肿瘤相鉴别,表现为实变或者磨玻璃影的肿瘤,常见的包括浸润性黏液腺癌(或称之为支气管肺泡细胞癌)以及淋巴瘤等。浸润性黏液腺癌往往呈匍匐生长,病灶进展相对较慢,且影像学可出现典型的「铺路石征」改变;淋巴瘤肺浸润影像学表现多样,病人可出现反复发热、全身淋巴结增大、以及乳酸脱氢酶明显升高等特征。血管炎合并肺泡出血患者也需鉴别,患者往往合并多系统损害,尤其是肾脏常常受累。此外还有肺不张、CTD-ILD,以及系统性疾病肺浸润等,都是需要鉴别的疾病。
综上,团队是如何对其进行下一步诊治的?患者入院后,我们首先予以鼻导管吸氧,莫西沙星抗感染,氨溴索化痰,以及呋塞米螺内酯利尿、倍他乐克控制心率。患者持续房颤,与心内科商量,患者现在是重度二尖瓣狭窄,但目前指南不推荐新型口服抗凝药物预防血栓,遂将抗凝调整为低分子肝素抗凝,患者咳嗽咳痰好转,无发热,每天间断咯橙红色痰液约10ml,心率控制在90~110次/分,仍为房颤心律,夜间能平卧。
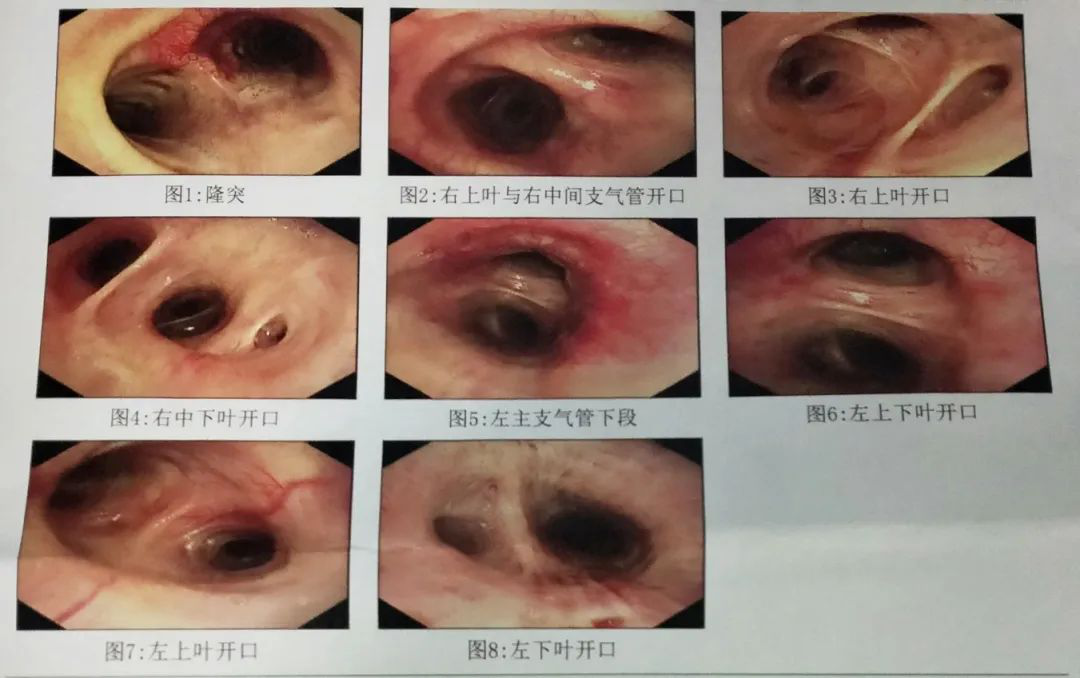

图5:在全麻下行支气管镜检查、纤维支气管检查及肺泡灌洗液
镜下见:声门、气管隆突未见异常,双侧及各级支气管少量脓性分泌物,支气管镜吸出后见左主支气管下段前外壁黏膜充血、肿胀;余双侧各级支气管黏膜光滑,管腔通畅。进一步支气管刷片未查见恶性细胞;痰涂片未查见 恶性细胞,普鲁士蓝染色(-) ;肺泡灌洗液未查见恶性细胞,普鲁士蓝染色(-) ;涂片、培养阴性;GM试验 0.51 GMI。
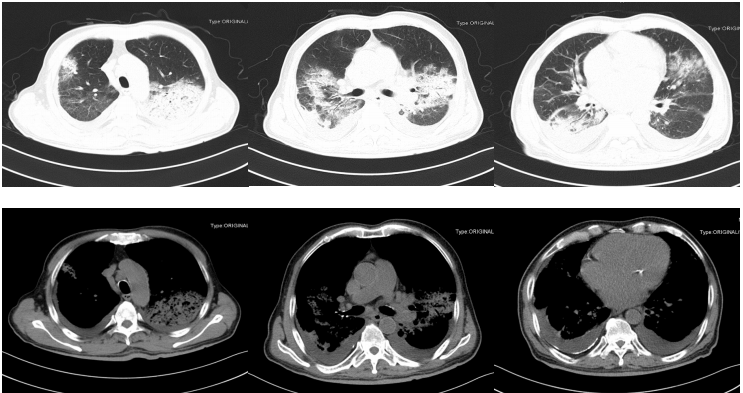
图6:(2019-4-10)复查胸部CT,抗感染治疗1周,复查胸部CT,病灶呈加重。
鉴于患者咳嗽咳痰症状有所缓解,目前感染及免疫系统疾病证据不足,停用莫西沙星,继续低分子肝素抗凝,患者未发热,咯血症状逐渐好转,一周后再次复查胸部CT提示双肺病灶较前吸收(图7)。
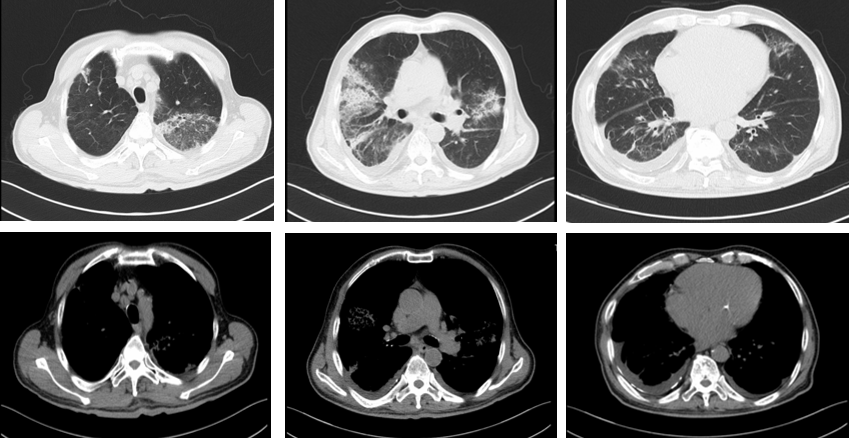
图7:再次复查胸部CT(2019-4-17)
繁杂的抗感染后发热、咯血有所好转,病灶吸收,后续如何诊治?……治疗时间轴能看出什么?行心脏手术依据何在?经验何在?
针对此前诊治全过程,团队召开疑难病例讨论会:
1、唐永江主治医师:该患者的一个重要特点是反反复复的双肺阴影,抗感染治疗效果不佳。按照双肺阴影的诊断思路,我们按照感染性、以及非感染性进行鉴别。该患者早期有发热、咳嗽等症状,血象提示轻微增高,但到我院来后,血常规、中性粒比例正常,且PCT等感染指标不高,院外抗感染治疗基本覆盖了常见病原体,而我们住院期间的进一步检查也没有发现病原体。因此,患者感染因素目前没有相关证据。该患者的病史中有一个最大特点就是有风湿性心脏病,二尖瓣重度狭窄,以及中度肺动脉高压,且既往因房颤长期使用华法林抗凝期间未监测INR,外院住院期间复查INR明显升高。因此,该患者不排除肺动脉高压抗凝过程中肺泡出血可能。
所以我们做了两方面工作:第一,患者持续房颤,与心内科商量,换用了出血风险较小且能监测的低分子肝素,密切监测患者咯血情况,评估咯血量与肺部表现得关系;第二、完善支气管镜,观察肺泡灌洗液颜色以及普鲁士蓝染色查找含铁血黄色细胞。结果发现,患者咯血量与肺病影像学关系较密切,咯血量减少的同时肺部病灶也有吸收,但是肺泡灌洗液未见典型鲜红色液体,普鲁士蓝染色也为阴性,针对这一点,用弥漫性肺泡出血不好解释。患者肺泡灌洗液结果解读需结合支气管肺泡灌洗操作流程来解释,如果肺泡灌洗液体量不够,可能回收的是支气管内的液体,而不是远端肺泡的液体,诊断弥漫性肺泡出血强调在影像学提示异常的亚段连续行支气管肺泡灌洗,依次灌入3次50-60ml生理盐水,如血性程度越来越重,则确诊肺泡出血;如患者无活动性出血或BALF无明显血性液体时,肺泡灌洗液普鲁士蓝染色阳性(>20%巨噬细胞染色阳性)有助于诊断。该患者需明确肺泡灌洗液体的量,必要时再次完善支气管镜检查,但患者目前影像学有吸收,一般情况也较好,拟联系心脏外科评估手术,术后复查影像学进一步明确。
2、李晓欧主治医师:该患者多次BNP检测正常,临床中常用来排除心衰。但心衰如果是左心室上游原因(如二尖瓣狭窄、乳头肌断裂引起的二尖瓣脱垂、急性二尖瓣反流)引起时,患者症状严重,BNP水平最初可能较低。在这些急性情况下,左室壁应力没有显著升高,所以缺乏明显的BNP生成,尽管BNP水平可能仍高于正常水平,但它们不会上升到心衰伴随左心室过载时相同的程度。因此,患者肺部病灶不排除肺水肿可能,在患者管理中仍需注意容量管理,适当负平衡。
3、杨小东教授:弥漫性肺泡出血基于病理表现,可分为肺毛细血管炎、温和性出血以及弥漫性肺泡损伤。病理除了弥漫性肺泡腔出血外,肺毛细血管炎病理还可见肺泡间隔中性粒细胞浸润,病因包括系统性血管炎、抗肾小球基底膜病、风湿性疾病、药物、特发性肺含铁血黄素沉着症、特发性肺毛细血管炎;而温和性肺泡出血肺泡间隔往往完整,无明显炎症浸润,常见于左室舒张末期压力升高合并出血性疾病或者抗凝治疗;而弥漫性肺泡损伤肺泡间隔水肿及肺泡腔内透明膜形成,临床中往往表现为ARDS。我们常说的弥漫性肺泡出血常指前两种。
4、梁宗安教授:该患者肺部情况主要表现为反复的双肺浸润影,抗感染治疗似乎吸收,但从多次的影像学变化情况和咯血相关性更大。因此,还是需考虑肺部表现与心脏基础疾病相关,患者未抗感染情况下肺部病灶有吸收,建议请心脏外科会诊积极干预二尖瓣狭窄问题,后期随访胸部CT。
经全科疑难讨论后,团队考虑该患者的肺部病灶与二尖瓣狭窄引起的肺动脉高压及早期抗凝治疗不当导致的弥漫性肺泡出血可能性大,遂将其转至心脏外科行「二尖瓣置换+三尖瓣成形术」。
术后,患者的呼吸道症状消失,复查心脏彩超示人工机械瓣功能未见明显异常,三尖瓣微量反流。术后复查胸部CT提示双肺病灶基本吸收(图8)
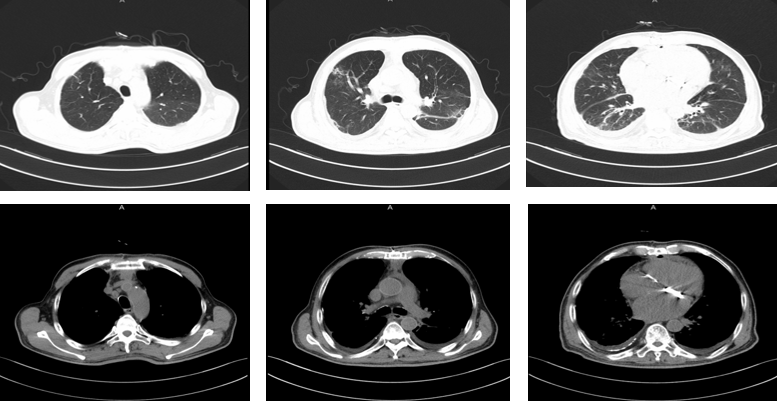
图8:术后胸部CT复查(2019-5-7)
至此,团队对该患者的最终诊断如下
1、弥漫性肺泡出血(DAH);
2、风湿性心脏病 二尖瓣狭窄(重度)伴关闭不全 心房颤动 心脏长大 心功II级;
3、二尖瓣置换+三尖瓣成形术后;
4、冠状动脉粥样硬化性心脏病;
5、肺动脉高压(中度);
6、2型糖尿病;
7、双侧胸腔积液。
诊断依据如下:
1、基础病史:风心病(二尖瓣狭窄),长期华法林抗凝,发病前期未监测INR;
2、从患者症状、影像学表现、以及抗凝治疗时间线图(图9)可以看出,患者影像学表现与咳痰特别是血痰相关,而与抗感染治疗强度相关性不大,特别是4-3到4-17号三次CT,第二次复查胸部CT肺部病灶增加,而在此基础上在停用抗感染治疗后反而病灶好转,充分说明肺部病灶很有可能是非感染因素所致。
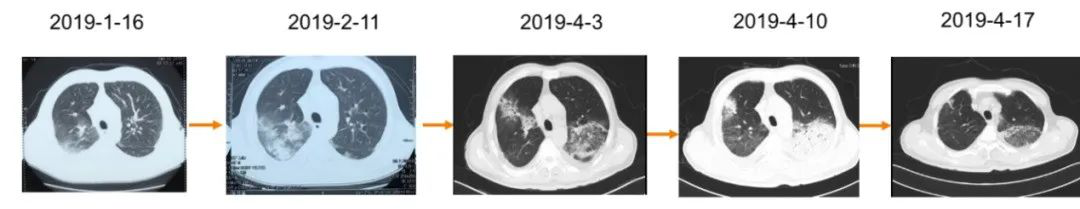
图9:患者抗凝治疗时间线图
回顾该患者自2019年1月16日到2019年4月17日的病史时间线图,从症状、治疗以及抗凝治疗上对比,我们可以更加直观地看到治疗效果:
2019年1月16日——患者症状:咳嗽、痰中带血;治疗:头孢他啶、左氧氟沙星、头孢曲松;抗凝治疗:华法林(未见INR结果)
2019年2月11日——患者症状:咳嗽、橙色痰;治疗:泰能、头孢哌酮他唑巴坦、HR诊断抗TB;抗凝治疗:华法林(INR 7.68);利伐沙班
2019年4月3日——患者症状:咳嗽、橙色痰;治疗:莫西沙星;抗凝治疗:华法林(INR 1.14)、低分子肝素
2019年4月10日——患者症状:咳嗽、橙色痰减少;治疗:无;抗凝治疗:低分子肝素
2019年4月17日——患者症状:少量咳嗽;治疗:无;抗凝治疗:低分子肝素
经验和体会
1、 根据我国2016年CAP诊治肺炎的临床诊断标准,在强调临床表现及影像学的同时,须除外肺结核、肺部肿瘤、非感染性非间质性疾病、肺水肿、肺不张、肺栓塞、肺嗜酸粒细胞浸润症及非血管炎等 后,可建立临床诊断。而在临床实践中,依据临床表现及影像学表现,的确很容易确定肺炎的诊断,但其鉴别诊断往往却容易被忽视,导致抗感染药物的滥用及疾病的误诊 。正如同指南中强调的诊治思路的第一步,就是在判断CAP诊断是否成立时需要注意与肺结核等特殊感染以及非感染病因进行鉴别。但鉴别诊断存在几个方面的困扰:
第一,感染和非感染的症状及影像学表现不具备特异性,很难单纯根据影像学进行鉴别;
第二,外周血白细胞及CRP在感染时可能升高,但某些非感染性疾病也可升高,PCT是目前用于判断细菌感染与否的重要标志物,但在一些全身炎症反应、以及急性肾损伤等疾病也可能明显升高,而比如血管炎等鉴别疾病往往也容易合并急性肾损伤;
第三,一些存在基础疾病的患者,可能在基础疾病上合并感染,感染及非感染因素合并往往导致诊治更为复杂。
因此,我们在肺炎的诊治过程中,更加强调标准化的病原学证据,同时需要综合考虑患者的综合情况,尽量用「一元论」解释,比如患者存在心功能不全和/或容量负荷过重的情况,就需要警惕肺水肿的可能;而多系统受累需警惕血管炎等系统性疾病;而疾病病程缓慢,感染中度症状轻需警惕肿瘤等可能;如果患者存在危险因素、典型胸痛咯血呼吸困难三联征、和/或DVT及右心功能障碍证据,需考虑肺栓塞引起的肺梗死。最重要的一点,患者无感染病原学证据以及抗感染无效,我们均需进一步排除非感染因素。
2、本患者诊治过程中充分体现肺炎鉴别诊断的临床思维。患者反复抗感染病灶反复,且合并心脏基础疾病、肺动脉高压、以及抗凝不当,就需要考虑非感染因素,而结合患者基础病史,考虑心脏基础疾病继发肺水肿以及肺泡出血的可能,诊治思路也围绕这方面展开:第一,虽然患者在辅助检查提示部分免疫指标无明显异常,但患者无相关症状体征,且临床表现及肺部影像学也非CTD-ILD常见表现,因此未进一步搜寻相关证据;第二,患者感染证据不足,结合既往诊治过程,感染在初始即初步排除,而特殊感染均具有其相应特征,结核感染的多形性,真菌感染的疾病进程规律,PCP患者细胞免疫缺陷及G试验升高,均有助于我们鉴别诊断,因此,虽然目前有NGS等新技术辅助感染诊断,但对临床表现、常规辅助检查、影像学、特别是诊疗诊治经过的仔细评估,仍是诊治思路的最根本。
参考文献
1. 中华医学会呼吸病学分会. 中国成人社区获得性肺炎诊断和治疗指南(2016年版). 中华结核和呼吸杂志 2016(4): 253-279.
2. 发热伴肺部阴影鉴别诊断共识专家组. 发热伴肺部阴影鉴别诊断专家共识. 中华结核和呼吸杂志 2016(3): 169-176.
专家介绍

唐永江
副主任医师,PCCM专培结业医师。四川大学华西临床医学院本科毕业,香港中文大学博士,美国康奈尔大学访问学者,中华医学会呼吸病学专委会呼吸危重症学组秘书,四川省医学会呼吸病学专委会介入学组委员兼秘书,主要从事呼吸危重症、肺血管疾病(血管炎)、以及肺部感染的临床及科研工作。


