我今天与大家讲讲「反向触发」,它在临床中时有发生,机械通气过程中如何识别及其临床意义?
一、人机对抗类型
「人机不同步」或「患者-呼吸机对抗」,简称人机对抗,它主要是机械通气与患者自主呼吸不同步的现象,根本原因是各种因素导致呼吸机的运行和患者自主呼吸不协调而出现的异常人机关系。
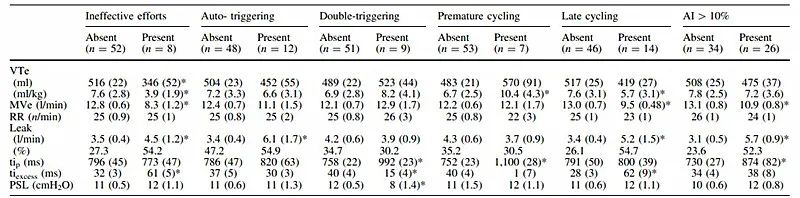
人机不同步的发生并不少见,它可以发生在我们呼吸的4个阶段里,如吸气触发(Inspiratory triggering),吸气(Inspiration),吸呼气转换(Termination of inspiration),以及呼气(Expiration)的阶段。
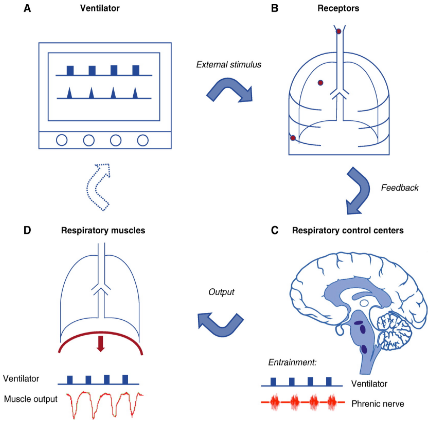
二、反向触发的作用机制
反向触发实际上是人机不同步的一个表现,主要发生在吸气阶段,首先看看反向触发的「概念」,实际上是在控制通气模式下,正是呼吸机的送气过程,诱导患者的呼吸中枢发放新的,或者与机械通气周期有一定程度偶联的呼吸节律,这一现象我们称之为呼吸拖带(Respiratory Entrainment),又称为「反向触发」。
它实质上是机体呼吸中枢在呼吸机周期性通气影响下对呼吸节律的再次重新设定,以使两者之间暂时保持一种稳定的关系,目前,反向触发仍然是一种我们远未充分认识的人机不同步类型。
反向触发中有这几个概念:
1、拖带比(entrainment ratio):
拖带比(entrainment ratio)是机械周期与神经呼吸周期的比例关系,1:1指1次机控通气对应1次神经呼吸,1:2指2次机控通气对应1次神经呼吸,以此类推。其中1:1是最常见也最稳定的,通常可持续较长时间,1:2则每10~12个呼吸周期容易被非拖带呼吸所打断。通过改变呼吸机的呼吸频率设置,可以改变拖带特征(如从1:1变为1:3),或者完全消除拖带的存在。
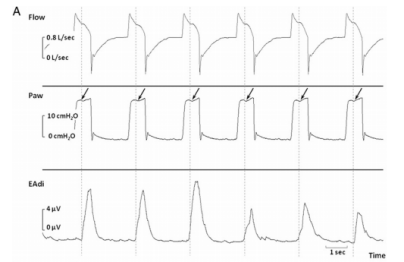

(图A拖带比1:1,B拖带比1:2)
2、呼吸叠加(Breath stacking):
在呼吸机潮气量输出末期出现患者的吸气努力,导致迅速发生第二次呼吸机送气。可能造成呼吸机输送气体量明显大于设定的潮气量。可以是反向触发的一种表现形式,也可以是「双吸气」。
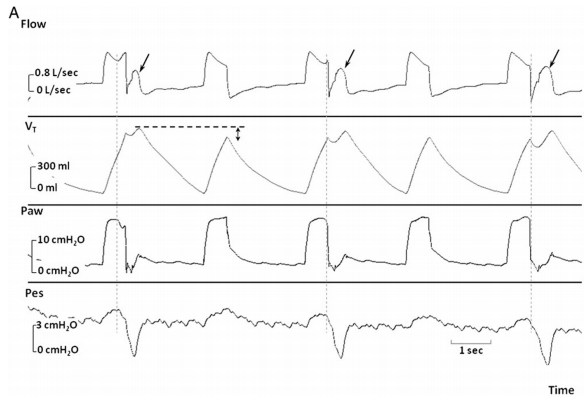
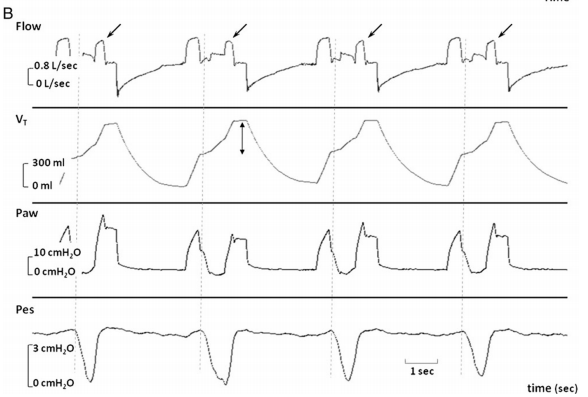
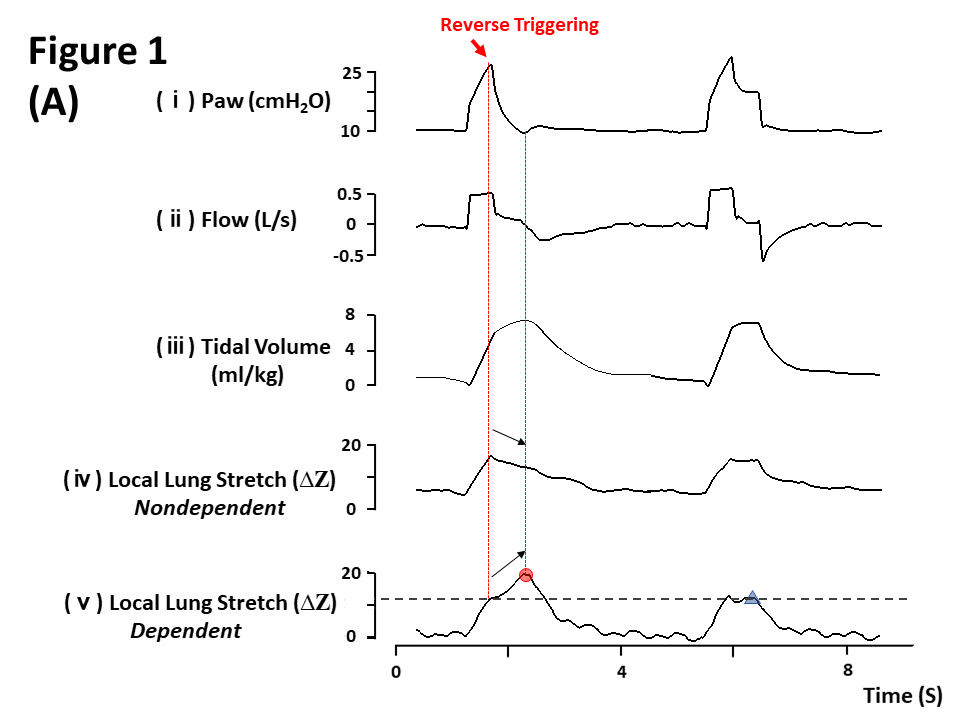
(A图中,我们可以看出反向触发导致了潮气量增加)
3、相位差(phase difference ,dP):
为神经呼吸周期与机械通气周期开始时间之间的时差迟滞,单位为秒(s)。考虑到周期的长短不同,采用相位角(the phase angle,θ)这一标准化的表达方式可以更准确地反映两者之间的关系,θ的计算公式为:θ=dP/Ttotmech×360°。
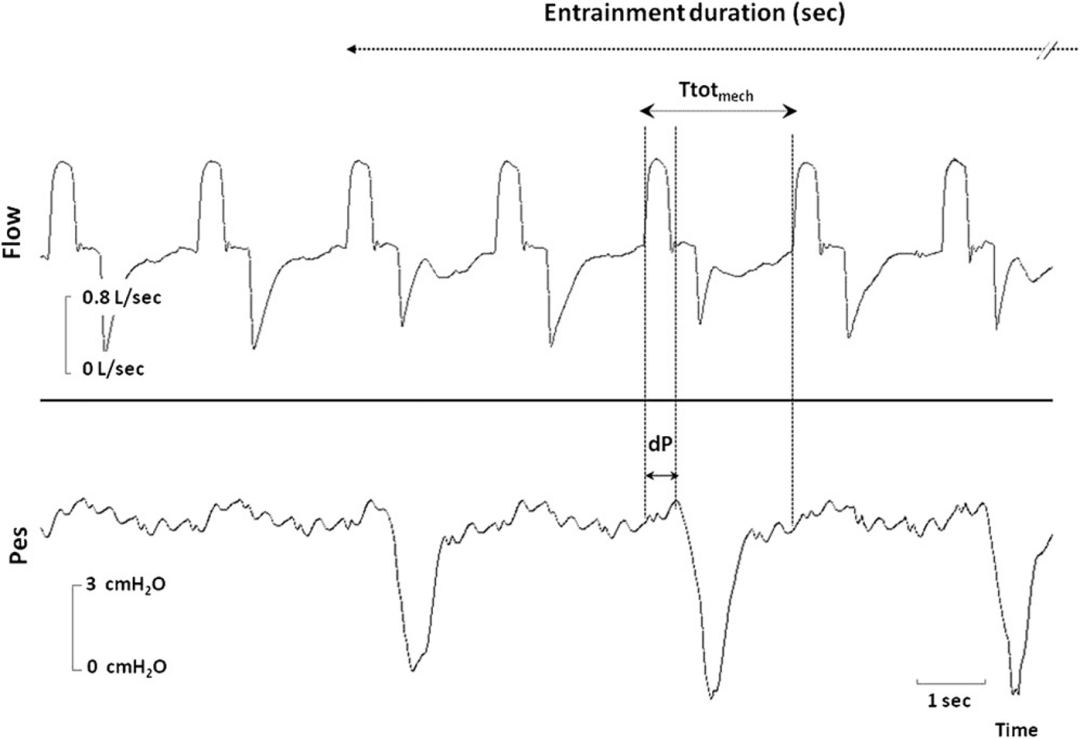
(这张图片为呼吸拖带示意图。对照流速波形及食道内压监测,可以判断出拖带比为1:2 。这个病例中,拖带时长为32.17s,相位差为0.66s,机械周期时长为2.29s。相位角的计算为θ=dP/Ttolmech × 360°=104°。)
三、如何识别反向触发?
反向触发仅依据波形识别较困难,但通过仔细观察呼吸机的各种波形,仍有可能发现蛛丝马迹。

是反向触发,还是双重触发?反向触发与双重触发产生的效果很相似,双重触发中1/3是反向触发,但是两者之间的病理生理不同,可以采取5s呼气阻断操作加以区分和识别。反向触发的呼吸以稳定且重复的方式发生。给予5s呼气阻断操作会抑制外部刺激,从而打断呼吸夹带,并防止反向触发。采取5s呼气阻断操作,反向触发患者自发努力会消失,而双重触发患者的自发努力会持续,并且更加剧烈。
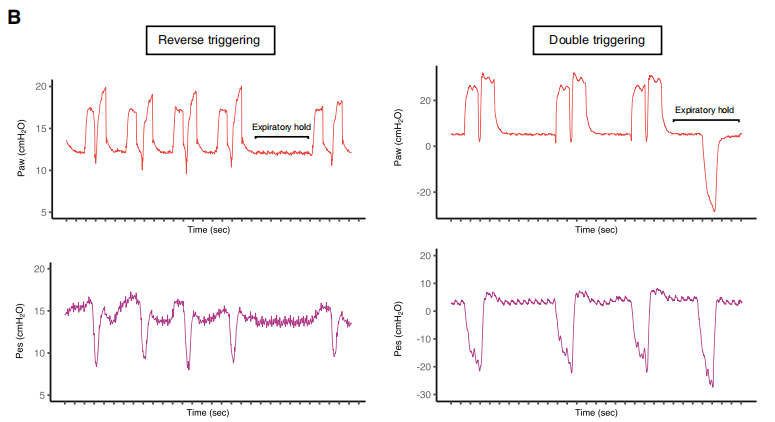
2021年发表在《Chest》的一篇文章,一项多中心观察性研究,早期ARDS中反向触发的发生率:

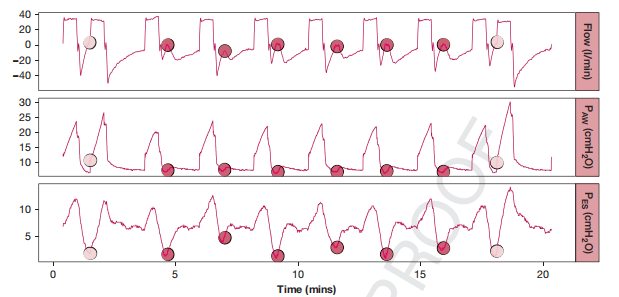
(上图显示反向触发不同步的患者呼吸波形示例。ARDS患者的流量、气道压(Paw)和食管压(Pes)记录。这些点表示脚本根据流量和Paw检测到反向触发的确切时间。呼吸机与患者用力的比例为1:1,浅圈点表示反向触发相关呼吸堆叠。无法触发呼吸机后部的患者的吸气努力用深圈点表示。)
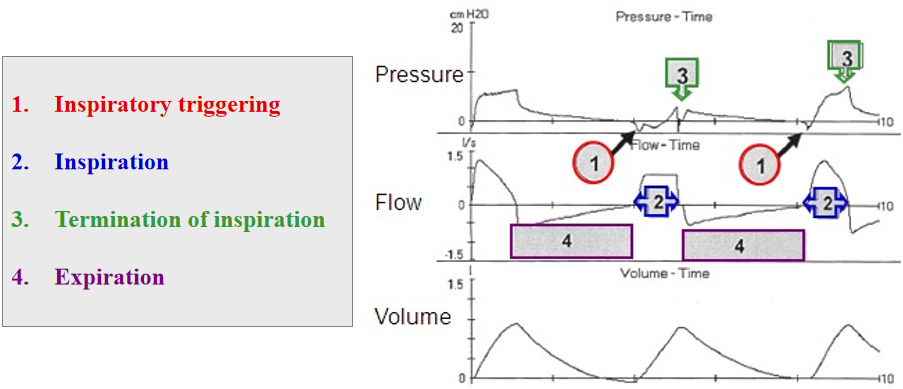
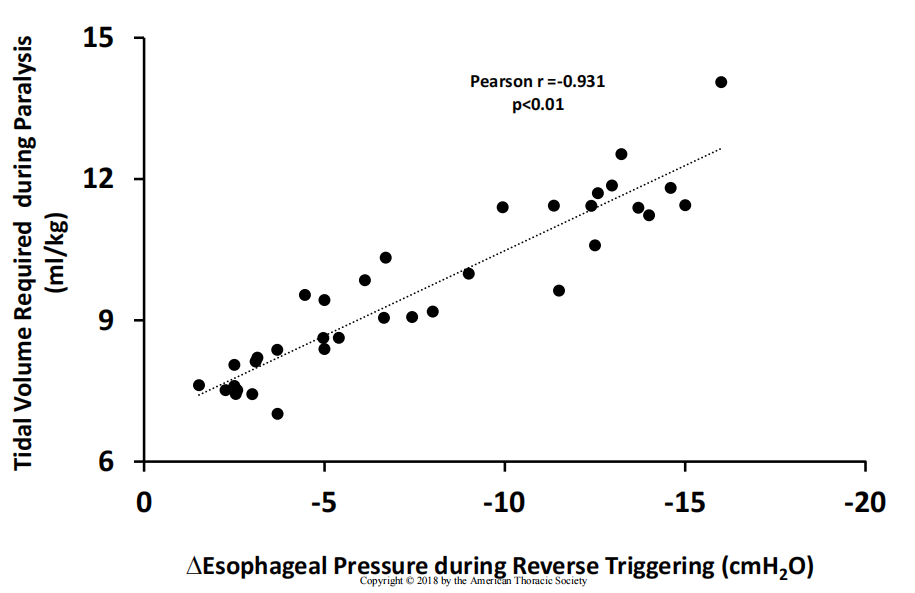
研究结果显示:50名受试者在记录过程中至少检测到一个单一反向触发事件,不同步率为4.8(0.3-14.3)次/min或占控制呼吸频率的17.7%(0.95-49.5)。无呼吸叠加的RT和有呼吸叠加的RT分别为4(0 - 12)次/分钟和0(0 - 1.5)次/分钟,无呼吸叠加的RT占97.3%(80.5-100),最常见的夹带比例为1:2和1:1。
这项研究还观察到RT与较低的潮气量(VT)(P= 0.019)和较低的芬太尼输注率(P= 0.018)独立相关,较低的VT和阿片类药物剂量增加了发生RT的可能性;另外,ARDS严重程度越大(p= 0.08),pH值越高(p= 0.053),APACHEII评分越低(p= 0.052),发生RT的可能性越高;还有,早期RT的存在与MV的终止时间无关,在对已知预测因子进行调整后,可能与降低90天住院死亡率有关,这种推测可能意味着RT对患者自主呼吸的几率增加可能是「有益」的。

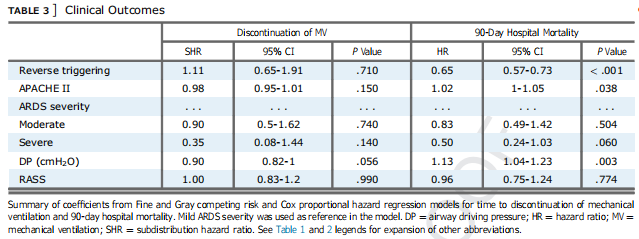
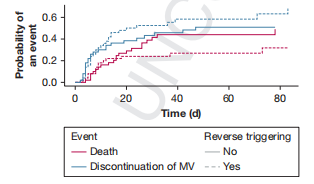
这篇也是2021年的文章,发表在《Am J Respir Crit Care Med》上:


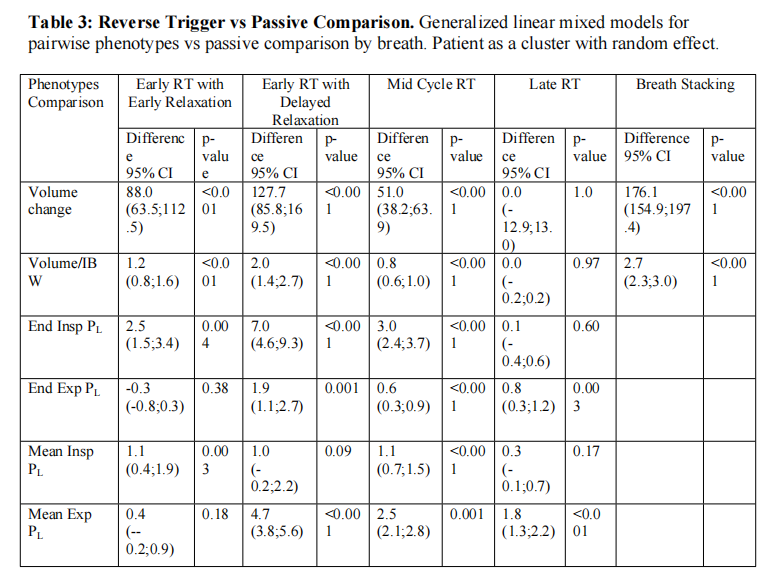
该研究共收集了55例应用压力调节容量控易通气(PRVC)模式的ARDS患者呼吸机波形资料,探讨四种RT表型伴或不伴呼吸叠加,及对患者吸气相和呼气相的影响。
由每个患者平均7.0 (4.5-8.5)分钟组成,共384.7分钟和10266次呼吸;在25名患者(45%)的1240次总呼吸(12.1%)中发现RT和呼吸叠加事件,在15名患者(27%)的160次总呼吸中发生了带有呼吸叠加的RT。中期RT是最常见的表型,RT频率变化很大。RT发生伴有吸气驱动的增加(平均4-10cmH2O)。
发现前期RT增加潮气量【88(64-113)ml】、吸气未跨肺压【3 (2-3)cmH2O】;前期RT伴延迟呼气的患者潮气量增加【128(86- 170)ml】、分别增加吸气末和平均呼气末跨肺压【7(5-9)cmH2O、5 ( 4-6)cmH2O];中段RT(始于吸气相、但最大吸气努力在呼气相)增加潮气量【51(38-64〕ml】,分别增加吸气未和平均呼气末跨肺压3(2-4)cmH2O、3(2-3) cmH2O】 ,同时伴有呼气不全;后期RT(呼气相出现)增加平均呼气跨肺压【2(1-2)cmH2O】、且导致呼吸不全。呼气叠加可导致潮气量增加【176(155-197)ml】。
四、反向触发与肺损伤
反向触发对于肺或膈肌损伤风险较低的患者而言,在某种程度上的允许性不同步可能是良性的,甚至是有益的。首先,反向触发的自主呼吸可增加患者的肌肉活动;其次,呼气期间主动收缩或延迟放松的反向触发可能会增加平均呼气压力并阻止完全呼气,从而起到微小肺复张的作用。
但是,反向触发也容易导致肺损伤的发生,主要机制可能与反向触发导致的呼吸叠加不同步而致过大的潮气量和过大的跨肺压有关,也可能与吸气努力过强时导致气体在不同肺区域移动造成的剪切力(钟摆效应)损伤相关。

五、如何处理反向触发?
1、镇静镇痛:
阿片类药物可影响呼吸中枢,镇静剂与阿片类药物联合使用可为接受机械通气的患者提供舒适感,控制疼病和呼吸困难,此有助于改善患者与呼吸机的相互作用。对于普通人机不同步,可使用镇静和镇痛来治疗,但深度镇静与更长的机械通气时间和ICU停留时间相关,是无效吸气努力的独立危险因素,所以也是有利有弊的。
有研究报道,当异步率高的患者中增加镇静时,呼吸叠加频率从41%下降到27%,也有人报道,当镇静被中断时,呼吸叠加率增加。
反向触发可触发高气道压力警报,通常情况下促使增加临床镇静水平,或者调整呼吸机。在急性呼吸窘迫综合征治疗的早期阶段,增加镇静和/或使用NMBA可能是优选的选择。
2、呼吸机设置方面:
反向触发源自呼吸夹带,所以修改夹带模式可以限制反向触发。
在理论上,修改夹带频率,也可影响分钟通气和二氧化碳水平,进而影响呼吸驱动,推测反向触发频率也与呼吸频率有关。
改变呼吸机上的呼吸频率会改变夹带特性或消除夹带,所以,增加强制呼吸频率可以消除患者的神经努力并破坏呼吸带动,还有,降低强制呼吸频率可能会导致患者在机械充气之前开始努力,也可有效地消除了夹带。
3、其他:
因为流量和压力输送控制不同,患者对呼吸机的响应不同,包括容量控制、PRVC、压力控制在内的其他呼吸机模式的影响也需要进一步研究,而反向触发的其他影响因素需要进一步探索。反向触发模式随时间推移的持久性以及整个患者群体的普遍性也不确定。
最后小结一下
机械通气过程中反向触发是一种未被我们充分认识的人机不同步,它可引起二次触发、呼吸叠加导致潮气量及跨肺压增加,可能加重呼吸机相关肺损伤。但一定程度上,反向触发也是有益的。反向触发的自主呼吸可增加患者的肌肉活动,其次呼气期间主动收缩或延迟放松的反向触发可能会增加平均呼气压力并阻止完全呼气,可以起到微小肺复张的作用。
关于反向触发,还需更多的临床识别、处理和研究,请各位专家批评指正。
参考文献
[1]Jeremy RB, Atul M, Taylor TB. Ventilator-induced lung injury. Clin Chest Med, 2016, 37(4): 633-646.
[2]Arthur SS, Marco RV. Ventilator-induced lung injury. N Engl J Med, 2013, 369(22): 2126-2136.
[3]Laurence V, Frédéric V, Jean R, et al. Patient-ventilator asynchrony during non-invasive ventilation for acute respiratory failure: a multicenter study. Intensive Care Med, 2009, 35(5): 840-846.
[4]Evangelia A, Aissam L, Nathalie R, et al. Mechanical ventilation-induced reverse-triggered breaths: a frequently unrecognized form of neuromechanical coupling. Chest, 2013, 143(4): 927-938.
[5]Pablo OR, Norberto T, Sebastián F, et al. Prevalence of reverse triggering in early ARDS: results from a multicenter observational study. Chest, 2021, 159(1): 186-195.
[6]Jose D, Michele B, Ewan CG. Monitoring patient-ventilator interaction by an end-expiratory occlusion maneuver. Intensive Care Med, 2020, 46(12): 2338-2341.
专家简介

罗红
教授,主任医师,博士生导师,中南大学湘雅二医院呼吸与危重症医学科主任,呼吸重症亚专科主任。中华医学会呼吸病学分会呼吸危重症学组委员、中国医师协会呼吸医师分会委员、中国医师协会呼吸医师分会危重症医学工作委员会副主任委员、中国残疾人康复协会肺康复专委会常委兼ICU肺康复学组副组长,湖南省医师协会呼吸医师分会会长,湖南省医学会呼吸康复委员会副主任委员。
本文由《呼吸界》编辑 Jerry 整理、排版


