慢性阻塞性肺疾病(慢阻肺病)全球创议(global initiative for chronic obstructive lung disease,GOLD)GOLD 2025是GOLD 2023的第二次更新,新增2023年 1月至2024年7月的164篇参考文献,在2024年11月11日发布。总体来说,GOLD 2025共分为五个章节,包括第一章定义和概述、第二章诊断和评估、第三章慢阻肺病的预防和管理、第四章慢阻肺病急性加重的管理以及第五章慢阻肺病合并症,同时删除原GOLD 2024的第六章(COVID-19与慢阻肺病)。GOLD 2025新增3张图片(图2.6 吸入支气管舒张剂前/后的肺功能检查;图3.22 当前使用LABA+ICS患者的管理;图5.1慢阻肺病合并肺动脉高压患者的可治疗特质及管理建议),并修改和更新了5张图片(图3.6 稳定期慢阻肺病患者的接种疫苗根据最新指南进行了更新;图3.9 随访期药物治疗中增加了恩塞芬汀和度普利尤单抗等相关内容;图4.11 降低慢阻肺病急性加重风险的措施中增加了度普利尤单抗;更新图3.18 慢阻肺病的维持期药物治疗;更新图4.2 慢阻肺病急性加重的诊断和评估)。
重要的内容变化之处在于修订和增加了以下12个方面:(1)增加有关肺功能变化轨迹的说明和参考文献,包括使用ERS网站上的免费软件来可视化肺功能变化;(2)增加有关微生态失衡的内容;(3)更新并扩充肺功能检查的内容;(4)更新慢阻肺病患者的心血管病风险;(5)更新慢阻肺病CT影像学检查,包括肺气肿、肺结节、气道以及慢阻肺病相关合并症等内容;(6)新增气候变化与慢阻肺病;(7)对慢阻肺病患者的推荐疫苗进行更新,与目前美国CDC的指南保持一致;(8)更新随访期治疗药物以及相应的图3.9以增加恩塞芬汀和度普利尤单抗等相关内容;(9)新增肺康复治疗的线上、线下及远程随访;(10)修订有关LABA+ICS患者停用ICS的说明,同时新增图3.22说明当前使用LABA+ICS患者的管理;(11)修订有关PDE3&PDE4抑制剂和其他减少急性加重药物的说明以反映最新有关恩塞芬汀和度普利尤单抗的证据;(12)新增肺动脉高压的内容,并使用图5.1加以说明。
本文介绍GOLD 2025关键点及更新要点。
第一章 慢阻肺病定义和概述
关键点
定义
•慢阻肺病是一种异质性疾病,其特征为慢性呼吸道症状(呼吸困难、咳嗽、咳痰、急性加重),这是由于气道(支气管炎、细支气管炎)和/或肺泡异常(肺气肿)所致,引起持续进行性加重的气流受限。
病因和危险因素
•分为遗传基因(G)-环境因素(E)-全生命期事件(T) (GETomics) ,造成肺组织破坏,改变肺正常发育或衰老过程。
•慢阻肺病的主要环境暴露因素是烟草烟雾、吸入室内外空气污染有毒颗粒和气体,但其他环境和宿主因素(包括肺发育异常和加速衰老)也可以促进发生。
•慢阻肺病最相关(但罕见)的遗传因素是SERPINA1基因突变导致1抗胰蛋白酶缺乏,其它基因突变与肺功能下降和慢阻肺病发生风险相关,但其相应的效应值较小。
诊断标准
•根据慢阻肺病定义、危险因素,肺量计检查吸入支气管舒张剂后FEV1/FVC<0.7提示存在不完全可逆的气流阻塞即确诊慢阻肺病。
•有些患者可能有呼吸系统症状和/或肺结构破坏(肺气肿)和/或生理异常(如FEV1下降、气体陷闭、过度充气、弥散功能下降、和/或FEV1快速下降)但不存在气流阻塞(吸入支气管舒张剂后FEV1/FVC≥0.7)。这些患者归属于“慢阻肺病前期”。保留比值的肺量计异常‘PRISm’用于筛选比值正常但肺通气功能异常的患者。这两部分人群是发生气流阻塞的高危人群,但并不是所有的患者都会发生气流阻塞。
临床表现
•慢阻肺病典型症状为呼吸困难、活动受限,和/或咳嗽伴或不伴有咳痰,可伴有呼吸症状的急性恶化,称为慢阻肺病急性加重,需要给予预防与治疗策略。
•慢阻肺病患者常存在其它共患病,影响疾病状态和预后,并需要针对性治疗。共患病与急性加重表现类似,并会加重急性加重发生。
新机遇
•慢阻肺病是常见的可防可治的疾病,但存在严重的漏诊和误诊,导致未治疗或不恰当治疗。早期正确诊断慢阻肺病具有重要的公共卫生意义。
•生命早期暴露包括烟草烟雾在内的其他环境因素会导致慢阻肺病,并影响青年人慢阻肺病的发生发展,关注慢阻肺病前期和PRISm有助于疾病预防、早期诊断并给予迅速恰当的干预治疗。
更新要点
1.肺功能轨迹:发育和衰老
正常人肺的生长和成熟延续至20-25岁(女性更早),此时肺功能达到巅峰。随后是较短的平台期,最后是由于肺生理性衰老导致的轻度肺功能下降阶段。这种正常肺功能轨迹可由于妊娠期、出生期、儿童期和青春期发生的影响肺生长(继而影响肺功能峰值)的病程,和/或缩短平台期和/或加速衰老期(继而随着年龄的增长,肺功能下降的正常速率加快)的病程发生改变。因此,不同个体在其一生中可能遵循不同的肺功能变化轨迹,既可能低于也可能高于正常轨迹。目前已充分证实,高于正常轨迹的个体更有可能实现健康老龄化,而低于正常轨迹的个体则患有呼吸、心血管及代谢疾病的风险增高,且早逝的几率更大。从这个角度来看,肺功能检查可以视为整体健康的标志。欧洲呼吸学会网站(gli-calculator.ersnet.org/lung_tracker/)现已提供免费下载软件,用户可利用该软件长期可视化和监测肺功能改变。
2.微生态失衡
已有研究发现慢阻肺病患者的多个部位(包括气道)中存在微生物群平衡的破坏,亦即微生态失衡。诸如吸烟和早产等不同的慢阻肺病风险因素会影响黏膜免疫,进而改变肠道和气道的微生物群。两者通过免疫互作以及微生物代谢物和多肽等相互作用,形成所谓的“肠-肺轴”。微生态失衡与慢阻肺病的发生以及急性加重等疾病特征相关,可能是通过破坏黏膜防御(形成恶性循环)及诱导免疫反应从而刺激肺部炎症。在病毒感染后和急性加重期间,慢阻肺病微生物群特征会发生变化,且抗生素、口服或吸入性糖皮质激素的使用会引发不同的改变。总体来看,微生态失衡可能在慢阻肺病的发生发展中起到一定作用,但目前纵向数据和干预性研究仍较少,需进一步研究以明确因果关系,并探索其在预后、诊断或治疗中的潜在应用。
第二章 慢阻肺病诊断和评估
关键点
•存在呼吸困难、慢性咳嗽或咳痰,有复发性下呼吸道感染史和/或有接触该疾病危险因素史的患者均应考虑慢阻肺病。肺功能检查是确诊慢阻肺病的必备条件。如吸入支气管舒张剂后一秒率(forced expiratory volume in one second/forced vital capacity,FEV1/FVC)<0.70,可确定存在持续气流阻塞。
•慢阻肺病评估的目标在于确定气流阻塞程度、疾病对患者健康状况的影响和远期不良风险(如慢阻肺病急性加重、住院或死亡),从而用以指导治疗。
•经初始治疗仍有持续症状的慢阻肺病患者应该进一步评估,包括测定肺容积、弥散功能、运动试验和/或胸部影像。
•慢阻肺病患者常合并心血管疾病、骨骼肌功能障碍、代谢综合征、骨质疏松、抑郁、焦虑、肺癌等多种慢性病(合并症)。对慢阻肺病患者均应积极寻找合并症,并给予正确治疗,因为它们独立于慢阻肺病所致气流阻塞的严重程度而影响健康状况、住院和死亡率。
更新要点
1.肺功能检查更新
GOLD 2025更新了肺功能检查的信息,目录中增加了新的小节“吸入支气管舒张剂前/后的肺功能检查”、“定义气流阻塞的肺功能检查标准”、“肺功能参考值的解释”、“气流阻塞严重程度分期”和“COVID-19”,并增加了更多关于LLN值、Z值和参考值的信息。
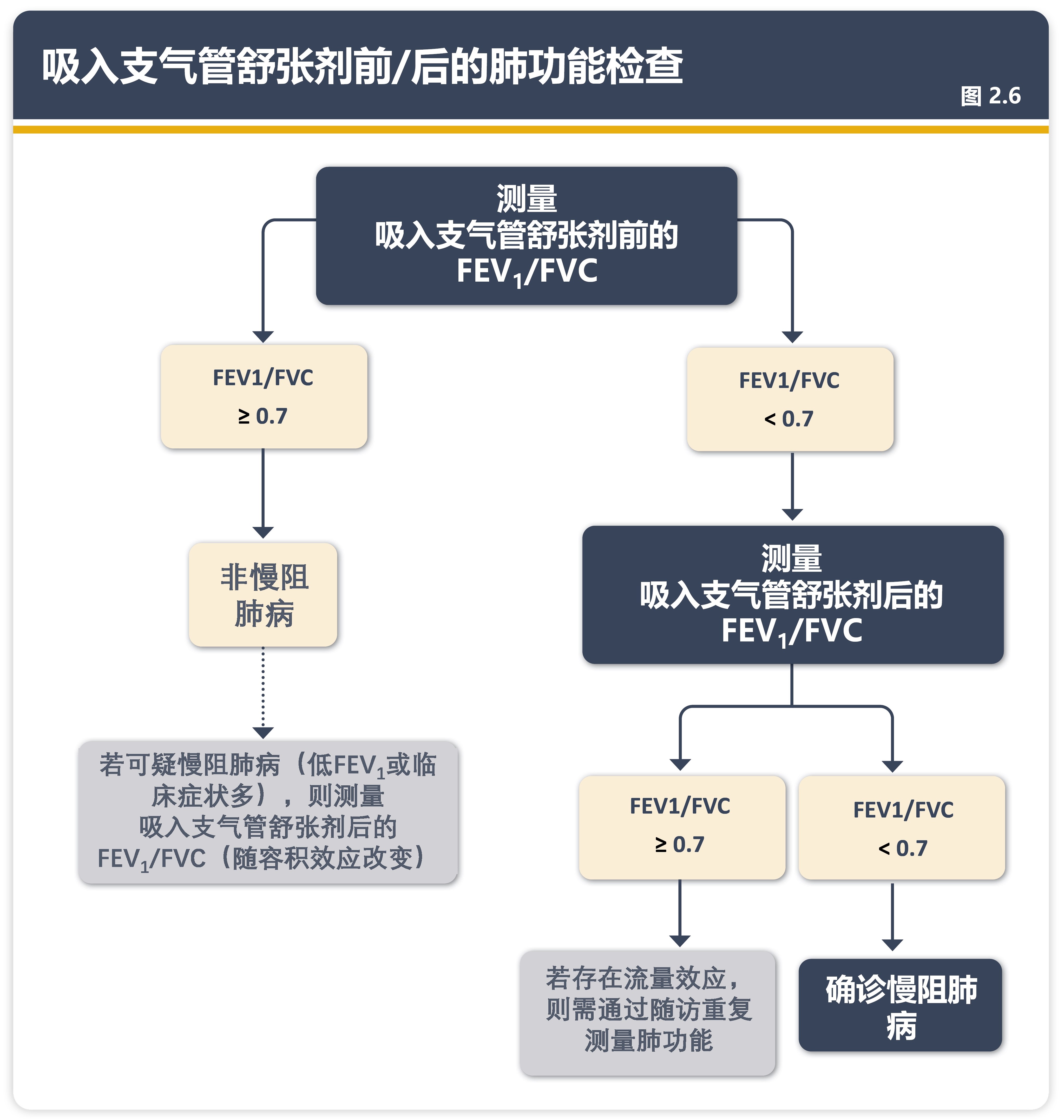
GOLD 2025增加了新的图2.6用以说明吸入支气管舒张剂前/后的肺功能检查流程。吸入支气管舒张剂前的肺功能检查可以用于初步评估有临床表现的患者是否存在气流阻塞。如果吸入支气管舒张剂前肺功能结果未显示气流阻塞(FEV1/FVC≥0.7),则无需进行吸入支气管舒张剂后的肺功能检查,除非该患者在临床上高度怀疑慢阻肺病,如低FEV1或临床症状多。这类患者建议行支气管舒张试验,其FEV1/FVC结果可能因容积效应而发生变化(FEV1/FVC <0.7),并需要进一步对病因进行调查和随访,包括重复的肺功能检查。如果使用支气管舒张剂前的肺功能结果已经显示有气流受限,则应使用吸入支气管舒张剂后的测定值来诊断慢阻肺病。吸入支气管舒张剂前FEV1/FVC<0.7而吸入支气管舒张剂后FEV1/FVC≥0.7的个体未来进展为慢阻肺病的风险很大,尤其对于吸入支气管舒张剂后FEV1/FVC在0.6-0.8的患者,未来可能发生持续的吸入支气管舒张剂后FEV1/FVC<0.7。当患者存在上述情况或有慢阻肺病危险因素的时候应密切随访并进行重复评估。
与GOLD 2024相比,GOLD 2025强调了使用Z值(观察值和测量均值之差与标准差的比值)是使用LLN值的一种等效方法。LLN值基于正态分布,并将底部5%的人群归类为异常。Z值为−1.645,相当于第5个百分位数。从科学或临床的角度来看,很难确定这些标准中的哪一项将提供最佳的慢阻肺病诊断准确性。全球肺功能创议(Global Lung Initiative,GLI)比较了使用Z值和使用固定比值解读肺功能测定结果的差异,同LLN一样,发现它们对部分患者的分类并不一致,但这是否具有临床意义仍不确定。
2.慢阻肺病心血管风险
GOLD 2025在初始评估部分增加了慢阻肺病心血管风险这一小节,分为慢阻肺病稳定期和急性加重期两部分介绍。临床稳定期慢阻肺病患者心血管疾病(cardiovascular diseases, CVD)发病率较高,包括高血压、冠心病、心衰和心律失常等,是慢阻肺病患者的主要死因。慢阻肺病和CVD的共存机制复杂,包括两者具有共同的危险因素(如衰老、吸烟),而慢阻肺病引起的持续性全身炎症、肺换气异常、肺过度充气以及劳力性呼吸困难会导致CVD的发生。此外,CVD也可能通过多种潜在机制导致慢阻肺病患者健康状况恶化,包括由于心肌收缩力异常引起的肺泡和支气管水肿、毛细血管后肺动脉高压以及骨骼肌氧输送减少导致的患者体力活动减少。因此需要对慢阻肺病患者是否存在重大CVD进行检查并治疗。GOLD 2025强调,在普通人群中使用现有的心血管风险评分,如Framingham或QRisk,可能会低估慢阻肺病患者的CVD风险。另外,肺功能指标(如FEV1)的纳入可能会增加标准心血管风险评分的预测价值,这些都值得进一步研究。在急性加重部分,GOLD 2025主要介绍了在慢阻肺病急性加重(Exacerbations of COPD, ECOPD)发作期间和之后,心肌梗死、心律失常和卒中等急性心血管事件的风险进一步增加,而且这种风险在出院后的最初几周仍然很高,甚至在一年后仍然显著增加。
3.CT评估内容
GOLD 2025将原影像学检查的CT段落细分为4小部分,更加细致地介绍了CT在慢阻肺病评估中的作用。GOLD 2025指出,肺低衰减区域百分比(定义为密度≤-950 Hounsfield单位的像素百分比)是CT上客观量化肺气肿的最常用方法。CT所反映的肺气肿与气流阻塞等肺部病理生理学指标所反应的肺气肿相关,也与症状、急性加重、肺癌风险、疾病进展和死亡风险的增加相关。此外,GOLD 2025新增了美国癌症协会的建议,即年龄在50-80岁之间、有20包年吸烟史的个人,无论戒烟多少年,都应考虑通过CT来筛查肺癌。与慢阻肺病相关的其他CT特征还包括气道异常。约30%的慢阻肺病患者CT可见支气管扩张。GOLD 2025补充了气道黏液栓也可在CT上显示并计数,从而创建黏液栓评分。胸部CT还可提供更多慢阻肺病合并症的信息,包括冠状动脉钙化、肺动脉扩张、骨密度、肌肉量、肺间质异常、食管裂孔疝和肝脏脂肪变性等。总之,对于存在持续急性加重、症状与肺功能结果不成比例、FEV1占预计值%<45%且伴有显著过度充气、或者符合肺癌筛查标准的患者,均应考虑胸部CT影像检查。
第三章 慢阻肺病预防和管理
关键点
•应大力鼓励和支持所有吸烟者戒烟。尼古丁替代治疗和药物治疗可有效提高长期戒烟率。由医疗专业人员提供的立法禁烟和咨询提高戒烟率。目前尚无证据支持电子烟作为戒烟辅助手段的有效性和安全性。
•主要治疗目标是减轻症状和降低未来急性加重的风险。慢阻肺病稳定期的管理策略主要基于症状评估和急性加重病史。
•药物治疗可减轻慢阻肺病症状,降低急性加重的频率和严重程度,并改善健康状况和运动耐量。数据显示,药物治疗有助于改善肺功能下降率、降低死亡率。
•每种药物治疗方案均应个体化,并根据症状的严重程度、急性加重风险、副作用、合并症、药物可及性和成本以及患者的反应、偏好和使用各种给药装置的能力进行指导。
•需要定期评估吸入装置使用技术。
•COVID-19疫苗对预防SARS-CoV-2感染非常有效,慢阻肺病患者应按照国家建议接种COVID-19疫苗。
•接种流感疫苗和肺炎球菌疫苗可降低下呼吸道感染的发病率。
•CDC建议:对于青春期未接种Tdap疫苗(dTaP/dTPa;百日咳、破伤风和白喉)的慢阻肺病患者,接种 Tdap 疫苗;所有慢阻肺病患者应常规接种带状疱疹疫苗;新型呼吸道合胞病毒(RSV)疫苗,适用于60岁以上和/或患有慢性心脏病或肺病的个体。
•肺康复治疗及其核心组分,包括与特定疾病教育相结合的运动训练,可以改善各个严重程度的慢阻肺病的运动能力、症状和生活质量。
•对于重度静息慢性低氧血症(PaO2≤55 mmHg或<60mmHg且有肺心病或继发性红细胞增多症)的患者,长期氧疗可提高生存率。
•对于静息或运动诱发的中度血氧饱和度降低的稳定期慢阻肺病患者,不应常规进行长期氧疗。然而,在评估患者是否需要补充氧疗时,必须考虑患者的个体因素。
•对于存在重度慢性高碳酸血症和急性呼吸衰竭住院史的患者,长期无创通气可能可以降低死亡率并预防再次住院。
•对于经优化的药物治疗仍无法治愈的晚期肺气肿患者,手术或支气管镜介入治疗可能有益。
•姑息疗法可有效控制晚期慢阻肺病患者的症状。
更新要点
1.气候变化与慢阻肺病
气候变化会导致极端天气事件频发,如高温、严寒、雷暴、沙尘暴等,对全球各地的死亡率均有显著影响。人群研究的结果显示,慢阻肺病患者因暴露于高温和寒冷而面临更高的死亡风险,其中寒冷导致的死亡风险高于高温。除了对死亡率的影响外,较高的室外温度与慢阻肺病患者住院风险增加相关,而较低的室外温度与急性加重风险增加相关。在个体水平对慢阻肺病患者的肺功能、症状与空气温度之间的关系进行的研究表明,室外温度较高与呼吸困难增加相关。室内温度较高与症状增多和SABA使用增加相关。室内和室外温度较低则与咳嗽和咳痰增加、SABA使用增加以及FEV1下降相关。在秋季、冬季和春季(平均室外最低温度为2.9℃,最高温度为10.1℃)室内温度≥21℃至少9小时的条件下,患者的健康状况较好。
气候变化对空气质量也有重大影响。臭氧水平与温度密切相关,因为它的产生取决于高温和阳光;而空气污染物的产生和扩散可能受到当地风、太阳辐射和降水模式的影响,特别是在城市地区。几项研究观察了空气污染和温度对慢阻肺病患者的交互影响。高温和空气污染对一般人群的死亡率和住院率具有协同效应。在寒冷情况或冬季,污染物对慢阻肺病患者住院和急诊的影响更大。包括PM2.5、NO2和臭氧在内的室外空气污染物不会加重室外温度对症状的影响,但较高的室内PM2.5和NO2浓度会放大较高的室内温度对症状带来的有害影响。目前关于温度和污染物对慢阻肺病患者症状和急性加重的相互作用的研究结果相互矛盾,这可能在一定程度上反映了影响暴露的行为差异,如避免外出、开窗和使用空调。慢阻肺病患者应根据世界卫生组织的建议,在寒冷天气保持室内温度高于18℃,在高温期间保持室内温度低于32℃,以减少不良健康影响。
2.疫苗接种
GOLD 2025根据最新CDC疫苗接种推荐指南对此部分进行更新,新增有关肺炎球菌疫苗的说明(PCV20覆盖了58%的菌株,而PCV21覆盖了84%的成人侵袭性菌株)。关于呼吸道合胞病毒(RSV)疫苗,新增相关流行病学证据,指出RSV感染与慢阻肺病急性加重相关。此外,增加说明COVID-19疫苗对需要住院、入住ICU或急诊科或急诊就诊的SARS-CoV-2感染非常有效,包括慢性呼吸系统疾病患者。
3.随访期药物治疗
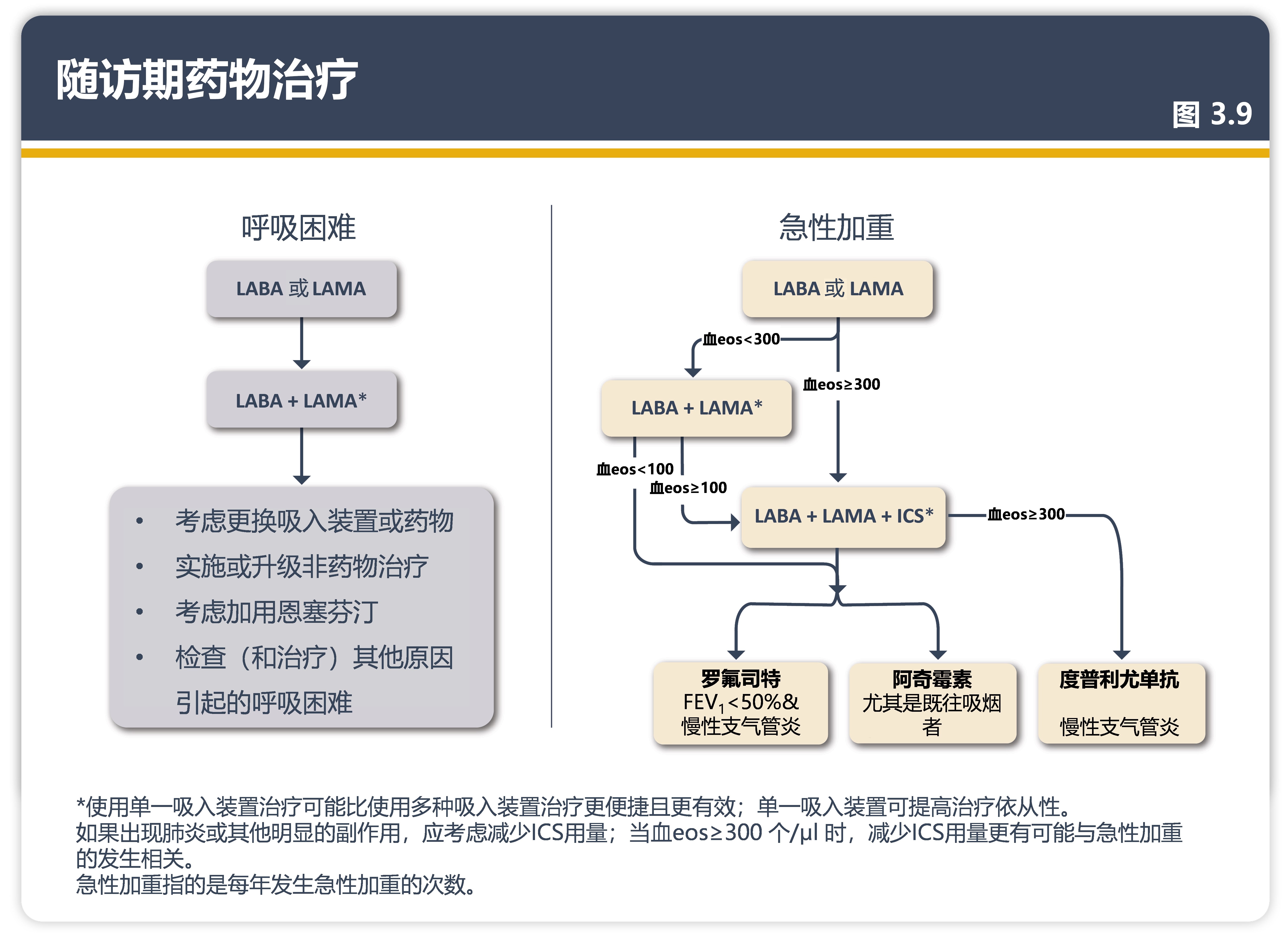
无论慢阻肺病患者初始治疗时的GOLD分期如何,随访期药物治疗方案可应用于任何已接受维持治疗的患者。如果初始治疗有效,则维持初始治疗方案。如果初始治疗无效,对于正在接受支气管舒张剂单药治疗的持续性呼吸困难或运动受限的患者,建议使用两种长效支气管舒张剂;如果加入第二种长效支气管舒张剂仍无法改善症状,建议考虑添加恩塞芬汀(如有)。如果患者接受LABA+LAMA+ICS治疗(或血嗜酸性粒细胞计数<100个/μL的患者)仍出现急性加重,对于其中血嗜酸性粒细胞≥300个/µl且有慢性支气管炎症状的患者可考虑加用度普利尤单抗。
4.肺康复治疗、教育和自我管理
目前研究最多的慢阻肺病远程医疗模式是肺康复和自我管理干预。肺康复是慢阻肺病远程医疗领域中研究质量最高的。一份临床实践指南报道,远程康复可以达到与面对面、中心肺康复相似的临床结局。建议为稳定期慢性呼吸系统疾病(尤其是慢阻肺病)的成人提供基于中心的肺康复或远程康复的选择。自我管理干预既改善了生活质量,又减少了住院次数。使用信息通信技术的远程教育和自我管理有可能缓解卫生从业者的工作压力,并改变了患者健康监测和为其提供医疗保健的方式。尽管目前在自我管理方面取得了许多进展,但使用数字技术进行远程自我管理仍存在许多尚未解决的问题和局限性。
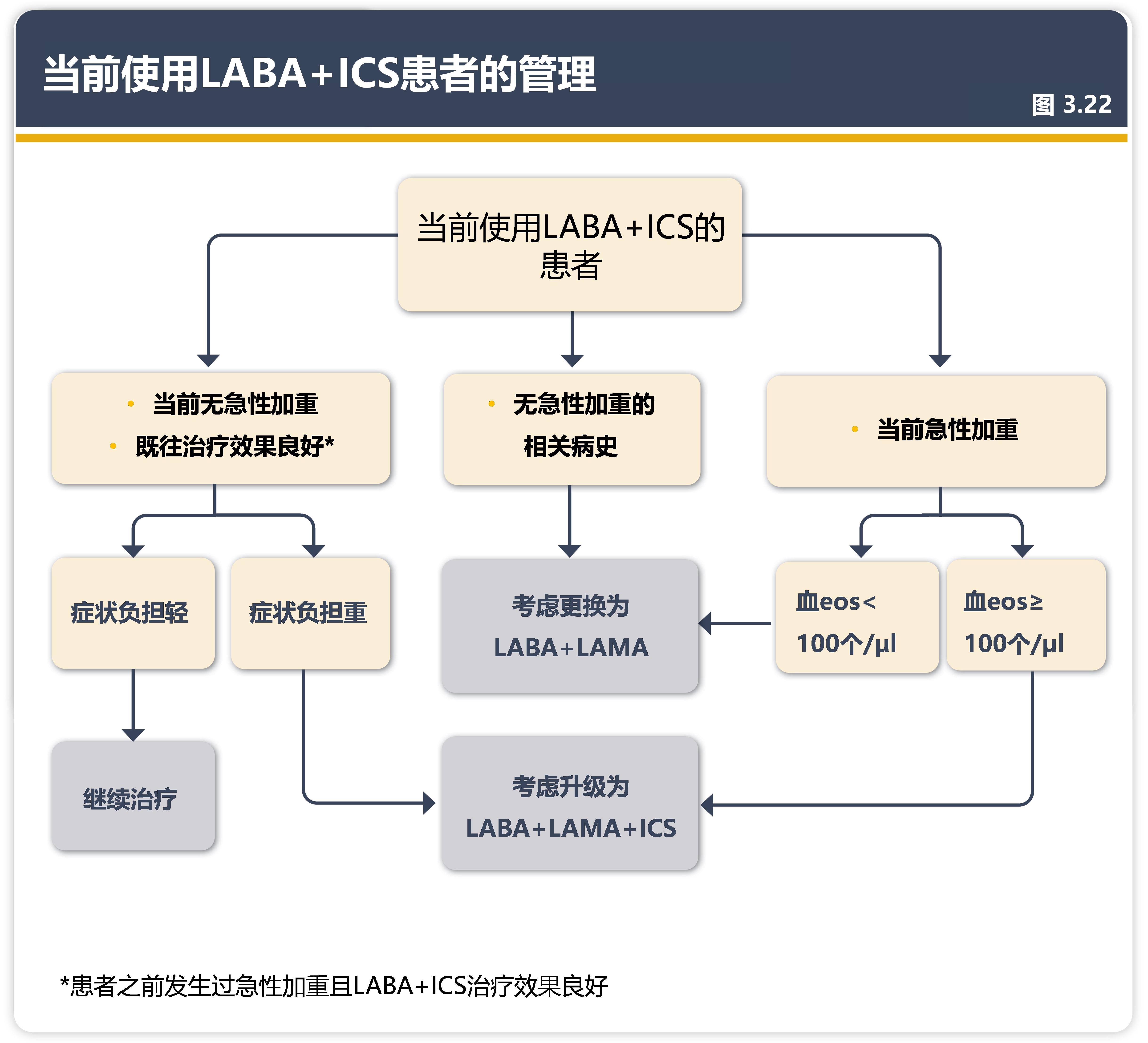
5.LABA+ICS患者停用ICS
在接受LABA+ICS治疗的患者中,停用ICS对肺功能、症状和/或急性加重的风险没有影响。最近的大型观察性队列对于停用ICS是否会对三联用药患者产生影响颇有争议。两项研究表明,停用ICS并未导致肺功能恶化或急性加重。另一方面,来自于西班牙的回顾性数据表明,停用ICS与急性加重、医疗资源利用和成本增加相关。这些差异可能源于分析方法的不同,例如混杂因素的存在。对于合并重症肺炎或真菌、分枝杆菌感染风险高的慢阻肺病患者,应考虑停用ICS,以降低其他感染的风险。血嗜酸性粒细胞计数≥300个/µl是停用ICS后不良后果风险增加的指标。
6.恩塞芬汀与度普利尤单抗
恩塞芬汀是一种新型的、第一种吸入型PDE3和PDE4双重抑制剂,具有抗炎活性和支气管扩张作用。抑制PDE3可通过调节环鸟苷酸水平引起平滑肌舒张。在平行对照3期临床试验中,通过标准雾化器给药的恩塞芬汀显著改善了肺功能和呼吸困难,但对生活质量的影响不一致。此外,这些研究的设计目的并非评估在LABA+LAMA或LABA+LAMA+ICS基础上加用恩塞芬汀的影响,因此难以在治疗方案中完全确定该药物的作用。研究未发现安全性或耐受性问题。恩塞芬汀目前只在美国上市。
度普利尤单抗是一种完全人源性单克隆抗体,可阻断白介素-4和白介素-13的共享受体成分。在两项大型、3期、双盲、随机试验中,在接受LABA+LAMA+ICS治疗的慢阻肺病、慢性支气管炎、在过去一年内有≥2次中度急性加重或≥1次重度急性加重病史以及血嗜酸性粒细胞计数≥300个/µL的患者中,接受度普利尤单抗治疗的患者在52周内,急性加重的发作更少,肺功能更好,健康状况发生显著改善。
第四章 慢阻肺病急性加重的管理
关键点
•慢阻肺病急性加重定义为14天内以呼吸困难和/或咳嗽和咳痰加重为特征的事件。慢阻肺病急性加重通常与气道感染、空气污染或其他肺部损伤引起的局部和全身炎症增加相关。
•由于这些症状并非慢阻肺病的特异性症状,应考虑相关的鉴别诊断,尤其是肺炎、充血性心力衰竭和肺栓塞。
•治疗慢阻肺病急性加重的目标是尽量降低当前急性加重的负面影响,并预防后续事件的发生。
•单用短效β2受体激动剂,联用或不联用短效抗胆碱能药物,推荐为急性加重的初始治疗。
•应尽快启用长效支气管舒张剂维持治疗。在频繁急性加重和血嗜酸性粒细胞水平升高的患者中,应考虑在双联支气管舒张剂方案基础上加用吸入性糖皮质激素。
•对重度急性加重的患者,全身性糖皮质激素可改善肺功能(FEV1)和氧合并缩短恢复时间(包括住院时间)。治疗持续时间通常不应超过5天。
•当存在指征时,可使用抗生素缩短恢复时间、降低早期复发风险、减少治疗失败和缩短住院持续时间。治疗持续时间应为5天。
•不建议使用甲基黄嘌呤,因为这会增加副作用风险。
•无创机械通气是慢阻肺病急性呼吸衰竭无绝对禁忌证患者的首选通气方式,因其可以改善气体交换,减少呼吸功和插管,缩短住院天数,提高生存率。
•急性加重的恢复时间会有差异,通常需要4-6周,一些患者无法恢复至急性加重前的功能状态。发生一次急性加重后,应开始采取适当措施预防急性加重。
更新要点
与GOLD 2024相比,GOLD 2025修订并更新了图4.11 降低慢阻肺病急性加重风险的措施和图4.2 慢阻肺病急性加重的诊断和评估,并在慢阻肺病急性加重的心肺风险及全身性糖皮质激素治疗中增添了几项研究。

第五章 慢阻肺病合并症
关键点
• 慢阻肺病常合并其他疾病,对预后有显著影响。
• 总体来说,合并症的存在不应改变慢阻肺病的治疗方案,并且合并症应按照常规标准进行治疗,与慢阻肺病的存在无关。
• 心血管疾病是慢阻肺病常见且重要的合并症。
• 肺癌在慢阻肺病患者中很常见,并且是导致死亡的主要原因。
• 根据对一般人群的建议,每年应对因吸烟导致慢阻肺病的人群进行一次低剂量CT扫描(LDCT)筛查肺癌。
• 由于暂无充足的数据确定获益大于危害,因此不建议每年对非吸烟导致慢阻肺病的人群进行LDCT来筛查肺癌。
• 骨质疏松和抑郁/焦虑是慢阻肺病常见的重要合并症,常被漏诊,并与不良的健康状况和预后相关。
• 胃食管反流(GERD)与慢阻肺病急性加重风险增加和健康状况差有关。
• 慢阻肺病患者出现新的或加重的呼吸道症状,发热和/或任何其他可能与COVID-19相关的症状,即使这些症状轻微,也应接受可能感染SARS-CoV-2或流感的检测。
• 当慢阻肺病是多种疾病治疗计划的一部分时,应注意确保治疗的简洁性,并尽量减少多药治疗。
更新要点
1.慢阻肺病合并肺动脉高压(PH-COPD)
在慢阻肺病合并症中,GOLD 2025新增有关肺动脉高压的说明。肺动脉高压(PH)定义为平均肺动脉压(mPAP)>20 mmHg,需通过右心导管检查进行评估。PH根据不同的病理生理机制、临床表现及治疗方式,分为五个不同的组别:动脉型肺动脉高压(PAH,第1组)、与左心疾病相关的PH(第2组)、与肺部疾病和/或低氧相关的PH(第3组)、慢性血栓栓塞性PH(CTEPH,第4组)以及机制不明和/或多因素引起的PH(第5组)。所有PH类型均可在慢阻肺病患者中发现并确诊。慢阻肺病患者通常伴有多种合并症和风险暴露因素,可能加重肺血管疾病的发生。因此,在慢阻肺病患者中诊断PH时,需要仔细分析导致mPAP升高的可能机制。这对于识别PH-COPD患者的可治疗特质至关重要。例如,CTEPH是一种在40岁以上患者中更为常见且可治疗的PH,并可能在慢阻肺病患者中被检测到。
轻度PH在慢阻肺病患者中很常见。据流行病学估计,25-30%的慢阻肺病患者表现为mPAP升高,这些患者大多数被归类为“第3组PH”或如果存在显著的左心疾病,则被归类为“第2组PH”。PH的存在与慢阻肺病的临床诊疗息息相关,因为PH会导致慢阻肺病患者医疗资源利用率增加、住院次数增多且预后不良。
PH-COPD患者的其中一个亚组表现出更为严重的PH,这在临床上尤为重要,因为PH可能是导致这些患者预后不良的主要因素。2022年ESC/ERS PH指南将重度PH-COPD定义为肺血管阻力(PVR)>5 WU。重度PH-COPD较为罕见,仅影响约5%的慢阻肺病患者。PH的严重程度是慢阻肺病预后的独立危险因素。患有重度PH-COPD的患者通常表现为轻中度气流受限、无或仅有轻微的高碳酸血症、DLco低于45%预测值,以及循环运动受限。对于这种慢阻肺病患者的表型,建议使用“肺血管表型”这一术语。
超声心动图是评估PH 及其严重程度的最佳无创工具。此外,NT-proBNP 升高以及 HRCT 上肺动脉和主动脉直径比值(PA:Ao 比值)增大提示可能存在PH-COPD。值得注意的是,肺动脉直径也与慢阻肺病急性加重的风险相关。PH-COPD患者应转诊至具有呼吸系统疾病治疗经验的PH 中心,接受右心导管检查和多学科评估,以指导治疗决策。建议对低氧血症患者进行长期氧疗。当慢阻肺病患者确诊PAH 时,其治疗应遵循2022年ESC/ERS 指南。对于这类患者,首选的治疗方案是初始单药治疗,如果达不到治疗目标,再进行谨慎的序贯联合治疗。当慢阻肺病患者确诊CTEPH时,需要多学科团队的评估来考虑是否需要进行肺动脉内膜切除术、血管成形术和/或 PH 药物治疗。非重度PH-COPD患者不建议使用PAH药物。对于重度PH-COPD患者,建议采用个体化治疗方法。在临床实践中,常使用磷酸二酯酶5抑制剂。然而,PERFECT 试验的结果显示,吸入曲前列环素并没有临床疗效且存在不良反应。因此,应鼓励进一步开展设计完善的随机对照试验,以便为在PH-COPD患者中使用或不使用 PAH 药物提供更为可靠的建议。

2.COVID-19和慢阻肺病
原GOLD 2024第六章节COVID-19与慢阻肺病迁移至GOLD 2025第五章节,并入慢阻肺病合并症范畴;远程患者随访的内容则迁移至第三章。
对于新发症状或原有呼吸道症状加重、发热和/或可能出现与COVID-19相关的其他任何症状(即使这些症状较轻)的慢阻肺病患者,应检测其是否可能感染SARS-CoV-2。这些患者应继续按照医嘱接受口服和吸入药物治疗慢阻肺病。保持物理距离并采取防护措施,或就地隔离,均不应导致这些患者被社会孤立和丧失活动能力。患者应通过远程通讯与朋友和家人保持联系,并继续保持积极心态,同时确保具有充足的药物。
COVID-19 感染症状与慢阻肺病的常见症状可能难以区分。超过 60% 的COVID-19患者发生咳嗽和呼吸困难,通常还伴有发热(>60%)以及疲劳、意识障碍、腹泻、恶心、呕吐、肌肉酸痛、嗅觉丧失、味觉障碍和头痛。在COVID-19患者中,最初的症状可能较轻,但肺功能可能会迅速恶化。症状较轻的前驱症状对于有潜在慢阻肺病的患者来说尤其棘手,因为他们的肺储备功能可能已经下降。缺乏对前驱症状的识别可能会延误早期诊断。数据表明,出现急性加重和疑似感染 COVID-19 的慢阻肺病患者很少评估前驱症状。对于出现急性加重症状(尤其是伴有发热、味觉或嗅觉受损或胃肠道不适)的慢阻肺病患者,始终要高度警惕COVID-19。
专家介绍
陈荣昌
广州医科大学附属第一医院 主任医师、二级教授、博士生导师;广医附一院广州呼吸健康研究院 前任院长;深圳市人民医院呼吸疾病研究所 特聘专家;中华医学会呼吸病学分会 前任主委;中华医学会呼吸病学分会慢阻肺学组 组长 ;中国医师协会呼吸病学分会 副会长;深圳市医学会呼吸病学分会 主委;国务院特殊津贴专家。
陈亚红
主任医师、教授、博士生导师,博士后合作导师;北京大学第三医院呼吸与危重症医学科副主任,北京大学医学部慢性气道疾病中心副主任,科研伦理综合办公室主任;专业特长:呼吸系统常见病及疑难危重症疾病;研究方向:气道慢性炎症疾病;中华医学会呼吸病学分会肺功能学组副组长;中国康复医学会呼吸康复专业委员会常委;北京慢性病防治与健康教育研究会呼吸病学专业委员会主任委员;中国抗癌协会肿瘤呼吸病学专业委员会常委;中华医学会呼吸病学分会慢阻肺学组委员;中国医师协会呼吸病分会慢阻肺工作委员会委员;中国基层呼吸疾病防治联盟副主席;中华结核和呼吸杂志、中华健康管理学杂志等编委、中华医学杂志英文版通讯编委;承担多项国家级和省部级科研基金,获得北京市科技新星计划支持和教育部新世纪优秀人才支持计划。研究结果获得北京市科技进步三等奖和中华医学科技奖三等奖。
梁振宇
广州医科大学附属第一医院/广州呼吸健康研究院 医学博士,博士后,副主任医师,硕士生导师;广医一院-国家呼吸临床研究中心-项目研究与随访部 副主任;中华医学会呼吸病学分会慢阻肺学组 秘书;广州市医师协会-青年医师分会 常委;广东省预防医学会-呼吸病预防与控制专委会 常委;广东省呼吸与健康学会-慢性呼吸疾病防治专委会 常委;广州市高层次人才(青年后备);主持国家自然科学基金(面上项目/临床专项)、广东省自然科学基金等项目8项。参与国家级项目9项。发表论文100余篇,其中第一/通讯作者30余篇。参编诊疗指南、专家共识8部。获广东省科技进步奖(二等奖)、广东省医学科技奖(二等奖)各1项。
* 文章仅供医疗卫生相关从业者阅读参考
本文完
责编:Jerry


